黑龙江省哈尔滨市南岗区2021-2022学年九年级下学期寒假检测化学试题(word版 含解析)
文档属性
| 名称 | 黑龙江省哈尔滨市南岗区2021-2022学年九年级下学期寒假检测化学试题(word版 含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 870.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-18 10:09:44 | ||
图片预览



文档简介
黑龙江省哈尔滨市南岗区九年级下学期寒假检测化学试题
一、单选题
1.下列物质的性质与用途对应关系错误的是
A.稀有气体一通电后能发光—制霓虹灯 B.石墨一质地软一作电极
C.一氧化碳—还原性一治炼金属 D.氢氧化钠一易潮解—作干燥剂
2.如图所示的食物中维生素含量比较丰富的是
A.西红柿
B.纯牛奶
C.米饭
D.鸡蛋
3.下列各组离子在水溶液中能大量共存的是
A.Cu2+、Na+、、OH- B.H+、K+、、Cl-
C.Mg2+、、OH-、 D.Na+、Ca2+ 、、Cl-
4.将密封良好的方便面从平原带到高原时,包装袋鼓起,是因为袋内的气体分子
A.间隔增大 B.质量增大 C.体积增大 D.个数增多
5.空气是一种宝贵的自然资源,分离液态空气不能得到的气体是
A.氧气 B.稀有气体 C.氦气 D.氢气
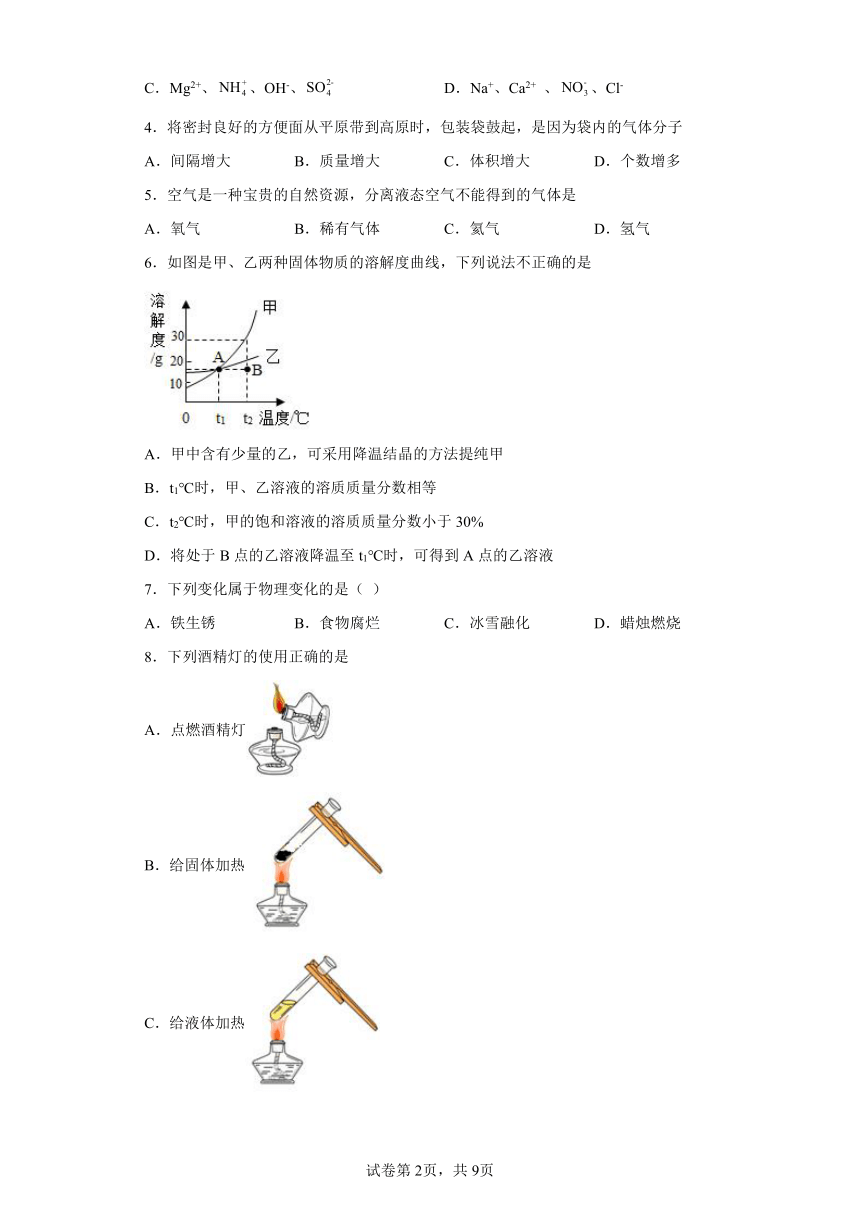
6.如图是甲、乙两种固体物质的溶解度曲线,下列说法不正确的是
A.甲中含有少量的乙,可采用降温结晶的方法提纯甲
B.t1℃时,甲、乙溶液的溶质质量分数相等
C.t2℃时,甲的饱和溶液的溶质质量分数小于30%
D.将处于B点的乙溶液降温至t1℃时,可得到A点的乙溶液
7.下列变化属于物理变化的是( )
A.铁生锈 B.食物腐烂 C.冰雪融化 D.蜡烛燃烧
8.下列酒精灯的使用正确的是
A.点燃酒精灯
B.给固体加热
C.给液体加热
D.熄灭酒精灯
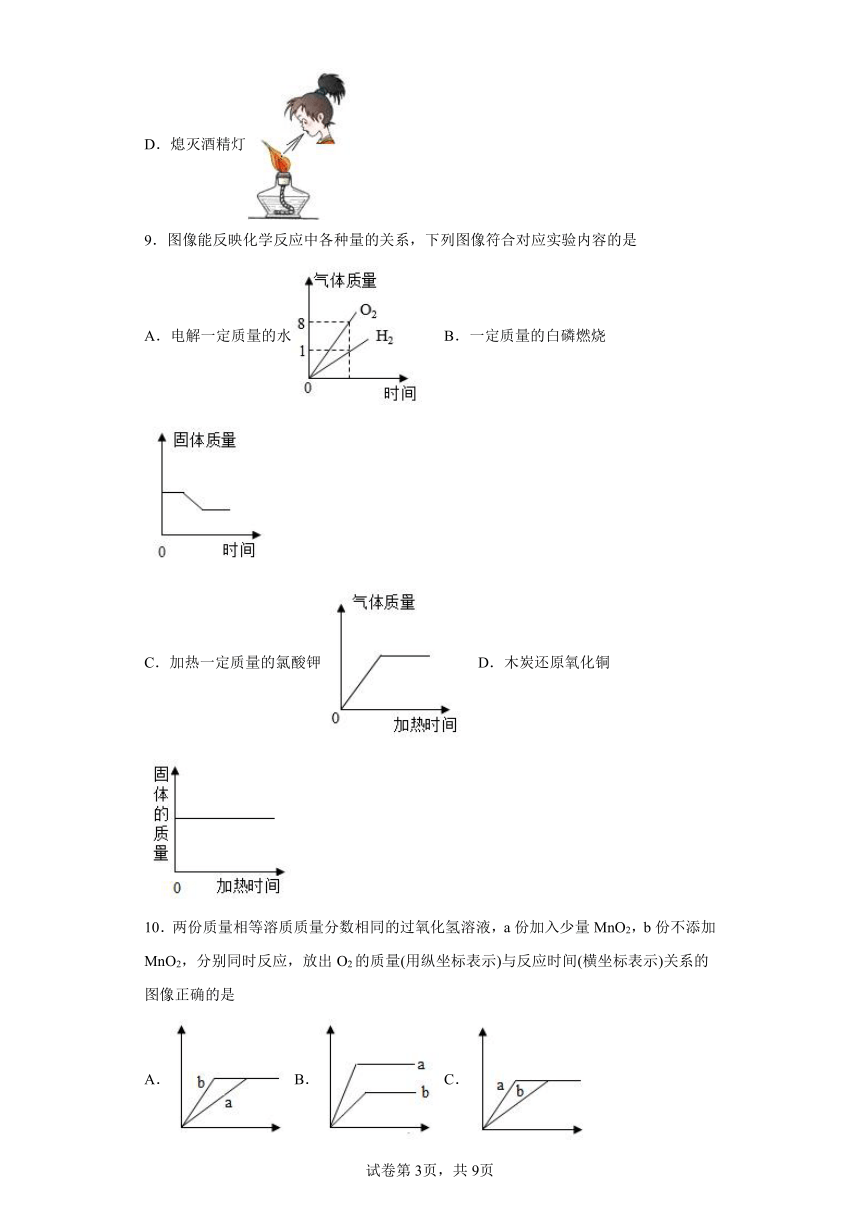
9.图像能反映化学反应中各种量的关系,下列图像符合对应实验内容的是
A.电解一定质量的水 B.一定质量的白磷燃烧
C.加热一定质量的氯酸钾 D.木炭还原氧化铜
10.两份质量相等溶质质量分数相同的过氧化氢溶液,a份加入少量MnO2,b份不添加MnO2,分别同时反应,放出O2的质量(用纵坐标表示)与反应时间(横坐标表示)关系的图像正确的是
A. B. C. D.
11.符号表征是学习,交流化学知识常用的手段,对下列图示分析正确的是( )
A.图①表示的是阴离子
B.图②③对应的元素在同一周期
C.图②是铝离子结构示意图
D.铁原子的核内质子数为55.85
12.碳酸钙在高温条件下发生如下反应:CaCO3CaO+CO2↑。将 100g 含CaCO3 质量分数为 80%的石灰石样品(杂质不发生反应,也不含钙元素),高温煅烧一段时间后,冷却,测得剩余固体中含钙元素的质量分数为 41%,则生成的 CaO 的质量约 为 ( )
A.28.0g B.44.8g C.56.0g D.78.0g
13.水是生产生活中不可缺少的物质。下列关于水的说法中正确的是
A.明矾溶液可以区分硬水和软水
B.在自来水厂净化水的过程中,发生的变化都是物理变化
C.水与过氧化氢的组成元素相同,均可用于制备氧气
D.为了节约用水,可以用工业废水直接浇灌农田
14.下列几种常见的食物中,维生素含量最丰富的是
A.米饭 B.苹果 C.蛋糕 D.大馍
二、多选题
15.下列叙述,其中不正确的是
A.与元素化学性质关系最密切的是原子的核外电子数
B.化学反应前后元素的种类不变
C.在化学变化中,分子可分原子也可分
D.1个水分子由2个氢原子和1个氧原子构成
三、填空题
16.(1)根据下列现象说明空气中存在的某种物质:
①酥脆的饼干在空气中变软,说明空气中含有________________;
②小白鼠在有空气的密闭容器中可存活一段时间,说明空气中含有_______________;
③澄清石灰水露置在空气中会逐渐变浑浊,说明空气中含有__________________。
(2)用分子、原子的观点解释以下问题:
①成熟的苹果会散发香味,说明______
②热胀冷缩现象说明_____
③分子,原子的本质区别是______
17.家用天然气主要成分是甲烷,通常条件下,甲烷是无色无味的气体,难溶于水,燃烧产生蓝色火焰,生成二氧化碳和水,现在出租车和一些公交车也使用了压缩天然气。请回答下列问题:
(1)甲烷的物理性质有________________,化学性质有________________。
(2)和汽油相比使用压缩天然气的好处是__________。
(3)写出甲烷燃烧的化学反应文字表达式_______。
(4)归纳是学习化学的常用方法,下列反应与甲烷燃烧属于同一类型的是_______(填序号);它们都是________________反应;属于分解反应的有_________。
a.
b.
c.
d.
18.生铁用途十分广泛。工业上利用赤铁矿(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如图:
回答下列问题:
(1)生铁属于____材料(填“合金”或“金属”)。“高炉气体”中的_____(填化学式)会导致酸雨。
(2)“煅烧”时:
①生成CO的反应之一为,该反应属于______反应(填基本反应类型)。
②用化学方程式表示利用CO炼铁的原理____________________。
(3)生活中铁制品锈蚀的过程,实际上是Fe与空气中____、___等发生化学反应的过程。下列措施能防止铁制品锈蚀的是____(填标号)。
A 涂油、喷漆 B 镀耐腐蚀的铬层
C 用盐水清洗 D 久置于酸性环境
19.从下列选项中,选择合适的物质字母序号填空:
A 熟石灰 B 碳酸钙 C 尿素 D 一氧化碳 E 氧气 F 小苏打
(1)能供给呼吸的气体是_____;(2)可用来改良酸性土壤的碱是_____;
(3)可用作补钙剂的是_____;(4)工业上炼铁常用作还原剂的气体是_____;
(5)可用作氮肥的是_____;(6)医疗上能用于治疗胃酸过多症的是_____。
四、推断题
20.如图所示A~F是初中化学常见的物质。图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出)。其中A是人体胃液中含有的酸,A和B发生中和反应可得到生活中常用的一种调味品,固体C常用于改良酸性土壤。
(1)A 的化学式为_____;B的溶液中存在的阴离子______。
(2) 长久敞口放置的B固体在空气中吸水潮解,此过程是________物理(填“物理”或“化学”)变化。
(3)E、F的物质类别相同,且E与F能反应放热,F也能与A溶液发生反应,则A与F反应的化学方程式为______。
(4)C与D反应可得到B,则C与D反应的化学方程式为_____。
五、实验题
21.以下是实验室常见的一些化学仪器,请回答下列问题:
(1)在上图中写出标数字的仪器名称:①_____________。
(2)用高锰酸钾制取氧气的符号表达式为_____________,在进行实验时,试管口应放_____________,以防止加热时_________________________;
(3)如图所示操作是探究木炭在氧气中燃烧的实验:
①在上述C操作中,为了使该物质与氧气完全反应,正确的操作方法是_____________。
②D操作中用烧杯倾倒的液体是_____________。
(4)通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室用加热氯化铵和消石灰的固体混合物制取氨气。实验室制取和收集氨气的装置组合是_______。
(5)如图是某学生设计的一种有洗气、检验、贮气等用途的装置。
①当用排空气法收集氧气时,瓶内没有水,气体从_____________(填“a”或“b”)处导管通入;
②当用排水法收集氧气时,应先将瓶内装满水,再将_____________(填“a”或“b”)处和发生装置连接。
六、科学探究题
22.化学兴趣小组的同学在探究碱的化学性质时,完成了如图甲所示的两个实验。实验后,小明同学将废液倒入同一废液缸中,发现混合废液浑浊并显红色。请你完成下列问题:
(1)A实验中发生反应的化学方程式为 _____ 。
(2)B实验中发生反应的现象是 _____ ,反应的化学方程式为 _____ 。
【提出问题】废液中,能使酚酞溶液变红的物质可能是哪些呢?
【作出猜想】猜想一:废液中,能使酚酞溶液变红的物质可能是氢氧化钠;
猜想二:废液中,能使酚酞溶液变红的物质还可能是 _____ ;
猜想三:废液中,能使酚酞溶液变红的物质还可能是氢氧化钠和氢氧化钙。
【实验验证】同学们对可能含有的碱性物质进行确定,取一定量的废液过滤,向滤液中逐滴加入稀盐酸,根据反应现象得到了如图乙所示的图像。
【结论】分析图像数据得出,废液中使酚酞溶液变红的物质一定是 _____ 和 _____ ,一定不是 _____ 。
【拓展提高】为了使以上废液实现安全排放,你的做法是: _____ 。
七、计算题
23.中国登山协会为纪念我们首次攀登珠穆朗玛峰成功50周年,再次组织攀登珠穆朗玛峰活动。阿旺扎西等一行登山运动员成功登顶。假如每位运动员冲顶时消耗自带的液氧4.8 g。求:
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.43 g·L-1)
(2)若在实验室用高锰酸钾为原料制取相同质量的氧气,需要多少千克的高锰酸钾?
(3)用这种方法给登山运动员供氧,是否可行?简述理由____________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【解析】
【详解】
A、稀有气体通电后能发出不同颜色的光,常用来制霓虹灯,故正确;
B、石墨能导电,可以作电极,故错误;
C、一氧化碳具有还原性,可以用来冶炼金属,故正确;
D、氢氧化钠易潮解,可以作干燥剂,故正确;
故选:B
2.A
【解析】
【详解】
A. 西红柿属于蔬菜,提供的主要营养素是维生素,选项正确;
B. 纯牛奶提供的营养素主要是蛋白质,选项错误;
C. 米饭的主要成分是淀粉,属于糖类,选项错误;
D. 鸡蛋,提供的营养素主要是蛋白质,选项错误。
故选A。
3.D
【解析】
【详解】
A、Cu2+、OH 两种离子能结合成氢氧化铜沉淀,不能大量共存,故A错误;
B、H+、两种离子能结合成水和二氧化碳,不能大量共存,故B错误;
C、Mg2+、与OH 离子,分别能结合成氢氧化镁沉淀、氨气和水,不能大量共存,故C错误;
D、四种离子间不能结合成沉淀、气体或水,能大量共存,故D正确。
故选D。
【点睛】
本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水。
4.A
【解析】
【详解】
此题结合实例考查引起气体压强变化的微观本质。从平原到高原外界压强减小,塑料袋内的压强等于原来的大气压,所以包装袋鼓起,气体分子间隔增大。
5.D
【解析】
【详解】
空气的成分(按体积分数):氮气(N2)78%,氧气(O2)21%,稀有气体0.94%,二氧化碳(CO2)0.03%,其它气体和杂质0.03%,空气中不含有氢气。
故选D
6.B
【解析】
【详解】
A、甲溶解度受温度变化影响较大,乙溶解度受温度变化影响较小,甲中含有少量的乙,可采用降温结晶的方法提纯甲,该选项说法正确;
B、t1℃时,甲、乙的饱和溶液的溶质质量分数相等,不是饱和溶液时,质量分数可能相等,也可能不相等,该选项说法不正确;
C、t2℃时,甲的饱和溶液的溶质质量分数:,小于30%,该选项说法正确;
D、将处于B点的乙溶液(不饱和溶液)降温至t1℃时,可得到A点的乙溶液(饱和溶液),该选项说法正确。
故选:B。
7.C
【解析】
【详解】
A、铁生锈的过程中有新物质铁锈生成,属于化学变化.错误;
B、食物腐烂的过程中有新物质生成,属于化学变化.错误;
C、冰雪融化的过程中没有新物质生成,属于物理变化.正确;
D、蜡烛燃烧能生成水和二氧化碳,属于化学变化.错误.
故选C.
8.C
【解析】
【详解】
A、不能使用一盏酒精灯去点燃另一盏酒精灯,图示错误。
B、给固体加热试管口要倾斜向下防止加热的固体放出水蒸气,在试管壁上遇冷液化成小液滴,流到热的试管底部,使试管底部骤冷,炸裂试管,图示错误。
C、给液体加热图示正确,符合题意。
D、熄灭酒精灯不能用嘴吹灭,而应该盖灭,图示错误。
故选C。
9.A
【解析】
【详解】
A、通电分解水,由反应的质量关系可知,生成氢气和氧气的质量比为1:8,故图像符合对应实验内容;
B、白磷燃烧生成五氧化二磷,由于的氧气参加反应,根据质量守恒定律,固体质量先增加,反应完全后质量保持不变,故图像不符合对应实验内容;
C、加热一段时间后氯酸钾才会分解产生氧气,随着反应的进行,氧气的质量增加,反应完成后质量保持不变,故图像不符合对应实验内容;
D、木炭还原氧化铜,反应生成二氧化碳气体和铜,由于有气体生成,根据质量守恒定律,固体质量先减少,反应完全后质量保持不变,故图像不符合对应实验内容。
故选A。
【点睛】
本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象。
10.C
【解析】
【详解】
由题意可知,二氧化锰为该反应的催化剂,可加快该化学反应的速率,但是不能使产物质量增加,故本题选C。
11.B
【解析】
【详解】
A、图①:质子数大于核外电子数,表示的是阳离子,不符合题意;
B、图②:质子数=核外电子数,表示原子,核外有3个电子层,③:质子数小于核外电子数,表示阴离子,是其原子得到一个电子后形成的,其原子核外有3个电子层,故图②③对应的元素在同一周期,都是第三周期,符合题意;
C、图②:质子数=核外电子数,表示原子,质子数=原子序数,13号元素是铝元素,表示铝原子结构示意图,不符合题意;
D、在元素周期表中,元素名称左上角的数字表示原子序数,原子序数=质子数=26,故铁原子的核内质子数为26,不符合题意。
故选B。
12.A
【解析】
【分析】
由质量守恒定律可知,钙元素的质量在反应前后不变。
【详解】
碳酸钙中钙元素的质量为,由质量守恒定律可知,钙元素的质量在反应前后不变,则反应后剩余固体的总质量为,二氧化碳的质量为
设氧化钙的质量为x
故选A。
【点睛】
由质量守恒定律可知,反应前后元素的质量和种类均不变。
13.C
【解析】
【详解】
检验硬水和软水用肥皂水,明矾是将一些难溶性物质转化为胶状物,A错误;
在自来水厂净化水的过程中,消毒时加入的漂白粉会生成新物质属化学变化,B错误;
水与过氧化氢的组成元素相同,均可用于制备氧气,C正确;
工业废水有污染物存在水中,不能直接浇灌农田,D错误。故选C。
14.B
【解析】
【详解】
A、米饭中富含淀粉,淀粉属于糖类,故选项错误;B、苹果中富含有维生素,故选项正确;C、蛋糕是以面粉、鸡蛋、白糖、油脂等为原料,富含糖类、蛋白质、油脂等,故选项错误;D、大馍中富含富含淀粉,淀粉属于糖类,故选项错误,故选B。
15.AC
【解析】
【分析】
【详解】
A、与元素化学性质关系最密切的是原子的最外层电子数,故选项错误;
B、化学反应前后元素的种类不变,故选项正确;
C、化学变化的实质是分子分裂成原子,原子重新组合成新的分子,在化学变化中,分子可分,原子不可分,故选项错误;
D、1个水分子(H2O)由2个氢原子和1个氧原子构成,故选项正确。
故选AC
16. 水蒸气 氧气 二氧化碳 分子是不断运动的
分子之间有间隔 在化学变化中分子可分原子不可分
【解析】
【详解】
(1)、①酥脆的饼干在空气中变软了,说明空气中含有水蒸气。
②因为氧气能够供给呼吸,小白鼠能够存活一段时间,说明空气中含有氧气。
③因为二氧化碳能够使澄清的石灰水,所以在空气中放置的澄清的石灰水变浑浊,可以说明空气中含有二氧化碳。
(2)、根据分子的性质判断,分子的性质有不断运动、有间隔、质量体积小等。所以
①苹果的香味可以散发出来说明分子是不断运动的。
②热胀冷缩说明分子可以变大也可以变小,所以说明分子之间有间隔。
③分子是由原子组成的,分子是化学反应的最小的粒子,而原子是不能通过化学反应再分解的。
17. 无色无味、难溶于水 具有可燃性 减少汽车尾气对空气的污染 b 氧化 a
【解析】
【详解】
(1)根据题意,甲烷是无色无味、难溶于水的气体,不需要通过化学变化就表现出来,属于甲烷的物理性质;甲烷燃烧产生蓝色火焰,生成二氧化碳和水,说明甲烷具有可燃性,可燃性属于化学性质;
(2)天然气燃烧生成了二氧化碳和水,使用压缩天然气燃料的汽车,和使用汽油相比可以减少汽车尾气对空气的污染;
(3)甲烷燃烧生成了二氧化碳和水,化学反应文字表达式为;
(4)根据可知,此反应是甲烷与氧气发生的反应,属于氧化反应;
a、,此反应符合“一变多”的特点,属于分解反应且没有氧气参加,不属于氧化反应,故选项错误;
b、,此反应有氧气参加反应,属于氧化反应,故选项正确;
c、,此反应符合“多变一”的特点,属于化合反应,且没有氧气参加,不属于氧化反应,故选项错误;
d、,此反应符合:一种单质与一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,且没有氧气参加,不属于氧化反应,故选项错误。
故选b。
18. 金属 SO2 化合 水 氧气 AB
【解析】
【详解】
(1)生铁属于金属材料;高炉气体中含有二氧化硫,二氧化硫会导致酸雨的形成。
(2)①碳和二氧化碳反应生成一氧化碳,反应物有两种,生成物有一种,该反应属于化合反应。
②利用CO炼铁的原理为一氧化碳与氧化铁反应生成铁和二氧化碳,化学方程式为:。
(3)铁生锈的过程实际上是铁与水和氧气反应的过程。
A、涂油、喷漆可以隔绝氧气和水,能防止铁生锈,故A项正确;
B、镀耐腐蚀的铬层可以隔绝氧气和水,防止铁生锈,故B项正确;
C、用盐水清洗不能防止铁生锈,反而会加快.铁制品生锈的速度,故C项错误;
D、久置于酸性的环境不能防止铁生锈,会加快铁制品生锈的速度,故D项错误。
故本题选AB。
19. E A B D C F
【解析】
【详解】
(1)能供给呼吸的气体是氧气;
(2)可用来改良酸性土壤的碱是熟石灰;
(3)可用作补钙剂的是碳酸钙;
(4)工业上炼铁常用作还原剂的气体是一氧化碳;
(5)可用作氮肥的是尿素;
(6)医疗上能用于治疗胃酸过多症的是小苏打。
20. HCl OH- 物理 CaO+2HCl=CaCl2+H2O Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
【解析】
【分析】
根据“A是人体胃液中含有的酸”,则A为稀盐酸,根据“A和B发生中和反应可得到生活中常用的一种调味品”,则B为氢氧化钠溶液;根据“固体C常用于改良酸性土壤”,则C为氢氧化钙,再根据框图,结合题目中的信息进行解答;
【详解】
(1)根据分析,A为稀盐酸,B为氢氧化钠溶液,故A的化学式为HCl;B的溶液中存在的阴离子氢氧根离子(OH-)。
(2)根据分析,B为氢氧化钠,长久敞口放置的B固体在空气中吸水潮解,此过程是物理变化。
(3)E、F的物质类别相同,且E与F能反应放热,F也能与A溶液发生反应,而 E同时可以是氢氧化钠和盐酸以及氢氧化钙转化的产物,所以E一定含有氢元素,所以E与F分别为水、氧化钙,故F与A反应的化学方程式为 CaO+2HCl=CaCl2+H2O。
(4)C根据与D反应可得到B,则D为碳酸钠,故C与D反应的化学方程式为 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
21. 长颈漏斗 一团棉花 高锰酸钾粉末随气流进入导管 从瓶口慢慢地伸到瓶底 澄清石灰水 AE a b
【解析】
【分析】
(1)熟悉常见仪器;
(2)根据高锰酸钾制取氧气原理和操作注意事项分析;
(3)根据炭和氧气的反应原理和注意事项分析;
(4)根据反应物状态、反应条件和气体的溶解性、密度选合适的装置;
(5)根据万用瓶的使用分析。
【详解】
(1)长颈漏斗方便加液体药品,锥形瓶常用的反应容器,故答案为:①长颈漏斗。
(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,符号表达式为:;加热高锰酸钾时,试管口要放一团棉花,是为了防止加热时高锰酸钾粉末随气流进入导管;
(3)上述操作探究的内容是探究木炭和氧气的反应,为了使木炭和氧气充分接触,正确的操作方法是从瓶口慢慢地伸到瓶底;生成的气体用澄清石灰水检验,D操作中用烧杯倾倒的液体是澄清石灰水;
(4)实验室用加热氯化铵和消石灰的固体混合物制取氨气,反应物是固体,反应需要加热,发生装置选A,通常情况下,氨气密度比空气小,极易溶于水,因此氨气只能用向下排空气法收集,选E,故装置组合是AE;
(5)当用排空气法收集氧气时,瓶内没有水,气体从a进入,因为氧气的密度比空气的密度大;当用排水法收集氧气时,应先在瓶中装满水,再在b处和发生装置连接,因为氧气不易溶于水,从短管进可以排出水。
【点睛】
本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和实验步骤等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。本考点是中考的重要考点之一,主要出现在实验题中。
22. NaOH+HCl=NaCl+H2O 产生白色沉淀 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 氢氧化钠和碳酸钠 氢氧化钠 碳酸钠 氢氧化钙 加入适量稀盐酸至溶液刚好变成无色
【解析】
【详解】
(1)A实验中,氢氧化钠和稀盐酸反应生成氯化钠和水,发生反应的化学方程式为NaOH+HCl=NaCl+H2O。
(2)B实验中,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,发生反应的现象是产生白色沉淀,反应的化学方程式为Na2CO3+ Ca(OH)2=CaCO3↓+2NaOH。
作出猜想:猜想一:废液中,能使酚酞溶液变红的物质可能是氢氧化钠;猜想二:废液中,能使酚酞溶液变红的物质还可能是氢氧化钠和碳酸钠;猜想三:废液中,能使酚酞溶液变红的物质还可能是氢氧化钠和氢氧化钙。
结论:分析图像数据得出,加入稀盐酸时先和氢氧化钠反应,氢氧化钠完全反应后,产生气体,说明溶液中含有碳酸钠,溶液中含有碳酸钠时一定不含有氢氧化钙,这是因为碳酸钠和氢氧化钙不能共存,因此废液中使酚酞溶液变红的物质一定是氢氧化钠和碳酸钠,一定不是氢氧化钙。
拓展提高:为了使以上废液实现安全排放,做法是:加入适量稀盐酸至溶液刚好变成无色,因为此时稀盐酸恰好和氢氧化钠、碳酸钠完全反应,溶液变为氯化钠溶液,对环境无污染。
23.(1)3.3566 L;(2)47.4 g;(3)不行。此法成本太高,经济上不合算;或在实验室制如此多氧气,耗时太长。
【解析】
【详解】
(1)根据密度公式可知,所需要氧气得体积是;
(2)假设需要高锰酸钾得质量为x,则有
2KMnO4K2MnO4+MnO2+O2
316 32
x 4.8g
x=47.4g
所以需要高锰酸钾得质量为47.4g;
(3)使用高锰酸钾制取氧气得方法不可行,因为高锰酸钾制取氧气的成本高,反应慢。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质的性质与用途对应关系错误的是
A.稀有气体一通电后能发光—制霓虹灯 B.石墨一质地软一作电极
C.一氧化碳—还原性一治炼金属 D.氢氧化钠一易潮解—作干燥剂
2.如图所示的食物中维生素含量比较丰富的是
A.西红柿
B.纯牛奶
C.米饭
D.鸡蛋
3.下列各组离子在水溶液中能大量共存的是
A.Cu2+、Na+、、OH- B.H+、K+、、Cl-
C.Mg2+、、OH-、 D.Na+、Ca2+ 、、Cl-
4.将密封良好的方便面从平原带到高原时,包装袋鼓起,是因为袋内的气体分子
A.间隔增大 B.质量增大 C.体积增大 D.个数增多
5.空气是一种宝贵的自然资源,分离液态空气不能得到的气体是
A.氧气 B.稀有气体 C.氦气 D.氢气
6.如图是甲、乙两种固体物质的溶解度曲线,下列说法不正确的是
A.甲中含有少量的乙,可采用降温结晶的方法提纯甲
B.t1℃时,甲、乙溶液的溶质质量分数相等
C.t2℃时,甲的饱和溶液的溶质质量分数小于30%
D.将处于B点的乙溶液降温至t1℃时,可得到A点的乙溶液
7.下列变化属于物理变化的是( )
A.铁生锈 B.食物腐烂 C.冰雪融化 D.蜡烛燃烧
8.下列酒精灯的使用正确的是
A.点燃酒精灯
B.给固体加热
C.给液体加热
D.熄灭酒精灯
9.图像能反映化学反应中各种量的关系,下列图像符合对应实验内容的是
A.电解一定质量的水 B.一定质量的白磷燃烧
C.加热一定质量的氯酸钾 D.木炭还原氧化铜
10.两份质量相等溶质质量分数相同的过氧化氢溶液,a份加入少量MnO2,b份不添加MnO2,分别同时反应,放出O2的质量(用纵坐标表示)与反应时间(横坐标表示)关系的图像正确的是
A. B. C. D.
11.符号表征是学习,交流化学知识常用的手段,对下列图示分析正确的是( )
A.图①表示的是阴离子
B.图②③对应的元素在同一周期
C.图②是铝离子结构示意图
D.铁原子的核内质子数为55.85
12.碳酸钙在高温条件下发生如下反应:CaCO3CaO+CO2↑。将 100g 含CaCO3 质量分数为 80%的石灰石样品(杂质不发生反应,也不含钙元素),高温煅烧一段时间后,冷却,测得剩余固体中含钙元素的质量分数为 41%,则生成的 CaO 的质量约 为 ( )
A.28.0g B.44.8g C.56.0g D.78.0g
13.水是生产生活中不可缺少的物质。下列关于水的说法中正确的是
A.明矾溶液可以区分硬水和软水
B.在自来水厂净化水的过程中,发生的变化都是物理变化
C.水与过氧化氢的组成元素相同,均可用于制备氧气
D.为了节约用水,可以用工业废水直接浇灌农田
14.下列几种常见的食物中,维生素含量最丰富的是
A.米饭 B.苹果 C.蛋糕 D.大馍
二、多选题
15.下列叙述,其中不正确的是
A.与元素化学性质关系最密切的是原子的核外电子数
B.化学反应前后元素的种类不变
C.在化学变化中,分子可分原子也可分
D.1个水分子由2个氢原子和1个氧原子构成
三、填空题
16.(1)根据下列现象说明空气中存在的某种物质:
①酥脆的饼干在空气中变软,说明空气中含有________________;
②小白鼠在有空气的密闭容器中可存活一段时间,说明空气中含有_______________;
③澄清石灰水露置在空气中会逐渐变浑浊,说明空气中含有__________________。
(2)用分子、原子的观点解释以下问题:
①成熟的苹果会散发香味,说明______
②热胀冷缩现象说明_____
③分子,原子的本质区别是______
17.家用天然气主要成分是甲烷,通常条件下,甲烷是无色无味的气体,难溶于水,燃烧产生蓝色火焰,生成二氧化碳和水,现在出租车和一些公交车也使用了压缩天然气。请回答下列问题:
(1)甲烷的物理性质有________________,化学性质有________________。
(2)和汽油相比使用压缩天然气的好处是__________。
(3)写出甲烷燃烧的化学反应文字表达式_______。
(4)归纳是学习化学的常用方法,下列反应与甲烷燃烧属于同一类型的是_______(填序号);它们都是________________反应;属于分解反应的有_________。
a.
b.
c.
d.
18.生铁用途十分广泛。工业上利用赤铁矿(主要成分是Fe2O3,还含少量SiO2等杂质)冶炼生铁的过程如图:
回答下列问题:
(1)生铁属于____材料(填“合金”或“金属”)。“高炉气体”中的_____(填化学式)会导致酸雨。
(2)“煅烧”时:
①生成CO的反应之一为,该反应属于______反应(填基本反应类型)。
②用化学方程式表示利用CO炼铁的原理____________________。
(3)生活中铁制品锈蚀的过程,实际上是Fe与空气中____、___等发生化学反应的过程。下列措施能防止铁制品锈蚀的是____(填标号)。
A 涂油、喷漆 B 镀耐腐蚀的铬层
C 用盐水清洗 D 久置于酸性环境
19.从下列选项中,选择合适的物质字母序号填空:
A 熟石灰 B 碳酸钙 C 尿素 D 一氧化碳 E 氧气 F 小苏打
(1)能供给呼吸的气体是_____;(2)可用来改良酸性土壤的碱是_____;
(3)可用作补钙剂的是_____;(4)工业上炼铁常用作还原剂的气体是_____;
(5)可用作氮肥的是_____;(6)医疗上能用于治疗胃酸过多症的是_____。
四、推断题
20.如图所示A~F是初中化学常见的物质。图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出)。其中A是人体胃液中含有的酸,A和B发生中和反应可得到生活中常用的一种调味品,固体C常用于改良酸性土壤。
(1)A 的化学式为_____;B的溶液中存在的阴离子______。
(2) 长久敞口放置的B固体在空气中吸水潮解,此过程是________物理(填“物理”或“化学”)变化。
(3)E、F的物质类别相同,且E与F能反应放热,F也能与A溶液发生反应,则A与F反应的化学方程式为______。
(4)C与D反应可得到B,则C与D反应的化学方程式为_____。
五、实验题
21.以下是实验室常见的一些化学仪器,请回答下列问题:
(1)在上图中写出标数字的仪器名称:①_____________。
(2)用高锰酸钾制取氧气的符号表达式为_____________,在进行实验时,试管口应放_____________,以防止加热时_________________________;
(3)如图所示操作是探究木炭在氧气中燃烧的实验:
①在上述C操作中,为了使该物质与氧气完全反应,正确的操作方法是_____________。
②D操作中用烧杯倾倒的液体是_____________。
(4)通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室用加热氯化铵和消石灰的固体混合物制取氨气。实验室制取和收集氨气的装置组合是_______。
(5)如图是某学生设计的一种有洗气、检验、贮气等用途的装置。
①当用排空气法收集氧气时,瓶内没有水,气体从_____________(填“a”或“b”)处导管通入;
②当用排水法收集氧气时,应先将瓶内装满水,再将_____________(填“a”或“b”)处和发生装置连接。
六、科学探究题
22.化学兴趣小组的同学在探究碱的化学性质时,完成了如图甲所示的两个实验。实验后,小明同学将废液倒入同一废液缸中,发现混合废液浑浊并显红色。请你完成下列问题:
(1)A实验中发生反应的化学方程式为 _____ 。
(2)B实验中发生反应的现象是 _____ ,反应的化学方程式为 _____ 。
【提出问题】废液中,能使酚酞溶液变红的物质可能是哪些呢?
【作出猜想】猜想一:废液中,能使酚酞溶液变红的物质可能是氢氧化钠;
猜想二:废液中,能使酚酞溶液变红的物质还可能是 _____ ;
猜想三:废液中,能使酚酞溶液变红的物质还可能是氢氧化钠和氢氧化钙。
【实验验证】同学们对可能含有的碱性物质进行确定,取一定量的废液过滤,向滤液中逐滴加入稀盐酸,根据反应现象得到了如图乙所示的图像。
【结论】分析图像数据得出,废液中使酚酞溶液变红的物质一定是 _____ 和 _____ ,一定不是 _____ 。
【拓展提高】为了使以上废液实现安全排放,你的做法是: _____ 。
七、计算题
23.中国登山协会为纪念我们首次攀登珠穆朗玛峰成功50周年,再次组织攀登珠穆朗玛峰活动。阿旺扎西等一行登山运动员成功登顶。假如每位运动员冲顶时消耗自带的液氧4.8 g。求:
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.43 g·L-1)
(2)若在实验室用高锰酸钾为原料制取相同质量的氧气,需要多少千克的高锰酸钾?
(3)用这种方法给登山运动员供氧,是否可行?简述理由____________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【解析】
【详解】
A、稀有气体通电后能发出不同颜色的光,常用来制霓虹灯,故正确;
B、石墨能导电,可以作电极,故错误;
C、一氧化碳具有还原性,可以用来冶炼金属,故正确;
D、氢氧化钠易潮解,可以作干燥剂,故正确;
故选:B
2.A
【解析】
【详解】
A. 西红柿属于蔬菜,提供的主要营养素是维生素,选项正确;
B. 纯牛奶提供的营养素主要是蛋白质,选项错误;
C. 米饭的主要成分是淀粉,属于糖类,选项错误;
D. 鸡蛋,提供的营养素主要是蛋白质,选项错误。
故选A。
3.D
【解析】
【详解】
A、Cu2+、OH 两种离子能结合成氢氧化铜沉淀,不能大量共存,故A错误;
B、H+、两种离子能结合成水和二氧化碳,不能大量共存,故B错误;
C、Mg2+、与OH 离子,分别能结合成氢氧化镁沉淀、氨气和水,不能大量共存,故C错误;
D、四种离子间不能结合成沉淀、气体或水,能大量共存,故D正确。
故选D。
【点睛】
本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水。
4.A
【解析】
【详解】
此题结合实例考查引起气体压强变化的微观本质。从平原到高原外界压强减小,塑料袋内的压强等于原来的大气压,所以包装袋鼓起,气体分子间隔增大。
5.D
【解析】
【详解】
空气的成分(按体积分数):氮气(N2)78%,氧气(O2)21%,稀有气体0.94%,二氧化碳(CO2)0.03%,其它气体和杂质0.03%,空气中不含有氢气。
故选D
6.B
【解析】
【详解】
A、甲溶解度受温度变化影响较大,乙溶解度受温度变化影响较小,甲中含有少量的乙,可采用降温结晶的方法提纯甲,该选项说法正确;
B、t1℃时,甲、乙的饱和溶液的溶质质量分数相等,不是饱和溶液时,质量分数可能相等,也可能不相等,该选项说法不正确;
C、t2℃时,甲的饱和溶液的溶质质量分数:,小于30%,该选项说法正确;
D、将处于B点的乙溶液(不饱和溶液)降温至t1℃时,可得到A点的乙溶液(饱和溶液),该选项说法正确。
故选:B。
7.C
【解析】
【详解】
A、铁生锈的过程中有新物质铁锈生成,属于化学变化.错误;
B、食物腐烂的过程中有新物质生成,属于化学变化.错误;
C、冰雪融化的过程中没有新物质生成,属于物理变化.正确;
D、蜡烛燃烧能生成水和二氧化碳,属于化学变化.错误.
故选C.
8.C
【解析】
【详解】
A、不能使用一盏酒精灯去点燃另一盏酒精灯,图示错误。
B、给固体加热试管口要倾斜向下防止加热的固体放出水蒸气,在试管壁上遇冷液化成小液滴,流到热的试管底部,使试管底部骤冷,炸裂试管,图示错误。
C、给液体加热图示正确,符合题意。
D、熄灭酒精灯不能用嘴吹灭,而应该盖灭,图示错误。
故选C。
9.A
【解析】
【详解】
A、通电分解水,由反应的质量关系可知,生成氢气和氧气的质量比为1:8,故图像符合对应实验内容;
B、白磷燃烧生成五氧化二磷,由于的氧气参加反应,根据质量守恒定律,固体质量先增加,反应完全后质量保持不变,故图像不符合对应实验内容;
C、加热一段时间后氯酸钾才会分解产生氧气,随着反应的进行,氧气的质量增加,反应完成后质量保持不变,故图像不符合对应实验内容;
D、木炭还原氧化铜,反应生成二氧化碳气体和铜,由于有气体生成,根据质量守恒定律,固体质量先减少,反应完全后质量保持不变,故图像不符合对应实验内容。
故选A。
【点睛】
本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象。
10.C
【解析】
【详解】
由题意可知,二氧化锰为该反应的催化剂,可加快该化学反应的速率,但是不能使产物质量增加,故本题选C。
11.B
【解析】
【详解】
A、图①:质子数大于核外电子数,表示的是阳离子,不符合题意;
B、图②:质子数=核外电子数,表示原子,核外有3个电子层,③:质子数小于核外电子数,表示阴离子,是其原子得到一个电子后形成的,其原子核外有3个电子层,故图②③对应的元素在同一周期,都是第三周期,符合题意;
C、图②:质子数=核外电子数,表示原子,质子数=原子序数,13号元素是铝元素,表示铝原子结构示意图,不符合题意;
D、在元素周期表中,元素名称左上角的数字表示原子序数,原子序数=质子数=26,故铁原子的核内质子数为26,不符合题意。
故选B。
12.A
【解析】
【分析】
由质量守恒定律可知,钙元素的质量在反应前后不变。
【详解】
碳酸钙中钙元素的质量为,由质量守恒定律可知,钙元素的质量在反应前后不变,则反应后剩余固体的总质量为,二氧化碳的质量为
设氧化钙的质量为x
故选A。
【点睛】
由质量守恒定律可知,反应前后元素的质量和种类均不变。
13.C
【解析】
【详解】
检验硬水和软水用肥皂水,明矾是将一些难溶性物质转化为胶状物,A错误;
在自来水厂净化水的过程中,消毒时加入的漂白粉会生成新物质属化学变化,B错误;
水与过氧化氢的组成元素相同,均可用于制备氧气,C正确;
工业废水有污染物存在水中,不能直接浇灌农田,D错误。故选C。
14.B
【解析】
【详解】
A、米饭中富含淀粉,淀粉属于糖类,故选项错误;B、苹果中富含有维生素,故选项正确;C、蛋糕是以面粉、鸡蛋、白糖、油脂等为原料,富含糖类、蛋白质、油脂等,故选项错误;D、大馍中富含富含淀粉,淀粉属于糖类,故选项错误,故选B。
15.AC
【解析】
【分析】
【详解】
A、与元素化学性质关系最密切的是原子的最外层电子数,故选项错误;
B、化学反应前后元素的种类不变,故选项正确;
C、化学变化的实质是分子分裂成原子,原子重新组合成新的分子,在化学变化中,分子可分,原子不可分,故选项错误;
D、1个水分子(H2O)由2个氢原子和1个氧原子构成,故选项正确。
故选AC
16. 水蒸气 氧气 二氧化碳 分子是不断运动的
分子之间有间隔 在化学变化中分子可分原子不可分
【解析】
【详解】
(1)、①酥脆的饼干在空气中变软了,说明空气中含有水蒸气。
②因为氧气能够供给呼吸,小白鼠能够存活一段时间,说明空气中含有氧气。
③因为二氧化碳能够使澄清的石灰水,所以在空气中放置的澄清的石灰水变浑浊,可以说明空气中含有二氧化碳。
(2)、根据分子的性质判断,分子的性质有不断运动、有间隔、质量体积小等。所以
①苹果的香味可以散发出来说明分子是不断运动的。
②热胀冷缩说明分子可以变大也可以变小,所以说明分子之间有间隔。
③分子是由原子组成的,分子是化学反应的最小的粒子,而原子是不能通过化学反应再分解的。
17. 无色无味、难溶于水 具有可燃性 减少汽车尾气对空气的污染 b 氧化 a
【解析】
【详解】
(1)根据题意,甲烷是无色无味、难溶于水的气体,不需要通过化学变化就表现出来,属于甲烷的物理性质;甲烷燃烧产生蓝色火焰,生成二氧化碳和水,说明甲烷具有可燃性,可燃性属于化学性质;
(2)天然气燃烧生成了二氧化碳和水,使用压缩天然气燃料的汽车,和使用汽油相比可以减少汽车尾气对空气的污染;
(3)甲烷燃烧生成了二氧化碳和水,化学反应文字表达式为;
(4)根据可知,此反应是甲烷与氧气发生的反应,属于氧化反应;
a、,此反应符合“一变多”的特点,属于分解反应且没有氧气参加,不属于氧化反应,故选项错误;
b、,此反应有氧气参加反应,属于氧化反应,故选项正确;
c、,此反应符合“多变一”的特点,属于化合反应,且没有氧气参加,不属于氧化反应,故选项错误;
d、,此反应符合:一种单质与一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,且没有氧气参加,不属于氧化反应,故选项错误。
故选b。
18. 金属 SO2 化合 水 氧气 AB
【解析】
【详解】
(1)生铁属于金属材料;高炉气体中含有二氧化硫,二氧化硫会导致酸雨的形成。
(2)①碳和二氧化碳反应生成一氧化碳,反应物有两种,生成物有一种,该反应属于化合反应。
②利用CO炼铁的原理为一氧化碳与氧化铁反应生成铁和二氧化碳,化学方程式为:。
(3)铁生锈的过程实际上是铁与水和氧气反应的过程。
A、涂油、喷漆可以隔绝氧气和水,能防止铁生锈,故A项正确;
B、镀耐腐蚀的铬层可以隔绝氧气和水,防止铁生锈,故B项正确;
C、用盐水清洗不能防止铁生锈,反而会加快.铁制品生锈的速度,故C项错误;
D、久置于酸性的环境不能防止铁生锈,会加快铁制品生锈的速度,故D项错误。
故本题选AB。
19. E A B D C F
【解析】
【详解】
(1)能供给呼吸的气体是氧气;
(2)可用来改良酸性土壤的碱是熟石灰;
(3)可用作补钙剂的是碳酸钙;
(4)工业上炼铁常用作还原剂的气体是一氧化碳;
(5)可用作氮肥的是尿素;
(6)医疗上能用于治疗胃酸过多症的是小苏打。
20. HCl OH- 物理 CaO+2HCl=CaCl2+H2O Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
【解析】
【分析】
根据“A是人体胃液中含有的酸”,则A为稀盐酸,根据“A和B发生中和反应可得到生活中常用的一种调味品”,则B为氢氧化钠溶液;根据“固体C常用于改良酸性土壤”,则C为氢氧化钙,再根据框图,结合题目中的信息进行解答;
【详解】
(1)根据分析,A为稀盐酸,B为氢氧化钠溶液,故A的化学式为HCl;B的溶液中存在的阴离子氢氧根离子(OH-)。
(2)根据分析,B为氢氧化钠,长久敞口放置的B固体在空气中吸水潮解,此过程是物理变化。
(3)E、F的物质类别相同,且E与F能反应放热,F也能与A溶液发生反应,而 E同时可以是氢氧化钠和盐酸以及氢氧化钙转化的产物,所以E一定含有氢元素,所以E与F分别为水、氧化钙,故F与A反应的化学方程式为 CaO+2HCl=CaCl2+H2O。
(4)C根据与D反应可得到B,则D为碳酸钠,故C与D反应的化学方程式为 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
21. 长颈漏斗 一团棉花 高锰酸钾粉末随气流进入导管 从瓶口慢慢地伸到瓶底 澄清石灰水 AE a b
【解析】
【分析】
(1)熟悉常见仪器;
(2)根据高锰酸钾制取氧气原理和操作注意事项分析;
(3)根据炭和氧气的反应原理和注意事项分析;
(4)根据反应物状态、反应条件和气体的溶解性、密度选合适的装置;
(5)根据万用瓶的使用分析。
【详解】
(1)长颈漏斗方便加液体药品,锥形瓶常用的反应容器,故答案为:①长颈漏斗。
(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,符号表达式为:;加热高锰酸钾时,试管口要放一团棉花,是为了防止加热时高锰酸钾粉末随气流进入导管;
(3)上述操作探究的内容是探究木炭和氧气的反应,为了使木炭和氧气充分接触,正确的操作方法是从瓶口慢慢地伸到瓶底;生成的气体用澄清石灰水检验,D操作中用烧杯倾倒的液体是澄清石灰水;
(4)实验室用加热氯化铵和消石灰的固体混合物制取氨气,反应物是固体,反应需要加热,发生装置选A,通常情况下,氨气密度比空气小,极易溶于水,因此氨气只能用向下排空气法收集,选E,故装置组合是AE;
(5)当用排空气法收集氧气时,瓶内没有水,气体从a进入,因为氧气的密度比空气的密度大;当用排水法收集氧气时,应先在瓶中装满水,再在b处和发生装置连接,因为氧气不易溶于水,从短管进可以排出水。
【点睛】
本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和实验步骤等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。本考点是中考的重要考点之一,主要出现在实验题中。
22. NaOH+HCl=NaCl+H2O 产生白色沉淀 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 氢氧化钠和碳酸钠 氢氧化钠 碳酸钠 氢氧化钙 加入适量稀盐酸至溶液刚好变成无色
【解析】
【详解】
(1)A实验中,氢氧化钠和稀盐酸反应生成氯化钠和水,发生反应的化学方程式为NaOH+HCl=NaCl+H2O。
(2)B实验中,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,发生反应的现象是产生白色沉淀,反应的化学方程式为Na2CO3+ Ca(OH)2=CaCO3↓+2NaOH。
作出猜想:猜想一:废液中,能使酚酞溶液变红的物质可能是氢氧化钠;猜想二:废液中,能使酚酞溶液变红的物质还可能是氢氧化钠和碳酸钠;猜想三:废液中,能使酚酞溶液变红的物质还可能是氢氧化钠和氢氧化钙。
结论:分析图像数据得出,加入稀盐酸时先和氢氧化钠反应,氢氧化钠完全反应后,产生气体,说明溶液中含有碳酸钠,溶液中含有碳酸钠时一定不含有氢氧化钙,这是因为碳酸钠和氢氧化钙不能共存,因此废液中使酚酞溶液变红的物质一定是氢氧化钠和碳酸钠,一定不是氢氧化钙。
拓展提高:为了使以上废液实现安全排放,做法是:加入适量稀盐酸至溶液刚好变成无色,因为此时稀盐酸恰好和氢氧化钠、碳酸钠完全反应,溶液变为氯化钠溶液,对环境无污染。
23.(1)3.3566 L;(2)47.4 g;(3)不行。此法成本太高,经济上不合算;或在实验室制如此多氧气,耗时太长。
【解析】
【详解】
(1)根据密度公式可知,所需要氧气得体积是;
(2)假设需要高锰酸钾得质量为x,则有
2KMnO4K2MnO4+MnO2+O2
316 32
x 4.8g
x=47.4g
所以需要高锰酸钾得质量为47.4g;
(3)使用高锰酸钾制取氧气得方法不可行,因为高锰酸钾制取氧气的成本高,反应慢。
答案第1页,共2页
答案第1页,共2页
同课章节目录
