安徽省阜阳市城南中学2021-2022学年下学期九年级化学开学作业检测卷(word版有答案)
文档属性
| 名称 | 安徽省阜阳市城南中学2021-2022学年下学期九年级化学开学作业检测卷(word版有答案) |  | |
| 格式 | doc | ||
| 文件大小 | 405.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-20 11:34:00 | ||
图片预览

文档简介
阜阳市城南中学2021-2022学年度(下)九年级
化学开学作业检测卷
可能用到的相对原子质量: Na-23 Cl-35.5 O-16 H-1 Ca-40 Zn-65 S-32
一、选择题(本大题包括12小题,每小题1分,共12分。每小题只有一个选项符合题意)
1.[2021安庆三模]中华传统文化博大精深。下列成语涉及化学变化的是 ( )
A.火上浇油 B.破釜沉舟 C.滴水成冰 D.聚沙成塔
2.(2019 广安)2019年5月5日-5月31日,邓小平图书馆开展了以“保护地球”为主题的网上竞答活动,下列做法不符合这一理念的是( )
A.废旧电池回收处理 B.用新能源汽车代替燃油汽车
C.提倡植树造林 D.任意排放“三废”
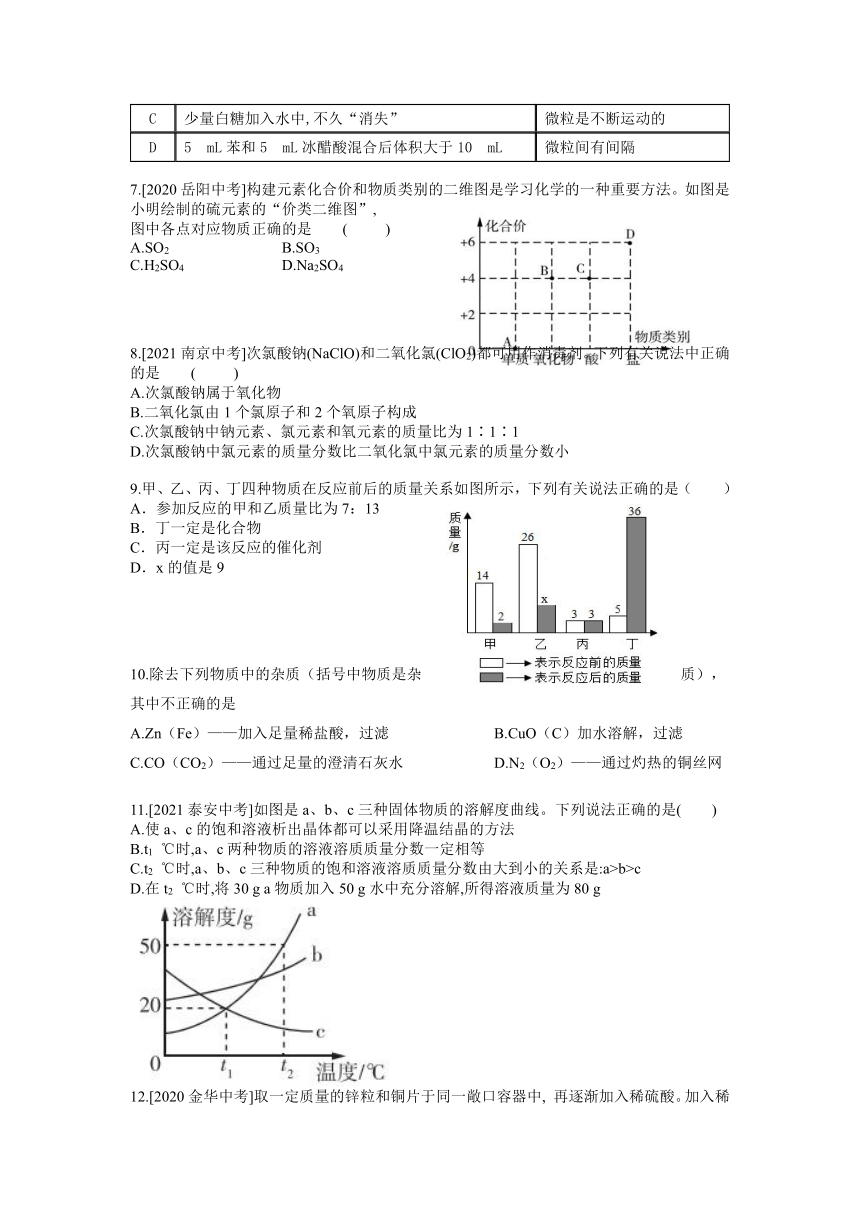
3.用下图所示实验装置进行CO2气体的制取,能达到实验目的是( )
4.在化学实验或日常生活中都应强化安全意识。下列做法符合安全要求的是 ( )
A.氢氧化钠不慎沾到皮肤上,立即用硫酸冲洗
B.一氧化碳还原氧化铁实验中,将尾气直接排放
C.使用酒精炉时,直接向燃着的炉内添加酒精
D.家中天然气泄漏时,关闭阀门并打开门窗通风
5.[2021连云港中考改编]氟在元素周期表中的相关信息如图所示,钠原子的结构示意图如图所示。下列说法正确的是 ( )
A.氟是一种金属元素
B.1个氟气分子中含有9个质子
C.钠原子在化学反应中易失去1个电子
D.F-和Na+的最外层电子数不相等
6.[2017安徽中考]下列实验事实不能作为相应观点的证据的是 ( )
选项 实验事实 观点
A 铁丝在氧气中燃烧后质量增大 化学反应前后质量守恒
B 水电解可得到氢气和氧气 分子是可分的
C 少量白糖加入水中,不久“消失” 微粒是不断运动的
D 5 mL苯和5 mL冰醋酸混合后体积大于10 mL 微粒间有间隔
7.[2020岳阳中考]构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是小明绘制的硫元素的“价类二维图”,
图中各点对应物质正确的是 ( )
A.SO2 B.SO3
C.H2SO4 D.Na2SO4
8.[2021南京中考]次氯酸钠(NaClO)和二氧化氯(ClO2)都可用作消毒剂。下列有关说法中正确的是 ( )
A.次氯酸钠属于氧化物
B.二氧化氯由1个氯原子和2个氧原子构成
C.次氯酸钠中钠元素、氯元素和氧元素的质量比为1∶1∶1
D.次氯酸钠中氯元素的质量分数比二氧化氯中氯元素的质量分数小
9.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法正确的是( )
A.参加反应的甲和乙质量比为7:13
B.丁一定是化合物
C.丙一定是该反应的催化剂
D.x的值是9
10.除去下列物质中的杂质(括号中物质是杂质),其中不正确的是
A.Zn(Fe)——加入足量稀盐酸,过滤 B.CuO(C)加水溶解,过滤
C.CO(CO2)——通过足量的澄清石灰水 D.N2(O2)——通过灼热的铜丝网
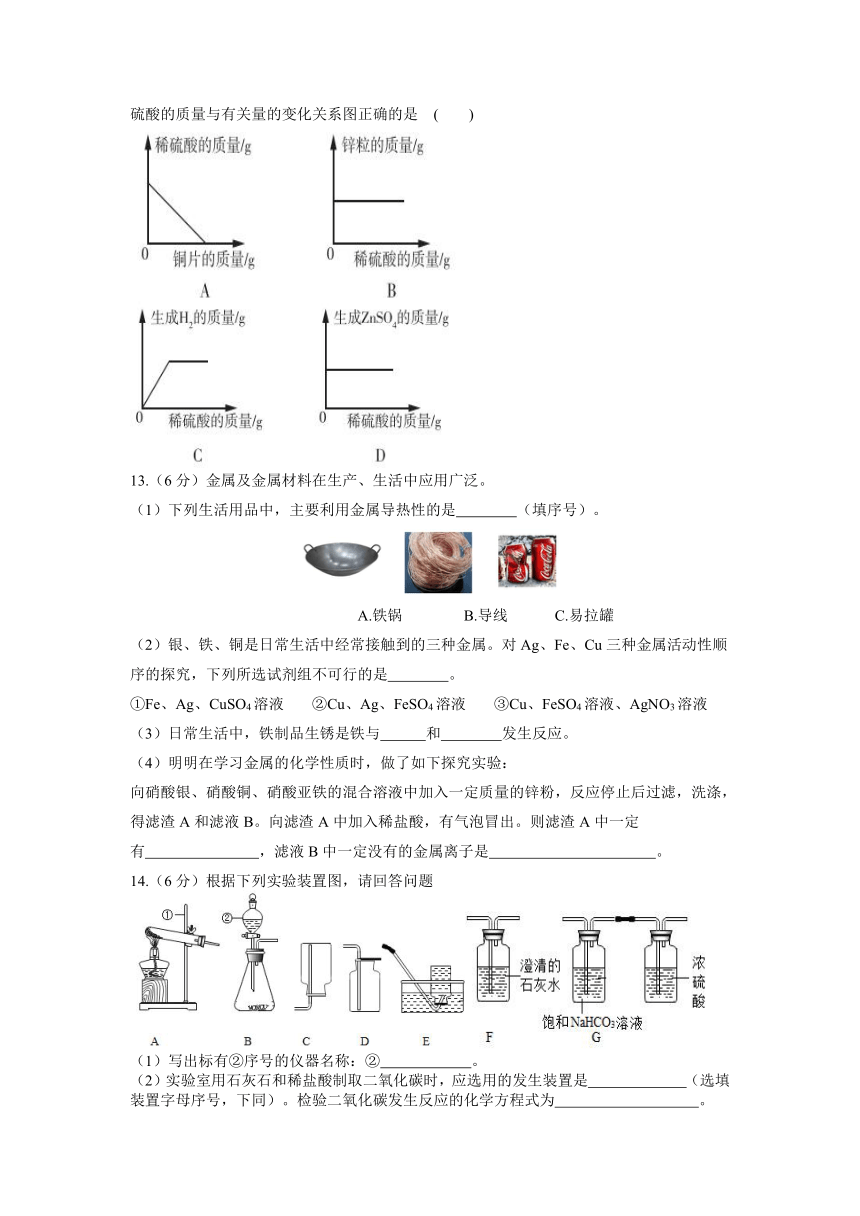
11.[2021泰安中考]如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是:a>b>c
D.在t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液质量为80 g
12.[2020金华中考]取一定质量的锌粒和铜片于同一敞口容器中, 再逐渐加入稀硫酸。加入稀硫酸的质量与有关量的变化关系图正确的是 ( )
13.(6分)金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是 (填序号)。
A.铁锅 B.导线 C.易拉罐
(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是 。
①Fe、Ag、CuSO4溶液 ②Cu、Ag、FeSO4溶液 ③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与 和 发生反应。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有 ,滤液B中一定没有的金属离子是 。
14.(6分)根据下列实验装置图,请回答问题
写出标有②序号的仪器名称:②分液漏斗 。
(2)实验室用石灰石和稀盐酸制取二氧化碳时,应选用的发生装置是 B(选填装置字母序号,下同)。检验二氧化碳发生反应的化学方程式为 CO2+Ca(OH)2=CaCO3↓+H2O。
(3)用排空气法收集气体时,导管口要接近集气瓶底部,其目的是为了把空气充分的排出来 。
(4)若要收集一瓶干燥纯净的二氧化碳,所选装置正确的连接顺序是气体
发生装置→G →D (选填装置字母序号)。
15.(5分)废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
已知:Sn+SnCl4 2SnCl2
(1)SnCl4中锡元素的化合价是 。
(2)铜的金属活动性比锡的 (填“强”或“弱”),固体A中一定含有的金属元素是 。
(3)写出步骤②发生反应的化学方程式 。
(4)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是 ,
(回答一点即可)。
16.(6+3).某化学兴趣小组的同学为了探究铁生锈的因素,设计了如图装置进行实验。实验时,他们将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察,试管底部有黑色固体。
请你一起参与分析,并完成后续实验设计。
【观察现象】 ①装置右侧U形管中的红墨水液面左高右低;②铁钉生锈,试管底部有黑色固体物质。 【提出问题】U形管中的红墨水液面为何左高右低?黑色固体物质又是什么?
【理论分析】该小组的回学根据学过的知识分析得知,红墨水液面左高右低的原因是 。
【猜想与假设】该小组中的小明同学猜测该黑色固体可能含有:①Fe,②Fe203,③FeCl3,④C四种物质。
【分析与验证】该实验小组同学根据小明的四种猜测做了以下分析:
(1)小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是 。
(2)该小组的同学不能确定黑色固体中是否含有铁单质,请你帮助他们设计方案进行确认:
实验步骤 实验现象 实验结论
你选的试剂是
【继续探究】请你继续设计实验探究影响铁钉生锈快慢的其他因素 。
注意:若答对第(3)(4)题奖励3分.化学试卷总分不超过40分。
过氧化钙晶体(CaO2 ·yH2O),常温为白色,能溶于酸,难溶于酒精。过氧化钙晶体组成的测定:
称取 21.6 克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化
钙晶体受热时会先失去结晶水,再继续加热会分解产生氧气)
(3) 根据上图可知 y=________。
(4) 350℃时发生反应的化学方程式为 。
17.(5分)某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0 g,再用100.0 g稀硫酸溶液逐滴滴入,实验情况如图所示,求:
(1)铜锌合金中,Zn的质量是__________g。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
答案:
1 2 3 4 5 6 7 8 9 10 11 12
A D B D C A D D B A C C
13. (6分) (1) A (2)2 (3)氧气和水 (4)银、铜、铁; Cu2+、Ag+
14. (6分) (1) 分液漏斗 (2) B CO2+Ca(OH)2==CaCO3+H2O (3)排尽装置内的空气,防止污染空气
(4) G D
15. (5分) (1)SnCl4中Cl的化合价为-1,根据化合物中正负化合价的代数和为零,可知SnCl4中Sn的化合价为+4;(2)在金属活动性顺序中铜排在锡之后,因此铜的金属活动性比锡弱,由于Sn+SnCl4 ==2SnCl2,因此向含铜、锡等金属粉中加入SnCl4溶液后,锡与SnCl4溶液反应,铜不能与SnCl4溶液反应,所以固体A中一定含有铜元素;(3)步骤②是电解反应的化学方程式为2SnCl2==Sn+SnCl4;(4)废旧电路板中含有塑料,若直接焚烧会污染环境,因此该工艺的主要优点是避免焚烧塑料产生污染,更加环保。
16. 【理论分析】因为铁钉生锈消耗了试管内的氧气,使试管内压强低于大气压,在外界大气压的作用下,装置中左侧导管中的液面升高,右侧导管中液面下降。故填:铁钉生锈消耗试管中的氧气,导致试管中压强减小。[分析与验证](1)小强同学认为一定含有碳,该结论也得到小组同学的认可,是因为铁钉是由铁碳合金制成的,且常温下碳不跟氧气、食盐水等物质反应,又呈黑色。故填:铁钉中含有碳。
(2)为了确定黑色固体中是否含有铁,可根据铁的化学性质设计实验。可选用试剂稀盐酸,实验现象为:不产生气泡;实验结论为:黑色固体中不含铁单质。(合理即可)
[继续探究]影响铁钉生锈快慢的其他因素有温度等。可以设计如下实验:将两支相同且洁净的铁钉分别置于两支试管中,然后分别加入等量的水,使铁钉部分处于水中,再将其中一支试管置于冰箱中(设置温度低于10℃),另一支置于冰箱外的实验台上(常温下),观察现象。
(3).y=8 (4). 2CaO2====2CaO+O2
17.(1) 6.5
(2) 由图可知,加入稀硫酸的质量为50 g时,恰好完全反应。
解:设所用稀硫酸溶液中溶质的质量分数是x,
Zn+H2SO4===ZnSO4+H2↑
65 98
6.5 g 50 g x
X=19.6%
答:所用稀硫酸溶液中溶质的质量分数是19.6%
化学开学作业检测卷
可能用到的相对原子质量: Na-23 Cl-35.5 O-16 H-1 Ca-40 Zn-65 S-32
一、选择题(本大题包括12小题,每小题1分,共12分。每小题只有一个选项符合题意)
1.[2021安庆三模]中华传统文化博大精深。下列成语涉及化学变化的是 ( )
A.火上浇油 B.破釜沉舟 C.滴水成冰 D.聚沙成塔
2.(2019 广安)2019年5月5日-5月31日,邓小平图书馆开展了以“保护地球”为主题的网上竞答活动,下列做法不符合这一理念的是( )
A.废旧电池回收处理 B.用新能源汽车代替燃油汽车
C.提倡植树造林 D.任意排放“三废”
3.用下图所示实验装置进行CO2气体的制取,能达到实验目的是( )
4.在化学实验或日常生活中都应强化安全意识。下列做法符合安全要求的是 ( )
A.氢氧化钠不慎沾到皮肤上,立即用硫酸冲洗
B.一氧化碳还原氧化铁实验中,将尾气直接排放
C.使用酒精炉时,直接向燃着的炉内添加酒精
D.家中天然气泄漏时,关闭阀门并打开门窗通风
5.[2021连云港中考改编]氟在元素周期表中的相关信息如图所示,钠原子的结构示意图如图所示。下列说法正确的是 ( )
A.氟是一种金属元素
B.1个氟气分子中含有9个质子
C.钠原子在化学反应中易失去1个电子
D.F-和Na+的最外层电子数不相等
6.[2017安徽中考]下列实验事实不能作为相应观点的证据的是 ( )
选项 实验事实 观点
A 铁丝在氧气中燃烧后质量增大 化学反应前后质量守恒
B 水电解可得到氢气和氧气 分子是可分的
C 少量白糖加入水中,不久“消失” 微粒是不断运动的
D 5 mL苯和5 mL冰醋酸混合后体积大于10 mL 微粒间有间隔
7.[2020岳阳中考]构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是小明绘制的硫元素的“价类二维图”,
图中各点对应物质正确的是 ( )
A.SO2 B.SO3
C.H2SO4 D.Na2SO4
8.[2021南京中考]次氯酸钠(NaClO)和二氧化氯(ClO2)都可用作消毒剂。下列有关说法中正确的是 ( )
A.次氯酸钠属于氧化物
B.二氧化氯由1个氯原子和2个氧原子构成
C.次氯酸钠中钠元素、氯元素和氧元素的质量比为1∶1∶1
D.次氯酸钠中氯元素的质量分数比二氧化氯中氯元素的质量分数小
9.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法正确的是( )
A.参加反应的甲和乙质量比为7:13
B.丁一定是化合物
C.丙一定是该反应的催化剂
D.x的值是9
10.除去下列物质中的杂质(括号中物质是杂质),其中不正确的是
A.Zn(Fe)——加入足量稀盐酸,过滤 B.CuO(C)加水溶解,过滤
C.CO(CO2)——通过足量的澄清石灰水 D.N2(O2)——通过灼热的铜丝网
11.[2021泰安中考]如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是:a>b>c
D.在t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液质量为80 g
12.[2020金华中考]取一定质量的锌粒和铜片于同一敞口容器中, 再逐渐加入稀硫酸。加入稀硫酸的质量与有关量的变化关系图正确的是 ( )
13.(6分)金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是 (填序号)。
A.铁锅 B.导线 C.易拉罐
(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是 。
①Fe、Ag、CuSO4溶液 ②Cu、Ag、FeSO4溶液 ③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与 和 发生反应。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有 ,滤液B中一定没有的金属离子是 。
14.(6分)根据下列实验装置图,请回答问题
写出标有②序号的仪器名称:②分液漏斗 。
(2)实验室用石灰石和稀盐酸制取二氧化碳时,应选用的发生装置是 B(选填装置字母序号,下同)。检验二氧化碳发生反应的化学方程式为 CO2+Ca(OH)2=CaCO3↓+H2O。
(3)用排空气法收集气体时,导管口要接近集气瓶底部,其目的是为了把空气充分的排出来 。
(4)若要收集一瓶干燥纯净的二氧化碳,所选装置正确的连接顺序是气体
发生装置→G →D (选填装置字母序号)。
15.(5分)废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
已知:Sn+SnCl4 2SnCl2
(1)SnCl4中锡元素的化合价是 。
(2)铜的金属活动性比锡的 (填“强”或“弱”),固体A中一定含有的金属元素是 。
(3)写出步骤②发生反应的化学方程式 。
(4)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是 ,
(回答一点即可)。
16.(6+3).某化学兴趣小组的同学为了探究铁生锈的因素,设计了如图装置进行实验。实验时,他们将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察,试管底部有黑色固体。
请你一起参与分析,并完成后续实验设计。
【观察现象】 ①装置右侧U形管中的红墨水液面左高右低;②铁钉生锈,试管底部有黑色固体物质。 【提出问题】U形管中的红墨水液面为何左高右低?黑色固体物质又是什么?
【理论分析】该小组的回学根据学过的知识分析得知,红墨水液面左高右低的原因是 。
【猜想与假设】该小组中的小明同学猜测该黑色固体可能含有:①Fe,②Fe203,③FeCl3,④C四种物质。
【分析与验证】该实验小组同学根据小明的四种猜测做了以下分析:
(1)小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是 。
(2)该小组的同学不能确定黑色固体中是否含有铁单质,请你帮助他们设计方案进行确认:
实验步骤 实验现象 实验结论
你选的试剂是
【继续探究】请你继续设计实验探究影响铁钉生锈快慢的其他因素 。
注意:若答对第(3)(4)题奖励3分.化学试卷总分不超过40分。
过氧化钙晶体(CaO2 ·yH2O),常温为白色,能溶于酸,难溶于酒精。过氧化钙晶体组成的测定:
称取 21.6 克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化
钙晶体受热时会先失去结晶水,再继续加热会分解产生氧气)
(3) 根据上图可知 y=________。
(4) 350℃时发生反应的化学方程式为 。
17.(5分)某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0 g,再用100.0 g稀硫酸溶液逐滴滴入,实验情况如图所示,求:
(1)铜锌合金中,Zn的质量是__________g。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
答案:
1 2 3 4 5 6 7 8 9 10 11 12
A D B D C A D D B A C C
13. (6分) (1) A (2)2 (3)氧气和水 (4)银、铜、铁; Cu2+、Ag+
14. (6分) (1) 分液漏斗 (2) B CO2+Ca(OH)2==CaCO3+H2O (3)排尽装置内的空气,防止污染空气
(4) G D
15. (5分) (1)SnCl4中Cl的化合价为-1,根据化合物中正负化合价的代数和为零,可知SnCl4中Sn的化合价为+4;(2)在金属活动性顺序中铜排在锡之后,因此铜的金属活动性比锡弱,由于Sn+SnCl4 ==2SnCl2,因此向含铜、锡等金属粉中加入SnCl4溶液后,锡与SnCl4溶液反应,铜不能与SnCl4溶液反应,所以固体A中一定含有铜元素;(3)步骤②是电解反应的化学方程式为2SnCl2==Sn+SnCl4;(4)废旧电路板中含有塑料,若直接焚烧会污染环境,因此该工艺的主要优点是避免焚烧塑料产生污染,更加环保。
16. 【理论分析】因为铁钉生锈消耗了试管内的氧气,使试管内压强低于大气压,在外界大气压的作用下,装置中左侧导管中的液面升高,右侧导管中液面下降。故填:铁钉生锈消耗试管中的氧气,导致试管中压强减小。[分析与验证](1)小强同学认为一定含有碳,该结论也得到小组同学的认可,是因为铁钉是由铁碳合金制成的,且常温下碳不跟氧气、食盐水等物质反应,又呈黑色。故填:铁钉中含有碳。
(2)为了确定黑色固体中是否含有铁,可根据铁的化学性质设计实验。可选用试剂稀盐酸,实验现象为:不产生气泡;实验结论为:黑色固体中不含铁单质。(合理即可)
[继续探究]影响铁钉生锈快慢的其他因素有温度等。可以设计如下实验:将两支相同且洁净的铁钉分别置于两支试管中,然后分别加入等量的水,使铁钉部分处于水中,再将其中一支试管置于冰箱中(设置温度低于10℃),另一支置于冰箱外的实验台上(常温下),观察现象。
(3).y=8 (4). 2CaO2====2CaO+O2
17.(1) 6.5
(2) 由图可知,加入稀硫酸的质量为50 g时,恰好完全反应。
解:设所用稀硫酸溶液中溶质的质量分数是x,
Zn+H2SO4===ZnSO4+H2↑
65 98
6.5 g 50 g x
X=19.6%
答:所用稀硫酸溶液中溶质的质量分数是19.6%
同课章节目录
