四川省江油市八校2021-2022学年九年级下学期开学考试化学试题(B卷)(word版有答案)
文档属性
| 名称 | 四川省江油市八校2021-2022学年九年级下学期开学考试化学试题(B卷)(word版有答案) |  | |
| 格式 | zip | ||
| 文件大小 | 179.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-24 14:38:43 | ||
图片预览



文档简介
2022年春四川省江油市八校联考(入学测试)
人教版九年级化学试卷
(B卷)
座位号 班级 姓名
一、选择题 (每小题4分,共36分)
1.苹果醋含有果胶,维他命,矿物质及酵素,其酸性成分能增强人体的免疫和抗病毒能力,具有明显降低血脂和排毒保健功能,苹果醋的生产过程中,属于化学变化的是( )
A.清洗苹果 B.把苹果捣碎
C.苹果发酵成醋 D.用纱布过滤后装瓶
2.下列关于分子和原子的叙述正确的是( )
A.物质只能由分子、原子构成
B.分子的质量一定大于原子的质量
C.同种原子可能构成不同分子
D.化学变化中分子数目一定发生变化
3.铁是一种应用广泛的金属。下列叙述错误的是( )
A.铁是地壳中含量第二多的金属
B.炼铁高炉中CO的生成属于化合反应
C.炼铁时CO与Fe2O3发生置换反应
D.用铁可以回收硝酸银废液中的银
4.下列实验方案不能达到目的的是( )
选项 实验方案 实验目的
A 用磁铁吸附 分离铜粉和铁粉
B 通过灼热的氧化铜 除去二氧化碳中少量的一氧化碳
C 用碳代替红磷在集气瓶中燃烧 测定空气中氧气的含量
D 在空气中灼烧 鉴别真金和假金(铜锌合金)
A.A B.B C.C D.D
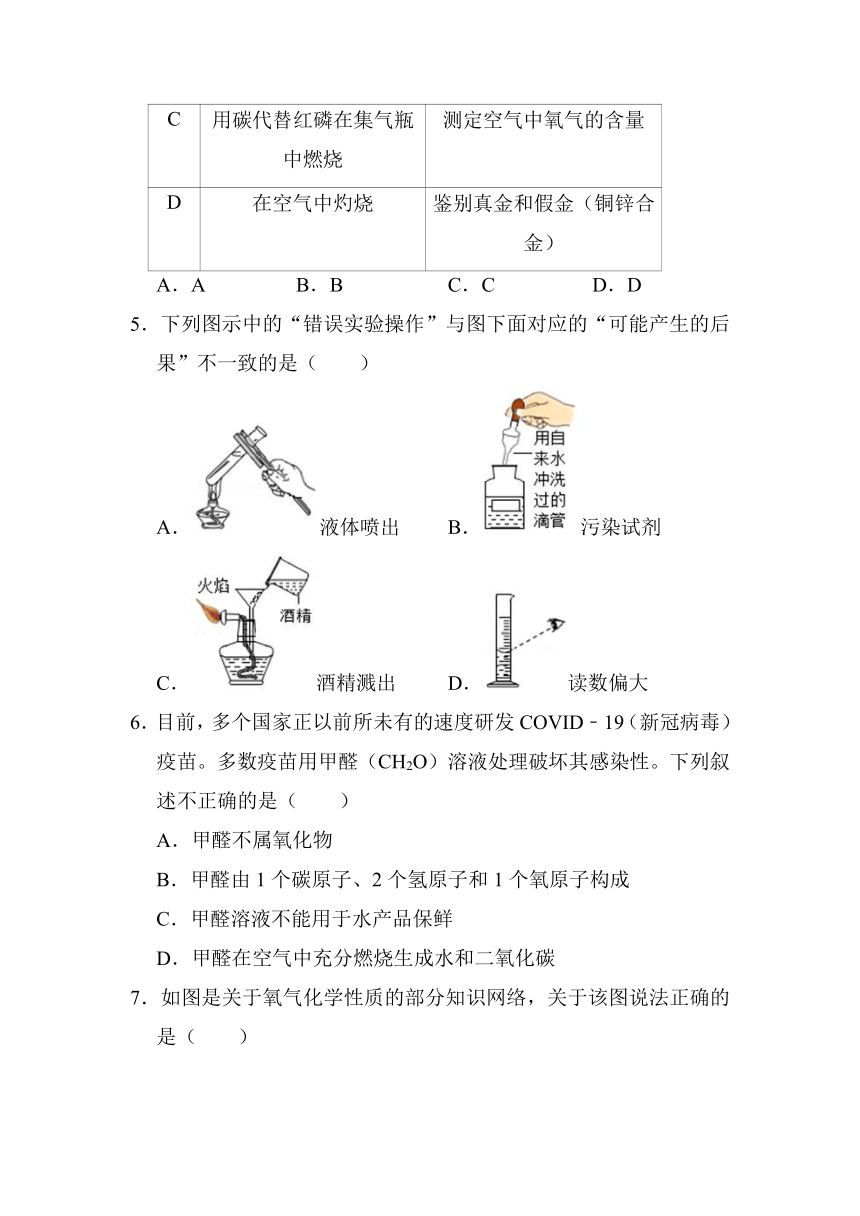
5.下列图示中的“错误实验操作”与图下面对应的“可能产生的后果”不一致的是( )
A.液体喷出 B.污染试剂
C.酒精溅出 D.读数偏大
6.目前,多个国家正以前所未有的速度研发COVID﹣19(新冠病毒)疫苗。多数疫苗用甲醛(CH2O)溶液处理破坏其感染性。下列叙述不正确的是( )
A.甲醛不属氧化物
B.甲醛由1个碳原子、2个氢原子和1个氧原子构成
C.甲醛溶液不能用于水产品保鲜
D.甲醛在空气中充分燃烧生成水和二氧化碳
7.如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )
A.Fe在Ⅰ、Ⅱ两类反应中的产物不相同
B.Ⅱ中Fe、Al氧化均能生成致密的氧化物薄膜,可阻止其进一步被氧化
C.S、P、Mg在氧气中燃烧均会产生大量白烟
D.Ⅰ类反应放出热量,Ⅱ类反应吸收热量
8.逻辑推理是化学学习中常见的思维方法。下列推理正确的是( )
A.原子也可以保持物质的化学性质,所以保持SO2的化学性质的最小粒子是硫原子和氧原子
B.单质是由同种元素组成的纯净物,所以含同种元素的物质都是单质
C.元素的种类决定于质子数,但质子数相等的粒子不一定属于同种元素
D.在不同物质中同种元素可以显示不同化合价,而在同种物质中同种元素的化合价一定相同
9.血红蛋白是一较复杂的化合物,相对分子质量为68000,已知其中铁元素的质量分数为0.33%,则平均每个血红蛋白分子中含有的铁原子个数为( )
A.1 B.2 C.3 D.4
二、非选择题(每小题2分,共47分)
10(6分).在某次实验课上,小东同学把一包铁粉和镁粉的混合物放入一定量的AgNO3溶液中,使其充分反应后过滤,得到滤渣和浅绿色滤液,据此回答下列问题:
(1)滤渣中一定含有 ,可能含有 (填化学式)。
(2)滤液中可能含有的溶质 (填化学式)。
(3)用化学方程式表示溶液变为浅绿色的原因 。
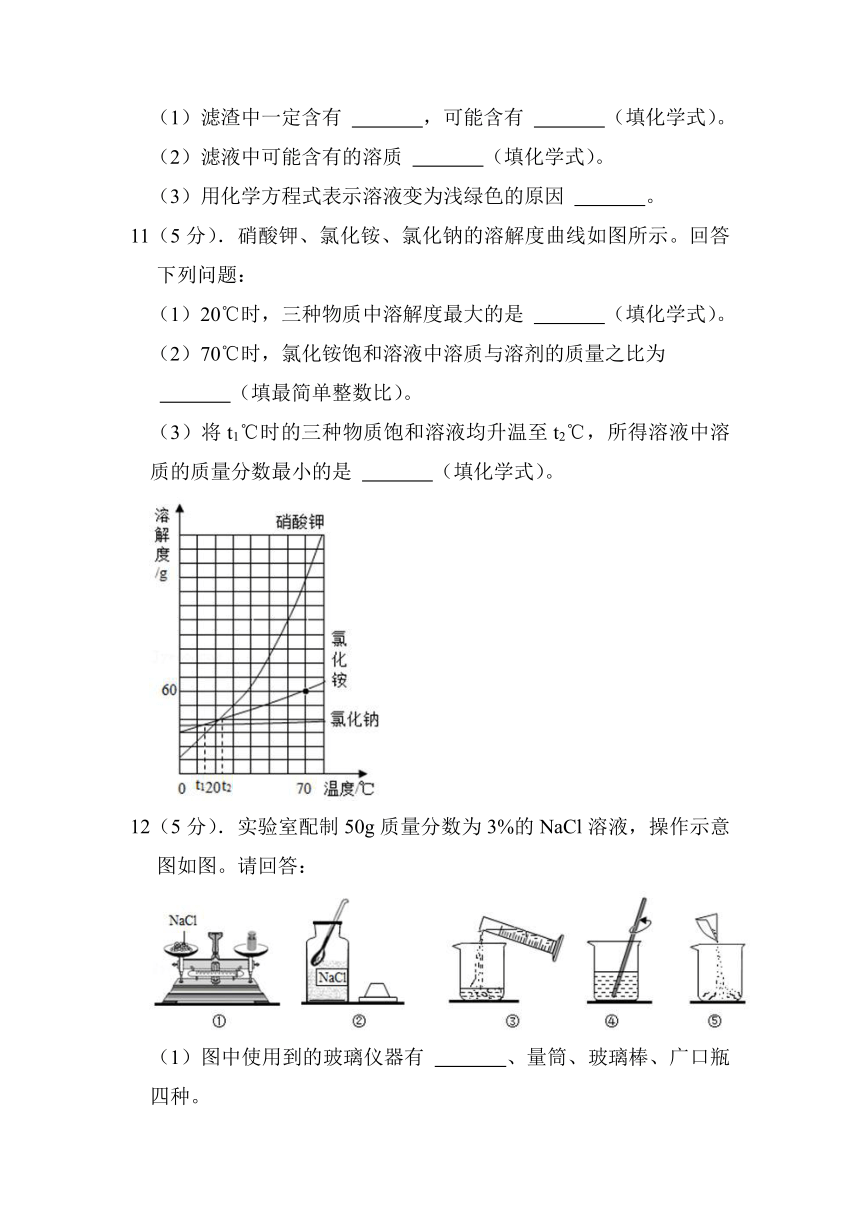
11(5分).硝酸钾、氯化铵、氯化钠的溶解度曲线如图所示。回答下列问题:
(1)20℃时,三种物质中溶解度最大的是 (填化学式)。
(2)70℃时,氯化铵饱和溶液中溶质与溶剂的质量之比为
(填最简单整数比)。
(3)将t1℃时的三种物质饱和溶液均升温至t2℃,所得溶液中溶质的质量分数最小的是 (填化学式)。
12(5分).实验室配制50g质量分数为3%的NaCl溶液,操作示意图如图。请回答:
(1)图中使用到的玻璃仪器有 、量筒、玻璃棒、广口瓶四种。
(2)图示中正确的操作顺序为 (填序号)。
(3)溶解时用玻璃棒搅拌的目的是 。
(4)取10g配制好的质量分数为3%的NaCl溶液,稀释成质量分数为1%的NaCl溶液,需加水 g。
13(12分).今年国庆假期,明明从黄河带回一瓶浑浊的河水,他在化学实验室模拟自来水厂的净水过程,最终制成蒸馏水,流程如图所示:
(1)流程中加入的A物质是 ,操作①的名称是 ,实验室进行该操作时需要用到的仪器为铁架台、 ;其中玻璃棒的作用是 。过滤后滤液仍然浑浊的原因可能是
(填序号)。
A.液面没有低于滤液边缘
B.滤纸没有紧贴漏斗内壁而留有气泡
C.滤纸破损
D.漏斗下端未紧贴烧杯内壁
(2)操作②主要是活性炭的 性除去一些异味和色素。
(3)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明是 (填“硬水”或“软水”),生活中硬水软化采用 方法,该方法属于 变化。
(4)如图是实验室制取蒸馏水的装置。仪器B的名称: 。实验时冷凝水应从 端进(a或b)。实验中加入的沸石(或碎瓷片) 催化剂(填是或不是)。
14(9分).实验课上,老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种,为确定该粉末的成分,同学们进行了如下探究,请你参与其中并回答问题。
【提出猜想】甲组:铜粉;乙组:氧化铁粉末;丙组: 。
【设计实验】
方案1:取少量红色粉末放入试管中,滴加足量的 (从下列试剂中选择:氯化钠溶液、稀盐酸、氢氧化钠溶液)振荡,若甲组猜想正确,则实验现象为 。
方案2:取10g红色粉末放入硬质玻璃管中,先通入CO,然后用酒精喷灯加热至完全反应,实验装置如图所示,停止加热并继续通入CO至装置冷却。实验过程中将反应后的气体通入虚线框内足量的氢氧化钙溶液中,该装置的作用有检验并吸收生成CO2和 等。
【数据处理】
①若乙组猜想正确,则硬质玻璃管内发生反应的化学方程式是 。
②若丙组猜想正确,等装置完全冷却到室温,重新称量氢氧化钙溶液的总质量增加了6.6g,则该氢氧化钙溶液吸收CO2生成沉淀质量为 ;原红色粉末中氧化铁的质量分数为 。
15(10分).人们生活的方方面面都与化学密切相关。回答下列问题:
(1)下列物品的主要成分属于合成材料的是 (填序号)。
a.纯棉T恤
b.保鲜膜
c.羊毛衫
d.电源插座外壳
(2)米粉的主要成分是淀粉,淀粉属于营养物质中的 ;油汤洒在衣服上,用洗衣液使油污较稳定分散于水中的现象称为 。
(3)建造房屋要使用大量钢材,防止钢材生锈的方法有
(写一种)。
(4)新能源汽车常用锂电池提供动力,Li+的结构示意图,x= 。前18号元素中和Li原子最外层电子数相同的金属元素是 。
(5)无土栽培时可用KNO3和NH4Cl配制营养液。区分KNO3和NH4Cl固体可选用的试剂是 。如图是KNO3和NH4Cl的溶解度曲线。26℃时,饱和NH4Cl溶液的质量分数为 (精确到0.1%);50℃时的两杯相同质量的饱和KNO3溶液和饱和NH4Cl溶液,均降温到26℃,所得两种溶液的质量 (填序号)。
a.KNO3溶液大
b.一样大
c.NH4Cl溶液大
d.无法确定
16(17分).我国高铁建设走在世界前列,修建高铁需要大量铁矿石来炼铁,进而炼钢。
(1)下列三种铁矿石的主要成分Fe2O3、Fe3O4、FeCO3中,含铁量最高的是 。高炉炼铁需要的原料有铁矿石、 、 和石灰石。
(2)要炼出含铁96%的生铁1000t,至少需要含氧化铁80%的赤铁矿多少吨?若高炉气体不加处理,理论上会向大气中排放CO2多少吨?(无计算过程不给分,计算结果保留整数。)
参考答案
一.选择题
1.C; 2.C; 3.C; 4.C; 5.C;
6.B; 7.A; 8.C; 9.D;
二.非选择题
10.Ag;Fe;AgNO3;Fe+2AgNO3=2Ag+Fe(NO3)2;
11.NH4Cl;3:5;KNO3;
12.烧杯;②①⑤③④;加快溶解速率;20;
13.明矾;过滤;漏斗、玻璃棒和烧杯;引流;AC;吸附;硬水;煮沸;化学;冷凝器;b;不是;
14.铜粉、氧化铁粉末的混合物;稀盐酸;固体不溶解;收集CO;Fe2O3+3CO2Fe+3CO2;15g;80%;
15.bd;糖类;乳化现象;刷漆;3;Na;熟石灰粉末;28.6%;c;
16.解: (1)Fe2O3、Fe3O4、 FeCO3的含铁量分别为:
,故含铁量最高的是Fe3O4 ;高炉炼铁需要的原料有铁矿石、焦炭、空气和石灰石,故填: Fe3O4;焦炭;空气;
(2)设至少需要赤铁矿的质量为x,反应产生CO2的质量为y
3CO+Fe2O3 2Fe+ 3CO2
160 112 132
80%x 1000tx96% y
x=1714t , y=1131t
答:至少需要含氧化铁80%的赤铁矿1714t ,理论上会向大气中排放CO21131t.
人教版九年级化学试卷
(B卷)
座位号 班级 姓名
一、选择题 (每小题4分,共36分)
1.苹果醋含有果胶,维他命,矿物质及酵素,其酸性成分能增强人体的免疫和抗病毒能力,具有明显降低血脂和排毒保健功能,苹果醋的生产过程中,属于化学变化的是( )
A.清洗苹果 B.把苹果捣碎
C.苹果发酵成醋 D.用纱布过滤后装瓶
2.下列关于分子和原子的叙述正确的是( )
A.物质只能由分子、原子构成
B.分子的质量一定大于原子的质量
C.同种原子可能构成不同分子
D.化学变化中分子数目一定发生变化
3.铁是一种应用广泛的金属。下列叙述错误的是( )
A.铁是地壳中含量第二多的金属
B.炼铁高炉中CO的生成属于化合反应
C.炼铁时CO与Fe2O3发生置换反应
D.用铁可以回收硝酸银废液中的银
4.下列实验方案不能达到目的的是( )
选项 实验方案 实验目的
A 用磁铁吸附 分离铜粉和铁粉
B 通过灼热的氧化铜 除去二氧化碳中少量的一氧化碳
C 用碳代替红磷在集气瓶中燃烧 测定空气中氧气的含量
D 在空气中灼烧 鉴别真金和假金(铜锌合金)
A.A B.B C.C D.D
5.下列图示中的“错误实验操作”与图下面对应的“可能产生的后果”不一致的是( )
A.液体喷出 B.污染试剂
C.酒精溅出 D.读数偏大
6.目前,多个国家正以前所未有的速度研发COVID﹣19(新冠病毒)疫苗。多数疫苗用甲醛(CH2O)溶液处理破坏其感染性。下列叙述不正确的是( )
A.甲醛不属氧化物
B.甲醛由1个碳原子、2个氢原子和1个氧原子构成
C.甲醛溶液不能用于水产品保鲜
D.甲醛在空气中充分燃烧生成水和二氧化碳
7.如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )
A.Fe在Ⅰ、Ⅱ两类反应中的产物不相同
B.Ⅱ中Fe、Al氧化均能生成致密的氧化物薄膜,可阻止其进一步被氧化
C.S、P、Mg在氧气中燃烧均会产生大量白烟
D.Ⅰ类反应放出热量,Ⅱ类反应吸收热量
8.逻辑推理是化学学习中常见的思维方法。下列推理正确的是( )
A.原子也可以保持物质的化学性质,所以保持SO2的化学性质的最小粒子是硫原子和氧原子
B.单质是由同种元素组成的纯净物,所以含同种元素的物质都是单质
C.元素的种类决定于质子数,但质子数相等的粒子不一定属于同种元素
D.在不同物质中同种元素可以显示不同化合价,而在同种物质中同种元素的化合价一定相同
9.血红蛋白是一较复杂的化合物,相对分子质量为68000,已知其中铁元素的质量分数为0.33%,则平均每个血红蛋白分子中含有的铁原子个数为( )
A.1 B.2 C.3 D.4
二、非选择题(每小题2分,共47分)
10(6分).在某次实验课上,小东同学把一包铁粉和镁粉的混合物放入一定量的AgNO3溶液中,使其充分反应后过滤,得到滤渣和浅绿色滤液,据此回答下列问题:
(1)滤渣中一定含有 ,可能含有 (填化学式)。
(2)滤液中可能含有的溶质 (填化学式)。
(3)用化学方程式表示溶液变为浅绿色的原因 。
11(5分).硝酸钾、氯化铵、氯化钠的溶解度曲线如图所示。回答下列问题:
(1)20℃时,三种物质中溶解度最大的是 (填化学式)。
(2)70℃时,氯化铵饱和溶液中溶质与溶剂的质量之比为
(填最简单整数比)。
(3)将t1℃时的三种物质饱和溶液均升温至t2℃,所得溶液中溶质的质量分数最小的是 (填化学式)。
12(5分).实验室配制50g质量分数为3%的NaCl溶液,操作示意图如图。请回答:
(1)图中使用到的玻璃仪器有 、量筒、玻璃棒、广口瓶四种。
(2)图示中正确的操作顺序为 (填序号)。
(3)溶解时用玻璃棒搅拌的目的是 。
(4)取10g配制好的质量分数为3%的NaCl溶液,稀释成质量分数为1%的NaCl溶液,需加水 g。
13(12分).今年国庆假期,明明从黄河带回一瓶浑浊的河水,他在化学实验室模拟自来水厂的净水过程,最终制成蒸馏水,流程如图所示:
(1)流程中加入的A物质是 ,操作①的名称是 ,实验室进行该操作时需要用到的仪器为铁架台、 ;其中玻璃棒的作用是 。过滤后滤液仍然浑浊的原因可能是
(填序号)。
A.液面没有低于滤液边缘
B.滤纸没有紧贴漏斗内壁而留有气泡
C.滤纸破损
D.漏斗下端未紧贴烧杯内壁
(2)操作②主要是活性炭的 性除去一些异味和色素。
(3)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明是 (填“硬水”或“软水”),生活中硬水软化采用 方法,该方法属于 变化。
(4)如图是实验室制取蒸馏水的装置。仪器B的名称: 。实验时冷凝水应从 端进(a或b)。实验中加入的沸石(或碎瓷片) 催化剂(填是或不是)。
14(9分).实验课上,老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种,为确定该粉末的成分,同学们进行了如下探究,请你参与其中并回答问题。
【提出猜想】甲组:铜粉;乙组:氧化铁粉末;丙组: 。
【设计实验】
方案1:取少量红色粉末放入试管中,滴加足量的 (从下列试剂中选择:氯化钠溶液、稀盐酸、氢氧化钠溶液)振荡,若甲组猜想正确,则实验现象为 。
方案2:取10g红色粉末放入硬质玻璃管中,先通入CO,然后用酒精喷灯加热至完全反应,实验装置如图所示,停止加热并继续通入CO至装置冷却。实验过程中将反应后的气体通入虚线框内足量的氢氧化钙溶液中,该装置的作用有检验并吸收生成CO2和 等。
【数据处理】
①若乙组猜想正确,则硬质玻璃管内发生反应的化学方程式是 。
②若丙组猜想正确,等装置完全冷却到室温,重新称量氢氧化钙溶液的总质量增加了6.6g,则该氢氧化钙溶液吸收CO2生成沉淀质量为 ;原红色粉末中氧化铁的质量分数为 。
15(10分).人们生活的方方面面都与化学密切相关。回答下列问题:
(1)下列物品的主要成分属于合成材料的是 (填序号)。
a.纯棉T恤
b.保鲜膜
c.羊毛衫
d.电源插座外壳
(2)米粉的主要成分是淀粉,淀粉属于营养物质中的 ;油汤洒在衣服上,用洗衣液使油污较稳定分散于水中的现象称为 。
(3)建造房屋要使用大量钢材,防止钢材生锈的方法有
(写一种)。
(4)新能源汽车常用锂电池提供动力,Li+的结构示意图,x= 。前18号元素中和Li原子最外层电子数相同的金属元素是 。
(5)无土栽培时可用KNO3和NH4Cl配制营养液。区分KNO3和NH4Cl固体可选用的试剂是 。如图是KNO3和NH4Cl的溶解度曲线。26℃时,饱和NH4Cl溶液的质量分数为 (精确到0.1%);50℃时的两杯相同质量的饱和KNO3溶液和饱和NH4Cl溶液,均降温到26℃,所得两种溶液的质量 (填序号)。
a.KNO3溶液大
b.一样大
c.NH4Cl溶液大
d.无法确定
16(17分).我国高铁建设走在世界前列,修建高铁需要大量铁矿石来炼铁,进而炼钢。
(1)下列三种铁矿石的主要成分Fe2O3、Fe3O4、FeCO3中,含铁量最高的是 。高炉炼铁需要的原料有铁矿石、 、 和石灰石。
(2)要炼出含铁96%的生铁1000t,至少需要含氧化铁80%的赤铁矿多少吨?若高炉气体不加处理,理论上会向大气中排放CO2多少吨?(无计算过程不给分,计算结果保留整数。)
参考答案
一.选择题
1.C; 2.C; 3.C; 4.C; 5.C;
6.B; 7.A; 8.C; 9.D;
二.非选择题
10.Ag;Fe;AgNO3;Fe+2AgNO3=2Ag+Fe(NO3)2;
11.NH4Cl;3:5;KNO3;
12.烧杯;②①⑤③④;加快溶解速率;20;
13.明矾;过滤;漏斗、玻璃棒和烧杯;引流;AC;吸附;硬水;煮沸;化学;冷凝器;b;不是;
14.铜粉、氧化铁粉末的混合物;稀盐酸;固体不溶解;收集CO;Fe2O3+3CO2Fe+3CO2;15g;80%;
15.bd;糖类;乳化现象;刷漆;3;Na;熟石灰粉末;28.6%;c;
16.解: (1)Fe2O3、Fe3O4、 FeCO3的含铁量分别为:
,故含铁量最高的是Fe3O4 ;高炉炼铁需要的原料有铁矿石、焦炭、空气和石灰石,故填: Fe3O4;焦炭;空气;
(2)设至少需要赤铁矿的质量为x,反应产生CO2的质量为y
3CO+Fe2O3 2Fe+ 3CO2
160 112 132
80%x 1000tx96% y
x=1714t , y=1131t
答:至少需要含氧化铁80%的赤铁矿1714t ,理论上会向大气中排放CO21131t.
同课章节目录
