甘肃省武威市民勤县第六中学2021-2022学年九年级下学期开学检测化学试题(word版有答案)
文档属性
| 名称 | 甘肃省武威市民勤县第六中学2021-2022学年九年级下学期开学检测化学试题(word版有答案) |  | |
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-16 21:22:32 | ||
图片预览


文档简介
(
学校
班级
姓名
考场
考号
密
封
线
内
不
要
答
题
)民勤六中2021—2022学年度第二学期开学质量检测试卷
九 年 级 化 学
可能用到的相对原子质量:C-12 H-1 O-16 N-14 Ca-40
一.选择题(每小题只有一个选项符合题意,共40分)
1.下列在厨房中发生的变化是物理变化的是( )
A.榨取果汁 B.冬瓜腐烂 C.铁锅生锈 D.煤气燃烧
2.实验结束后,如图所示仪器的放置方法正确的是( )
3.下列说法不正确的是( )
A.硫在空气中燃烧,产生淡蓝色火焰
B.电解水时,正负两极产生气体的体积比为 1:2
C.红磷在空气中燃烧时产生大量白烟 D.氧气的化学性质比较活泼,具有可燃性
4.物质的性质决定物质的用途,下列物质的用途由其物理性质决定的是( )
A.酒精作燃料 B.铁锅作炊具 C.二氧化碳用于灭火 D.氮气作保护气
5.下列物质中,属于纯净物的是( )
A.白酒 B.加碘盐 C.食用醋 D.干冰
6.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )
A.碘酒 B.食醋 C.生理盐水 D.牛奶
7.下列物质中,由原子直接构成的是( )
A.水 B.二氧化碳 C.氯化钠 D. 水银
8.下列说法正确的是( )
A.水蒸发过程中,水分子、氢原子和氧原子都没变,是物理变化,而分解过氧化氢的过程中过氧化氢分子、氢原子和氧原子都发生了改变,属于化学变化
B.一切物质都由分子构成,分子又由原子构成,所以分子比原子大
C.气球易被压缩是因为分子间有间隔
D.双氧水(H2O2)和水(H2O)都是由氢元素和氧元素组成的,所以它们的化学性质相同
9.我国饮用矿泉水的基本类别是碳酸水、硅酸水和锶水。此外还有锌、锂、溴、碘及硒矿泉水等,这里的锌、锂、溴、碘、硒是指( )
A.原子 B.分子 C.元素 D.单质
(
+2
)10.下列化学用语书写正确的是( )
A.Mg:+2价的镁原子 B.三个二氧化硫分子:3SO2
C.水中氧元素的化合价为-2:H2O2- D.一个钙离子:Ca+2
11.石油除主要含有碳、氢元素外,还含有少量的硫与氦等。下列有关石油的说法不正确的是( )
A.石油是可燃物 B.石油是不可再生能源
C.石油不能充分燃烧会生成一氧化碳、二氧化硫等有害气体
D.油罐起火,消防队员用高压水枪向油罐喷水,是为了降低石油的着火点
12.液化石油气中掺入过多二甲醚(C2H6O)会对液化气罐的配件产生腐蚀,严重会造成爆炸。下列关于二甲醚的说法错误的是( )
A.由C、H、O三种元素组成 B.相对分子质量为46
C.是一种氧化物 D.碳、氢、氧三种元素的质量比为12:3:8
13.在反应3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O中的X的化学式是:( )
A. N2 B. NO C. NO2 D. N2O5
14.以下是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管a进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
15.下列有关二氧化碳的检验、制备和用途能达到目的的是( )
A.干冰用于人工降雨
B.二氧化碳气体通入紫色石蕊试液中,溶液变蓝
C.用块状石灰石和稀硫酸迅速制备大量二氧化碳
D.将燃着的木条伸入集气瓶,火焰立即熄灭,证明瓶内原有气体就是二氧化碳
16.把X、Y、Z三种金属分别加入稀盐酸中,Y表面有气泡产生,X、Z无明显变化;再把X放到Z的硝酸盐溶液中,X的表面有固体析出,则三种金属的活动性顺序是( )
A.Y>X>Z B.Y>Z>X C.X>Z>Y D.Z>X>Y
17.类推是学习化学的一种重要方法。下列类推正确的是( )
A.燃烧过程中伴随着发光发热,所以有发光发热现象的变化都是燃烧
B.置换反应一定有单质生成,有单质生成的反应不一定是置换反应
C.单质中只含有一种元素,则只含有一种元素的物质一定是单质
D.氧化物都含氧元素,所以含氧元素的化合物都是氧化物
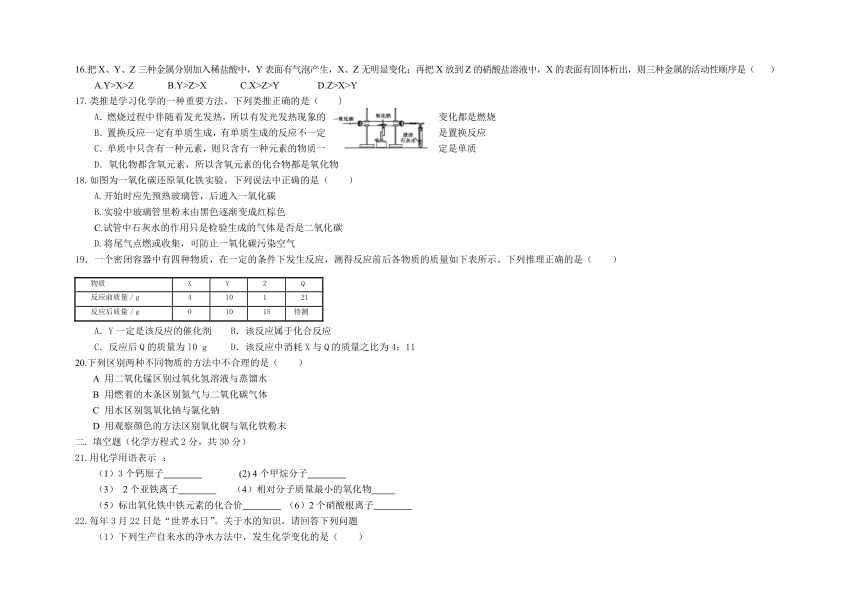
18.如图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
A.开始时应先预热玻璃管,后通入一氧化碳
B.实验中玻璃管里粉末由黑色逐渐变成红棕色
C.试管中石灰水的作用只是检验生成的气体是否是二氧化碳
D.将尾气点燃或收集,可防止一氧化碳污染空气
19.一个密闭容器中有四种物质,在一定的条件下发生反应,测得反应前后各物质的质量如下表所示。下列推理正确的是( )
物质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g O 10 15 待测
A.Y一定是该反应的催化剂 B.该反应属于化合反应
C.反应后Q的质量为l0 g D.该反应中消耗X与Q的质量之比为4:11
20.下列区别两种不同物质的方法中不合理的是( )
A 用二氧化锰区别过氧化氢溶液与蒸馏水
B 用燃着的木条区别氮气与二氧化碳气体
C 用水区别氢氧化钠与氯化钠
D 用观察颜色的方法区别氧化铜与氧化铁粉末
填空题(化学方程式2分,共30分)
21.用化学用语表示 :
(1)3个钙原子 (2) 4个甲烷分子
(3) 2个亚铁离子 (4)相对分子质量最小的氧化物
(5)标出氧化铁中铁元素的化合价 (6)2个硝酸根离子
22.每年3月22日是“世界水日”。关于水的知识,请回答下列问题
(1)下列生产自来水的净水方法中,发生化学变化的是( )
A.沉淀 B.过滤 C.吸附 D.消毒
(2)实验室常用过滤的方法对混浊液体进行提纯,此操作中需要用到的玻璃仪器有:玻璃棒、烧杯、 (填仪器名称);生活中常用 的方法将硬水软化。
(3)有关水的组成和结构的叙述中,正确的是( )
A.水是由水分子构成的 B.水分子的相对分子质量是18g
C.水中氢、氧元素的质量比为 2:1 D.水分子是由氢原子和氧原子构成的
(4)向河水中加明矾和漂白粉净化后,河水可作为生活用水,其中明矾的作用是 ,漂白粉中的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙中氯元素的化合价是 。
(5)“节约用水,从我做起。”请你任举一例生活中节约用水的措施:
。
23.现代社会对能源的需求量越来越大,能源的开发和利用倍受人类关注.
(1)化石燃料包括煤、 和天然气.化石燃料燃烧排放的气体会污染环境,其中含有形成酸雨的主要气体,其化学式为 .
(2)化石燃料不可再生,开发和利用新能源迫在眉睫,氢能作为理想的能源,重要原因是它的燃烧产物无污染,用化学反应方程式表示为 .
24.铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀。
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
(3)用下列试剂验证这三种金属的活动性顺序,能达到目的的是 (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
25.长期存放石灰水的试剂瓶内壁常附有一层白色物质,请用化学方程式表示其形成原因: :不能用铁制容器配制波尔多液(含有硫酸铜)的原因 (用化学方程式表示)
26.已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如下图所示。
(
E
↓
) (
C
) (
A
) (
+澄清石灰水
②
)
(
高温
①
)
(
D
) (
B
)
请回答:(1)C的化学式为 ;D的化学式为 。[来
(2)A中金属元素的化合价是 ,
(3)反应①的化学方程式为 ;该反应的基本类型是 。
三.实验题(化学方程式2分,共22分)
27.(1)用于夹持试管的仪器是 ;(2)取用粉末状药品时一般选用
(3)用于吸取和滴加少量液体的是 ;
(4)常用于给物质加热的仪器是 ;
28.根据下列实验装置图,按要求回答下列问题:
实验室制取CO2的化学方程式为 ;制取并收集该气体应选择的装置是 (填序号);若想控制反应速率,可以将仪器②用
代替;检验该气体的方法是 ;
(2)如果选择与制取CO2相同的发生装置来制取O2,则发生反应的化学方程式为 ,如果要制得较纯净的氧气应该选择装置_____收集,如用E收集O2,如何验满: 。
29.小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动:【出处:】
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液……【铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
【预测】三种金属在金属活动性顺序表中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
实验一 实验二 实验三
实验 方
实验 现象 铬片表面产生气泡缓慢,溶液变蓝色 ____________ 铝片表面产生气泡较快
结论 铬能与稀硫酸发生反应,反应较慢 铜不与稀硫酸反应 ____________[来源:]
三种金属在金属活动性顺序表中的相对位置关系是_________(填序号)
【回答问题】(1)用砂纸打磨金属片的目的是____________。
(2)实验一所发生反应的化学方程式是____________________________。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序表中的相对位置关系,小燕认为不可行,理由是_______________________。2【归纳】比较金属活动性强弱的方法有①________ __________________;②________________________________。
四.计算题(共8分)
30、“珍爱生命,拒绝毒品”是每个公民的社会责任。但在某些娱乐场所,还有人服用俗称“摇头丸”的毒品,该毒品能使人手舞足蹈,呈癫狂状态,严重危害人的身心健康和社会稳定。有一种“摇头丸”的化学式为 C12HxO2N,测得其相对分子质量为209。试回答下列问题:
(1)该物质的一个分子中,氢原子个数 x= 。氮元素的质量分数为 (结果保留到 0.1%)
(2)该物质中,碳元素与氧元素的质量之比为 (最简整数比)。
(3)燃烧该物质,下列物质中不可能产生的是 (填序号)。
①CO ②H2O ③NO ④CO2 ⑤SO2
反应前 反应后
实验 数据 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯和其中混合物的质量
100.0 g 12.0 g 107.6 g
31.石灰石是重要的建筑材料,小江同学为了测定石灰石中碳酸钙的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。(假设石灰石样品中的杂质不与盐酸反应也不溶于水)
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是 克。
(2)该样品中碳酸钙的质量分数是多少?
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
A D D B D D D C C B D C B A A A B D B D
21.(1)2Ca; (2)4CH4; (3)2Fe2+; (4)H2O (5)Fe2O3 (6) 2NO3-
22.(1)D;(2)漏斗 煮沸;(3)A D(4)吸附水中悬浮物质,使其沉淀 +1
(5)用淘米水浇花等
23.(1)石油 SO2;(2)2H2 + O2=2H2O
24.(1)铝 (2)大 (3)B
25.(1)Ca(OH)2+CO2 =CaCO3 +H2O;(2)Fe+CuSO4==Cu+FeSO4
26.(1)CO2 Cu (2)+2 (3) C+2 CuO== 2Cu+ CO2 置换反应
27.(1)试管夹 (2)药匙 (3)胶头滴管 (4)酒精灯
28.(1)CaCO3 +2HCl==CaCl2 =H2O +CO2 BE 分液漏斗
将气体通入澄清的石灰水中
(2)2H2O2== 2H2O +O2 C 将带火星的木条放到集气瓶口,如木条复燃,说明氧气已满
29.(1)铜片表面无变化 铝能与稀硫酸发生反应,反应较快 ②②②②②
(1)除去金属表面的氧化物 (2)Cr +H2SO4 =CrSO4 +H2
(3)无法判断铬和铝的活动性强弱 可根据金属能否与酸反应及反应的快慢判断
可根据金属能否与盐溶液反应判断
(1)19 6.7%; (2)9:2 (3)⑤ ;
29.生成二氧化碳的质量为12g+100g-107.6g=4.4g;
设样品中碳酸钙的质量为x,则
CaCO3 +2HCl==CaCl2 =H2O +CO2
100 44
X 4.4g
解得x=10g;
该石灰石样品中CaCO3的质量分数(10/12)×100%=83.3%;
学校
班级
姓名
考场
考号
密
封
线
内
不
要
答
题
)民勤六中2021—2022学年度第二学期开学质量检测试卷
九 年 级 化 学
可能用到的相对原子质量:C-12 H-1 O-16 N-14 Ca-40
一.选择题(每小题只有一个选项符合题意,共40分)
1.下列在厨房中发生的变化是物理变化的是( )
A.榨取果汁 B.冬瓜腐烂 C.铁锅生锈 D.煤气燃烧
2.实验结束后,如图所示仪器的放置方法正确的是( )
3.下列说法不正确的是( )
A.硫在空气中燃烧,产生淡蓝色火焰
B.电解水时,正负两极产生气体的体积比为 1:2
C.红磷在空气中燃烧时产生大量白烟 D.氧气的化学性质比较活泼,具有可燃性
4.物质的性质决定物质的用途,下列物质的用途由其物理性质决定的是( )
A.酒精作燃料 B.铁锅作炊具 C.二氧化碳用于灭火 D.氮气作保护气
5.下列物质中,属于纯净物的是( )
A.白酒 B.加碘盐 C.食用醋 D.干冰
6.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )
A.碘酒 B.食醋 C.生理盐水 D.牛奶
7.下列物质中,由原子直接构成的是( )
A.水 B.二氧化碳 C.氯化钠 D. 水银
8.下列说法正确的是( )
A.水蒸发过程中,水分子、氢原子和氧原子都没变,是物理变化,而分解过氧化氢的过程中过氧化氢分子、氢原子和氧原子都发生了改变,属于化学变化
B.一切物质都由分子构成,分子又由原子构成,所以分子比原子大
C.气球易被压缩是因为分子间有间隔
D.双氧水(H2O2)和水(H2O)都是由氢元素和氧元素组成的,所以它们的化学性质相同
9.我国饮用矿泉水的基本类别是碳酸水、硅酸水和锶水。此外还有锌、锂、溴、碘及硒矿泉水等,这里的锌、锂、溴、碘、硒是指( )
A.原子 B.分子 C.元素 D.单质
(
+2
)10.下列化学用语书写正确的是( )
A.Mg:+2价的镁原子 B.三个二氧化硫分子:3SO2
C.水中氧元素的化合价为-2:H2O2- D.一个钙离子:Ca+2
11.石油除主要含有碳、氢元素外,还含有少量的硫与氦等。下列有关石油的说法不正确的是( )
A.石油是可燃物 B.石油是不可再生能源
C.石油不能充分燃烧会生成一氧化碳、二氧化硫等有害气体
D.油罐起火,消防队员用高压水枪向油罐喷水,是为了降低石油的着火点
12.液化石油气中掺入过多二甲醚(C2H6O)会对液化气罐的配件产生腐蚀,严重会造成爆炸。下列关于二甲醚的说法错误的是( )
A.由C、H、O三种元素组成 B.相对分子质量为46
C.是一种氧化物 D.碳、氢、氧三种元素的质量比为12:3:8
13.在反应3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O中的X的化学式是:( )
A. N2 B. NO C. NO2 D. N2O5
14.以下是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管a进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
15.下列有关二氧化碳的检验、制备和用途能达到目的的是( )
A.干冰用于人工降雨
B.二氧化碳气体通入紫色石蕊试液中,溶液变蓝
C.用块状石灰石和稀硫酸迅速制备大量二氧化碳
D.将燃着的木条伸入集气瓶,火焰立即熄灭,证明瓶内原有气体就是二氧化碳
16.把X、Y、Z三种金属分别加入稀盐酸中,Y表面有气泡产生,X、Z无明显变化;再把X放到Z的硝酸盐溶液中,X的表面有固体析出,则三种金属的活动性顺序是( )
A.Y>X>Z B.Y>Z>X C.X>Z>Y D.Z>X>Y
17.类推是学习化学的一种重要方法。下列类推正确的是( )
A.燃烧过程中伴随着发光发热,所以有发光发热现象的变化都是燃烧
B.置换反应一定有单质生成,有单质生成的反应不一定是置换反应
C.单质中只含有一种元素,则只含有一种元素的物质一定是单质
D.氧化物都含氧元素,所以含氧元素的化合物都是氧化物
18.如图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
A.开始时应先预热玻璃管,后通入一氧化碳
B.实验中玻璃管里粉末由黑色逐渐变成红棕色
C.试管中石灰水的作用只是检验生成的气体是否是二氧化碳
D.将尾气点燃或收集,可防止一氧化碳污染空气
19.一个密闭容器中有四种物质,在一定的条件下发生反应,测得反应前后各物质的质量如下表所示。下列推理正确的是( )
物质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g O 10 15 待测
A.Y一定是该反应的催化剂 B.该反应属于化合反应
C.反应后Q的质量为l0 g D.该反应中消耗X与Q的质量之比为4:11
20.下列区别两种不同物质的方法中不合理的是( )
A 用二氧化锰区别过氧化氢溶液与蒸馏水
B 用燃着的木条区别氮气与二氧化碳气体
C 用水区别氢氧化钠与氯化钠
D 用观察颜色的方法区别氧化铜与氧化铁粉末
填空题(化学方程式2分,共30分)
21.用化学用语表示 :
(1)3个钙原子 (2) 4个甲烷分子
(3) 2个亚铁离子 (4)相对分子质量最小的氧化物
(5)标出氧化铁中铁元素的化合价 (6)2个硝酸根离子
22.每年3月22日是“世界水日”。关于水的知识,请回答下列问题
(1)下列生产自来水的净水方法中,发生化学变化的是( )
A.沉淀 B.过滤 C.吸附 D.消毒
(2)实验室常用过滤的方法对混浊液体进行提纯,此操作中需要用到的玻璃仪器有:玻璃棒、烧杯、 (填仪器名称);生活中常用 的方法将硬水软化。
(3)有关水的组成和结构的叙述中,正确的是( )
A.水是由水分子构成的 B.水分子的相对分子质量是18g
C.水中氢、氧元素的质量比为 2:1 D.水分子是由氢原子和氧原子构成的
(4)向河水中加明矾和漂白粉净化后,河水可作为生活用水,其中明矾的作用是 ,漂白粉中的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙中氯元素的化合价是 。
(5)“节约用水,从我做起。”请你任举一例生活中节约用水的措施:
。
23.现代社会对能源的需求量越来越大,能源的开发和利用倍受人类关注.
(1)化石燃料包括煤、 和天然气.化石燃料燃烧排放的气体会污染环境,其中含有形成酸雨的主要气体,其化学式为 .
(2)化石燃料不可再生,开发和利用新能源迫在眉睫,氢能作为理想的能源,重要原因是它的燃烧产物无污染,用化学反应方程式表示为 .
24.铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀。
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
(3)用下列试剂验证这三种金属的活动性顺序,能达到目的的是 (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
25.长期存放石灰水的试剂瓶内壁常附有一层白色物质,请用化学方程式表示其形成原因: :不能用铁制容器配制波尔多液(含有硫酸铜)的原因 (用化学方程式表示)
26.已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如下图所示。
(
E
↓
) (
C
) (
A
) (
+澄清石灰水
②
)
(
高温
①
)
(
D
) (
B
)
请回答:(1)C的化学式为 ;D的化学式为 。[来
(2)A中金属元素的化合价是 ,
(3)反应①的化学方程式为 ;该反应的基本类型是 。
三.实验题(化学方程式2分,共22分)
27.(1)用于夹持试管的仪器是 ;(2)取用粉末状药品时一般选用
(3)用于吸取和滴加少量液体的是 ;
(4)常用于给物质加热的仪器是 ;
28.根据下列实验装置图,按要求回答下列问题:
实验室制取CO2的化学方程式为 ;制取并收集该气体应选择的装置是 (填序号);若想控制反应速率,可以将仪器②用
代替;检验该气体的方法是 ;
(2)如果选择与制取CO2相同的发生装置来制取O2,则发生反应的化学方程式为 ,如果要制得较纯净的氧气应该选择装置_____收集,如用E收集O2,如何验满: 。
29.小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动:【出处:】
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液……【铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
【预测】三种金属在金属活动性顺序表中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
实验一 实验二 实验三
实验 方
实验 现象 铬片表面产生气泡缓慢,溶液变蓝色 ____________ 铝片表面产生气泡较快
结论 铬能与稀硫酸发生反应,反应较慢 铜不与稀硫酸反应 ____________[来源:]
三种金属在金属活动性顺序表中的相对位置关系是_________(填序号)
【回答问题】(1)用砂纸打磨金属片的目的是____________。
(2)实验一所发生反应的化学方程式是____________________________。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序表中的相对位置关系,小燕认为不可行,理由是_______________________。2【归纳】比较金属活动性强弱的方法有①________ __________________;②________________________________。
四.计算题(共8分)
30、“珍爱生命,拒绝毒品”是每个公民的社会责任。但在某些娱乐场所,还有人服用俗称“摇头丸”的毒品,该毒品能使人手舞足蹈,呈癫狂状态,严重危害人的身心健康和社会稳定。有一种“摇头丸”的化学式为 C12HxO2N,测得其相对分子质量为209。试回答下列问题:
(1)该物质的一个分子中,氢原子个数 x= 。氮元素的质量分数为 (结果保留到 0.1%)
(2)该物质中,碳元素与氧元素的质量之比为 (最简整数比)。
(3)燃烧该物质,下列物质中不可能产生的是 (填序号)。
①CO ②H2O ③NO ④CO2 ⑤SO2
反应前 反应后
实验 数据 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯和其中混合物的质量
100.0 g 12.0 g 107.6 g
31.石灰石是重要的建筑材料,小江同学为了测定石灰石中碳酸钙的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。(假设石灰石样品中的杂质不与盐酸反应也不溶于水)
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是 克。
(2)该样品中碳酸钙的质量分数是多少?
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
A D D B D D D C C B D C B A A A B D B D
21.(1)2Ca; (2)4CH4; (3)2Fe2+; (4)H2O (5)Fe2O3 (6) 2NO3-
22.(1)D;(2)漏斗 煮沸;(3)A D(4)吸附水中悬浮物质,使其沉淀 +1
(5)用淘米水浇花等
23.(1)石油 SO2;(2)2H2 + O2=2H2O
24.(1)铝 (2)大 (3)B
25.(1)Ca(OH)2+CO2 =CaCO3 +H2O;(2)Fe+CuSO4==Cu+FeSO4
26.(1)CO2 Cu (2)+2 (3) C+2 CuO== 2Cu+ CO2 置换反应
27.(1)试管夹 (2)药匙 (3)胶头滴管 (4)酒精灯
28.(1)CaCO3 +2HCl==CaCl2 =H2O +CO2 BE 分液漏斗
将气体通入澄清的石灰水中
(2)2H2O2== 2H2O +O2 C 将带火星的木条放到集气瓶口,如木条复燃,说明氧气已满
29.(1)铜片表面无变化 铝能与稀硫酸发生反应,反应较快 ②②②②②
(1)除去金属表面的氧化物 (2)Cr +H2SO4 =CrSO4 +H2
(3)无法判断铬和铝的活动性强弱 可根据金属能否与酸反应及反应的快慢判断
可根据金属能否与盐溶液反应判断
(1)19 6.7%; (2)9:2 (3)⑤ ;
29.生成二氧化碳的质量为12g+100g-107.6g=4.4g;
设样品中碳酸钙的质量为x,则
CaCO3 +2HCl==CaCl2 =H2O +CO2
100 44
X 4.4g
解得x=10g;
该石灰石样品中CaCO3的质量分数(10/12)×100%=83.3%;
同课章节目录
