沪教版(全国)化学九年级上册阶段专题训练(二) 分子、原子、离子(word版有答案)
文档属性
| 名称 | 沪教版(全国)化学九年级上册阶段专题训练(二) 分子、原子、离子(word版有答案) |  | |
| 格式 | docx | ||
| 文件大小 | 319.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-26 07:19:51 | ||
图片预览


文档简介
专题训练(二) 分子、原子、离子
一、选择题
1.下列物质由分子构成的是 ( )
A.氢气 B.水银
C.氯化钠 D.金属镁
2.[2020·郴州] 下列现象从分子的角度加以解释,其中错误的是 ( )
A.墙内开花墙外可闻到香味是因为分子在不断运动
B.固体难压缩是因为分子间的间隔很小
C.气体受热膨胀是因为分子间的间隔增大
D.二氧化碳能溶解在水中是因为分子很小
3.我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的微粒是 ( )
A.分子 B.原子
C.离子 D.中子
4.[2020·聊城] 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是 ( )
A.分子由原子构成,分子比原子大
B.水遇冷凝结成冰,水分子停止了运动
C.原子是最小的粒子,不可再分
D.氯化钠是由钠离子和氯离子构成的
5.[2020·株洲] 下列微观示意图中,黑球代表氢原子,白球代表氯原子,其中代表混合物的是 ( )
6.19世纪初阿伏伽德罗提出了分子的概念,他认为:①一切物质都是由分子构成的;②分子是由原子构成的;③原子不能构成物质;④分子的质量等于构成它的原子的质量之和。从所学知识看,上述观点中存在明显不足的是( )
A.①③ B.①②
C.③④ D.②③④
7.示结构示意图中表示阳离子的是( )
8.下列对分子、原子、离子的认识正确的是 ( )
A.同种分子排列方式不同,化学性质不同
B.在干冰中,分子因相互作用而静止不动
C.同种原子按不同方式结合,可以构成不同的物质
D.原子得失电子形成离子后,原子核发生了变化
9.一个碳12原子的质量为m kg,一个A原子的质量为a kg,则它的相对原子质量为( )
A. B.
C. D.
10.小明从示某粒子结构示意图中,获取了下列信息,其中错误的是 ( )
A.表示阴离子 B.核电荷数为12
C.有两个电子层 D. 表示相对稳定结构
11.下列关于Mg、Mg2+两种微粒的判断中,不正确的是 ( )
A.核电荷数相同 B.质量几乎相等
C.Mg2+比Mg稳定 D.电子层数相同
12.电解水的过程可用示,粒子运动变化的先后顺序是 ( )
A.①②③④ B.①②④③
C.④③①② D.④①②③
二、填空题
13.在初中化学学习中,我们初步认识了物质的微观结构。
(1)在铜、二氧化碳这两种物质中,由原子直接构成的物质是 , 由分子直接构成的物质是 。
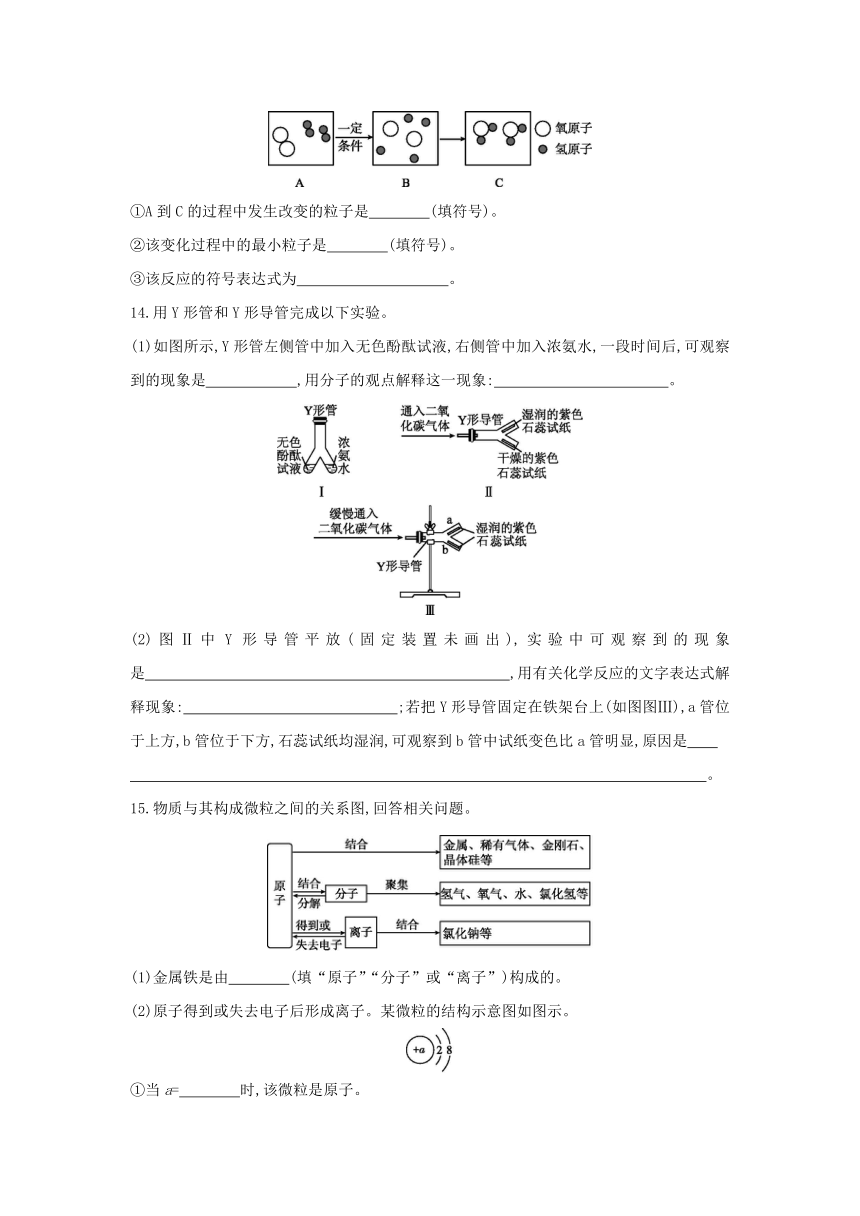
(2)如图示是某化学反应的微观模拟图,根据图示回答下列问题。
①A到C的过程中发生改变的粒子是 (填符号)。
②该变化过程中的最小粒子是 (填符号)。
③该反应的符号表达式为 。
14.用Y形管和Y形导管完成以下实验。
(1)如图所示,Y形管左侧管中加入无色酚酞试液,右侧管中加入浓氨水,一段时间后,可观察到的现象是 ,用分子的观点解释这一现象: 。
(2)图Ⅱ中Y形导管平放(固定装置未画出),实验中可观察到的现象是 ,用有关化学反应的文字表达式解释现象: ;若把Y形导管固定在铁架台上(如图图Ⅲ),a管位于上方,b管位于下方,石蕊试纸均湿润,可观察到b管中试纸变色比a管明显,原因是
。
15.物质与其构成微粒之间的关系图,回答相关问题。
(1)金属铁是由 (填“原子”“分子”或“离子”)构成的。
(2)原子得到或失去电子后形成离子。某微粒的结构示意图如图示。
①当a= 时,该微粒是原子。
②当a=8时,该微粒是 (填“原子”“阳离子”或“阴离子”),其符号为 。
16.模型是联系宏观与微观的桥梁。
(1)钠原子的结构示意图。
①x的数值为 。
②“11”指的是 。
③钠原子在化学反应中易失去一个电子形成 (填离子符号)。
(2)是氢分子和氧分子运动的示意图。
①在A、B、C中,能比较得出“温度越高,分子运动速率越快”的是 (填字母)。
②从图中可知,影响分子运动速率的因素除温度外,还有 。
③举一个能说明“温度升高,分子运动速率加快”的生活事例: 。
17.氯化钠和醋酸(CH3COOH)是厨房中常见的调味品,回答下列问题。
(1)构成氯化钠的微粒是 (填符号)。
(2)氯化钠的相对分子质量为 。
(3)醋酸的相对分子质量为 。
答案
1.A
2.D 墙内开花墙外可闻到香味,说明分子在不断运动,使人们闻到花香;固体难压缩,说明固体分子间的间隔很小;气体受热膨胀,是因为受热使分子间的间隔增大;二氧化碳能溶解在水中,说明分子在不断运动且分子之间有间隔。
3.B 碳化硅的结构类似于金刚石的结构,金刚石是由原子构成的,所以构成碳化硅的微粒是原子。
4.D 原子构成的分子,其分子比构成它的原子大,如图果分子中不含该原子,则分子不一定比该原子大;分子在不断运动,水结成冰,水分子仍在运动;原子是化学变化中的最小粒子,但结构上原子仍然可以分;氯化钠是由钠离子与氯离子构成的。
5.D A、B、C中均只有一种分子,属于纯净物;D中有三种分子,属于混合物。
6.A 分子、原子、离子均可直接构成物质。
7.B 8.C
9.C 相对原子质量是某原子的实际质量与一个碳12原子质量的的比值。
10.A 该粒子的质子数>核外电子数,属于阳离子。
11.D Mg和Mg2+是同种元素形成的不同微粒,质子数相同,质子数=核电荷数,则核电荷数也相同;镁原子失去电子形成镁离子,电子的质量很小,通常忽略不计,故两者质量几乎相等;镁离子是相对稳定结构,镁原子易失去电子,不稳定;镁原子失去最外层电子形成镁离子,故二者的电子层数不同。
12.C 在化学变化过程(有分子参与和生成)中,分子分裂成原子,原子重组组合成新的分子。
13. (1)铜 二氧化碳
(2)①H2、O2 ②H、O
③H2+O2H2O
(2)①在化学变化中,分子种类发生改变,故A到C的过程中发生改变的粒子是氢分子和氧分子,符号分别为H2、O2;②原子在化学变化中不发生改变,该变化过程中的最小粒子是氧原子和氢原子,符号分别为O、H;③由化学反应的微观模拟图可知,该反应是氢气和氧气在一定条件下反应生成水,符号表达式为H2+O2H2O。
14.(1)无色酚酞试液变红 分子在不断运动
(2)湿润的紫色石蕊试纸变红,干燥的紫色石蕊试纸无明显变化 水+二氧化碳碳酸 二氧化碳的密度比空气的密度大,二氧化碳主要从b管中通过
15.(1)原子
(2)①10 ②阴离子 O2-
16.(1)①8
②钠原子的核电荷数为11(合理即可)
③Na+
(2)①BC ②分子种类
③湿衣服在阳光下比在阴凉处干得快(合理即可)
17.(1)Na+、Cl- (2)58.5 (3)60
一、选择题
1.下列物质由分子构成的是 ( )
A.氢气 B.水银
C.氯化钠 D.金属镁
2.[2020·郴州] 下列现象从分子的角度加以解释,其中错误的是 ( )
A.墙内开花墙外可闻到香味是因为分子在不断运动
B.固体难压缩是因为分子间的间隔很小
C.气体受热膨胀是因为分子间的间隔增大
D.二氧化碳能溶解在水中是因为分子很小
3.我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的微粒是 ( )
A.分子 B.原子
C.离子 D.中子
4.[2020·聊城] 分子、原子和离子都是构成物质的基本粒子,下列说法正确的是 ( )
A.分子由原子构成,分子比原子大
B.水遇冷凝结成冰,水分子停止了运动
C.原子是最小的粒子,不可再分
D.氯化钠是由钠离子和氯离子构成的
5.[2020·株洲] 下列微观示意图中,黑球代表氢原子,白球代表氯原子,其中代表混合物的是 ( )
6.19世纪初阿伏伽德罗提出了分子的概念,他认为:①一切物质都是由分子构成的;②分子是由原子构成的;③原子不能构成物质;④分子的质量等于构成它的原子的质量之和。从所学知识看,上述观点中存在明显不足的是( )
A.①③ B.①②
C.③④ D.②③④
7.示结构示意图中表示阳离子的是( )
8.下列对分子、原子、离子的认识正确的是 ( )
A.同种分子排列方式不同,化学性质不同
B.在干冰中,分子因相互作用而静止不动
C.同种原子按不同方式结合,可以构成不同的物质
D.原子得失电子形成离子后,原子核发生了变化
9.一个碳12原子的质量为m kg,一个A原子的质量为a kg,则它的相对原子质量为( )
A. B.
C. D.
10.小明从示某粒子结构示意图中,获取了下列信息,其中错误的是 ( )
A.表示阴离子 B.核电荷数为12
C.有两个电子层 D. 表示相对稳定结构
11.下列关于Mg、Mg2+两种微粒的判断中,不正确的是 ( )
A.核电荷数相同 B.质量几乎相等
C.Mg2+比Mg稳定 D.电子层数相同
12.电解水的过程可用示,粒子运动变化的先后顺序是 ( )
A.①②③④ B.①②④③
C.④③①② D.④①②③
二、填空题
13.在初中化学学习中,我们初步认识了物质的微观结构。
(1)在铜、二氧化碳这两种物质中,由原子直接构成的物质是 , 由分子直接构成的物质是 。
(2)如图示是某化学反应的微观模拟图,根据图示回答下列问题。
①A到C的过程中发生改变的粒子是 (填符号)。
②该变化过程中的最小粒子是 (填符号)。
③该反应的符号表达式为 。
14.用Y形管和Y形导管完成以下实验。
(1)如图所示,Y形管左侧管中加入无色酚酞试液,右侧管中加入浓氨水,一段时间后,可观察到的现象是 ,用分子的观点解释这一现象: 。
(2)图Ⅱ中Y形导管平放(固定装置未画出),实验中可观察到的现象是 ,用有关化学反应的文字表达式解释现象: ;若把Y形导管固定在铁架台上(如图图Ⅲ),a管位于上方,b管位于下方,石蕊试纸均湿润,可观察到b管中试纸变色比a管明显,原因是
。
15.物质与其构成微粒之间的关系图,回答相关问题。
(1)金属铁是由 (填“原子”“分子”或“离子”)构成的。
(2)原子得到或失去电子后形成离子。某微粒的结构示意图如图示。
①当a= 时,该微粒是原子。
②当a=8时,该微粒是 (填“原子”“阳离子”或“阴离子”),其符号为 。
16.模型是联系宏观与微观的桥梁。
(1)钠原子的结构示意图。
①x的数值为 。
②“11”指的是 。
③钠原子在化学反应中易失去一个电子形成 (填离子符号)。
(2)是氢分子和氧分子运动的示意图。
①在A、B、C中,能比较得出“温度越高,分子运动速率越快”的是 (填字母)。
②从图中可知,影响分子运动速率的因素除温度外,还有 。
③举一个能说明“温度升高,分子运动速率加快”的生活事例: 。
17.氯化钠和醋酸(CH3COOH)是厨房中常见的调味品,回答下列问题。
(1)构成氯化钠的微粒是 (填符号)。
(2)氯化钠的相对分子质量为 。
(3)醋酸的相对分子质量为 。
答案
1.A
2.D 墙内开花墙外可闻到香味,说明分子在不断运动,使人们闻到花香;固体难压缩,说明固体分子间的间隔很小;气体受热膨胀,是因为受热使分子间的间隔增大;二氧化碳能溶解在水中,说明分子在不断运动且分子之间有间隔。
3.B 碳化硅的结构类似于金刚石的结构,金刚石是由原子构成的,所以构成碳化硅的微粒是原子。
4.D 原子构成的分子,其分子比构成它的原子大,如图果分子中不含该原子,则分子不一定比该原子大;分子在不断运动,水结成冰,水分子仍在运动;原子是化学变化中的最小粒子,但结构上原子仍然可以分;氯化钠是由钠离子与氯离子构成的。
5.D A、B、C中均只有一种分子,属于纯净物;D中有三种分子,属于混合物。
6.A 分子、原子、离子均可直接构成物质。
7.B 8.C
9.C 相对原子质量是某原子的实际质量与一个碳12原子质量的的比值。
10.A 该粒子的质子数>核外电子数,属于阳离子。
11.D Mg和Mg2+是同种元素形成的不同微粒,质子数相同,质子数=核电荷数,则核电荷数也相同;镁原子失去电子形成镁离子,电子的质量很小,通常忽略不计,故两者质量几乎相等;镁离子是相对稳定结构,镁原子易失去电子,不稳定;镁原子失去最外层电子形成镁离子,故二者的电子层数不同。
12.C 在化学变化过程(有分子参与和生成)中,分子分裂成原子,原子重组组合成新的分子。
13. (1)铜 二氧化碳
(2)①H2、O2 ②H、O
③H2+O2H2O
(2)①在化学变化中,分子种类发生改变,故A到C的过程中发生改变的粒子是氢分子和氧分子,符号分别为H2、O2;②原子在化学变化中不发生改变,该变化过程中的最小粒子是氧原子和氢原子,符号分别为O、H;③由化学反应的微观模拟图可知,该反应是氢气和氧气在一定条件下反应生成水,符号表达式为H2+O2H2O。
14.(1)无色酚酞试液变红 分子在不断运动
(2)湿润的紫色石蕊试纸变红,干燥的紫色石蕊试纸无明显变化 水+二氧化碳碳酸 二氧化碳的密度比空气的密度大,二氧化碳主要从b管中通过
15.(1)原子
(2)①10 ②阴离子 O2-
16.(1)①8
②钠原子的核电荷数为11(合理即可)
③Na+
(2)①BC ②分子种类
③湿衣服在阳光下比在阴凉处干得快(合理即可)
17.(1)Na+、Cl- (2)58.5 (3)60
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
