【名师新编,备战2014高中学业水平考试】2013-2014高中化学名师专题指导(学业考纲+考点整合+水平达标):第三讲 物质的组成、性质与分类(51张ppt)
文档属性
| 名称 | 【名师新编,备战2014高中学业水平考试】2013-2014高中化学名师专题指导(学业考纲+考点整合+水平达标):第三讲 物质的组成、性质与分类(51张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 698.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-02-15 08:22:03 | ||
图片预览









文档简介
课件51张PPT。第三讲 物质的组成、性质与分类物质的组成与分类?知识回顾
一、物质的组成
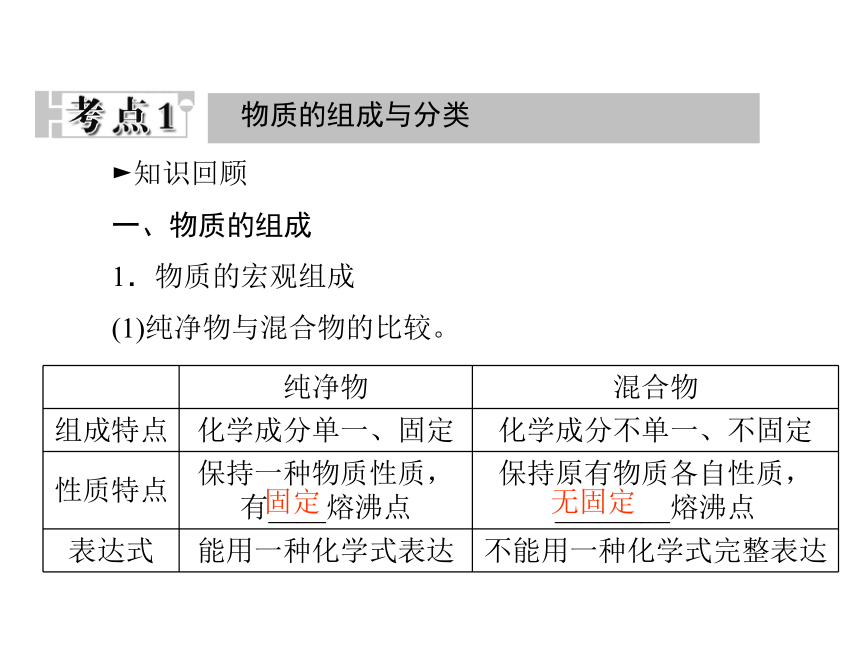
1.物质的宏观组成
(1)纯净物与混合物的比较。固定无固定(2)单质:由________元素组成的________。金属单质在常温下除________为液态外,其余呈固态,非金属单质在常温下除________为液态外,其余呈气态或固态。
(3)化合物:指由两种或两种以________元素组成的________。含碳化合物中个别物质如:CO、CO2、H2CO3、碳酸盐等,具有________特性列入无机物范畴外,其余的__________一般列入有机物范畴。同种纯净物HgBr2上 纯净物无机物含碳化合物2.物质的微观组成
(1)分子是保持物质________的一种微粒。如:H2、He、CO2、HNO3。
(2)原子是化学变化中的________微粒。如:Fe、S、Ne。
(3)离子是带电的原子或________。如:
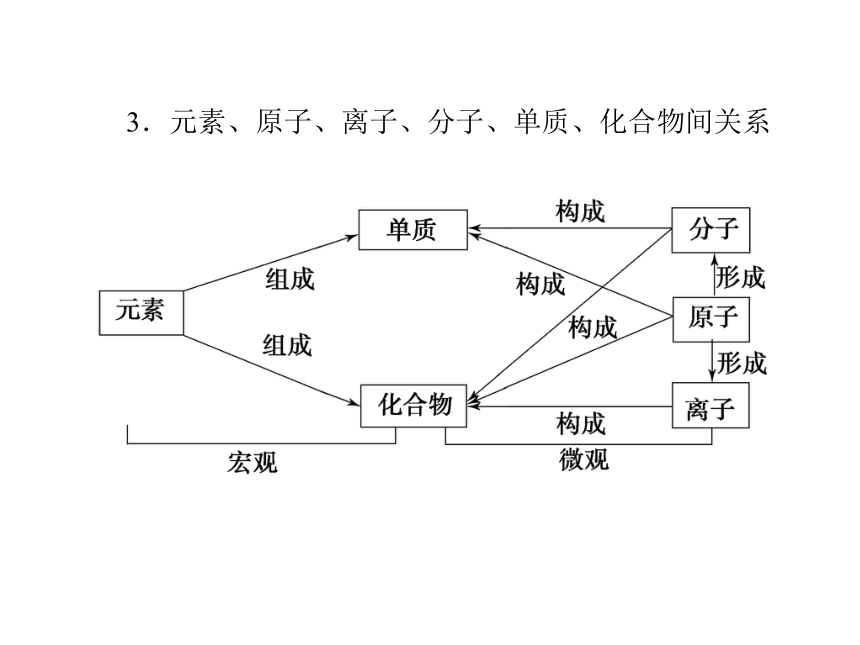
(4)基团是不带电的原子或________。如:甲基—CH3、羟基—OH、羧基—COOH。化学性质最小原子团原子团3.元素、原子、离子、分子、单质、化合物间关系二、物质的分类
1.分类方法
(1)物质的树状分类:对同一类物质再分类。如:对Na2SO4进行树状分类可分为______、________、________、正盐等。
(2)物质的交叉分类:对同一种物质进行交叉分类。如:对Na2SO4进行交叉分类,按阳离子属于________、按阴离子属于________、________。纯净物无机物盐钠盐硫酸盐含氧酸盐2.物质分类的一般标准
(1)根据物质是否由同种微粒组成分为________和________。
(2)纯净物根据元素组成分为________(游离态)和________(化合态)。
(3)根据化合物的性质分为________、________、________、________、氢化物等。
(4)根据分散质颗粒大小可将分散系分为______、________、________、________等。纯净物混合物单质化合物酸碱盐氧化物悬浊液乳浊液胶体溶液 (5)依据化学键类型将化合物分为________化合物、________化合物。
(6)根据化合物在水溶液中或熔化状态下是否导电可分为________和________。
(7)依据在氧化还原反应中元素化合价的变化分为________、________。
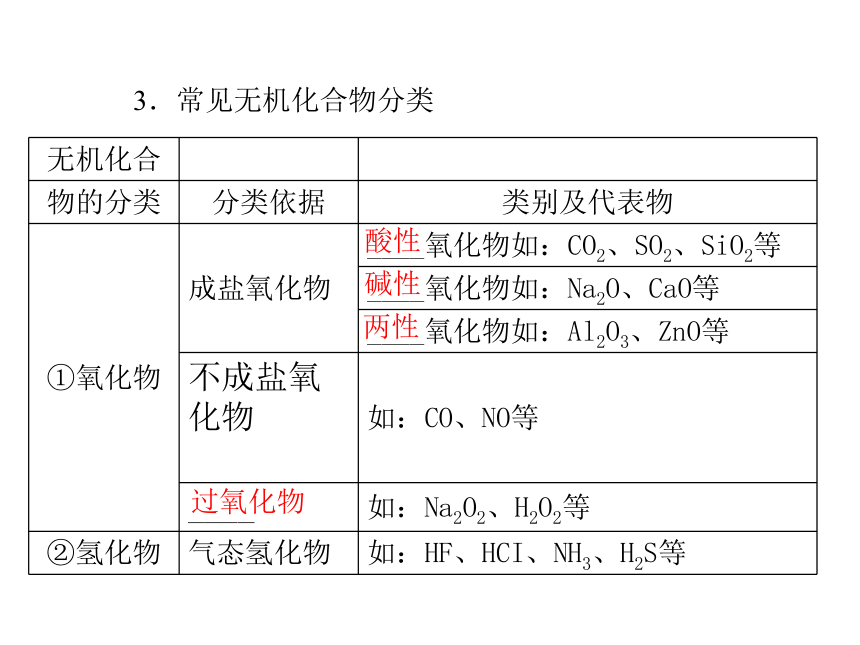
离子共价电解质非电解质氧化剂还原剂3.常见无机化合物分类酸性碱性两性过氧化物强弱强易难HNO3H2SO4HNO3H2SO4 含氧可溶性难溶性强弱正盐酸式盐碱式盐【例1】 (2012年广东学业水平考试)分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A.K2CO3和K2O都属于盐
B.H2SO4和HNO3都属于酸
C.KOH和Na2CO3都属于碱
D.Na2O和Na2SiO3都属于氧化物解析:K2CO3、Na2CO3、Na2SiO3是盐,K2O、Na2O是氧化物,H2SO4和HNO3是酸。
答案:B注:该题在2010年广东学业考试11题、2011广东学业22题水平考试均重复出现。
易错提醒:1.普通玻璃、合金、天然矿物原料、高分子聚合物、熔化后的结晶水合物、半导体元件材料、同素异形体的混合物不是纯净物。石英材料、结晶水合物是纯净物。
2.具有特殊化学性质的部分原子或原子团,不带电荷的称作基,带电荷的称作根(或离子)。
3.酸式盐:酸中的部分氢被中和的产物。如NaHCO3等。
4.碱式盐:碱中的OH-部分被中和的产物。如Cu2(OH)2CO3等。?课堂练习
1.(2011年广东学业水平考试)下列物质属于单质的是( )
A.石墨 B.硫铁矿
C.青铜 D.碳素墨水解析:石墨属于单质,硫铁矿、青铜、碳素墨水属于混合物。
答案:A2.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A.Na2CO3和Na2S都属于盐
B.H2SO4和NaHCO3都属于酸
C.烧碱和纯碱都属于碱
D.H2O和Na2SO3都属于氧化物解析:NaHCO3都属于酸式盐;纯碱是Na2CO3不属于碱,属于盐;Na2SO3不属于氧化物。
答案:A物质的性质?知识回顾
1.物理性质:一般指物质的________、________、________、________、溶解性、导电性、导热性、密度、硬度等,均是可以通过观察方法和测量方法来研究的性质。
2.化学性质:一般指物质的________性、________性、________性、________性、热稳定性等,是物质在发生化学反应时表现出来的性质。颜色状态气味熔沸点酸碱氧化还原【例2】 下列物质的用途与共化学性质有关的是( )
A.用甲烷制造燃料电池
B.用石墨作铅笔芯
C.用铝制容器盛装浓硫酸
D.用液氨作制冷剂解析:利用甲烷还原性制造燃料电池。利用石墨硬度小作铅笔芯。利用铝与浓硫酸发生钝化反应,形成保护膜盛装浓硫酸。液氨易挥发吸热作制冷剂。
答案:AC?课堂练习
3.(2012年广东学业水平考试)在标准状况下呈液态的物质为( )
A.C B.O2
C.CH3CH2OH D.Cl2解析:标准状况下C是固体,O2、Cl2是气体,CH3CH2OH是液体。
答案:C4.(2012年广东水平考试)金属铝及其合金广泛用于电气工业和飞机制造业等领域,属于铝的化学性质的是( )
A.具有延展性
B.能与NaOH溶液反应
C.具有导电性
D.相对密度为2.7 g/cm3解析:铝与NaOH溶液反应是通过化学反应表现出的性质。
答案:B酸、碱、盐、氧化物?知识回顾
1.酸:在水溶液中电离所产生的阳离子_________的化合物。酸的通性有:
(1)酸能使酸碱指示剂变色(如石蕊遇酸变________)。
(2)酸与活泼金属反应生成盐和H2。
(3)酸与碱或碱性氧化物反应生成盐和水。
(4)酸与盐发生复分解反应。全部是H+红 2.碱:在水溶液中电离出的阴离子____________的化合物。碱的通性有:
(1)能使酸碱指示剂变色(如石蕊遇碱变蓝,如酚酞变红)。
(2)碱与酸或酸性氧化物反应生成盐和水。
3.盐:是酸、碱中和的产物。钾盐、钠盐、硝酸盐、醋酸盐、铵盐都________溶于水,碳酸盐、磷酸盐、硫化物、亚硫酸盐等其中大多数________溶于水。金属钾、钠、钙等非常活泼金属与盐溶液只能置换出________气。全部是OH-易不氢4.氧化物:氧化物是由氧和________元素组成的化合物。
(1)酸性氧化物:与________反应生成________的氧化物,酸性氧化物中元素的价态必须与对应的酸和盐中的价态一致。酸性氧化物大多是非金属氧化物(如CO2等),也可以是金属氧化物(如Mn2O7等)。
(2)碱性氧化物:能与______反应生成________的氧化物(如Na2O等)。碱性氧化物一定是________氧化物。
(3)两性氧化物:能与________反应生成______的氧化物(如Al2O3)。另一种碱盐和水酸盐和水金属酸或碱盐和水(4)不成盐氧化物:不能直接与酸、碱反应生成盐和水,或者没有对应价态的酸、碱或盐的氧化物(如NO、NO2、CO等)。
(5)Na2O2、H2O2等为过氧化物,不属于碱性氧化物。
5.酸、碱、盐和低价(一般+3价及其以下金属氧化物)金属氧化物是电解质。【例3】 在物质分类中,前者包括后者的是( )
A.氧化物、Na2O2 B.酸、CH3COOH
C.碱、氨水 D.酸式盐、NaHS解析:选项A正确,氧化物包括过氧化物,Na2O2;选项B正确,属于过氧化物。酸包括无机酸和有机酸,乙酸属于有机酸;选项C错误,氨水不是纯净物,是混合物;选项D正确,酸式盐包括含氧酸式盐和无氧酸式盐,NaHS属于无氧酸式盐。
答案:ABD易错提醒:1.金属与HNO3反应不产生氢气。
2.金属钾、钠、钙等非常活泼金属与盐溶液反应,只能置换出氢气,不能置换出其他金属。
3.NO2能与水反应生产HNO3,但不属于酸性氧化物,属于不成盐氧化物。
4.NH3不属于碱,NH3·H2O属于易溶性弱碱。Al(OH)3、H3AlO3、HAlO2·H2O既属于酸,也属于碱是两性物质。
5.水溶液中显酸性的物质不一定都是酸。如强酸的酸式盐NaHSO4水溶液呈强酸性,但NaHSO4属于盐。
6.碱与盐发生复分解反应的条件是:反应物都可溶,产物中至少有一种是沉淀,气体或难电离的物质。7.水溶液中显碱性的物质不一定都是碱。如Na2CO3、NaHCO3水溶液呈碱性。
8.酸式盐溶解度一般比正盐大,碱式盐溶解度一般比正盐小。但NaHCO3溶解度小于Na2CO3。
9.酸式盐受热比对应正盐易分解。
10.H2SiO3、H4SiO4、高级脂肪酸是不溶性酸;NaOH、KOH、Ba(OH)2、NH3·H2O(弱碱)是可溶性碱;二价以上金属阳离子形成的碱一般不溶于水。?课堂练习
5.(2011年广东学业水平考试)下列物质的水溶液显酸性的是( )
A.烧碱 B.生石灰
C.食醋 D.小苏打解析:食醋显酸性,其他显碱性。
答案:C6.(2011年广东水平测试)物质的量浓度相同的下列物质的水溶液,酸性最强的是( )
A.HCl B.H2SO4
C.CH3COOH D.NaCl解析:H2SO4为二元强酸,酸性最强。
答案:B分散系?知识回顾
1.溶液、浊液、胶体三种分散系比较无2.胶体聚沉方法:主要有: ______、加入______、加入带相反电荷的胶粒的胶体。无1 nm~
100 nm均匀、较
稳定有能加热电解质【例4】 (2012年广东学业考试)能产生丁达尔效应的是( )
A.酒精 B.CuSO4溶液
C.Fe(OH)3胶体 D.生理盐水解析:能产生丁达尔效应的物质是胶体分散系。溶液分散系不能产生丁达尔效应。酒精、CuSO4溶液、生理盐水都属于溶液分散系,不能产生丁达尔效应。
答案:C
易错提醒:胶体与溶液、浊液的本质区别是分散质粒子直径的大小。根据有无丁达尔现象可以鉴别胶体与溶液。?课堂练习
7.关于Fe(OH)3胶体的说法正确的是( )
A.属悬浊液
B.分散质是水
C.能产生丁达尔效应
D.可完全电离成Fe3+和OH-解析:Fe(OH)3胶体中,水是分散剂,Fe(OH)3胶粒是分散质,Fe(OH)3不能完全电离成Fe3+和OH-。
答案:C8.(2011年广东学业水平考试)下列实例中与胶体性质有关的是( )
A.用明矾净水
B.用食醋除去水垢
C.用石膏使豆浆变成豆腐
D.用含Al(OH)3的药物治疗胃酸过多解析:A项,明矾与水反应生成的Al(OH)3胶粒,能吸附水中的泥沙,起到净水作用,与胶体性质有关;C项,用石膏使豆浆中蛋白质发生聚沉,变成豆腐,与胶体性质有关。
答案:AC一、单选题考点一 物质的组成与分类1.(2012年广东学业水平考试)营养麦片含有多种成分,其中属于无机物是( )
A.玉米粉 B.大豆粉
C.Na2HPO4 D.白砂糖解析:Na2HPO4属于无机物。
答案:C2.(2012年广东学业水平考试)实验中将KCl和NaCl研磨均匀,得到的样品为( )
A.混合物 B.单质
C.纯净物 D.化合物解析:KCl和NaCl研磨后的物质含有两种不同化学成分组成的物质,属于混合物。
答案:A3.(2011年广东学业水平考试)下列物质属于混合物的是( )
A.纯碱 B.小苏打
C.烧碱 D.漂白粉解析:漂白粉含有CaCl2和Ca(ClO)2,属于混合物。
答案:D考点二 物质的性质6.下列各组物质能用简单物理方法区别的是( )
A.乙酸和乙醇 B.金刚石和水晶玻璃
C.小苏打和纯碱 D.石膏粉和熟石灰解析:乙酸和乙醇均与水互溶;小苏打和纯碱均易溶于水;金刚石和水晶玻璃都是无色透明的晶体,金刚石比水晶玻璃硬度大,金刚石可在水晶玻璃上刻画出痕迹;石膏粉和熟石灰均是白色粉末、微溶于水。
答案:B7.通常用活性炭去除冰箱中的异味,主要利用了活性炭的( )
A.吸附性 B.还原性
C.稳定性 D.氧化性解析:活性炭有较大表面积,具有较强吸附有异味气体的能力。
答案:A8.有固定的熔点,且熔点逐渐降低的一组物质是( )
A.HBr、HCl、H2O B.食盐、干冰、钾
C.柴油、煤油、汽油 D.KI、I2、O2解析:KI是高熔点离子化合物,I2是低熔点固态单质,易升华,O2常温呈气态。
答案:D考点三 酸、碱、盐、氧化物11.(2012年广东学业水平考试)溶于水后能形成酸的物质是( )
A.SO2 B.NaCl
C.Na2O D.NaOH解析:SO2溶于水后与水反应生成H2SO3。
答案:A12.(2012年广东学业水平考试)溶于水后溶液呈碱性的物质是( )
A.NO2 B.HCl
C.SO2 D.Na2O2解析:NO2溶于水有硝酸生成;HCl溶于水生成盐酸,SO2溶于水生成H2SO3溶液呈酸性;Na2O2溶于水有NaOH生成。
答案:D13.用下图表示的一些物质或概念间的从属关系中不正确的是( )解析:盐有无机酸盐和有机酸盐,有机酸盐属于有机物。碱性氧化物都是金属氧化物。
答案:B考点四 分散系16.(2012年广东学业水平考试)当光束通过下列分散系时,可能产生丁达尔效应的是( )
A.NaHCO3溶液 B.蔗糖溶液
C.CuSO4溶液 D.Fe(OH)3胶体解析:NaHCO3溶液、蔗糖溶液、CuSO4溶液不属于胶体分散系,均不能产生丁达尔效应。
答案:D17.关于Fe(OH)3胶体的说法不正确的是( )
A.不能透过滤纸
B.Fe(OH)3胶粒直径大小在1~100 nm之间
C.能产生丁达尔效应
D.可将FeCl3浓溶液滴入沸水制得解析:Fe(OH)3胶体能透过滤纸。
答案:A18.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A.都有丁达尔现象
B.都呈红褐色
C.分散质颗粒直径都在1~100 nm之间
D.都能通过滤纸解析:溶液和胶体分散系中的分散质粒子都能通过滤纸。
答案:D感谢您的使用,退出请按ESC键本小节结束
一、物质的组成
1.物质的宏观组成
(1)纯净物与混合物的比较。固定无固定(2)单质:由________元素组成的________。金属单质在常温下除________为液态外,其余呈固态,非金属单质在常温下除________为液态外,其余呈气态或固态。
(3)化合物:指由两种或两种以________元素组成的________。含碳化合物中个别物质如:CO、CO2、H2CO3、碳酸盐等,具有________特性列入无机物范畴外,其余的__________一般列入有机物范畴。同种纯净物HgBr2上 纯净物无机物含碳化合物2.物质的微观组成
(1)分子是保持物质________的一种微粒。如:H2、He、CO2、HNO3。
(2)原子是化学变化中的________微粒。如:Fe、S、Ne。
(3)离子是带电的原子或________。如:
(4)基团是不带电的原子或________。如:甲基—CH3、羟基—OH、羧基—COOH。化学性质最小原子团原子团3.元素、原子、离子、分子、单质、化合物间关系二、物质的分类
1.分类方法
(1)物质的树状分类:对同一类物质再分类。如:对Na2SO4进行树状分类可分为______、________、________、正盐等。
(2)物质的交叉分类:对同一种物质进行交叉分类。如:对Na2SO4进行交叉分类,按阳离子属于________、按阴离子属于________、________。纯净物无机物盐钠盐硫酸盐含氧酸盐2.物质分类的一般标准
(1)根据物质是否由同种微粒组成分为________和________。
(2)纯净物根据元素组成分为________(游离态)和________(化合态)。
(3)根据化合物的性质分为________、________、________、________、氢化物等。
(4)根据分散质颗粒大小可将分散系分为______、________、________、________等。纯净物混合物单质化合物酸碱盐氧化物悬浊液乳浊液胶体溶液 (5)依据化学键类型将化合物分为________化合物、________化合物。
(6)根据化合物在水溶液中或熔化状态下是否导电可分为________和________。
(7)依据在氧化还原反应中元素化合价的变化分为________、________。
离子共价电解质非电解质氧化剂还原剂3.常见无机化合物分类酸性碱性两性过氧化物强弱强易难HNO3H2SO4HNO3H2SO4 含氧可溶性难溶性强弱正盐酸式盐碱式盐【例1】 (2012年广东学业水平考试)分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A.K2CO3和K2O都属于盐
B.H2SO4和HNO3都属于酸
C.KOH和Na2CO3都属于碱
D.Na2O和Na2SiO3都属于氧化物解析:K2CO3、Na2CO3、Na2SiO3是盐,K2O、Na2O是氧化物,H2SO4和HNO3是酸。
答案:B注:该题在2010年广东学业考试11题、2011广东学业22题水平考试均重复出现。
易错提醒:1.普通玻璃、合金、天然矿物原料、高分子聚合物、熔化后的结晶水合物、半导体元件材料、同素异形体的混合物不是纯净物。石英材料、结晶水合物是纯净物。
2.具有特殊化学性质的部分原子或原子团,不带电荷的称作基,带电荷的称作根(或离子)。
3.酸式盐:酸中的部分氢被中和的产物。如NaHCO3等。
4.碱式盐:碱中的OH-部分被中和的产物。如Cu2(OH)2CO3等。?课堂练习
1.(2011年广东学业水平考试)下列物质属于单质的是( )
A.石墨 B.硫铁矿
C.青铜 D.碳素墨水解析:石墨属于单质,硫铁矿、青铜、碳素墨水属于混合物。
答案:A2.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A.Na2CO3和Na2S都属于盐
B.H2SO4和NaHCO3都属于酸
C.烧碱和纯碱都属于碱
D.H2O和Na2SO3都属于氧化物解析:NaHCO3都属于酸式盐;纯碱是Na2CO3不属于碱,属于盐;Na2SO3不属于氧化物。
答案:A物质的性质?知识回顾
1.物理性质:一般指物质的________、________、________、________、溶解性、导电性、导热性、密度、硬度等,均是可以通过观察方法和测量方法来研究的性质。
2.化学性质:一般指物质的________性、________性、________性、________性、热稳定性等,是物质在发生化学反应时表现出来的性质。颜色状态气味熔沸点酸碱氧化还原【例2】 下列物质的用途与共化学性质有关的是( )
A.用甲烷制造燃料电池
B.用石墨作铅笔芯
C.用铝制容器盛装浓硫酸
D.用液氨作制冷剂解析:利用甲烷还原性制造燃料电池。利用石墨硬度小作铅笔芯。利用铝与浓硫酸发生钝化反应,形成保护膜盛装浓硫酸。液氨易挥发吸热作制冷剂。
答案:AC?课堂练习
3.(2012年广东学业水平考试)在标准状况下呈液态的物质为( )
A.C B.O2
C.CH3CH2OH D.Cl2解析:标准状况下C是固体,O2、Cl2是气体,CH3CH2OH是液体。
答案:C4.(2012年广东水平考试)金属铝及其合金广泛用于电气工业和飞机制造业等领域,属于铝的化学性质的是( )
A.具有延展性
B.能与NaOH溶液反应
C.具有导电性
D.相对密度为2.7 g/cm3解析:铝与NaOH溶液反应是通过化学反应表现出的性质。
答案:B酸、碱、盐、氧化物?知识回顾
1.酸:在水溶液中电离所产生的阳离子_________的化合物。酸的通性有:
(1)酸能使酸碱指示剂变色(如石蕊遇酸变________)。
(2)酸与活泼金属反应生成盐和H2。
(3)酸与碱或碱性氧化物反应生成盐和水。
(4)酸与盐发生复分解反应。全部是H+红 2.碱:在水溶液中电离出的阴离子____________的化合物。碱的通性有:
(1)能使酸碱指示剂变色(如石蕊遇碱变蓝,如酚酞变红)。
(2)碱与酸或酸性氧化物反应生成盐和水。
3.盐:是酸、碱中和的产物。钾盐、钠盐、硝酸盐、醋酸盐、铵盐都________溶于水,碳酸盐、磷酸盐、硫化物、亚硫酸盐等其中大多数________溶于水。金属钾、钠、钙等非常活泼金属与盐溶液只能置换出________气。全部是OH-易不氢4.氧化物:氧化物是由氧和________元素组成的化合物。
(1)酸性氧化物:与________反应生成________的氧化物,酸性氧化物中元素的价态必须与对应的酸和盐中的价态一致。酸性氧化物大多是非金属氧化物(如CO2等),也可以是金属氧化物(如Mn2O7等)。
(2)碱性氧化物:能与______反应生成________的氧化物(如Na2O等)。碱性氧化物一定是________氧化物。
(3)两性氧化物:能与________反应生成______的氧化物(如Al2O3)。另一种碱盐和水酸盐和水金属酸或碱盐和水(4)不成盐氧化物:不能直接与酸、碱反应生成盐和水,或者没有对应价态的酸、碱或盐的氧化物(如NO、NO2、CO等)。
(5)Na2O2、H2O2等为过氧化物,不属于碱性氧化物。
5.酸、碱、盐和低价(一般+3价及其以下金属氧化物)金属氧化物是电解质。【例3】 在物质分类中,前者包括后者的是( )
A.氧化物、Na2O2 B.酸、CH3COOH
C.碱、氨水 D.酸式盐、NaHS解析:选项A正确,氧化物包括过氧化物,Na2O2;选项B正确,属于过氧化物。酸包括无机酸和有机酸,乙酸属于有机酸;选项C错误,氨水不是纯净物,是混合物;选项D正确,酸式盐包括含氧酸式盐和无氧酸式盐,NaHS属于无氧酸式盐。
答案:ABD易错提醒:1.金属与HNO3反应不产生氢气。
2.金属钾、钠、钙等非常活泼金属与盐溶液反应,只能置换出氢气,不能置换出其他金属。
3.NO2能与水反应生产HNO3,但不属于酸性氧化物,属于不成盐氧化物。
4.NH3不属于碱,NH3·H2O属于易溶性弱碱。Al(OH)3、H3AlO3、HAlO2·H2O既属于酸,也属于碱是两性物质。
5.水溶液中显酸性的物质不一定都是酸。如强酸的酸式盐NaHSO4水溶液呈强酸性,但NaHSO4属于盐。
6.碱与盐发生复分解反应的条件是:反应物都可溶,产物中至少有一种是沉淀,气体或难电离的物质。7.水溶液中显碱性的物质不一定都是碱。如Na2CO3、NaHCO3水溶液呈碱性。
8.酸式盐溶解度一般比正盐大,碱式盐溶解度一般比正盐小。但NaHCO3溶解度小于Na2CO3。
9.酸式盐受热比对应正盐易分解。
10.H2SiO3、H4SiO4、高级脂肪酸是不溶性酸;NaOH、KOH、Ba(OH)2、NH3·H2O(弱碱)是可溶性碱;二价以上金属阳离子形成的碱一般不溶于水。?课堂练习
5.(2011年广东学业水平考试)下列物质的水溶液显酸性的是( )
A.烧碱 B.生石灰
C.食醋 D.小苏打解析:食醋显酸性,其他显碱性。
答案:C6.(2011年广东水平测试)物质的量浓度相同的下列物质的水溶液,酸性最强的是( )
A.HCl B.H2SO4
C.CH3COOH D.NaCl解析:H2SO4为二元强酸,酸性最强。
答案:B分散系?知识回顾
1.溶液、浊液、胶体三种分散系比较无2.胶体聚沉方法:主要有: ______、加入______、加入带相反电荷的胶粒的胶体。无1 nm~
100 nm均匀、较
稳定有能加热电解质【例4】 (2012年广东学业考试)能产生丁达尔效应的是( )
A.酒精 B.CuSO4溶液
C.Fe(OH)3胶体 D.生理盐水解析:能产生丁达尔效应的物质是胶体分散系。溶液分散系不能产生丁达尔效应。酒精、CuSO4溶液、生理盐水都属于溶液分散系,不能产生丁达尔效应。
答案:C
易错提醒:胶体与溶液、浊液的本质区别是分散质粒子直径的大小。根据有无丁达尔现象可以鉴别胶体与溶液。?课堂练习
7.关于Fe(OH)3胶体的说法正确的是( )
A.属悬浊液
B.分散质是水
C.能产生丁达尔效应
D.可完全电离成Fe3+和OH-解析:Fe(OH)3胶体中,水是分散剂,Fe(OH)3胶粒是分散质,Fe(OH)3不能完全电离成Fe3+和OH-。
答案:C8.(2011年广东学业水平考试)下列实例中与胶体性质有关的是( )
A.用明矾净水
B.用食醋除去水垢
C.用石膏使豆浆变成豆腐
D.用含Al(OH)3的药物治疗胃酸过多解析:A项,明矾与水反应生成的Al(OH)3胶粒,能吸附水中的泥沙,起到净水作用,与胶体性质有关;C项,用石膏使豆浆中蛋白质发生聚沉,变成豆腐,与胶体性质有关。
答案:AC一、单选题考点一 物质的组成与分类1.(2012年广东学业水平考试)营养麦片含有多种成分,其中属于无机物是( )
A.玉米粉 B.大豆粉
C.Na2HPO4 D.白砂糖解析:Na2HPO4属于无机物。
答案:C2.(2012年广东学业水平考试)实验中将KCl和NaCl研磨均匀,得到的样品为( )
A.混合物 B.单质
C.纯净物 D.化合物解析:KCl和NaCl研磨后的物质含有两种不同化学成分组成的物质,属于混合物。
答案:A3.(2011年广东学业水平考试)下列物质属于混合物的是( )
A.纯碱 B.小苏打
C.烧碱 D.漂白粉解析:漂白粉含有CaCl2和Ca(ClO)2,属于混合物。
答案:D考点二 物质的性质6.下列各组物质能用简单物理方法区别的是( )
A.乙酸和乙醇 B.金刚石和水晶玻璃
C.小苏打和纯碱 D.石膏粉和熟石灰解析:乙酸和乙醇均与水互溶;小苏打和纯碱均易溶于水;金刚石和水晶玻璃都是无色透明的晶体,金刚石比水晶玻璃硬度大,金刚石可在水晶玻璃上刻画出痕迹;石膏粉和熟石灰均是白色粉末、微溶于水。
答案:B7.通常用活性炭去除冰箱中的异味,主要利用了活性炭的( )
A.吸附性 B.还原性
C.稳定性 D.氧化性解析:活性炭有较大表面积,具有较强吸附有异味气体的能力。
答案:A8.有固定的熔点,且熔点逐渐降低的一组物质是( )
A.HBr、HCl、H2O B.食盐、干冰、钾
C.柴油、煤油、汽油 D.KI、I2、O2解析:KI是高熔点离子化合物,I2是低熔点固态单质,易升华,O2常温呈气态。
答案:D考点三 酸、碱、盐、氧化物11.(2012年广东学业水平考试)溶于水后能形成酸的物质是( )
A.SO2 B.NaCl
C.Na2O D.NaOH解析:SO2溶于水后与水反应生成H2SO3。
答案:A12.(2012年广东学业水平考试)溶于水后溶液呈碱性的物质是( )
A.NO2 B.HCl
C.SO2 D.Na2O2解析:NO2溶于水有硝酸生成;HCl溶于水生成盐酸,SO2溶于水生成H2SO3溶液呈酸性;Na2O2溶于水有NaOH生成。
答案:D13.用下图表示的一些物质或概念间的从属关系中不正确的是( )解析:盐有无机酸盐和有机酸盐,有机酸盐属于有机物。碱性氧化物都是金属氧化物。
答案:B考点四 分散系16.(2012年广东学业水平考试)当光束通过下列分散系时,可能产生丁达尔效应的是( )
A.NaHCO3溶液 B.蔗糖溶液
C.CuSO4溶液 D.Fe(OH)3胶体解析:NaHCO3溶液、蔗糖溶液、CuSO4溶液不属于胶体分散系,均不能产生丁达尔效应。
答案:D17.关于Fe(OH)3胶体的说法不正确的是( )
A.不能透过滤纸
B.Fe(OH)3胶粒直径大小在1~100 nm之间
C.能产生丁达尔效应
D.可将FeCl3浓溶液滴入沸水制得解析:Fe(OH)3胶体能透过滤纸。
答案:A18.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A.都有丁达尔现象
B.都呈红褐色
C.分散质颗粒直径都在1~100 nm之间
D.都能通过滤纸解析:溶液和胶体分散系中的分散质粒子都能通过滤纸。
答案:D感谢您的使用,退出请按ESC键本小节结束
同课章节目录
