【名师新编,备战2014高中学业水平考试】2013-2014高中化学名师专题指导(学业考纲+考点整合+水平达标):第六讲 氧化还原反应(39张ppt)
文档属性
| 名称 | 【名师新编,备战2014高中学业水平考试】2013-2014高中化学名师专题指导(学业考纲+考点整合+水平达标):第六讲 氧化还原反应(39张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 627.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-02-15 08:24:25 | ||
图片预览










文档简介
(共39张PPT)
第六讲 氧化还原反应
考点概览 考纲要求
1.氧化还原反应判断
2.氧化剂与还原剂判断
3.物质的氧化性与还原性 1.了解氧化还原反应的本质是电子的转移
2.了解常见的氧化还原反应
氧化还原反应判断
知识回顾
1.氧化反应与还原反应
(1)氧化反应:反应物________电子,化合价________的反应。
(2)还原反应:反应物________电子,化合价________的反应。
(3)氧化还原反应:在反应过程中氧化反应和还原反应同时发生,元素________发生变化。
2.氧化还原反应实质:在反应过程中有________转移或偏移。
失去
升高
得到
降低
化合价
电子
3.氧化还原反应判断方法:根据元素化合价变化和反应类型判断。
(1)有元素________变化的反应是氧化还原反应。________元素化合价变化的化学反应是非氧化还原反应。
(2)有________参加的化合反应、有单质生成的________反应和________反应是氧化还原反应,________反应不是氧化还原反应。
化合价
没有
单质
分解
置换
复分解
【例1】 下列化工生产过程所发生的反应不属于氧化还原反应的是( )
A.用淀粉制葡萄糖
B.用铝土矿制金属铝
C.用氯气和消石灰制漂白粉
D.用氢气和氮气合成氨
解析:在酶催化剂作用下淀粉水解制葡萄糖过程中C、H、O元素化合价均无变化,不属于氧化还原反应。B项中铝元素的化合价由+3价变为0价,C项中Cl元素的化合价由0价变为-l和+1价,D项中H由0价变为+1价,N由0价变为-3价,所以B、C、D都是氧化还原反应。
答案:A
课堂练习
1.(2012年广东学业水平考试)下列过程中发生氧化还原反应的是( )
A.Cu和稀HNO3反应
B.Fe的导电
C.Na2CO3溶液与盐酸反应
D.CaCO3高温分解
解析:Cu和稀HNO3反应,化合价发生了变化,属于氧化还原反应。
答案:A
2.硝酸铵在不同条件下分解可以得到不同的产物,下列各组物质中肯定不可能是硝酸铵分解产物的是( )
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
解析:化合物中的+1价氢元素不能氧化-3价的氮元素。
答案:D
氧化剂与还原剂判断
知识回顾
1.氧化剂:在反应中元素化合价升高,________电子的物质,表现出________性,发生________反应,氧化其他物质而自身被________。
2.还原剂:在反应中元素化合价降低,________电子的物质,表现出________性,发生________反应,还原其他物质而自身被________。
得到
氧化
还原
还原
失去
还原
氧化
氧化
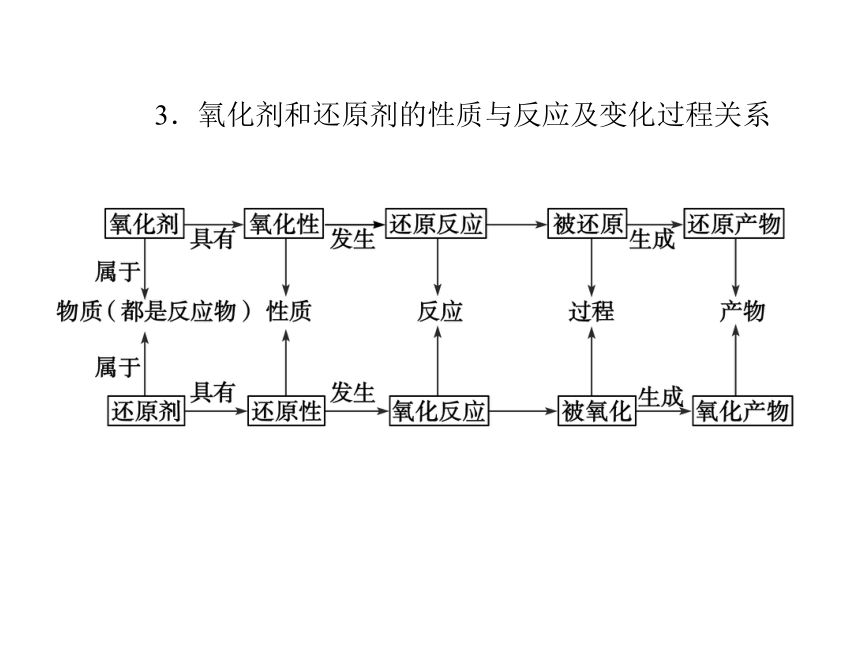
3.氧化剂和还原剂的性质与反应及变化过程关系
4.常见氧化剂与还原剂
(1)常见氧化剂:
①活泼非金属单质,如:O2、O3、Cl2、Br2。
②高价态的金属阳离子,如:Fe3+、Cu2+、Ag+。
③高价态或较高价态的含氧化合物,如:PbO2、NO2、MnO2。
④氧化性酸,如:HClO、HNO3、浓硫酸。
⑤高价含氧酸盐,如:KMnO4、KClO3、K2FeO4。
⑥过氧化物,如:H2O2、Na2O2等。
(2)常见还原剂:
①活泼金属,如:K、Na、Mg、Al、Zn、Fe。
②不太活泼的非金属单质,如:H2、C、Si。
③低价态的金属阳离子,如:Fe2+。
④非金属阴离子,如:S2-、I-、Br-等。
⑤低价态或较低价的化合物,如:CO、NO、H2S、CH4、SO2、Na2SO3、KI、FeSO4、NH3。
【例2】 对于反应SiO2+2C Si+2CO↑下列说法正确的是( )
A.SiO2是氧化剂
B.CO是氧化剂
C.Si是还原剂
D.C是还原剂
解析:A项正确,SiO2是反应物,硅元素化合价降低,发生还原反应,作氧化剂。B项错误,CO是氧化产物。C项错误,Si是还原产物。D项正确,C是反应物,C元素化合价升高,发生氧化反应,作还原剂。
答案:AD
易错提醒:同素异形体之间的转化有单质参加和生成,但元素价态不变,不属于氧化还原反应,但属于化学变化。如:金刚石转变为石墨,氧气转变为臭氧。
课堂练习
3.用CO还原氧化铁:Fe2O3+3CO===3CO2+ Fe,在该反应中( )
A.Fe 做还原剂
B.Fe2O3做氧化剂
C.铁元素的化合价降低
D.铁元素化合价升高
解析:Fe 元素化合价由+3降低到0,化合价降低,Fe2O3是氧化剂。
答案:BC
4.在Fe2O3+3CO 2Fe+3CO2的反应中( )
A.Fe作还原剂
B.Fe2O3是氧化剂
C.铁元素化合价降低
D.铁元素化合价升高
解析:反应中Fe2O3中铁元素化合价由+3降低到0,化合价降低,Fe2O3是氧化剂。
答案:BC
氧化还原反应规律
强氧化剂+强还原剂→弱还原剂 + 弱氧化剂
(还原产物)(氧化产物)
2.氧化性强弱顺序为:氧化剂________氧化产物。
3.还原性强弱顺序为:还原剂________还原产物。
4.氧化还原反应遵循质量守恒定律:即氧化剂________总数=还原剂________总数。
大于
大于
得电子
失电子
5.元素化合价与元素氧化还原性:
(1)当元素处于最高化合价时只表现氧化性。如:Cu2+、Al3+。
(2)当元素处于最低化合价时只表现还原性。如:I-、Cl-。
(3)当元素处于中间价态时,在同一反应或不同反应中既可表现氧化性作氧化剂,又可表现还原性作还原剂,如:SO2、Fe2+等。
【例3】 从海水中提取溴,主要反应为:2Br-+Cl2===Br2+2Cl-,下列说法正确的是( )
A.溴离子表现氧化性
B.氯气表现氧化性
C.还原性氯离子比溴离子强
D.氧化性氯气比溴单质强
解析:A项错误,溴离子化合价升高,表现还原性;B项正确,氯元素化合价降低,表现氧化性;C项错误,还原性溴离子比氯离子强;D项正确。
答案:BD
课堂练习
5.(2012年广东学业水平考试)将Cl2通入自来水中杀菌消毒,主要是利用了Cl2和H2O生成的HClO的( )
A.氧化性 B.酸性
C.还原性 D.稳定性
解析:HClO在杀菌消毒过程中主要表现出氧化性,氧化细菌的蛋白质分子,将细菌杀死。
答案:A
6.氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.生成1 mol N2有6 mol电子转移
D.该反应属于复分解反应
解析:选项D错误,该反应中氮元素和氯元素化合价均发生变化,属于氧化还原反应。
答案:D
一、单选题
考点一 氧化还原反应判断
1.关于氧化还原反应的说法中正确的是( )
A.元素化合价发生变化的反应是氧化还原反应
B.分解反应一定是氧化还原反应
C.原子得到电子后,元素的化合价一定升高
D.化合反应一定是氧化还原反应
解析:A项正确。B、C、D三项错误,分解反应和化合反应不一定是氧化还原反应;原子得到电子后,元素的化合价一定降低。
答案:A
2.古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
A.野火烧不尽,春风吹又生
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.粉身碎骨浑不怕,要留清白在人间
D.爆竹声中一岁除,春风送暖入屠苏
解析:块状白色石灰石发生CaCO3 CaO+CO2分解反应烧制成粉末状的生石灰。选项A、B含有燃烧现象,选项D含有火药爆炸现象。
答案:C
解析:C项中H2O2中氧元素化合价由-1价升高为0价和降低为-2价,属于氧化还原反应。
答案:C
考点二 氧化剂与还原剂判断
8.钠与水反应:2Na+2H2O===H2+2NaOH,在该反应中( )
A.H2作还原剂 B.H2O作氧化剂
C.钠元素的化合价降低 D.氢元素化合价升高
解析:水中的部分H由+1价降低为0价,H2O做氧化剂。
答案:B
9.在氯气溶于水时发生反应:Cl2+H2O===HCl+HClO,在该反应中( )
A.H2O是氧化剂
B.H2O是还原剂
C.Cl2只作氧化剂
D.Cl2既作氧化剂又作还原剂
解析:该反应中氯元素的化合价既有升高,又有降低,Cl2既作氧化剂又作还原剂。
答案:D
10.生产泡沫橡胶过程中,有如下一个反应:2H2O2 ===== 2H2O+O2↑。该反应中H2O2( )
A.既不是氧化剂,也不是还原剂
B.既是氧化剂又是还原剂
C.仅为氧化剂
D.仅为还原剂
解析:氧元素化合价分别由-1价升高为0价和降低为-2价,H2O2既是氧化剂又是还原剂。
答案:B
考点三 氧化还原反应规律
解析:Na、Cl-、Cu分别呈最低价态,只有还原性。
答案:B
16.在下列反应中,硫元素表现出氧化性的是( )
A.稀硫酸与锌反应
B.二氧化硫与氧气反应
C.浓硫酸与铜反应
D.三氧化硫与水反应
解析:浓硫酸与铜反应生成的SO2中S元素化合价由+6价降低为+4,硫元素表现出氧化性。
答案:C
17.下列过程能同时生成两种盐的是( )
A.碳在空气中燃烧
B.NaOH溶液吸收Cl2
C.硫在O2中燃烧,产物用水吸收
D.在一定条件下H2和N2反应,产物用水吸收
解析:NaOH溶液吸收Cl2,生成氯化钠和次氯酸钠。
答案:B
解析:选项A、B、D三项的反应均无元素化合价变化,不属于氧化还原反应。选项C,Zn→Zn2+、H+→H2锌和氢两种元素价态均发生变化,属于氧化还原反应。
答案:ABD
22.下列工业生产过程中,涉及氧化还原反应的是( )
A.用S制备H2SO4
B.用CaCO3、Na2CO3、SiO2生产玻璃
C.将海水中的MgSO4转变为金属Mg
D.用NO2生产HNO3
23.(2012年广东学业水平考试)氢气还原氧化铜:CuO+H2===Cu+H2O,在该反应中( )
A.CuO作还原剂 B.CuO作氧化剂
C.铜元素化合价降低 D.铜元素化合价升高
解析:Cu由+2价降低到0价,CuO是氧化剂。H元素化合价由0价升高为+1价,H2是还原剂。(与2011年广东学业水平考试64题相同)
答案:BC
第六讲 氧化还原反应
考点概览 考纲要求
1.氧化还原反应判断
2.氧化剂与还原剂判断
3.物质的氧化性与还原性 1.了解氧化还原反应的本质是电子的转移
2.了解常见的氧化还原反应
氧化还原反应判断
知识回顾
1.氧化反应与还原反应
(1)氧化反应:反应物________电子,化合价________的反应。
(2)还原反应:反应物________电子,化合价________的反应。
(3)氧化还原反应:在反应过程中氧化反应和还原反应同时发生,元素________发生变化。
2.氧化还原反应实质:在反应过程中有________转移或偏移。
失去
升高
得到
降低
化合价
电子
3.氧化还原反应判断方法:根据元素化合价变化和反应类型判断。
(1)有元素________变化的反应是氧化还原反应。________元素化合价变化的化学反应是非氧化还原反应。
(2)有________参加的化合反应、有单质生成的________反应和________反应是氧化还原反应,________反应不是氧化还原反应。
化合价
没有
单质
分解
置换
复分解
【例1】 下列化工生产过程所发生的反应不属于氧化还原反应的是( )
A.用淀粉制葡萄糖
B.用铝土矿制金属铝
C.用氯气和消石灰制漂白粉
D.用氢气和氮气合成氨
解析:在酶催化剂作用下淀粉水解制葡萄糖过程中C、H、O元素化合价均无变化,不属于氧化还原反应。B项中铝元素的化合价由+3价变为0价,C项中Cl元素的化合价由0价变为-l和+1价,D项中H由0价变为+1价,N由0价变为-3价,所以B、C、D都是氧化还原反应。
答案:A
课堂练习
1.(2012年广东学业水平考试)下列过程中发生氧化还原反应的是( )
A.Cu和稀HNO3反应
B.Fe的导电
C.Na2CO3溶液与盐酸反应
D.CaCO3高温分解
解析:Cu和稀HNO3反应,化合价发生了变化,属于氧化还原反应。
答案:A
2.硝酸铵在不同条件下分解可以得到不同的产物,下列各组物质中肯定不可能是硝酸铵分解产物的是( )
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
解析:化合物中的+1价氢元素不能氧化-3价的氮元素。
答案:D
氧化剂与还原剂判断
知识回顾
1.氧化剂:在反应中元素化合价升高,________电子的物质,表现出________性,发生________反应,氧化其他物质而自身被________。
2.还原剂:在反应中元素化合价降低,________电子的物质,表现出________性,发生________反应,还原其他物质而自身被________。
得到
氧化
还原
还原
失去
还原
氧化
氧化
3.氧化剂和还原剂的性质与反应及变化过程关系
4.常见氧化剂与还原剂
(1)常见氧化剂:
①活泼非金属单质,如:O2、O3、Cl2、Br2。
②高价态的金属阳离子,如:Fe3+、Cu2+、Ag+。
③高价态或较高价态的含氧化合物,如:PbO2、NO2、MnO2。
④氧化性酸,如:HClO、HNO3、浓硫酸。
⑤高价含氧酸盐,如:KMnO4、KClO3、K2FeO4。
⑥过氧化物,如:H2O2、Na2O2等。
(2)常见还原剂:
①活泼金属,如:K、Na、Mg、Al、Zn、Fe。
②不太活泼的非金属单质,如:H2、C、Si。
③低价态的金属阳离子,如:Fe2+。
④非金属阴离子,如:S2-、I-、Br-等。
⑤低价态或较低价的化合物,如:CO、NO、H2S、CH4、SO2、Na2SO3、KI、FeSO4、NH3。
【例2】 对于反应SiO2+2C Si+2CO↑下列说法正确的是( )
A.SiO2是氧化剂
B.CO是氧化剂
C.Si是还原剂
D.C是还原剂
解析:A项正确,SiO2是反应物,硅元素化合价降低,发生还原反应,作氧化剂。B项错误,CO是氧化产物。C项错误,Si是还原产物。D项正确,C是反应物,C元素化合价升高,发生氧化反应,作还原剂。
答案:AD
易错提醒:同素异形体之间的转化有单质参加和生成,但元素价态不变,不属于氧化还原反应,但属于化学变化。如:金刚石转变为石墨,氧气转变为臭氧。
课堂练习
3.用CO还原氧化铁:Fe2O3+3CO===3CO2+ Fe,在该反应中( )
A.Fe 做还原剂
B.Fe2O3做氧化剂
C.铁元素的化合价降低
D.铁元素化合价升高
解析:Fe 元素化合价由+3降低到0,化合价降低,Fe2O3是氧化剂。
答案:BC
4.在Fe2O3+3CO 2Fe+3CO2的反应中( )
A.Fe作还原剂
B.Fe2O3是氧化剂
C.铁元素化合价降低
D.铁元素化合价升高
解析:反应中Fe2O3中铁元素化合价由+3降低到0,化合价降低,Fe2O3是氧化剂。
答案:BC
氧化还原反应规律
强氧化剂+强还原剂→弱还原剂 + 弱氧化剂
(还原产物)(氧化产物)
2.氧化性强弱顺序为:氧化剂________氧化产物。
3.还原性强弱顺序为:还原剂________还原产物。
4.氧化还原反应遵循质量守恒定律:即氧化剂________总数=还原剂________总数。
大于
大于
得电子
失电子
5.元素化合价与元素氧化还原性:
(1)当元素处于最高化合价时只表现氧化性。如:Cu2+、Al3+。
(2)当元素处于最低化合价时只表现还原性。如:I-、Cl-。
(3)当元素处于中间价态时,在同一反应或不同反应中既可表现氧化性作氧化剂,又可表现还原性作还原剂,如:SO2、Fe2+等。
【例3】 从海水中提取溴,主要反应为:2Br-+Cl2===Br2+2Cl-,下列说法正确的是( )
A.溴离子表现氧化性
B.氯气表现氧化性
C.还原性氯离子比溴离子强
D.氧化性氯气比溴单质强
解析:A项错误,溴离子化合价升高,表现还原性;B项正确,氯元素化合价降低,表现氧化性;C项错误,还原性溴离子比氯离子强;D项正确。
答案:BD
课堂练习
5.(2012年广东学业水平考试)将Cl2通入自来水中杀菌消毒,主要是利用了Cl2和H2O生成的HClO的( )
A.氧化性 B.酸性
C.还原性 D.稳定性
解析:HClO在杀菌消毒过程中主要表现出氧化性,氧化细菌的蛋白质分子,将细菌杀死。
答案:A
6.氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.生成1 mol N2有6 mol电子转移
D.该反应属于复分解反应
解析:选项D错误,该反应中氮元素和氯元素化合价均发生变化,属于氧化还原反应。
答案:D
一、单选题
考点一 氧化还原反应判断
1.关于氧化还原反应的说法中正确的是( )
A.元素化合价发生变化的反应是氧化还原反应
B.分解反应一定是氧化还原反应
C.原子得到电子后,元素的化合价一定升高
D.化合反应一定是氧化还原反应
解析:A项正确。B、C、D三项错误,分解反应和化合反应不一定是氧化还原反应;原子得到电子后,元素的化合价一定降低。
答案:A
2.古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是( )
A.野火烧不尽,春风吹又生
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.粉身碎骨浑不怕,要留清白在人间
D.爆竹声中一岁除,春风送暖入屠苏
解析:块状白色石灰石发生CaCO3 CaO+CO2分解反应烧制成粉末状的生石灰。选项A、B含有燃烧现象,选项D含有火药爆炸现象。
答案:C
解析:C项中H2O2中氧元素化合价由-1价升高为0价和降低为-2价,属于氧化还原反应。
答案:C
考点二 氧化剂与还原剂判断
8.钠与水反应:2Na+2H2O===H2+2NaOH,在该反应中( )
A.H2作还原剂 B.H2O作氧化剂
C.钠元素的化合价降低 D.氢元素化合价升高
解析:水中的部分H由+1价降低为0价,H2O做氧化剂。
答案:B
9.在氯气溶于水时发生反应:Cl2+H2O===HCl+HClO,在该反应中( )
A.H2O是氧化剂
B.H2O是还原剂
C.Cl2只作氧化剂
D.Cl2既作氧化剂又作还原剂
解析:该反应中氯元素的化合价既有升高,又有降低,Cl2既作氧化剂又作还原剂。
答案:D
10.生产泡沫橡胶过程中,有如下一个反应:2H2O2 ===== 2H2O+O2↑。该反应中H2O2( )
A.既不是氧化剂,也不是还原剂
B.既是氧化剂又是还原剂
C.仅为氧化剂
D.仅为还原剂
解析:氧元素化合价分别由-1价升高为0价和降低为-2价,H2O2既是氧化剂又是还原剂。
答案:B
考点三 氧化还原反应规律
解析:Na、Cl-、Cu分别呈最低价态,只有还原性。
答案:B
16.在下列反应中,硫元素表现出氧化性的是( )
A.稀硫酸与锌反应
B.二氧化硫与氧气反应
C.浓硫酸与铜反应
D.三氧化硫与水反应
解析:浓硫酸与铜反应生成的SO2中S元素化合价由+6价降低为+4,硫元素表现出氧化性。
答案:C
17.下列过程能同时生成两种盐的是( )
A.碳在空气中燃烧
B.NaOH溶液吸收Cl2
C.硫在O2中燃烧,产物用水吸收
D.在一定条件下H2和N2反应,产物用水吸收
解析:NaOH溶液吸收Cl2,生成氯化钠和次氯酸钠。
答案:B
解析:选项A、B、D三项的反应均无元素化合价变化,不属于氧化还原反应。选项C,Zn→Zn2+、H+→H2锌和氢两种元素价态均发生变化,属于氧化还原反应。
答案:ABD
22.下列工业生产过程中,涉及氧化还原反应的是( )
A.用S制备H2SO4
B.用CaCO3、Na2CO3、SiO2生产玻璃
C.将海水中的MgSO4转变为金属Mg
D.用NO2生产HNO3
23.(2012年广东学业水平考试)氢气还原氧化铜:CuO+H2===Cu+H2O,在该反应中( )
A.CuO作还原剂 B.CuO作氧化剂
C.铜元素化合价降低 D.铜元素化合价升高
解析:Cu由+2价降低到0价,CuO是氧化剂。H元素化合价由0价升高为+1价,H2是还原剂。(与2011年广东学业水平考试64题相同)
答案:BC
同课章节目录
