人教版九年级化学下学期开学测试练习A卷(含解析)
文档属性
| 名称 | 人教版九年级化学下学期开学测试练习A卷(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 420.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-02 21:12:10 | ||
图片预览



文档简介
人教版九年级下学期化学开学测试练习
A卷
【满分:100分】
一、选择题:(本大题共15小题,每小题3分,共45分,给出的四个选项中,只有一项是符合题目要求的)
1.下列过程中,没有化学变化发生的是( )
A.古人钻木取火 B.探究分子不断运动
C.烧制陶瓷 D.霓虹灯发光
2.2022年全国生态环境保护大会强调,“十四五”时期,我国生态文明建设进入了以降碳为重点战略方向、推动减污降碳协同增效、促进经济社会发展全面绿色转型、实现生态环境质量改善由量变到质变的关键时期,下列措施不符合这一理念的是( )
A.过年城市燃放烟花爆竹 B.生活垃圾进行分类回收
C.大力推进植树造林工程 D.开发使用新型绿色能源
3.分别点燃相同两根火柴,将其中一根火柴头竖直向上,另一根火柴头倾斜向下,如图所示。小明发现第一根火柴不能持续燃烧,第二根火柴更容易持续燃烧。该实验现象说明,物质燃烧必须具备的条件是( )
A.物质具有可燃性 B.可燃物与充足氧气接触
C.可燃物的温度达到其自身的着火点 D.可燃物要倾斜放置
4.生物体中含有多种氨基酸,下列有关甘氨酸[](其分子结构如下图所示)的叙述正确的是( )
A.甘氨酸属于氧化物
B.甘氨酸中碳原子与氢原子的个数比为24:5
C.甘氨酸是由碳、氢、氧、氮四种原子构成的
D.一个甘氨酸分子中含有10个原子
5.生活中处处有化学,氧循环和碳循环是自然界中的重要循环。分析两种循环,其中不正确的是( )
A.碳循环和氧循环过程中均发生了化学变化,我们每个人了都参与碳循环和氧循环
B.两种循环各自独立,彼此之间无联系
C.通过减少化石燃料的使用和大力植树造林以控制二氧化碳的排放量
D.碳循环和氧循环有利于维持自然界中氧气和二氧化碳含量的相对稳定
6.铷(Rb)原子钟被称作北斗卫星的“心脏”、下图为铷原子的结构示意图,下列说法不正确的是( )
A.铷原子核内的质子数为37 B.铷原子在化学变化中容易失去1个电子
C.铷原子的核外电子分5层排布 D.氯化铷的化学式为
7.具有启普发生器功能的简易装置是( )
A. B. C. D.
8.国外大学生发明了一种能吃的“固体”水球,其原理与生蛋黄类似,将水包裹在一层由褐藻做成的可食用薄膜中。饮用时,将水球直接放入嘴中吃即可。下列说法中正确的是( )
A.该水球是混合物 B.该水球是水的固体
C.该水球中的水分子静止不动 D.该水球中的水分子间没有间隔
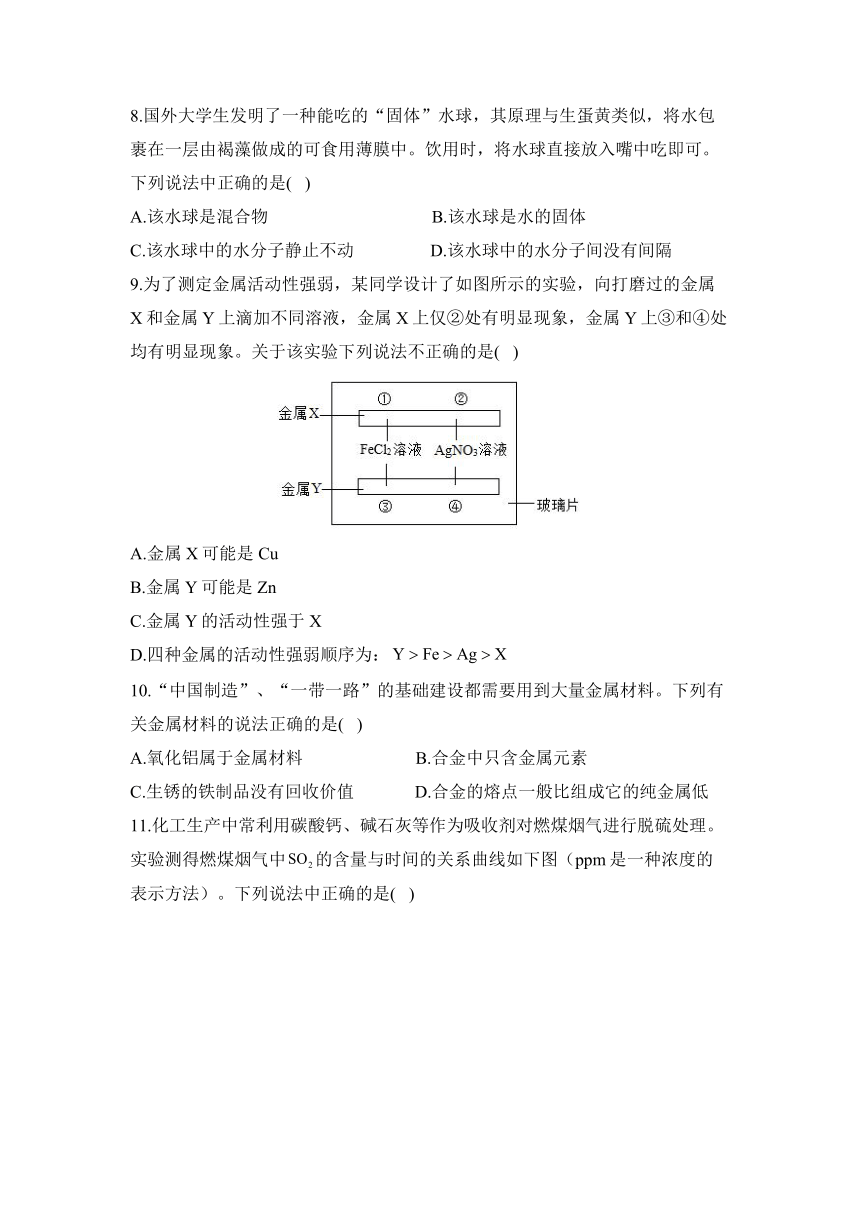
9.为了测定金属活动性强弱,某同学设计了如图所示的实验,向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有明显现象,金属Y上③和④处均有明显现象。关于该实验下列说法不正确的是( )
A.金属X可能是Cu
B.金属Y可能是Zn
C.金属Y的活动性强于X
D.四种金属的活动性强弱顺序为:
10.“中国制造”、“一带一路”的基础建设都需要用到大量金属材料。下列有关金属材料的说法正确的是( )
A.氧化铝属于金属材料 B.合金中只含金属元素
C.生锈的铁制品没有回收价值 D.合金的熔点一般比组成它的纯金属低
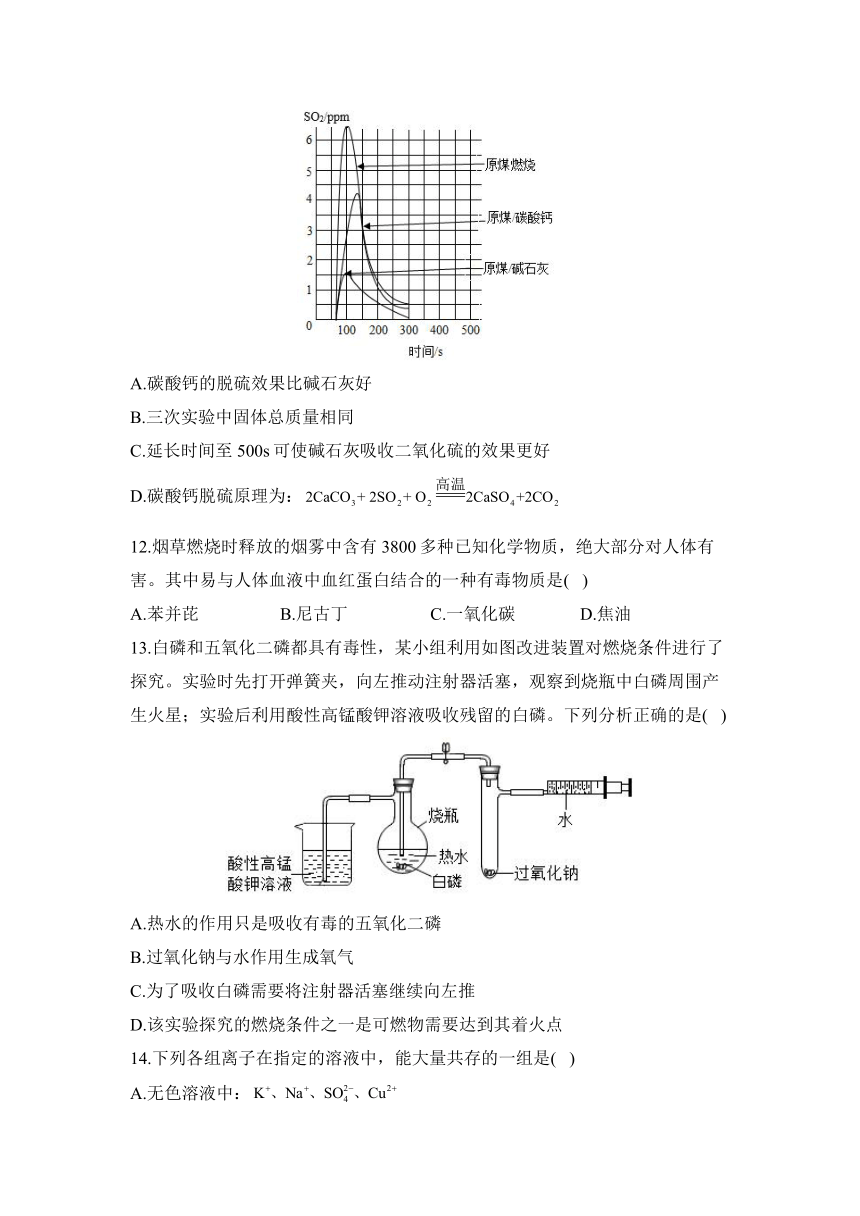
11.化工生产中常利用碳酸钙、碱石灰等作为吸收剂对燃煤烟气进行脱硫处理。实验测得燃煤烟气中的含量与时间的关系曲线如下图(ppm是一种浓度的表示方法)。下列说法中正确的是( )
A.碳酸钙的脱硫效果比碱石灰好
B.三次实验中固体总质量相同
C.延长时间至500s可使碱石灰吸收二氧化硫的效果更好
D.碳酸钙脱硫原理为:
12.烟草燃烧时释放的烟雾中含有3800多种已知化学物质,绝大部分对人体有害。其中易与人体血液中血红蛋白结合的一种有毒物质是( )
A.苯并芘 B.尼古丁 C.一氧化碳 D.焦油
13.白磷和五氧化二磷都具有毒性,某小组利用如图改进装置对燃烧条件进行了探究。实验时先打开弹簧夹,向左推动注射器活塞,观察到烧瓶中白磷周围产生火星;实验后利用酸性高锰酸钾溶液吸收残留的白磷。下列分析正确的是( )
A.热水的作用只是吸收有毒的五氧化二磷
B.过氧化钠与水作用生成氧气
C.为了吸收白磷需要将注射器活塞继续向左推
D.该实验探究的燃烧条件之一是可燃物需要达到其着火点
14.下列各组离子在指定的溶液中,能大量共存的一组是( )
A.无色溶液中:
B.酸性溶液中:
C.pH=11 溶液中:
D.含有大量的溶液中:
15.工业上使用一种国产低温催化剂生产氢气的反应过程如下图所示:
下列说法正确的是( )
A.该微观反应过程中出现了四种氧化物
B.该反应中只有C、H两种元素的化合价都发生了改变
C.该反应中的个数比为2:1
D.该反应可以实现CO的100%转化
二、填空题(本大题共2小题,共20分)
16.(12分)按要求回答下列问题:
(1)按要求写出化学用语或含义
①2个碳酸根离子________; ②氦气________;
③表示________; ④表示________;
(2)配平下列化学方程式(数字“1”不省略)
①______________________________
②_______________NO________+________
17.(8分)A~G为实验室中未贴标签的7种溶液。已知7种溶液分别为:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、稀盐酸、氢氧化钠溶液和氢氧化钾溶液。
(1)G为蓝色,则G中溶质为(写化学式)__________。
(2)用pH试纸检测其余溶液的pH,测得E的pH=7, E为_________溶液。
(3)将A、B、C、D、F溶液两两混合,观察到的现象记录如右图所示(图中“——”代表无明显现象)。图中所发生的反应共有_______个。写出C与D反应的化学方程式_________。
三、实验题(本大题共2小题,共计27分)
18.(15分)为了证明在低温条件下是发生化学反应的催化剂,某同学进行如下探究:
【提出问题】在低温下是的催化剂吗?
【设计实验】实验室某同学称取一份0.5g和两份1.5g并设计如图实验,你认为大试管装___________,小试管装___________;若实验成功,实验时,A、B两个集气瓶内均有气泡产生,但不同的是___________。
【讨论交流】
(1)上述实验探究了催化剂的___________性质,在此基础上还要继续探究,实验是___________。
(2)在某同学设计的实验结束后,先撤走酒精灯,你会看到的现象是___________。请写出实验室用氯酸钾制氧气的符号表达式为___________;
19.(12分)NaCl和在不同温度下的溶解度数据如下表。
温度/℃ 0 10 20 30 40 50
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0
29.4 33.3 37.2 41.4 45.8 50.4
(1)50℃时NaCl的溶解度是_____g。
(2)如图是NaCl和的溶解度曲线,则的溶解度曲线是_____(填“a”或“b”)。t℃时,若饱和NaCl溶液和饱和溶液中溶质的质量相等,则下列说法不正确的是_____(填字母)。
A.两种溶液中溶剂的质量相等
B.两种溶液中溶质质量分数相等
C.t℃大于20℃
(3)20℃时,将mgNaCl不饱和溶液平均分为三份,并分别进行如下操作:
据此分析,x=_____,mgNaCl不饱和溶液中水的质量为_____g。
四、计算题(共8分)
20.“中国高铁,世界第一”。高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是,请计算生产5.9t镍,理论上需要氧化镍的质量?
答案以及解析
1.答案:D
解析:没有新物质生成的变化是物理变化;有新物质生成的变化是化学变化,物理变化和化学变化的本质区别是有无新物质生成,据此判断。
A、古人钻木取火,木材燃烧生成了二氧化碳等新物质,属于化学变化,不符合题意;
B、实验中氨水使酚酞试液变红,有新物质生成,属于化学变化,不符合题意;
C、烧瓷器的过程是瓷土中矿物从无规混合到成为部分结晶的过程,有新物质生产,是化学变化,不符合题意;
D、霓虹灯发光是稀有气体通电发光,没有新物质生成,属于物理变化,符合题意。
2.答案:A
解析:A、过年城市燃放烟花爆竹,会产生二氧化硫等污染物,污染空气,符合题意;
B、生活垃圾进行分类回收,可以实现资源的有效利用,减少污染物的排放,保护环境,不符合题意;
C、大力推进植树造林工程,可以改善空气质量,保护环境,不符合题意;
D、开发使用新型绿色能源,可以减少化石燃料的使用,减少污染物的排放,保护环境,不符合题意。
3.答案:C
解析:火柴头竖直向上时,火柴梗的温度上升的慢,不容易达到着火点,因此不容易持续燃烧;火柴头斜向下时,火焰不断加热火柴梗,容易达到火柴梗的着火点而继续燃烧,因此该现象说明燃烧的条件是可燃物温度达到着火点;
4.答案:D
解析:A、氧化物是指由两种元素组成且其中一种是氧元素的化合物,甘氨酸[],含有碳元素、氢元素、氮元素、氧元素,不属于氧化物,故A不正确;
B、甘氨酸[],甘氨酸中碳原子与氢原子的个数比为2:5,故B不正确;
C、甘氨酸是由甘氨酸分子构成的,故C不正确;
D、甘氨酸[],一个甘氨酸分子中含有个原子,故D正确。
5.答案:B
解析:A、人体的呼吸作用消耗氧气和葡萄糖,生成二氧化碳和水,属于化学变化,是自然界中碳循环和氧循环的一部分,不符合题意;
B、人体的呼吸作用消耗氧气产生二氧化碳,植物的光合作用消耗二氧化碳,释放氧气,因此两种循环之间彼此联系,符合题意;
C、自然界中的二氧化碳的主要来源是化石燃料的燃烧,因此减少化石燃料燃烧有助于减少二氧化碳的排放,不符合题意;
D、通过呼吸作用和光合作用实现碳循环和氧循环,可以维持自然界中氧气和二氧化碳的相对稳定,不符合题意;
6.答案:D
解析:由题图可知铷原子的最外层电子数是1,在化学反应中易失去一个电子形成,在化合物中显+1价,即氯化铷的化学式为RbCl,D不正确。
7.答案:B
解析:A、该装置不具有启普发生器的功能,因为左边与外界相通,不符合题意;
B、该装置可将固体置于多孔隔板上,通过长颈漏斗添加稀盐酸,通过开关止水夹,控制固液的接触和分离,实现反应的发生和停止,具有启普发生器的原理,符合题意;
C、该装置不具有启普发生器的功能,应增加止水夹,不符合题意;
D、该装置不具有启普发生器的功能,分液漏斗只能控制药品的滴加速率,从而控制反应速率,不符合题意。
8.答案:A
解析:A、根据题意,该水球是由水和可食用薄膜混合而成,属于混合物,选项正确;
B、该水球中的水在常温下是液体,选项错误;
C、构成物质的分子在不停的做无规则运动,不会静止不动,选项错误;
D、构成物质的分子之间都存在间隔,选项错误;
9.答案:D
解析:A、向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有现象,说明了X金属的活动性比铁弱,比银活泼,金属X可能是Cu,说法正确;
B、金属Y上③和④处均有明显现象,说明了Y金属位于铁、银的前面,金属Y可能是Zn,说法正确;
C、Y活动强于铁、银的前面,X金属的活动性比铁弱,所以金属Y的活动性强于X,说法正确;
D、向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有现象,说明了X金属的活动性比铁弱,比银活泼,金属Y上③和④处均有明显现象,说明了Y金属位于铁、银的前面,由此可得出金属的活动性强弱是:Y、Fe、X、Ag,说法错误。
10.答案:D
解析:A、氧化铝是氧化物,不属于金属材料,A说法错误,不符合题意;B、合金是金属和金属或金属和非金属熔合而成的具有金属特性的物质,生铁和钢就是铁和碳的合金,B说法错误,不符合题意;C、生锈的铁制品可以回收炼铁,节约资源、保护环境,C说法错误,不符合题意;D、合金的熔点一般比组成它的纯金属低,D说法正确,符合题意。故选D。
11.答案:D
解析:A、由图可知,燃煤烟气中的含量碱石灰比碳酸钙低,故碱石灰的脱硫效果比碳酸钙好,故A错误;
B、该实验为验证碳酸钙、碱石灰作为吸收剂对燃煤烟气进行脱硫处理的效果,故应该控制变量,实验时要称取3份质量相等的原煤,故B错误;
C、由图可知,碱石灰在300s时,燃煤烟气中的含量最低,脱硫效果已经达到最好,延长时间至500s,并不能提高二氧化硫的吸收效率,不可使碱石灰吸收二氧化硫的效果更好,故C错误;
D、碳酸钙脱硫原理为碳酸钙与二氧化硫和氧气在高温下反应生成硫酸钙和二氧化碳,反应方程式书写正确,故D正确;
12.答案:C
解析:A、苯并芘对人体有害,但是不易与人体血液中血红蛋白结合,不符合题意;
B、尼古丁对人体有害,但是不易与人体血液中血红蛋白结合,不符合题意;
C、一氧化碳能与血红蛋白结合,而且结合能力很强,大约是氧气的200-300倍。结合了一氧化碳的血红蛋白不能再与氧气结合,人就会缺氧窒息死亡。符合题意。
D、焦油不易与人体血液中血红蛋白结合,不符合题意;
13.答案:B
解析:A、热水可以吸收有毒的五氧化二磷,同时还具有加热白磷和隔绝氧气的作用,故选项错误;
B、向左推动注射器活塞,观察到烧瓶中白磷周围产生火星,说明过氧化钠与水反应生成氧气,故选项正确;
C、用酸性高锰酸钾溶液吸收白磷,溶液要倒吸到烧瓶中,故注射器活塞应往右拉,使烧瓶内压强减小,酸性高锰酸钾溶液倒吸,故选项错误;
D、通过实验装置可以判断此实验是探究燃烧条件之一是需要有氧气,故选项错误。
14.答案:B
解析:A、铜离子为蓝色的,不能存在于无色溶液中,选项不符合题意;
B、酸性溶液中含有氢离子,镁离子、钠离子、硫酸根离子、氯离子均不与氢离子发生反应,且四种离子之间不能生成沉淀、水或气体,能大量共存,选项符合题意;
C、pH=11溶液中含有氢氧根离子,氢氧根离子与铁离子能结合生成氢氧化铁沉淀,不能大量共存,选项不符合题意;
D、钡离子能与硫酸根离子能结合生成硫酸钡沉淀,不能大量共存,选项不符合题意。
15.答案:B
解析:由微观反应示意图可知,该反应是由水和一氧化碳在低温催化剂的作用下反应生成二氧化碳和氢气,化学方程式为:。
A、氧化物是由两种元素组成,且其中一种元素是氧元素的化合物,所以一氧化碳、水和二氧化碳均属于氧化物,故说法错误;
B、该反应中只有C、H两种元素的化合价都发生了改变,C的化合价由+2价变成+4价,H的化合价由+1价变成0价,O的化合价没有变化,故说法正确;
C、由化学方程式可知,参加反应的水分子与二氧化碳分子的个数比为1:1,故说法错误;
D、该反应不可以实现CO的100%转化,故说法错误;
16.答案:(1);He;在氧化亚铁中铁元素的化合价为+2价;一个铝离子(2)1;3;2;3;4;6;5;6
解析:(1)①离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故2个碳酸根离子表示为:;
②氦气是由氦原子构成的物质,由原子构成的物质化学式就是该元素的元素符号,故氦气表示为:;
③位于元素或原子团的正上方,表示元素或原子团的化合价。,故表示:在氧化亚铁中铁元素的化合价为+2价;
④由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,故表示为:一个铝离子;
(2)配平就是将反应前后原子的个数通过化学计量数使其相等。
①根据质量守恒定律, 化学反应前后,原子的种类和数目不变,反应物中含2个碳原子,故二氧化碳的化学计量数为2,反应物中含6个氢原子,故水的化学计量数为3,生成物中含7个氧原子,故氧气的化学计量数为3,化学方程式为:,故填:1;3;2;3;
②反应物中氢原子的个数是3,生成物中氢原子的个数是2,最小公倍数是6,故氨气的化学计量数为2,水的化学计量数为3,则一氧化氮的化学计量数为3,则氮气的化学计量数为,全部乘以2,则化学方程式为:,故填:4;6;5;6。
17.答案:(1) (2)氯化钠 (3)5/五;
解析:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、稀盐酸、氢氧化钠溶液和氢氧化钾溶液中硫酸铜溶液为蓝色,其他溶液为无色。澄清的石灰水、碳酸钠溶液、氢氧化钠溶液和氢氧化钾溶液为碱性,pH>7。氯化钠溶液为中性,pH=7,硫酸铜溶液、稀盐酸为酸性,pH<7。
(1)根据题干提供的信息分析可知,G是蓝色溶液,则G是硫酸铜溶液,其化学式为:;
(2)根据题干提供的信息分析可知,E的pH=7,则E是氯化钠溶液;
(3)C和D混合有气体产生,则C和D是盐酸和碳酸钠溶液,D和A混合有沉淀生成,则D是碳酸钠溶液,A是石灰水,C是盐酸。B和F是氢氧化钠溶液或氢氧化钾溶液,G是硫酸铜,E是氯化钠,带入验证,推断合理。
在图中,石灰水能和盐酸和碳酸钠反应,盐酸还能和氢氧化钠溶液及氢氧化钾反应,盐酸能和碳酸钠反应,共发生了5个反应。
C与D是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:。
18.答案:氯酸钾/;氯酸钾和二氧化锰(或、);B瓶中产生气泡速率比A瓶中快;能够改变反应速率;探究二氧化锰质量和化学性质在反应前后是否改变;水进入两支试管中,大试管炸裂;
解析:【设计实验】根据实验目的是在低温下是否是的催化剂,如图所示,大试管直接由酒精灯加热温度较高因此应装有氯酸钾,而小试管未直接加热温度较低因此装有氯酸钾和二氧化锰;实验时,A、B两个集气瓶内均有气泡产生,B瓶中产生气泡速率比A瓶中快,说明二氧化锰在低温下能够改变氯酸钾的反应速率。故填:氯酸钾;氯酸钾和二氧化锰;B瓶中产生气泡速率比A瓶中快;
【讨论交流】(1)上述实验探究了催化剂能够改变反应速率。故填:能够改变反应速率;
催化剂的定义是能够改变其他物质的反应速率而本身的质量和化学性质不变,故在此基础上还要继续探究,实验是:探究二氧化锰质量和化学性质在反应前后是否改变;
(2)在某同学设计的实验结束后,先撤走酒精灯,会使试管内的温度降低而气体体积变小,在气压差的作用下水会倒流入热的大试管内使大试管受热不均而炸裂,小试管温度较低不会炸裂,因此现象是:水进入两支试管中,大试管炸裂;
氯酸钾在二氧化锰作催化剂的条件下加热生成氯化钾和氧气,符号表达式是:。
19.答案:(1)37.0 (2)a;C (3)4.6;105
解析:(2)由题表中数据可知氯化铵的溶解度随温度变化较大,故应是曲线a。t℃时,氯化钠和氯化铵的溶解度相等,则10℃(3)第一份溶液蒸发10g水后析出1g固体,所得溶液为该温度下NaCl的饱和溶液,标记为①。第二份溶液蒸发的过程可看作在①的基础上再蒸发10g水,即从20℃氯化钠的饱和溶液中再蒸发10g水,20℃时氯化钠的溶解度是36g,蒸发10g水可析出3.6g氯化钠固体,则析出固体的总质量为1g+3.6g=4.6g。第三份溶液蒸发的过程也可看作在①的基础上蒸干,即从饱和溶液中又析出了9g固体,则蒸发的水的质量为10g×(9g÷3.6g)=25g,第一份溶液蒸发了10g水,即蒸干总共蒸发了35g水,即每份氯化钠溶液中都含有35g水、10g氯化钠,每份溶液是mg氯化钠溶液的三分之一,则mg氯化钠溶液中水的质量为35g×3=105g。
20.答案:解:设理论上需要氧化镍的质量为。
答:理论上需要氧化镍的质量为7.5t。
A卷
【满分:100分】
一、选择题:(本大题共15小题,每小题3分,共45分,给出的四个选项中,只有一项是符合题目要求的)
1.下列过程中,没有化学变化发生的是( )
A.古人钻木取火 B.探究分子不断运动
C.烧制陶瓷 D.霓虹灯发光
2.2022年全国生态环境保护大会强调,“十四五”时期,我国生态文明建设进入了以降碳为重点战略方向、推动减污降碳协同增效、促进经济社会发展全面绿色转型、实现生态环境质量改善由量变到质变的关键时期,下列措施不符合这一理念的是( )
A.过年城市燃放烟花爆竹 B.生活垃圾进行分类回收
C.大力推进植树造林工程 D.开发使用新型绿色能源
3.分别点燃相同两根火柴,将其中一根火柴头竖直向上,另一根火柴头倾斜向下,如图所示。小明发现第一根火柴不能持续燃烧,第二根火柴更容易持续燃烧。该实验现象说明,物质燃烧必须具备的条件是( )
A.物质具有可燃性 B.可燃物与充足氧气接触
C.可燃物的温度达到其自身的着火点 D.可燃物要倾斜放置
4.生物体中含有多种氨基酸,下列有关甘氨酸[](其分子结构如下图所示)的叙述正确的是( )
A.甘氨酸属于氧化物
B.甘氨酸中碳原子与氢原子的个数比为24:5
C.甘氨酸是由碳、氢、氧、氮四种原子构成的
D.一个甘氨酸分子中含有10个原子
5.生活中处处有化学,氧循环和碳循环是自然界中的重要循环。分析两种循环,其中不正确的是( )
A.碳循环和氧循环过程中均发生了化学变化,我们每个人了都参与碳循环和氧循环
B.两种循环各自独立,彼此之间无联系
C.通过减少化石燃料的使用和大力植树造林以控制二氧化碳的排放量
D.碳循环和氧循环有利于维持自然界中氧气和二氧化碳含量的相对稳定
6.铷(Rb)原子钟被称作北斗卫星的“心脏”、下图为铷原子的结构示意图,下列说法不正确的是( )
A.铷原子核内的质子数为37 B.铷原子在化学变化中容易失去1个电子
C.铷原子的核外电子分5层排布 D.氯化铷的化学式为
7.具有启普发生器功能的简易装置是( )
A. B. C. D.
8.国外大学生发明了一种能吃的“固体”水球,其原理与生蛋黄类似,将水包裹在一层由褐藻做成的可食用薄膜中。饮用时,将水球直接放入嘴中吃即可。下列说法中正确的是( )
A.该水球是混合物 B.该水球是水的固体
C.该水球中的水分子静止不动 D.该水球中的水分子间没有间隔
9.为了测定金属活动性强弱,某同学设计了如图所示的实验,向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有明显现象,金属Y上③和④处均有明显现象。关于该实验下列说法不正确的是( )
A.金属X可能是Cu
B.金属Y可能是Zn
C.金属Y的活动性强于X
D.四种金属的活动性强弱顺序为:
10.“中国制造”、“一带一路”的基础建设都需要用到大量金属材料。下列有关金属材料的说法正确的是( )
A.氧化铝属于金属材料 B.合金中只含金属元素
C.生锈的铁制品没有回收价值 D.合金的熔点一般比组成它的纯金属低
11.化工生产中常利用碳酸钙、碱石灰等作为吸收剂对燃煤烟气进行脱硫处理。实验测得燃煤烟气中的含量与时间的关系曲线如下图(ppm是一种浓度的表示方法)。下列说法中正确的是( )
A.碳酸钙的脱硫效果比碱石灰好
B.三次实验中固体总质量相同
C.延长时间至500s可使碱石灰吸收二氧化硫的效果更好
D.碳酸钙脱硫原理为:
12.烟草燃烧时释放的烟雾中含有3800多种已知化学物质,绝大部分对人体有害。其中易与人体血液中血红蛋白结合的一种有毒物质是( )
A.苯并芘 B.尼古丁 C.一氧化碳 D.焦油
13.白磷和五氧化二磷都具有毒性,某小组利用如图改进装置对燃烧条件进行了探究。实验时先打开弹簧夹,向左推动注射器活塞,观察到烧瓶中白磷周围产生火星;实验后利用酸性高锰酸钾溶液吸收残留的白磷。下列分析正确的是( )
A.热水的作用只是吸收有毒的五氧化二磷
B.过氧化钠与水作用生成氧气
C.为了吸收白磷需要将注射器活塞继续向左推
D.该实验探究的燃烧条件之一是可燃物需要达到其着火点
14.下列各组离子在指定的溶液中,能大量共存的一组是( )
A.无色溶液中:
B.酸性溶液中:
C.pH=11 溶液中:
D.含有大量的溶液中:
15.工业上使用一种国产低温催化剂生产氢气的反应过程如下图所示:
下列说法正确的是( )
A.该微观反应过程中出现了四种氧化物
B.该反应中只有C、H两种元素的化合价都发生了改变
C.该反应中的个数比为2:1
D.该反应可以实现CO的100%转化
二、填空题(本大题共2小题,共20分)
16.(12分)按要求回答下列问题:
(1)按要求写出化学用语或含义
①2个碳酸根离子________; ②氦气________;
③表示________; ④表示________;
(2)配平下列化学方程式(数字“1”不省略)
①______________________________
②_______________NO________+________
17.(8分)A~G为实验室中未贴标签的7种溶液。已知7种溶液分别为:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、稀盐酸、氢氧化钠溶液和氢氧化钾溶液。
(1)G为蓝色,则G中溶质为(写化学式)__________。
(2)用pH试纸检测其余溶液的pH,测得E的pH=7, E为_________溶液。
(3)将A、B、C、D、F溶液两两混合,观察到的现象记录如右图所示(图中“——”代表无明显现象)。图中所发生的反应共有_______个。写出C与D反应的化学方程式_________。
三、实验题(本大题共2小题,共计27分)
18.(15分)为了证明在低温条件下是发生化学反应的催化剂,某同学进行如下探究:
【提出问题】在低温下是的催化剂吗?
【设计实验】实验室某同学称取一份0.5g和两份1.5g并设计如图实验,你认为大试管装___________,小试管装___________;若实验成功,实验时,A、B两个集气瓶内均有气泡产生,但不同的是___________。
【讨论交流】
(1)上述实验探究了催化剂的___________性质,在此基础上还要继续探究,实验是___________。
(2)在某同学设计的实验结束后,先撤走酒精灯,你会看到的现象是___________。请写出实验室用氯酸钾制氧气的符号表达式为___________;
19.(12分)NaCl和在不同温度下的溶解度数据如下表。
温度/℃ 0 10 20 30 40 50
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0
29.4 33.3 37.2 41.4 45.8 50.4
(1)50℃时NaCl的溶解度是_____g。
(2)如图是NaCl和的溶解度曲线,则的溶解度曲线是_____(填“a”或“b”)。t℃时,若饱和NaCl溶液和饱和溶液中溶质的质量相等,则下列说法不正确的是_____(填字母)。
A.两种溶液中溶剂的质量相等
B.两种溶液中溶质质量分数相等
C.t℃大于20℃
(3)20℃时,将mgNaCl不饱和溶液平均分为三份,并分别进行如下操作:
据此分析,x=_____,mgNaCl不饱和溶液中水的质量为_____g。
四、计算题(共8分)
20.“中国高铁,世界第一”。高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是,请计算生产5.9t镍,理论上需要氧化镍的质量?
答案以及解析
1.答案:D
解析:没有新物质生成的变化是物理变化;有新物质生成的变化是化学变化,物理变化和化学变化的本质区别是有无新物质生成,据此判断。
A、古人钻木取火,木材燃烧生成了二氧化碳等新物质,属于化学变化,不符合题意;
B、实验中氨水使酚酞试液变红,有新物质生成,属于化学变化,不符合题意;
C、烧瓷器的过程是瓷土中矿物从无规混合到成为部分结晶的过程,有新物质生产,是化学变化,不符合题意;
D、霓虹灯发光是稀有气体通电发光,没有新物质生成,属于物理变化,符合题意。
2.答案:A
解析:A、过年城市燃放烟花爆竹,会产生二氧化硫等污染物,污染空气,符合题意;
B、生活垃圾进行分类回收,可以实现资源的有效利用,减少污染物的排放,保护环境,不符合题意;
C、大力推进植树造林工程,可以改善空气质量,保护环境,不符合题意;
D、开发使用新型绿色能源,可以减少化石燃料的使用,减少污染物的排放,保护环境,不符合题意。
3.答案:C
解析:火柴头竖直向上时,火柴梗的温度上升的慢,不容易达到着火点,因此不容易持续燃烧;火柴头斜向下时,火焰不断加热火柴梗,容易达到火柴梗的着火点而继续燃烧,因此该现象说明燃烧的条件是可燃物温度达到着火点;
4.答案:D
解析:A、氧化物是指由两种元素组成且其中一种是氧元素的化合物,甘氨酸[],含有碳元素、氢元素、氮元素、氧元素,不属于氧化物,故A不正确;
B、甘氨酸[],甘氨酸中碳原子与氢原子的个数比为2:5,故B不正确;
C、甘氨酸是由甘氨酸分子构成的,故C不正确;
D、甘氨酸[],一个甘氨酸分子中含有个原子,故D正确。
5.答案:B
解析:A、人体的呼吸作用消耗氧气和葡萄糖,生成二氧化碳和水,属于化学变化,是自然界中碳循环和氧循环的一部分,不符合题意;
B、人体的呼吸作用消耗氧气产生二氧化碳,植物的光合作用消耗二氧化碳,释放氧气,因此两种循环之间彼此联系,符合题意;
C、自然界中的二氧化碳的主要来源是化石燃料的燃烧,因此减少化石燃料燃烧有助于减少二氧化碳的排放,不符合题意;
D、通过呼吸作用和光合作用实现碳循环和氧循环,可以维持自然界中氧气和二氧化碳的相对稳定,不符合题意;
6.答案:D
解析:由题图可知铷原子的最外层电子数是1,在化学反应中易失去一个电子形成,在化合物中显+1价,即氯化铷的化学式为RbCl,D不正确。
7.答案:B
解析:A、该装置不具有启普发生器的功能,因为左边与外界相通,不符合题意;
B、该装置可将固体置于多孔隔板上,通过长颈漏斗添加稀盐酸,通过开关止水夹,控制固液的接触和分离,实现反应的发生和停止,具有启普发生器的原理,符合题意;
C、该装置不具有启普发生器的功能,应增加止水夹,不符合题意;
D、该装置不具有启普发生器的功能,分液漏斗只能控制药品的滴加速率,从而控制反应速率,不符合题意。
8.答案:A
解析:A、根据题意,该水球是由水和可食用薄膜混合而成,属于混合物,选项正确;
B、该水球中的水在常温下是液体,选项错误;
C、构成物质的分子在不停的做无规则运动,不会静止不动,选项错误;
D、构成物质的分子之间都存在间隔,选项错误;
9.答案:D
解析:A、向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有现象,说明了X金属的活动性比铁弱,比银活泼,金属X可能是Cu,说法正确;
B、金属Y上③和④处均有明显现象,说明了Y金属位于铁、银的前面,金属Y可能是Zn,说法正确;
C、Y活动强于铁、银的前面,X金属的活动性比铁弱,所以金属Y的活动性强于X,说法正确;
D、向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有现象,说明了X金属的活动性比铁弱,比银活泼,金属Y上③和④处均有明显现象,说明了Y金属位于铁、银的前面,由此可得出金属的活动性强弱是:Y、Fe、X、Ag,说法错误。
10.答案:D
解析:A、氧化铝是氧化物,不属于金属材料,A说法错误,不符合题意;B、合金是金属和金属或金属和非金属熔合而成的具有金属特性的物质,生铁和钢就是铁和碳的合金,B说法错误,不符合题意;C、生锈的铁制品可以回收炼铁,节约资源、保护环境,C说法错误,不符合题意;D、合金的熔点一般比组成它的纯金属低,D说法正确,符合题意。故选D。
11.答案:D
解析:A、由图可知,燃煤烟气中的含量碱石灰比碳酸钙低,故碱石灰的脱硫效果比碳酸钙好,故A错误;
B、该实验为验证碳酸钙、碱石灰作为吸收剂对燃煤烟气进行脱硫处理的效果,故应该控制变量,实验时要称取3份质量相等的原煤,故B错误;
C、由图可知,碱石灰在300s时,燃煤烟气中的含量最低,脱硫效果已经达到最好,延长时间至500s,并不能提高二氧化硫的吸收效率,不可使碱石灰吸收二氧化硫的效果更好,故C错误;
D、碳酸钙脱硫原理为碳酸钙与二氧化硫和氧气在高温下反应生成硫酸钙和二氧化碳,反应方程式书写正确,故D正确;
12.答案:C
解析:A、苯并芘对人体有害,但是不易与人体血液中血红蛋白结合,不符合题意;
B、尼古丁对人体有害,但是不易与人体血液中血红蛋白结合,不符合题意;
C、一氧化碳能与血红蛋白结合,而且结合能力很强,大约是氧气的200-300倍。结合了一氧化碳的血红蛋白不能再与氧气结合,人就会缺氧窒息死亡。符合题意。
D、焦油不易与人体血液中血红蛋白结合,不符合题意;
13.答案:B
解析:A、热水可以吸收有毒的五氧化二磷,同时还具有加热白磷和隔绝氧气的作用,故选项错误;
B、向左推动注射器活塞,观察到烧瓶中白磷周围产生火星,说明过氧化钠与水反应生成氧气,故选项正确;
C、用酸性高锰酸钾溶液吸收白磷,溶液要倒吸到烧瓶中,故注射器活塞应往右拉,使烧瓶内压强减小,酸性高锰酸钾溶液倒吸,故选项错误;
D、通过实验装置可以判断此实验是探究燃烧条件之一是需要有氧气,故选项错误。
14.答案:B
解析:A、铜离子为蓝色的,不能存在于无色溶液中,选项不符合题意;
B、酸性溶液中含有氢离子,镁离子、钠离子、硫酸根离子、氯离子均不与氢离子发生反应,且四种离子之间不能生成沉淀、水或气体,能大量共存,选项符合题意;
C、pH=11溶液中含有氢氧根离子,氢氧根离子与铁离子能结合生成氢氧化铁沉淀,不能大量共存,选项不符合题意;
D、钡离子能与硫酸根离子能结合生成硫酸钡沉淀,不能大量共存,选项不符合题意。
15.答案:B
解析:由微观反应示意图可知,该反应是由水和一氧化碳在低温催化剂的作用下反应生成二氧化碳和氢气,化学方程式为:。
A、氧化物是由两种元素组成,且其中一种元素是氧元素的化合物,所以一氧化碳、水和二氧化碳均属于氧化物,故说法错误;
B、该反应中只有C、H两种元素的化合价都发生了改变,C的化合价由+2价变成+4价,H的化合价由+1价变成0价,O的化合价没有变化,故说法正确;
C、由化学方程式可知,参加反应的水分子与二氧化碳分子的个数比为1:1,故说法错误;
D、该反应不可以实现CO的100%转化,故说法错误;
16.答案:(1);He;在氧化亚铁中铁元素的化合价为+2价;一个铝离子(2)1;3;2;3;4;6;5;6
解析:(1)①离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故2个碳酸根离子表示为:;
②氦气是由氦原子构成的物质,由原子构成的物质化学式就是该元素的元素符号,故氦气表示为:;
③位于元素或原子团的正上方,表示元素或原子团的化合价。,故表示:在氧化亚铁中铁元素的化合价为+2价;
④由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,故表示为:一个铝离子;
(2)配平就是将反应前后原子的个数通过化学计量数使其相等。
①根据质量守恒定律, 化学反应前后,原子的种类和数目不变,反应物中含2个碳原子,故二氧化碳的化学计量数为2,反应物中含6个氢原子,故水的化学计量数为3,生成物中含7个氧原子,故氧气的化学计量数为3,化学方程式为:,故填:1;3;2;3;
②反应物中氢原子的个数是3,生成物中氢原子的个数是2,最小公倍数是6,故氨气的化学计量数为2,水的化学计量数为3,则一氧化氮的化学计量数为3,则氮气的化学计量数为,全部乘以2,则化学方程式为:,故填:4;6;5;6。
17.答案:(1) (2)氯化钠 (3)5/五;
解析:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、稀盐酸、氢氧化钠溶液和氢氧化钾溶液中硫酸铜溶液为蓝色,其他溶液为无色。澄清的石灰水、碳酸钠溶液、氢氧化钠溶液和氢氧化钾溶液为碱性,pH>7。氯化钠溶液为中性,pH=7,硫酸铜溶液、稀盐酸为酸性,pH<7。
(1)根据题干提供的信息分析可知,G是蓝色溶液,则G是硫酸铜溶液,其化学式为:;
(2)根据题干提供的信息分析可知,E的pH=7,则E是氯化钠溶液;
(3)C和D混合有气体产生,则C和D是盐酸和碳酸钠溶液,D和A混合有沉淀生成,则D是碳酸钠溶液,A是石灰水,C是盐酸。B和F是氢氧化钠溶液或氢氧化钾溶液,G是硫酸铜,E是氯化钠,带入验证,推断合理。
在图中,石灰水能和盐酸和碳酸钠反应,盐酸还能和氢氧化钠溶液及氢氧化钾反应,盐酸能和碳酸钠反应,共发生了5个反应。
C与D是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:。
18.答案:氯酸钾/;氯酸钾和二氧化锰(或、);B瓶中产生气泡速率比A瓶中快;能够改变反应速率;探究二氧化锰质量和化学性质在反应前后是否改变;水进入两支试管中,大试管炸裂;
解析:【设计实验】根据实验目的是在低温下是否是的催化剂,如图所示,大试管直接由酒精灯加热温度较高因此应装有氯酸钾,而小试管未直接加热温度较低因此装有氯酸钾和二氧化锰;实验时,A、B两个集气瓶内均有气泡产生,B瓶中产生气泡速率比A瓶中快,说明二氧化锰在低温下能够改变氯酸钾的反应速率。故填:氯酸钾;氯酸钾和二氧化锰;B瓶中产生气泡速率比A瓶中快;
【讨论交流】(1)上述实验探究了催化剂能够改变反应速率。故填:能够改变反应速率;
催化剂的定义是能够改变其他物质的反应速率而本身的质量和化学性质不变,故在此基础上还要继续探究,实验是:探究二氧化锰质量和化学性质在反应前后是否改变;
(2)在某同学设计的实验结束后,先撤走酒精灯,会使试管内的温度降低而气体体积变小,在气压差的作用下水会倒流入热的大试管内使大试管受热不均而炸裂,小试管温度较低不会炸裂,因此现象是:水进入两支试管中,大试管炸裂;
氯酸钾在二氧化锰作催化剂的条件下加热生成氯化钾和氧气,符号表达式是:。
19.答案:(1)37.0 (2)a;C (3)4.6;105
解析:(2)由题表中数据可知氯化铵的溶解度随温度变化较大,故应是曲线a。t℃时,氯化钠和氯化铵的溶解度相等,则10℃
20.答案:解:设理论上需要氧化镍的质量为。
答:理论上需要氧化镍的质量为7.5t。
同课章节目录
