重庆市石柱县第一初级中学2024-2025学年九年级下学期期中考试化学试题(含答案)
文档属性
| 名称 | 重庆市石柱县第一初级中学2024-2025学年九年级下学期期中考试化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 934.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-30 15:53:31 | ||
图片预览


文档简介
石柱第一初级中学2025年春定时作业(2)
化学试题
本次考试可能用到的:C-12 H-1 Cl-35.5 Ca-40
一、选择题(每小题只有一个正确答案。每小题2分,15题共30分)
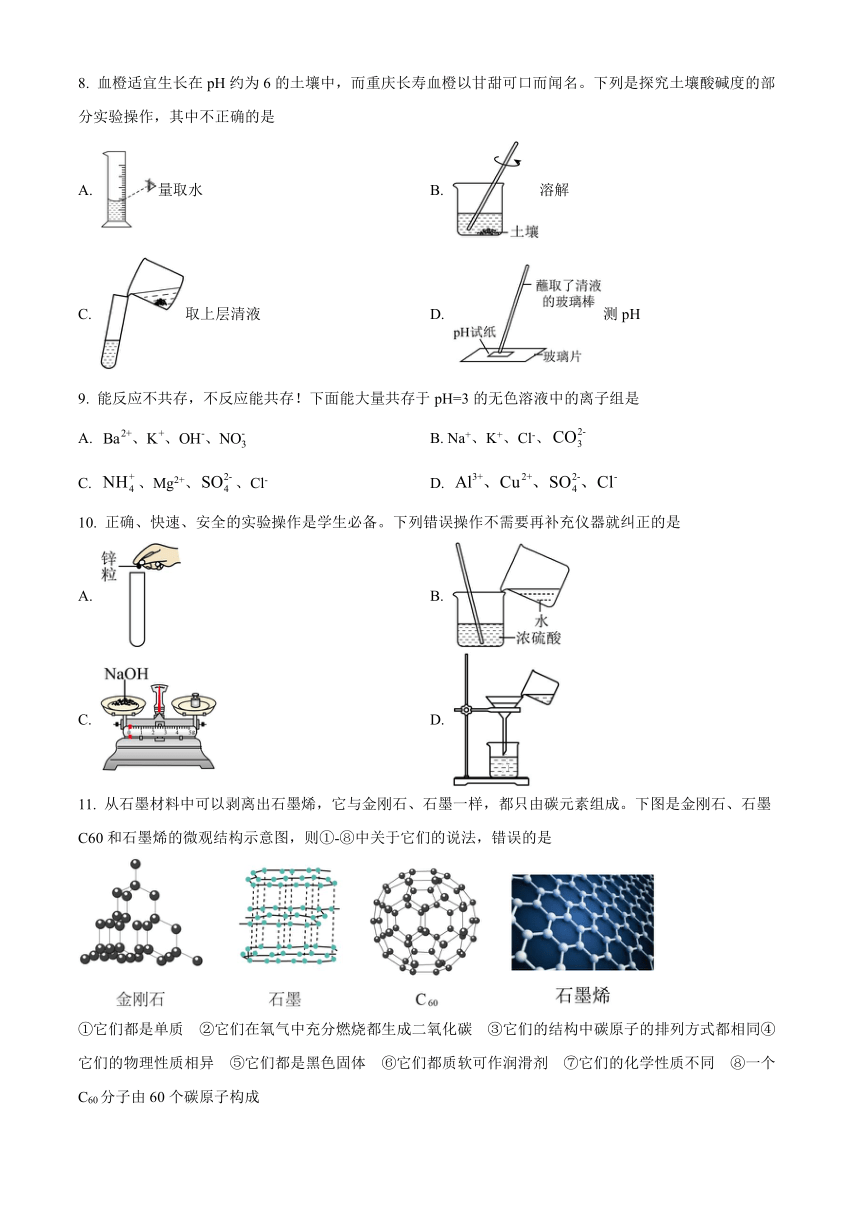
1. 《茶经·三之造》是唐代陆羽所著,书中记载人们常喝的茶叶的制作过程:“晴采之,蒸之,捣之,拍之,焙之,穿之,封之,茶之干矣”。则下列操作中最有可能发生化学变化的是
A. 采之 B. 捣之 C. 焙之 D. 封之
2. 靓仔们,上个月消防队在我校做了消防宣传,讲到的干粉灭火器,它是利用压缩气体吹干粉(主要含有磷酸二氢铵)来灭火,若气体是可利用的空气中含量最多的气体,则该气体是
A. H2O B. O2 C. 稀有气体 D. N2
3. 好的生活习惯成就健康人生。下列饮食习惯科学合理的是
A. 大量出汗后常饮用含无机盐的饮料 B. 不忍浪费,即使食物霉变仍然食用
C. 为了保持身材,只吃蔬菜和水果 D. 将“地沟油”加工处理后再食用
4. 用下列四套实验装置制取O2气体,由于装置错误导致可能收集不到O2的是
A. B. C. D.
5. 我欲除去N2中混有的少量CO2、CO、H2和水蒸气,需进行以下操作:①通过NaOH溶液,②通过浓H2SO4,③通过灼热的CuO。骄子们,告诉俺,正确的操作顺序是
A ①②③ B. ①③② C. ②①③ D. ③①②
6. 下图是一个化学反应的微观示意图,你能从下面示意图中获取的正确信息的是
A. 反应前后原子的种类与数目发生改变 B. 反应前两种分子的个数比是1:2
C. 反应前后分子种类不发生改变 D. 该反应的基本类型是化合反应
7. 煤、石油、天然气是重要的三大化石燃料,下列关于化石燃料的叙述错误的是
A. 石油分馏可得到多种产品 B. 石油是一种纯净物
C. 煤、石油、天然气是不可再生能源 D. 天然气是燃料中最清洁的
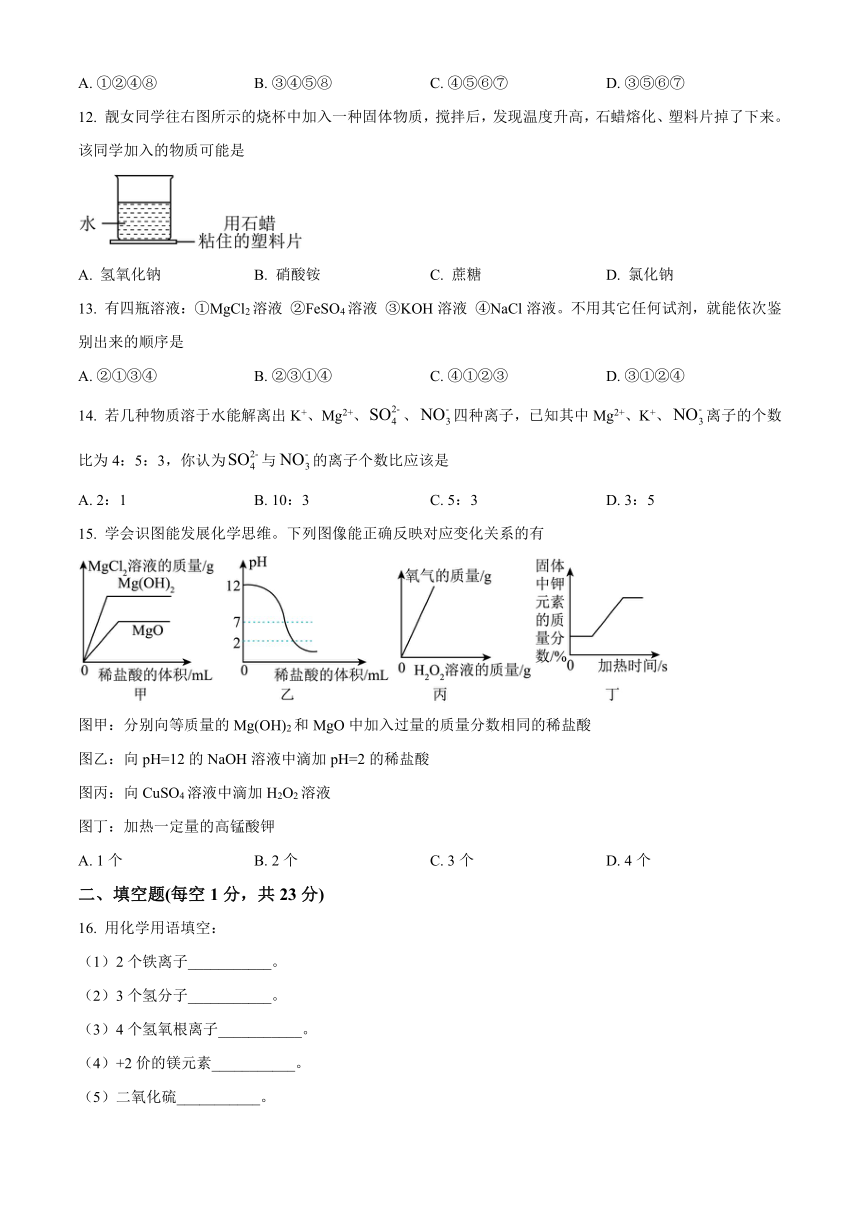
8. 血橙适宜生长在pH约为6的土壤中,而重庆长寿血橙以甘甜可口而闻名。下列是探究土壤酸碱度的部分实验操作,其中不正确的是
A. 量取水 B. 溶解
C. 取上层清液 D. 测pH
9. 能反应不共存,不反应能共存!下面能大量共存于pH=3的无色溶液中的离子组是
A. B. Na+、K+、Cl-、
C. 、Mg2+、、Cl- D.
10. 正确、快速、安全的实验操作是学生必备。下列错误操作不需要再补充仪器就纠正的是
A. B.
C. D.
11. 从石墨材料中可以剥离出石墨烯,它与金刚石、石墨一样,都只由碳元素组成。下图是金刚石、石墨C60和石墨烯的微观结构示意图,则①-⑧中关于它们的说法,错误的是
①它们都是单质 ②它们在氧气中充分燃烧都生成二氧化碳 ③它们的结构中碳原子的排列方式都相同④它们的物理性质相异 ⑤它们都是黑色固体 ⑥它们都质软可作润滑剂 ⑦它们的化学性质不同 ⑧一个C60分子由60个碳原子构成
A. ①②④⑧ B. ③④⑤⑧ C. ④⑤⑥⑦ D. ③⑤⑥⑦
12. 靓女同学往右图所示的烧杯中加入一种固体物质,搅拌后,发现温度升高,石蜡熔化、塑料片掉了下来。该同学加入的物质可能是
A. 氢氧化钠 B. 硝酸铵 C. 蔗糖 D. 氯化钠
13. 有四瓶溶液:①MgCl2溶液 ②FeSO4溶液 ③KOH溶液 ④NaCl溶液。不用其它任何试剂,就能依次鉴别出来的顺序是
A. ②①③④ B. ②③①④ C. ④①②③ D. ③①②④
14. 若几种物质溶于水能解离出K+、Mg2+、、四种离子,已知其中Mg2+、K+、离子的个数比为4:5:3,你认为与的离子个数比应该是
A. 2:1 B. 10:3 C. 5:3 D. 3:5
15. 学会识图能发展化学思维。下列图像能正确反映对应变化关系的有
图甲:分别向等质量的Mg(OH)2和MgO中加入过量的质量分数相同的稀盐酸
图乙:向pH=12的NaOH溶液中滴加pH=2的稀盐酸
图丙:向CuSO4溶液中滴加H2O2溶液
图丁:加热一定量的高锰酸钾
A. 1个 B. 2个 C. 3个 D. 4个
二、填空题(每空1分,共23分)
16. 用化学用语填空:
(1)2个铁离子___________。
(2)3个氢分子___________。
(3)4个氢氧根离子___________。
(4)+2价的镁元素___________。
(5)二氧化硫___________。
17. 某校五楼寝室,学生熄灯就寝后,一同学违规点蜡烛看书,不小心引燃蚊帐,导致火灾。就此事件回答下列问题:
(1)从物质燃烧的条件看,蚊帐是_____。
(2)该同学慌忙打开房门,致使火势迅速扩大,其原因是_____。
(3)同寝室同学惊醒后,一边拨打“119”,一边采取了下列自救措施,其中正确的是_____(填序号).A用湿毛巾捂住口鼻迅速逃离 B跳楼逃生 C藏在桌子底下等待救援
(4)消防队员用高压水枪喷水将大火扑灭,水灭火的原理是_____。
18. 如图为A、B两种固体物质的溶解度曲线。
(1)在___℃时,A、B两种物质的溶解度相等。
(2)t2℃时,100g水中溶解____gA物质恰好饱和,该饱和溶液中溶质的质量分数为_______。若要把该饱和溶液稀释成质量分数为1 0%的溶液,应加水______g。
(3)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是_______。
19. 我校化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号为A、B、C、D、E,然后两两混合进行实验,其部分实验现象如下表所示(说明:硫酸钙看作可溶物)
实验 A+B B+C B+D C+D
现象 产生沉淀 产生气体 产生沉淀 产生沉淀
(1)写出E中溶质的化学式:___________。
(2)写出A与B反应的化学方程式:___________。
(3)写出B与C反应的化学方程式:___________。
(4)写出C与D反应的化学方程式:___________。
20. 金属的发现与使用推动社会的发展,部分金属的发展历程如图所示。请回答下列问题:
(1)据上图分析,金属的发现历程与金属的___________有关。
(2)铝被广泛应用,除了因为改进铝的冶炼方法使其成本降低,还由于铝具有很好的抗腐蚀性,铝制品抗腐蚀的原因是___________(填化学方程式)。
(3)我国早在西汉时期就有“湿法炼铜”的记载,在《淮南万毕术》一书中就写道“曾青(硫酸铜溶液)得铁则化为铜”,请写出与之相关的化学方程式:___________。
(4)一定能验证Fe、R、Cu(R活动性位于铁、铜之间)金属活动性顺序的是___________(填字母)。
A. Fe、Cu、R、稀盐酸 B. 硝酸亚铁溶液、Cu、R盐溶液 C. Fe、R盐溶液、Cu
(5)话说:新教材新气象,新旧教材在编排上有很多变化,其中关于实验的小图标是一个比较新颖的地方。请问:新教材的诸多演示实验和分组实验中,必不可少的图标是___________。
A. 护目镜 B. 明火
C. 排风 D. 洗手
三、实验探究题(每空1分,共12分)
21. 根据电解水的实验装置图完成下列问题:
(1)指出电源的正、负极,左边为___________,右边为___________,事先往水里加少量硫酸钠,目的是为了___________。
(2)左边试管中产生的是___________,右边试管中产生的是___________,其反应的化学方程式___________,由以上实验事实得出结论:说明水是由___________组成的。
22. 某化学兴趣小组按照课本上的实验对质量守恒定律进行探究
(1)充分反应后冷却,天平不平衡的是___________,分析原因___________。
(2)A中气球的变化情况是___________
(3)B中与之相关的化学方程式:___________。
(4)若把C中的药品换为硫酸铜溶液和硝酸钠溶液进行实验,天平始终保持平衡。能否验证质量守恒定律?理由是___________。
四、计算题
23. 甄蔻琪同学将150mL稀盐酸(密度为1.1g/cm3)加入盛有53g石灰石的烧杯中,恰好完全反应(杂质不溶于水,也不与稀盐酸及生成物反应),反应后烧杯中物质的总质量为196g。计算:
(1)反应生成二氧化碳的质量___________。
(2)反应结束后溶液中溶质的质量分数。
参考答案
1-15:CDACD DBACB DABCB
16.(1)2Fe3+
(2)3H2 (3)4OH-
(4)
(5)SO2
17. ①. 可燃物 ②. 增加了氧气的量 ③. A ④. 将可燃物的温度降低到到着火点以下
18.①. t1 ②. 25 ③. 20% ④. 125 ⑤. B
19.(1)NaOH
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
(4)H2SO4+BaCl2=BaSO4↓+2HCl
20.(1)金属活动性
(2)4Al+3O2=2Al2O3
Fe+CuSO4=FeSO4+Cu
C
(5)AD
21.(1) ①. 负极 ②. 正极 ③. 增强水的导电性
(2) ①. 氢气##H2 ②. 氧气##O2 ③. ④. 氢元素和氧元素
22.(1) ①. B ②. B装置中反应生成的二氧化碳逸散到空气中 (2)先膨胀后变小
(3)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(4)不能验证质量守恒定律。理由是硫酸铜溶液和硝酸钠溶液混合后不会发生化学反应
23.(1)22g##22克
(2)设石灰石中碳酸钙的质量为x,生成氯化钙的质量为y。
x=50g
y=55.5g
反应后溶液的质量=196g (53g 50g)=193g(杂质质量为53g 50g=3g,溶液质量等于反应后总质量减去杂质质量)。则反应结束后溶液中溶质(氯化钙)的质量分数为。
答:反应结束后溶液中溶质的质量分数为28.8%。
化学试题
本次考试可能用到的:C-12 H-1 Cl-35.5 Ca-40
一、选择题(每小题只有一个正确答案。每小题2分,15题共30分)
1. 《茶经·三之造》是唐代陆羽所著,书中记载人们常喝的茶叶的制作过程:“晴采之,蒸之,捣之,拍之,焙之,穿之,封之,茶之干矣”。则下列操作中最有可能发生化学变化的是
A. 采之 B. 捣之 C. 焙之 D. 封之
2. 靓仔们,上个月消防队在我校做了消防宣传,讲到的干粉灭火器,它是利用压缩气体吹干粉(主要含有磷酸二氢铵)来灭火,若气体是可利用的空气中含量最多的气体,则该气体是
A. H2O B. O2 C. 稀有气体 D. N2
3. 好的生活习惯成就健康人生。下列饮食习惯科学合理的是
A. 大量出汗后常饮用含无机盐的饮料 B. 不忍浪费,即使食物霉变仍然食用
C. 为了保持身材,只吃蔬菜和水果 D. 将“地沟油”加工处理后再食用
4. 用下列四套实验装置制取O2气体,由于装置错误导致可能收集不到O2的是
A. B. C. D.
5. 我欲除去N2中混有的少量CO2、CO、H2和水蒸气,需进行以下操作:①通过NaOH溶液,②通过浓H2SO4,③通过灼热的CuO。骄子们,告诉俺,正确的操作顺序是
A ①②③ B. ①③② C. ②①③ D. ③①②
6. 下图是一个化学反应的微观示意图,你能从下面示意图中获取的正确信息的是
A. 反应前后原子的种类与数目发生改变 B. 反应前两种分子的个数比是1:2
C. 反应前后分子种类不发生改变 D. 该反应的基本类型是化合反应
7. 煤、石油、天然气是重要的三大化石燃料,下列关于化石燃料的叙述错误的是
A. 石油分馏可得到多种产品 B. 石油是一种纯净物
C. 煤、石油、天然气是不可再生能源 D. 天然气是燃料中最清洁的
8. 血橙适宜生长在pH约为6的土壤中,而重庆长寿血橙以甘甜可口而闻名。下列是探究土壤酸碱度的部分实验操作,其中不正确的是
A. 量取水 B. 溶解
C. 取上层清液 D. 测pH
9. 能反应不共存,不反应能共存!下面能大量共存于pH=3的无色溶液中的离子组是
A. B. Na+、K+、Cl-、
C. 、Mg2+、、Cl- D.
10. 正确、快速、安全的实验操作是学生必备。下列错误操作不需要再补充仪器就纠正的是
A. B.
C. D.
11. 从石墨材料中可以剥离出石墨烯,它与金刚石、石墨一样,都只由碳元素组成。下图是金刚石、石墨C60和石墨烯的微观结构示意图,则①-⑧中关于它们的说法,错误的是
①它们都是单质 ②它们在氧气中充分燃烧都生成二氧化碳 ③它们的结构中碳原子的排列方式都相同④它们的物理性质相异 ⑤它们都是黑色固体 ⑥它们都质软可作润滑剂 ⑦它们的化学性质不同 ⑧一个C60分子由60个碳原子构成
A. ①②④⑧ B. ③④⑤⑧ C. ④⑤⑥⑦ D. ③⑤⑥⑦
12. 靓女同学往右图所示的烧杯中加入一种固体物质,搅拌后,发现温度升高,石蜡熔化、塑料片掉了下来。该同学加入的物质可能是
A. 氢氧化钠 B. 硝酸铵 C. 蔗糖 D. 氯化钠
13. 有四瓶溶液:①MgCl2溶液 ②FeSO4溶液 ③KOH溶液 ④NaCl溶液。不用其它任何试剂,就能依次鉴别出来的顺序是
A. ②①③④ B. ②③①④ C. ④①②③ D. ③①②④
14. 若几种物质溶于水能解离出K+、Mg2+、、四种离子,已知其中Mg2+、K+、离子的个数比为4:5:3,你认为与的离子个数比应该是
A. 2:1 B. 10:3 C. 5:3 D. 3:5
15. 学会识图能发展化学思维。下列图像能正确反映对应变化关系的有
图甲:分别向等质量的Mg(OH)2和MgO中加入过量的质量分数相同的稀盐酸
图乙:向pH=12的NaOH溶液中滴加pH=2的稀盐酸
图丙:向CuSO4溶液中滴加H2O2溶液
图丁:加热一定量的高锰酸钾
A. 1个 B. 2个 C. 3个 D. 4个
二、填空题(每空1分,共23分)
16. 用化学用语填空:
(1)2个铁离子___________。
(2)3个氢分子___________。
(3)4个氢氧根离子___________。
(4)+2价的镁元素___________。
(5)二氧化硫___________。
17. 某校五楼寝室,学生熄灯就寝后,一同学违规点蜡烛看书,不小心引燃蚊帐,导致火灾。就此事件回答下列问题:
(1)从物质燃烧的条件看,蚊帐是_____。
(2)该同学慌忙打开房门,致使火势迅速扩大,其原因是_____。
(3)同寝室同学惊醒后,一边拨打“119”,一边采取了下列自救措施,其中正确的是_____(填序号).A用湿毛巾捂住口鼻迅速逃离 B跳楼逃生 C藏在桌子底下等待救援
(4)消防队员用高压水枪喷水将大火扑灭,水灭火的原理是_____。
18. 如图为A、B两种固体物质的溶解度曲线。
(1)在___℃时,A、B两种物质的溶解度相等。
(2)t2℃时,100g水中溶解____gA物质恰好饱和,该饱和溶液中溶质的质量分数为_______。若要把该饱和溶液稀释成质量分数为1 0%的溶液,应加水______g。
(3)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是_______。
19. 我校化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号为A、B、C、D、E,然后两两混合进行实验,其部分实验现象如下表所示(说明:硫酸钙看作可溶物)
实验 A+B B+C B+D C+D
现象 产生沉淀 产生气体 产生沉淀 产生沉淀
(1)写出E中溶质的化学式:___________。
(2)写出A与B反应的化学方程式:___________。
(3)写出B与C反应的化学方程式:___________。
(4)写出C与D反应的化学方程式:___________。
20. 金属的发现与使用推动社会的发展,部分金属的发展历程如图所示。请回答下列问题:
(1)据上图分析,金属的发现历程与金属的___________有关。
(2)铝被广泛应用,除了因为改进铝的冶炼方法使其成本降低,还由于铝具有很好的抗腐蚀性,铝制品抗腐蚀的原因是___________(填化学方程式)。
(3)我国早在西汉时期就有“湿法炼铜”的记载,在《淮南万毕术》一书中就写道“曾青(硫酸铜溶液)得铁则化为铜”,请写出与之相关的化学方程式:___________。
(4)一定能验证Fe、R、Cu(R活动性位于铁、铜之间)金属活动性顺序的是___________(填字母)。
A. Fe、Cu、R、稀盐酸 B. 硝酸亚铁溶液、Cu、R盐溶液 C. Fe、R盐溶液、Cu
(5)话说:新教材新气象,新旧教材在编排上有很多变化,其中关于实验的小图标是一个比较新颖的地方。请问:新教材的诸多演示实验和分组实验中,必不可少的图标是___________。
A. 护目镜 B. 明火
C. 排风 D. 洗手
三、实验探究题(每空1分,共12分)
21. 根据电解水的实验装置图完成下列问题:
(1)指出电源的正、负极,左边为___________,右边为___________,事先往水里加少量硫酸钠,目的是为了___________。
(2)左边试管中产生的是___________,右边试管中产生的是___________,其反应的化学方程式___________,由以上实验事实得出结论:说明水是由___________组成的。
22. 某化学兴趣小组按照课本上的实验对质量守恒定律进行探究
(1)充分反应后冷却,天平不平衡的是___________,分析原因___________。
(2)A中气球的变化情况是___________
(3)B中与之相关的化学方程式:___________。
(4)若把C中的药品换为硫酸铜溶液和硝酸钠溶液进行实验,天平始终保持平衡。能否验证质量守恒定律?理由是___________。
四、计算题
23. 甄蔻琪同学将150mL稀盐酸(密度为1.1g/cm3)加入盛有53g石灰石的烧杯中,恰好完全反应(杂质不溶于水,也不与稀盐酸及生成物反应),反应后烧杯中物质的总质量为196g。计算:
(1)反应生成二氧化碳的质量___________。
(2)反应结束后溶液中溶质的质量分数。
参考答案
1-15:CDACD DBACB DABCB
16.(1)2Fe3+
(2)3H2 (3)4OH-
(4)
(5)SO2
17. ①. 可燃物 ②. 增加了氧气的量 ③. A ④. 将可燃物的温度降低到到着火点以下
18.①. t1 ②. 25 ③. 20% ④. 125 ⑤. B
19.(1)NaOH
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
(4)H2SO4+BaCl2=BaSO4↓+2HCl
20.(1)金属活动性
(2)4Al+3O2=2Al2O3
Fe+CuSO4=FeSO4+Cu
C
(5)AD
21.(1) ①. 负极 ②. 正极 ③. 增强水的导电性
(2) ①. 氢气##H2 ②. 氧气##O2 ③. ④. 氢元素和氧元素
22.(1) ①. B ②. B装置中反应生成的二氧化碳逸散到空气中 (2)先膨胀后变小
(3)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(4)不能验证质量守恒定律。理由是硫酸铜溶液和硝酸钠溶液混合后不会发生化学反应
23.(1)22g##22克
(2)设石灰石中碳酸钙的质量为x,生成氯化钙的质量为y。
x=50g
y=55.5g
反应后溶液的质量=196g (53g 50g)=193g(杂质质量为53g 50g=3g,溶液质量等于反应后总质量减去杂质质量)。则反应结束后溶液中溶质(氯化钙)的质量分数为。
答:反应结束后溶液中溶质的质量分数为28.8%。
同课章节目录
