第五单元 燃料与二氧化碳 练习 (含答案) 2025-2026学年化学科粤版九年级上册
文档属性
| 名称 | 第五单元 燃料与二氧化碳 练习 (含答案) 2025-2026学年化学科粤版九年级上册 |  | |
| 格式 | docx | ||
| 文件大小 | 247.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-28 15:51:04 | ||
图片预览




文档简介
第五单元 燃料与二氧化碳
(满分:100分 时间:60分钟)
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.我国自主开发的长征系列运载火箭“长三丙”,其第三级火箭发动机采用的燃料是液态氢,助燃剂是液态氧。下列有关叙述不正确的是 ( )
A.在相同条件下氢气密度比空气大 B.液态氢燃烧不会造成环境污染
C.氧气可以支持燃烧 D.氢气变成液态氢是物理变化
2.碳家族的成员很多,用途很广。下列关于碳的应用与其性质不对应的是 ( )
A.木炭作燃料——碳有可燃性 B.利用石墨作电极材料——石墨具有导电性
C.金刚石作钻探机的钻头——金刚石坚硬 D.用墨汁书写的字画经久不褪色——碳有还原性
3.(2024济南中考)2024年5月15日“全国低碳日”的活动主题是“绿色低碳,美丽中国”。下列选项中,不符合绿色低碳生活方式的是 ( )
A.日常生活中,尽量多使用一次性餐具
B.节约用电,及时关闭不使用的电器
C.尽量选择步行、骑行或公交等方式出行
D.减少使用塑料袋和过度包装物
4.在实验室制取二氧化碳的实验中,下列装置和操作正确且规范的是( )
A.检查装置气密性 B.加入大理石 C.制取CO2 D.收集CO2
5.下列关于化石燃料的说法正确的是 ( )
A.化石燃料都属于可再生能源 B.煤完全燃烧时不会产生污染
C.石油为原料能制造合成纤维 D.石油是一种化工产品
6.如图为金刚石、石墨和C60的结构模型图,图中小球代表碳原子。下列说法不正确的是 ( )
A.原子的排列方式改变,则构成的物质种类改变
B.相同元素组成的不同物质,在足量的氧气中完全燃烧,产物相同
C.相同元素组成的不同物质,化学性质相同
D.在特定的条件下,石墨既可转化为金刚石,也可转化为C60
7.下列有关二氧化碳的事实或实验现象与相关解释或结论一致的是 ( )
选项 事实或实验现象 解释或结论
A 干冰能制造舞台云雾 干冰升华吸热
B CO2可用排水法收集 CO2不溶于水
C CO2可使燃烧的蜡烛熄灭 CO2不供给呼吸
D CO2通入紫色石蕊溶液,液体变红 CO2能使石蕊溶液变红
8.如图为CH4(甲烷,天然气主要成分)的转化和资源化利用。下列说法不正确的是 ( )
A.转化①属于化合反应
B.转化②发生了物理变化
C.转化③中催化剂不需要不断添加
D.转化④在常温下进行,可采用过氧化氢溶液和MnO2制取O2的发生装置
9.如图表示自然界中存在的三大循环(水循环、氧循环、碳循环)。根据图示判断,下列说法中错误的是 ( )
A.“水循环”主要是由水分子的运动引起的
B.每个人都在参与三大循环
C.碳、氧循环有利于维持大气中O2与CO2的相对稳定
D.自然界中消耗O2的主要途径是绿色植物的光合作用
10.(2024德阳中考)大量排放的CO2造成了碳循环的失衡,导致大气温室效应加剧,修复大气中CO2含量的平衡必定要“降碳”。下列说法错误的是 ( )
A.大规模开采和利用化石燃料,会导致大气中CO2含量持续升高
B.将CO2压入地下实现碳封存,CO2分子间隔变小、运动停止
C.CO2被绿色植物光合作用吸收,CO2分子变成了其他分子
D.江河湖海的水体吸收CO2过程中既有物理变化,又有化学变化
11.下列关于碳及其化合物的说法中,正确的是 ( )
A.石墨耐高温、滑腻,常用来作高温润滑剂
B.用燃烧的方法除去CO2中少量的CO
C.在室内放一盆水可防止CO中毒
D.CO和CO2都是空气污染物
12.推理是学习化学的一种重要方法,以下推理正确的是 ( )
A.碳单质具有可燃性,则含有碳元素的物质都具有可燃性
B.氧气能支持燃烧,所以常用作燃料
C.组成单质的元素种类是一种,由同一种元素组成的物质一定是单质
D.点燃可燃性气体之前要验纯,所以点燃H2之前也要验纯
13.(2025泉州丰泽区月考)为探究二氧化碳的部分性质,设计实验装置如图(夹持仪器省略),焐热干冰位置的玻璃管。下列说法正确的是( )
A.a处试纸先变红色,发生分解反应
B.c处试纸变红色,使石蕊变色的是CO2
C.d处火焰先熄灭,CO2不支持燃烧
D.b与c、d与e现象对比均可证明CO2密度比空气大
14.碳及其化合物存在如下转化关系:CCOCO2X(“”表示一种物质会一步转化成另一种物质)。下列有关说法错误的是 ( )
A.由C转化为CO2的过程中碳元素的化合价依次升高
B.CO只能通过与O2反应转化为CO2
C.CO2可通过与C反应转化为CO,化学方程式为C+CO22CO
D.X可能是碳酸或碳酸钙
15.已知相同条件下,气体体积比等于气体分子个数之比。现有20 mL O2、CO、CO2的混合气体,在密闭容器中用电火花引燃,充分反应后恢复到原来状态,体积减小了2 mL,再通过足量的石灰水后又减少10 mL,最后剩余气体能使带火星的木条复燃。原混合气体中O2、CO、CO2的体积比可能是 ( )
A.1∶6∶3 B.3∶5∶2 C.3∶1∶6 D.5∶2∶3
二、填空题(本题共3小题,共19分)
16.(5分)不同的碳单质有不同的结构,也就有不同的性质和用途。
(1)“石墨炸弹”能够导致高压输电线短路,破坏供电系统,这种“炸弹”主要利用了石墨的 ,而生活中石墨可用作铅笔芯,是因为石墨是黑色的且 。
(2)牛津大学的化学家首次制造出由18个碳原子组成的环形纯碳分子,称为C18,它具有半导体功能。C18的相对分子质量为 ,该物质在空气中完全燃烧的化学方程式为 。
(3)木炭、活性炭的主要成分是碳单质,它们能用于净水是因为具有 的结构。
17.(8分)(2024天津中考)环境保护、能源利用和新材料使用被人们广泛关注。
(1)目前,人们使用的燃料大多来自化石燃料,如煤、石油和天然气等。化石燃料属于 (填“可再生”或“不可再生”)能源。
(2)近日,国务院颁布《2024—2025年节能减碳行动方案》。生产、生活中有以下做法:①发展绿色公共交通 ②开发太阳能、风能等能源 ③植树造林 ④发展火力发电。下列选项符合节能减碳的是 (填字母)。
A.①②③ B.②③④ C.①②③④
(3)含有氮化硅(Si3N4)的高温结构陶瓷用于火箭发动机。二氧化硅(SiO2)、碳单质和氮气在高温条件下反应生成氮化硅和一氧化碳,该反应的化学方程式为 。
(4)2023年,我国首次掺氢天然气管道燃爆试验成功,掺氢天然气能改善天然气的品质。某掺氢天然气(假设该混合气仅含CH4和H2)中氢元素的质量分数为40%,则混合气体充分燃烧后生成CO2和H2O的质量比为 (填最简整数比)。
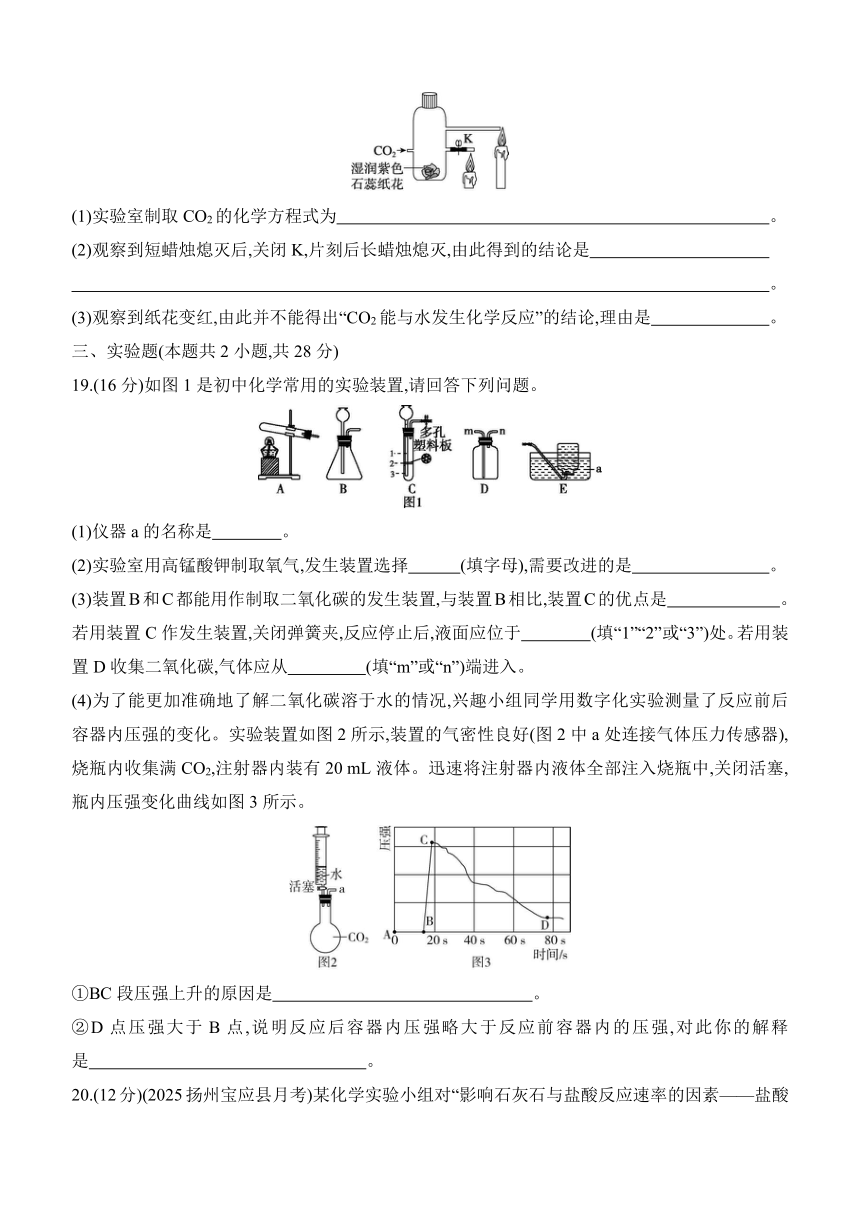
18.(6分)用如图实验验证CO2的性质。
(1)实验室制取CO2的化学方程式为 。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是
。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是 。
三、实验题(本题共2小题,共28分)
19.(16分)如图1是初中化学常用的实验装置,请回答下列问题。
(1)仪器a的名称是 。
(2)实验室用高锰酸钾制取氧气,发生装置选择 (填字母),需要改进的是 。
(3)装置B和C都能用作制取二氧化碳的发生装置,与装置B相比,装置C的优点是 。若用装置C作发生装置,关闭弹簧夹,反应停止后,液面应位于 (填“1”“2”或“3”)处。若用装置D收集二氧化碳,气体应从 (填“m”或“n”)端进入。
(4)为了能更加准确地了解二氧化碳溶于水的情况,兴趣小组同学用数字化实验测量了反应前后容器内压强的变化。实验装置如图2所示,装置的气密性良好(图2中a处连接气体压力传感器),烧瓶内收集满CO2,注射器内装有20 mL液体。迅速将注射器内液体全部注入烧瓶中,关闭活塞,瓶内压强变化曲线如图3所示。
①BC段压强上升的原因是 。
②D点压强大于B点,说明反应后容器内压强略大于反应前容器内的压强,对此你的解释是 。
20.(12分)(2025扬州宝应县月考)某化学实验小组对“影响石灰石与盐酸反应速率的因素——盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与:
【进行实验】室温下,选用20 mL不同浓度的盐酸(4%和6%)分别与1 g颗粒状或块状的石灰石进行实验(固定夹持仪器略去)。
(1)判断石灰石中CaCO3完全反应的实验现象是 。
(2)按如图装置进行实验,在装试剂前先 。开始时,应将20 mL稀盐酸 (填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
【处理数据】实验小组进行实验后,获得的相关实验数据如表所示:
实验编号 盐酸的浓度(均取20 mL) 取1 g石灰石固体形状 前30 s内收集到的二氧化碳体积/mL
a 4% 颗粒 64.0
b 4% 块状 40.4
c 6% 颗粒 98.2
d 6% 块状 65.3
(3)从上述实验数据可以得出:
①要比较不同浓度盐酸对反应速率的影响,可选择的实验编号是 (写一组),由此可得到的结论: 。
②石灰石颗粒大小对反应速率的影响的结论:其他条件相同时,石灰石颗粒越大,反应的速率越 。
四、计算题(本题共1小题,共8分)
21.某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其他成分可溶于水,但不参与反应)。
(1)该实验中,装置的气密性对测定结果 (填“有”或“无”)影响。
(2)计算该补钙剂中碳酸钙的质量分数。
【详解答案】
1.A
2.D
3.A 解析:日常生活中,尽量多使用一次性餐具,增加了资源的消耗、二氧化碳的排放,不符合绿色低碳生活方式。
4.D
5.C 解析:化石燃料包括煤、石油和天然气,化石燃料在短期内不能从自然界得到补充,属于不可再生能源;煤中含有硫元素、氮元素,完全燃烧时生成的二氧化硫、二氧化氮等溶于水会形成酸雨,对环境造成污染;石油是直接从地下开采出来的,不是化工产品,化工产品是经过化学加工得到的。
6.C
7.A 解析:干冰升华吸热,使温度降低,能制造舞台云雾,A正确;二氧化碳能溶于水且与水反应,一般不能用排水法收集,B错误;CO2可使燃烧的蜡烛熄灭,是因为二氧化碳不能燃烧、不能支持燃烧,C错误;CO2通入紫色石蕊溶液,液体变红,是因为二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,D错误。
8.A 解析:转化①是甲烷在氧气中燃烧生成二氧化碳和水,该反应的生成物是两种,不是化合反应; 转化②中气态甲烷转化为液态甲烷,只是状态发生改变,没有新物质生成,属于物理变化;催化剂的质量和化学性质在反应前后不变,转化③中催化剂不需要不断添加;转化④的反应物是碳化铝固体和水,反应物是固体和液体,反应在常温下进行,属于固液常温型,可采用过氧化氢溶液和MnO2制取O2的发生装置。
9.D 解析:水由水分子构成,“水循环”主要是由水分子的运动引起的;人类在进行呼吸作用以及其他各项生理活动,所以每个人都在参与三大循环; 碳、氧循环有利于维持大气中O2与CO2的相对稳定,维持生态平衡; 自然界中产生O2的主要途径是绿色植物的光合作用,消耗O2的主要途径是物质的燃烧、生物的呼吸作用等。
10.B 解析:化石燃料包括煤、石油、天然气,化石燃料燃烧产生CO2气体,导致空气中二氧化碳含量升高;将CO2压入地下封存时,CO2分子间的间隔会变小,但不会停止运动;绿色植物光合作用是将CO2在一定条件下转化为O2,CO2分子变成了其他分子;CO2溶于水属于物理变化,与水发生反应生成碳酸属于化学变化。
11.A 解析:二氧化碳中含有少量的一氧化碳,二氧化碳既不能燃烧,也不支持燃烧,所以一氧化碳不能燃烧;一氧化碳难溶于水,在室内放一盆水不能防止CO中毒;二氧化碳不属于空气污染物。
12.D 解析:碳单质具有可燃性,但含有碳元素的物质不一定具有可燃性,如碳酸钙等;氧气能支持燃烧,但没有可燃性,不能作燃料;组成单质的元素种类是一种,但由同一种元素组成的物质不一定是单质,如金刚石和石墨的混合物。
13.D 解析:a处试纸不会变色,干燥的二氧化碳不能使石蕊变色,A错误;c处试纸变红色,使石蕊变色的是二氧化碳和水反应生成的碳酸,碳酸显酸性,而不是二氧化碳,B错误;e处火焰先熄灭,CO2不支持燃烧,密度比空气大,下面的火柴先熄灭,C错误;b与c、d与e现象对比时都是下面的先出现相应的现象,故均可证明CO2密度比空气大,D正确。
14.B 解析:由物质的转化和化合价原则可知,由C转化为CO2的过程中碳元素的化合价依次升高,A正确;CO在加热还原金属氧化物反应时也能生成CO2,B错误;CO2可通过与C反应转化为CO,化学方程式为C+CO22CO,C正确;由于二氧化碳能与水化合生成碳酸,碳酸易分解生成二氧化碳和水,二氧化碳能与氢氧化钙反应生成碳酸钙,碳酸钙高温分解又生成二氧化碳,则X可能是碳酸或碳酸钙,D正确。
15.D 解析:一氧化碳与氧气反应生成二氧化碳,体积会减小,2 mL一氧化碳与1 mL氧气反应生成2 mL二氧化碳,气体体积减小1 mL,实验中体积减小了2 mL,所以参加反应的一氧化碳是4 mL,消耗氧气是2 mL,生成二氧化碳4 mL,通过石灰水,减少了10 mL,说明二氧化碳的总体积是10 mL,生成的二氧化碳是4 mL,则原来的二氧化碳为10 mL-4 mL=6 mL,最后剩余的气体能使带火星的木条复燃是氧气,所以氧气的体积为20 mL-2 mL-10 mL+2 mL =10 mL,氧气、一氧化碳、二氧化碳的体积比为10 mL∶4 mL∶6 mL=5∶2∶3。
16.(1)导电性 硬度小 (2)216 C18+18O218CO2 (3)疏松多孔
17.(1)不可再生 (2)A
(3)3SiO2+6C+2N2Si3N4+6CO
(4)11∶18
解析:(3)二氧化硅(SiO2)、碳单质和氮气在高温条件下反应生成氮化硅和一氧化碳,该反应的化学方程式为3SiO2+6C+2N2Si3N4+6CO。(4)某掺氢天然气(假设该混合气仅含CH4和H2)中氢元素的质量分数为40%,设氢元素的质量为40m,则碳元素的质量为60m,氢元素完全燃烧生成水,则生成水的质量为40m÷,碳元素完全燃烧生成二氧化碳,则生成二氧化碳的质量为60m÷,混合气体充分燃烧后生成CO2和H2O的质量比为(60m÷)∶(40m÷)=11∶18。
18.(1)CaCO3+2HClCaCl2+CO2↑+H2O (2)二氧化碳密度比空气大,不燃烧也不支持燃烧 (3)没有排除二氧化碳使纸花变红的可能,没有对照实验
19.(1)水槽 (2)A 在试管口放一团棉花
(3)可以控制反应的发生和停止 3 m
(4)①液体注入烧瓶造成气体被压缩,压强增大 ②二氧化碳溶于水的体积小于所加水的体积
20.(1)不再产生气泡
(2)检查装置气密性 快速
(3)①a与c(或b与d) 其他条件相同时,盐酸浓度越大,反应速率越快
②慢
21.解:(1)无
(2)根据质量守恒定律,生成二氧化碳的质量为370 g-363.4 g=6.6 g,则
设该补钙剂中碳酸钙的质量分数为x。
CaCO3+2HClCaCl2+H2O+CO2↑
100 44
20 g×x 6.6 g
= x=75%
答:该补钙剂中碳酸钙的质量分数为75%。
(满分:100分 时间:60分钟)
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.我国自主开发的长征系列运载火箭“长三丙”,其第三级火箭发动机采用的燃料是液态氢,助燃剂是液态氧。下列有关叙述不正确的是 ( )
A.在相同条件下氢气密度比空气大 B.液态氢燃烧不会造成环境污染
C.氧气可以支持燃烧 D.氢气变成液态氢是物理变化
2.碳家族的成员很多,用途很广。下列关于碳的应用与其性质不对应的是 ( )
A.木炭作燃料——碳有可燃性 B.利用石墨作电极材料——石墨具有导电性
C.金刚石作钻探机的钻头——金刚石坚硬 D.用墨汁书写的字画经久不褪色——碳有还原性
3.(2024济南中考)2024年5月15日“全国低碳日”的活动主题是“绿色低碳,美丽中国”。下列选项中,不符合绿色低碳生活方式的是 ( )
A.日常生活中,尽量多使用一次性餐具
B.节约用电,及时关闭不使用的电器
C.尽量选择步行、骑行或公交等方式出行
D.减少使用塑料袋和过度包装物
4.在实验室制取二氧化碳的实验中,下列装置和操作正确且规范的是( )
A.检查装置气密性 B.加入大理石 C.制取CO2 D.收集CO2
5.下列关于化石燃料的说法正确的是 ( )
A.化石燃料都属于可再生能源 B.煤完全燃烧时不会产生污染
C.石油为原料能制造合成纤维 D.石油是一种化工产品
6.如图为金刚石、石墨和C60的结构模型图,图中小球代表碳原子。下列说法不正确的是 ( )
A.原子的排列方式改变,则构成的物质种类改变
B.相同元素组成的不同物质,在足量的氧气中完全燃烧,产物相同
C.相同元素组成的不同物质,化学性质相同
D.在特定的条件下,石墨既可转化为金刚石,也可转化为C60
7.下列有关二氧化碳的事实或实验现象与相关解释或结论一致的是 ( )
选项 事实或实验现象 解释或结论
A 干冰能制造舞台云雾 干冰升华吸热
B CO2可用排水法收集 CO2不溶于水
C CO2可使燃烧的蜡烛熄灭 CO2不供给呼吸
D CO2通入紫色石蕊溶液,液体变红 CO2能使石蕊溶液变红
8.如图为CH4(甲烷,天然气主要成分)的转化和资源化利用。下列说法不正确的是 ( )
A.转化①属于化合反应
B.转化②发生了物理变化
C.转化③中催化剂不需要不断添加
D.转化④在常温下进行,可采用过氧化氢溶液和MnO2制取O2的发生装置
9.如图表示自然界中存在的三大循环(水循环、氧循环、碳循环)。根据图示判断,下列说法中错误的是 ( )
A.“水循环”主要是由水分子的运动引起的
B.每个人都在参与三大循环
C.碳、氧循环有利于维持大气中O2与CO2的相对稳定
D.自然界中消耗O2的主要途径是绿色植物的光合作用
10.(2024德阳中考)大量排放的CO2造成了碳循环的失衡,导致大气温室效应加剧,修复大气中CO2含量的平衡必定要“降碳”。下列说法错误的是 ( )
A.大规模开采和利用化石燃料,会导致大气中CO2含量持续升高
B.将CO2压入地下实现碳封存,CO2分子间隔变小、运动停止
C.CO2被绿色植物光合作用吸收,CO2分子变成了其他分子
D.江河湖海的水体吸收CO2过程中既有物理变化,又有化学变化
11.下列关于碳及其化合物的说法中,正确的是 ( )
A.石墨耐高温、滑腻,常用来作高温润滑剂
B.用燃烧的方法除去CO2中少量的CO
C.在室内放一盆水可防止CO中毒
D.CO和CO2都是空气污染物
12.推理是学习化学的一种重要方法,以下推理正确的是 ( )
A.碳单质具有可燃性,则含有碳元素的物质都具有可燃性
B.氧气能支持燃烧,所以常用作燃料
C.组成单质的元素种类是一种,由同一种元素组成的物质一定是单质
D.点燃可燃性气体之前要验纯,所以点燃H2之前也要验纯
13.(2025泉州丰泽区月考)为探究二氧化碳的部分性质,设计实验装置如图(夹持仪器省略),焐热干冰位置的玻璃管。下列说法正确的是( )
A.a处试纸先变红色,发生分解反应
B.c处试纸变红色,使石蕊变色的是CO2
C.d处火焰先熄灭,CO2不支持燃烧
D.b与c、d与e现象对比均可证明CO2密度比空气大
14.碳及其化合物存在如下转化关系:CCOCO2X(“”表示一种物质会一步转化成另一种物质)。下列有关说法错误的是 ( )
A.由C转化为CO2的过程中碳元素的化合价依次升高
B.CO只能通过与O2反应转化为CO2
C.CO2可通过与C反应转化为CO,化学方程式为C+CO22CO
D.X可能是碳酸或碳酸钙
15.已知相同条件下,气体体积比等于气体分子个数之比。现有20 mL O2、CO、CO2的混合气体,在密闭容器中用电火花引燃,充分反应后恢复到原来状态,体积减小了2 mL,再通过足量的石灰水后又减少10 mL,最后剩余气体能使带火星的木条复燃。原混合气体中O2、CO、CO2的体积比可能是 ( )
A.1∶6∶3 B.3∶5∶2 C.3∶1∶6 D.5∶2∶3
二、填空题(本题共3小题,共19分)
16.(5分)不同的碳单质有不同的结构,也就有不同的性质和用途。
(1)“石墨炸弹”能够导致高压输电线短路,破坏供电系统,这种“炸弹”主要利用了石墨的 ,而生活中石墨可用作铅笔芯,是因为石墨是黑色的且 。
(2)牛津大学的化学家首次制造出由18个碳原子组成的环形纯碳分子,称为C18,它具有半导体功能。C18的相对分子质量为 ,该物质在空气中完全燃烧的化学方程式为 。
(3)木炭、活性炭的主要成分是碳单质,它们能用于净水是因为具有 的结构。
17.(8分)(2024天津中考)环境保护、能源利用和新材料使用被人们广泛关注。
(1)目前,人们使用的燃料大多来自化石燃料,如煤、石油和天然气等。化石燃料属于 (填“可再生”或“不可再生”)能源。
(2)近日,国务院颁布《2024—2025年节能减碳行动方案》。生产、生活中有以下做法:①发展绿色公共交通 ②开发太阳能、风能等能源 ③植树造林 ④发展火力发电。下列选项符合节能减碳的是 (填字母)。
A.①②③ B.②③④ C.①②③④
(3)含有氮化硅(Si3N4)的高温结构陶瓷用于火箭发动机。二氧化硅(SiO2)、碳单质和氮气在高温条件下反应生成氮化硅和一氧化碳,该反应的化学方程式为 。
(4)2023年,我国首次掺氢天然气管道燃爆试验成功,掺氢天然气能改善天然气的品质。某掺氢天然气(假设该混合气仅含CH4和H2)中氢元素的质量分数为40%,则混合气体充分燃烧后生成CO2和H2O的质量比为 (填最简整数比)。
18.(6分)用如图实验验证CO2的性质。
(1)实验室制取CO2的化学方程式为 。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是
。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是 。
三、实验题(本题共2小题,共28分)
19.(16分)如图1是初中化学常用的实验装置,请回答下列问题。
(1)仪器a的名称是 。
(2)实验室用高锰酸钾制取氧气,发生装置选择 (填字母),需要改进的是 。
(3)装置B和C都能用作制取二氧化碳的发生装置,与装置B相比,装置C的优点是 。若用装置C作发生装置,关闭弹簧夹,反应停止后,液面应位于 (填“1”“2”或“3”)处。若用装置D收集二氧化碳,气体应从 (填“m”或“n”)端进入。
(4)为了能更加准确地了解二氧化碳溶于水的情况,兴趣小组同学用数字化实验测量了反应前后容器内压强的变化。实验装置如图2所示,装置的气密性良好(图2中a处连接气体压力传感器),烧瓶内收集满CO2,注射器内装有20 mL液体。迅速将注射器内液体全部注入烧瓶中,关闭活塞,瓶内压强变化曲线如图3所示。
①BC段压强上升的原因是 。
②D点压强大于B点,说明反应后容器内压强略大于反应前容器内的压强,对此你的解释是 。
20.(12分)(2025扬州宝应县月考)某化学实验小组对“影响石灰石与盐酸反应速率的因素——盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与:
【进行实验】室温下,选用20 mL不同浓度的盐酸(4%和6%)分别与1 g颗粒状或块状的石灰石进行实验(固定夹持仪器略去)。
(1)判断石灰石中CaCO3完全反应的实验现象是 。
(2)按如图装置进行实验,在装试剂前先 。开始时,应将20 mL稀盐酸 (填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
【处理数据】实验小组进行实验后,获得的相关实验数据如表所示:
实验编号 盐酸的浓度(均取20 mL) 取1 g石灰石固体形状 前30 s内收集到的二氧化碳体积/mL
a 4% 颗粒 64.0
b 4% 块状 40.4
c 6% 颗粒 98.2
d 6% 块状 65.3
(3)从上述实验数据可以得出:
①要比较不同浓度盐酸对反应速率的影响,可选择的实验编号是 (写一组),由此可得到的结论: 。
②石灰石颗粒大小对反应速率的影响的结论:其他条件相同时,石灰石颗粒越大,反应的速率越 。
四、计算题(本题共1小题,共8分)
21.某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其他成分可溶于水,但不参与反应)。
(1)该实验中,装置的气密性对测定结果 (填“有”或“无”)影响。
(2)计算该补钙剂中碳酸钙的质量分数。
【详解答案】
1.A
2.D
3.A 解析:日常生活中,尽量多使用一次性餐具,增加了资源的消耗、二氧化碳的排放,不符合绿色低碳生活方式。
4.D
5.C 解析:化石燃料包括煤、石油和天然气,化石燃料在短期内不能从自然界得到补充,属于不可再生能源;煤中含有硫元素、氮元素,完全燃烧时生成的二氧化硫、二氧化氮等溶于水会形成酸雨,对环境造成污染;石油是直接从地下开采出来的,不是化工产品,化工产品是经过化学加工得到的。
6.C
7.A 解析:干冰升华吸热,使温度降低,能制造舞台云雾,A正确;二氧化碳能溶于水且与水反应,一般不能用排水法收集,B错误;CO2可使燃烧的蜡烛熄灭,是因为二氧化碳不能燃烧、不能支持燃烧,C错误;CO2通入紫色石蕊溶液,液体变红,是因为二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,D错误。
8.A 解析:转化①是甲烷在氧气中燃烧生成二氧化碳和水,该反应的生成物是两种,不是化合反应; 转化②中气态甲烷转化为液态甲烷,只是状态发生改变,没有新物质生成,属于物理变化;催化剂的质量和化学性质在反应前后不变,转化③中催化剂不需要不断添加;转化④的反应物是碳化铝固体和水,反应物是固体和液体,反应在常温下进行,属于固液常温型,可采用过氧化氢溶液和MnO2制取O2的发生装置。
9.D 解析:水由水分子构成,“水循环”主要是由水分子的运动引起的;人类在进行呼吸作用以及其他各项生理活动,所以每个人都在参与三大循环; 碳、氧循环有利于维持大气中O2与CO2的相对稳定,维持生态平衡; 自然界中产生O2的主要途径是绿色植物的光合作用,消耗O2的主要途径是物质的燃烧、生物的呼吸作用等。
10.B 解析:化石燃料包括煤、石油、天然气,化石燃料燃烧产生CO2气体,导致空气中二氧化碳含量升高;将CO2压入地下封存时,CO2分子间的间隔会变小,但不会停止运动;绿色植物光合作用是将CO2在一定条件下转化为O2,CO2分子变成了其他分子;CO2溶于水属于物理变化,与水发生反应生成碳酸属于化学变化。
11.A 解析:二氧化碳中含有少量的一氧化碳,二氧化碳既不能燃烧,也不支持燃烧,所以一氧化碳不能燃烧;一氧化碳难溶于水,在室内放一盆水不能防止CO中毒;二氧化碳不属于空气污染物。
12.D 解析:碳单质具有可燃性,但含有碳元素的物质不一定具有可燃性,如碳酸钙等;氧气能支持燃烧,但没有可燃性,不能作燃料;组成单质的元素种类是一种,但由同一种元素组成的物质不一定是单质,如金刚石和石墨的混合物。
13.D 解析:a处试纸不会变色,干燥的二氧化碳不能使石蕊变色,A错误;c处试纸变红色,使石蕊变色的是二氧化碳和水反应生成的碳酸,碳酸显酸性,而不是二氧化碳,B错误;e处火焰先熄灭,CO2不支持燃烧,密度比空气大,下面的火柴先熄灭,C错误;b与c、d与e现象对比时都是下面的先出现相应的现象,故均可证明CO2密度比空气大,D正确。
14.B 解析:由物质的转化和化合价原则可知,由C转化为CO2的过程中碳元素的化合价依次升高,A正确;CO在加热还原金属氧化物反应时也能生成CO2,B错误;CO2可通过与C反应转化为CO,化学方程式为C+CO22CO,C正确;由于二氧化碳能与水化合生成碳酸,碳酸易分解生成二氧化碳和水,二氧化碳能与氢氧化钙反应生成碳酸钙,碳酸钙高温分解又生成二氧化碳,则X可能是碳酸或碳酸钙,D正确。
15.D 解析:一氧化碳与氧气反应生成二氧化碳,体积会减小,2 mL一氧化碳与1 mL氧气反应生成2 mL二氧化碳,气体体积减小1 mL,实验中体积减小了2 mL,所以参加反应的一氧化碳是4 mL,消耗氧气是2 mL,生成二氧化碳4 mL,通过石灰水,减少了10 mL,说明二氧化碳的总体积是10 mL,生成的二氧化碳是4 mL,则原来的二氧化碳为10 mL-4 mL=6 mL,最后剩余的气体能使带火星的木条复燃是氧气,所以氧气的体积为20 mL-2 mL-10 mL+2 mL =10 mL,氧气、一氧化碳、二氧化碳的体积比为10 mL∶4 mL∶6 mL=5∶2∶3。
16.(1)导电性 硬度小 (2)216 C18+18O218CO2 (3)疏松多孔
17.(1)不可再生 (2)A
(3)3SiO2+6C+2N2Si3N4+6CO
(4)11∶18
解析:(3)二氧化硅(SiO2)、碳单质和氮气在高温条件下反应生成氮化硅和一氧化碳,该反应的化学方程式为3SiO2+6C+2N2Si3N4+6CO。(4)某掺氢天然气(假设该混合气仅含CH4和H2)中氢元素的质量分数为40%,设氢元素的质量为40m,则碳元素的质量为60m,氢元素完全燃烧生成水,则生成水的质量为40m÷,碳元素完全燃烧生成二氧化碳,则生成二氧化碳的质量为60m÷,混合气体充分燃烧后生成CO2和H2O的质量比为(60m÷)∶(40m÷)=11∶18。
18.(1)CaCO3+2HClCaCl2+CO2↑+H2O (2)二氧化碳密度比空气大,不燃烧也不支持燃烧 (3)没有排除二氧化碳使纸花变红的可能,没有对照实验
19.(1)水槽 (2)A 在试管口放一团棉花
(3)可以控制反应的发生和停止 3 m
(4)①液体注入烧瓶造成气体被压缩,压强增大 ②二氧化碳溶于水的体积小于所加水的体积
20.(1)不再产生气泡
(2)检查装置气密性 快速
(3)①a与c(或b与d) 其他条件相同时,盐酸浓度越大,反应速率越快
②慢
21.解:(1)无
(2)根据质量守恒定律,生成二氧化碳的质量为370 g-363.4 g=6.6 g,则
设该补钙剂中碳酸钙的质量分数为x。
CaCO3+2HClCaCl2+H2O+CO2↑
100 44
20 g×x 6.6 g
= x=75%
答:该补钙剂中碳酸钙的质量分数为75%。
同课章节目录
