第三单元 维持生命的物质——氧气、水 专题训练三 探究影响实验室制取氧气速率的因素 同步练习(含答案)
文档属性
| 名称 | 第三单元 维持生命的物质——氧气、水 专题训练三 探究影响实验室制取氧气速率的因素 同步练习(含答案) | 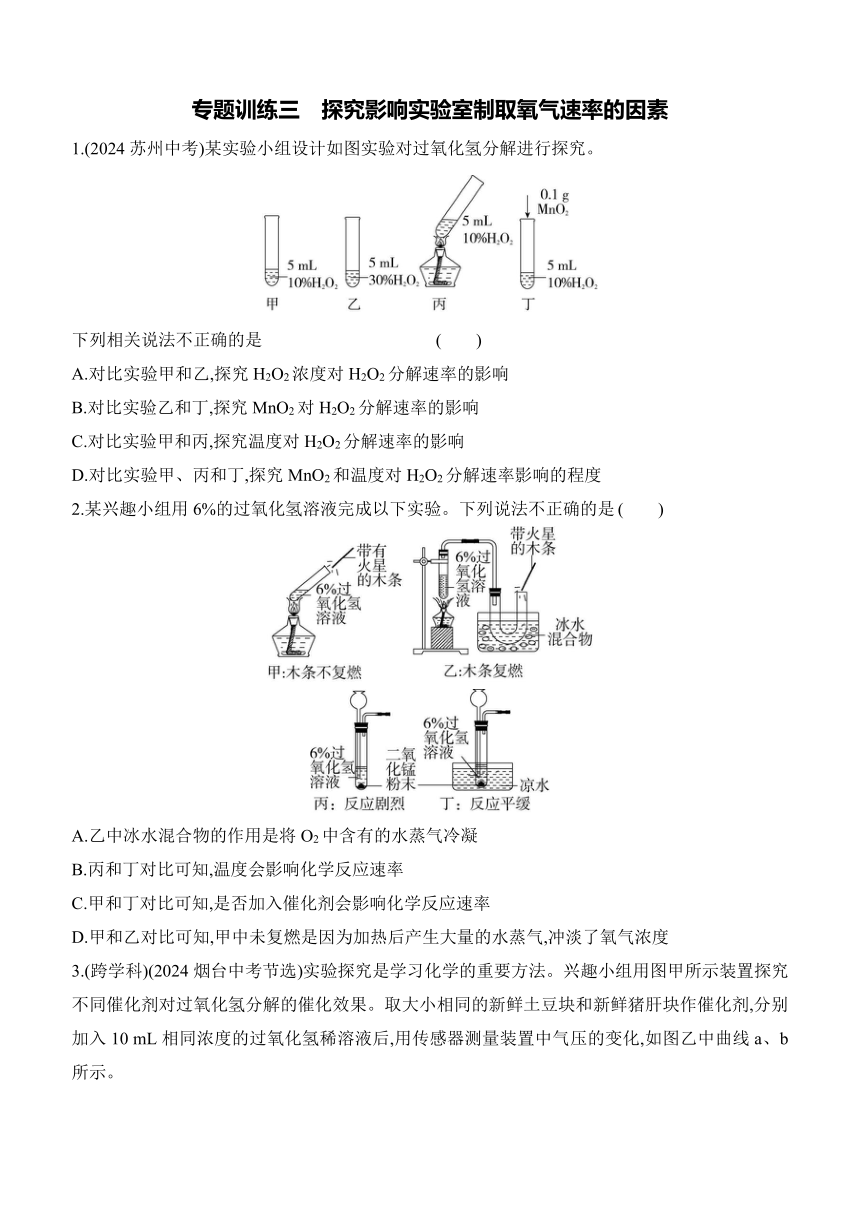 | |
| 格式 | docx | ||
| 文件大小 | 143.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-28 21:51:18 | ||
图片预览



文档简介
专题训练三 探究影响实验室制取氧气速率的因素
1.(2024苏州中考)某实验小组设计如图实验对过氧化氢分解进行探究。
下列相关说法不正确的是 ( )
A.对比实验甲和乙,探究H2O2浓度对H2O2分解速率的影响
B.对比实验乙和丁,探究MnO2对H2O2分解速率的影响
C.对比实验甲和丙,探究温度对H2O2分解速率的影响
D.对比实验甲、丙和丁,探究MnO2和温度对H2O2分解速率影响的程度
2.某兴趣小组用6%的过氧化氢溶液完成以下实验。下列说法不正确的是 ( )
A.乙中冰水混合物的作用是将O2中含有的水蒸气冷凝
B.丙和丁对比可知,温度会影响化学反应速率
C.甲和丁对比可知,是否加入催化剂会影响化学反应速率
D.甲和乙对比可知,甲中未复燃是因为加热后产生大量的水蒸气,冲淡了氧气浓度
3.(跨学科)(2024烟台中考节选)实验探究是学习化学的重要方法。兴趣小组用图甲所示装置探究不同催化剂对过氧化氢分解的催化效果。取大小相同的新鲜土豆块和新鲜猪肝块作催化剂,分别加入10 mL相同浓度的过氧化氢稀溶液后,用传感器测量装置中气压的变化,如图乙中曲线a、b所示。
(1)结合实验和曲线a、b分析,两种催化剂中催化效率更高的是 。
(2)从曲线a、b的变化可以看出,过氧化氢分解的反应是 (填“放热”或“吸热”)反应,加猪肝块催化的过氧化氢完全反应所用的时间大约是 (填“30”“65”或“120”)s。
(3)曲线a、b最终达到相同的压强,说明 。
4.(2024重庆A中考改编)氧气在医疗急数、化工生产等领域都有重要应用。
(1)从元素守恒角度看,下列物质不能用于制取氧气的是 (填字母)。
A.水(H2O)
B. 高锰酸钾(KMnO4)
C. 氯化钠(NaCl)
(2)某探究小组进行了“催化剂等因素对过氧化氢分解的影响”的系列探究,该小组分别取1 g不同的催化剂,再加入溶质质量分数5%的过氧化氢溶液20 mL,进行了如下实验:
序号 催化剂 温度 实验现象
甲 二氧化锰粉末 常温 持续产生气泡,速率适中,气流平稳
乙 红砖粉末 60 ℃ 持续产生气泡,速率适中,气流平稳
丙 红砖小颗粒 常温 缓慢,有少量气泡逸出
丁 块状红砖 常温 十分缓慢,几乎看不到气泡
①写出实验甲中发生反应文字表达式:
。
②二氧化锰粉末与红砖粉末对过氧化氢溶液分解具有相同的催化效果,你认为此结论是否科学
(填“是”或“否”)。理由是 。
③能说明催化剂的催化效果与其形态有关的实验组合是 (填实验序号)。
④在一定温度下,另取2 g红砖小颗粒,向其中加入8%的过氧化氢溶液20 mL,继续实验,发现产生气泡的速率明显比实验丙快。请分析可能的原因:
(至少写两条)。
5.“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁(化学式Fe2O3)能否作过氧化氢溶液分解的催化剂 如果能,其催化效果如何
【实验探究】
实验步骤 实验现象
① ,并分别在A、B两支试管中插入带火星的木条,观察现象 A试管中 ,带火星木条复燃。 B试管中无明显现象
②待A试管中没有现象发生时,重新加入 ,并把带火星的木条伸入试管内,如此反复多次试验,观察现象 试管内均产生大量气泡。 带火星木条均复燃
③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、 所得固体质量仍为a克
④取5 mL 5%过氧化氢溶液放入C试管中,向C试管中放入a克氧化铁粉末;向D试管中加入 和 克二氧化锰粉末,观察现象 现象略
【实验结论】
(1)实验②③证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(2)写出氧化铁催化过氧化氢发生反应的文字表达式: 。
【实验评论】实验设计④的目的是
。
【知识拓展】查阅资料得知,氧化铜、硫酸铜溶液、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法正确的是 (填字母)。
A.同一个化学反应可以有多种催化剂
B.MnO2 只能作为过氧化氢溶液分解的催化剂
C.催化剂只加快反应速率
D.作催化剂的物质不能是其他反应的反应物或生成物
【详解答案】
1.B 解析:根据控制变量法,甲和乙的变量是过氧化氢的浓度,则对比实验甲和乙,探究H2O2浓度对H2O2分解速率的影响;实验乙和丁的变量有浓度和二氧化锰,变量不唯一,则甲、乙不能探究MnO2对H2O2分解速率的影响;甲和丙的变量是温度不同,丙的温度高,反应速率快,则对比实验甲和丙,探究温度对H2O2分解速率的影响;根据C项的分析,对比甲和丙可以探究温度对H2O2分解速率的影响,对比实验甲、丁,变量是二氧化锰,则可以探究MnO2对H2O2分解速率的影响。
2.C 解析:甲、乙实验中唯一的不同点是乙实验将生成的氧气用冰水混合物对气体进行了冷却,由甲实验木条不复燃,而乙木条复燃对比可知,乙中冰水混合物的作用是将水蒸气冷凝;丙、丁中唯一的不同点是丁将反应容器放在了凉水中,温度低,反应平缓,丙是在常温下,反应剧烈,二者对比可知,温度会影响化学反应速率;甲、丁中反应物的温度不同,无法证明加入催化剂会影响化学反应速度;甲、乙实验中唯一的不同点是乙将生成的氧气用冰水混合物对气体进行了冷却,由甲实验木条不复燃,而乙木条复燃对比可知,甲中未复燃是因为加热后产生大量的水蒸气,冲淡了氧气浓度。
3.(1)猪肝块 (2)放热 30 (3)催化剂只改变化学反应速率,不改变生成物的质量
解析:(1)由图乙可知,相同时间内猪肝块作催化剂使装置内压强变化更大,说明相同时间内猪肝块作催化剂对过氧化氢分解产生的氧气更多,则两种催化剂中催化效率更高的是猪肝块。(2)由图乙可知,装置内压强先增大后减小,是因为反应产生气体使装置内压强增大,反应结束后温度降低使装置内压强减小,说明过氧化氢分解的反应是放热反应;由图乙可知,30 s时加猪肝块催化的过氧化氢使装置内压强达到最大,说明加猪肝块催化的过氧化氢完全反应所用的时间大约是30 s。(3)该实验为取大小相同的新鲜土豆块和新鲜猪肝块作催化剂,分别加入10 mL相同浓度的过氧化氢稀溶液,由图乙可知,曲线a、b最终达到相同的压强,说明最终生成氧气的体积相同,说明催化剂只改变化学反应速率,不改变生成物的质量。
4.(1)C (2)①过氧化氢水+氧气 ②否 实验温度不同,没有控制变量 ③丙、丁 ④在其他条件相同时,红砖小颗粒更多,催化效果更好;过氧化氢溶液浓度更高,反应更快(或温度更高,反应更快)
解析:(1)反应前后元素种类不变,制取氧气的试剂中应含有氧元素,氯化钠不含氧元素,所以不能用于氧气制取。(2)①实验甲发生的反应为过氧化氢在二氧化锰作催化剂的条件下分解生成水和氧气。②由表中甲乙实验数据可知,实验时除催化剂的种类不同,实验的温度也不同,没有控制变量,所以不能用于比较两种催化剂的催化效果,故实验结论不科学。③丙和丁只有催化剂的形态不同,可以用于探究催化剂的催化效果与催化剂的形态有关。④新增实验与实验丙对比变量为催化剂的质量和过氧化氢溶液的浓度不同,(温度也可能不同)所以造成产生气泡速率明显比实验丙快,可能是过氧化氢溶液浓度更高,使反应更快;也可能是温度更高,造成催化效果更好;或是红砖小颗粒的质量大,与过氧化氢溶液接触更充分,使催化效果更好。
5.【实验探究】①分别量取5 mL 5%过氧化氢溶液放入A、B两支试管中,向A试管加入a克氧化铁粉末 产生大量气泡
②过氧化氢溶液 ③称量 ④5 mL 5%过氧化氢溶液 a
【实验结论】(1)质量 化学性质 (2)过氧化氢水+氧气
【实验评论】比较二氧化锰与氧化铁对过氧化氢分解的催化效果
【知识拓展】A
解析:探究氧化铁能否作过氧化氢溶液分解的催化剂,需要设计对比实验,验证氧化铁是否改变过氧化氢分解的速率,所以分别量取5 mL 5%过氧化氢溶液放入A、B两支试管中,向A试管加入a克氧化铁粉末,在氧化铁的催化作用下,过氧化氢迅速分解产生了大量的氧气,所以观察到A试管中产生大量气泡,使带火星木条复燃;向A试管再次加入过氧化氢溶液,验证氧化铁是否还能改变反应速率,化学性质是否改变;实验设计④比较二氧化锰与氧化铁对过氧化氢分解的催化效果,所以C、D两个试管中过氧化氢溶液的质量、浓度一样,二氧化锰和氧化铁的质量一样,控制变量形成对比实验。MnO2不是只能作为过氧化氢溶液分解的催化剂,也可以作其他反应的催化剂;催化剂可以加快也可减慢反应的速率;作催化剂的物质可以是其他反应的反应物或生成物。
1.(2024苏州中考)某实验小组设计如图实验对过氧化氢分解进行探究。
下列相关说法不正确的是 ( )
A.对比实验甲和乙,探究H2O2浓度对H2O2分解速率的影响
B.对比实验乙和丁,探究MnO2对H2O2分解速率的影响
C.对比实验甲和丙,探究温度对H2O2分解速率的影响
D.对比实验甲、丙和丁,探究MnO2和温度对H2O2分解速率影响的程度
2.某兴趣小组用6%的过氧化氢溶液完成以下实验。下列说法不正确的是 ( )
A.乙中冰水混合物的作用是将O2中含有的水蒸气冷凝
B.丙和丁对比可知,温度会影响化学反应速率
C.甲和丁对比可知,是否加入催化剂会影响化学反应速率
D.甲和乙对比可知,甲中未复燃是因为加热后产生大量的水蒸气,冲淡了氧气浓度
3.(跨学科)(2024烟台中考节选)实验探究是学习化学的重要方法。兴趣小组用图甲所示装置探究不同催化剂对过氧化氢分解的催化效果。取大小相同的新鲜土豆块和新鲜猪肝块作催化剂,分别加入10 mL相同浓度的过氧化氢稀溶液后,用传感器测量装置中气压的变化,如图乙中曲线a、b所示。
(1)结合实验和曲线a、b分析,两种催化剂中催化效率更高的是 。
(2)从曲线a、b的变化可以看出,过氧化氢分解的反应是 (填“放热”或“吸热”)反应,加猪肝块催化的过氧化氢完全反应所用的时间大约是 (填“30”“65”或“120”)s。
(3)曲线a、b最终达到相同的压强,说明 。
4.(2024重庆A中考改编)氧气在医疗急数、化工生产等领域都有重要应用。
(1)从元素守恒角度看,下列物质不能用于制取氧气的是 (填字母)。
A.水(H2O)
B. 高锰酸钾(KMnO4)
C. 氯化钠(NaCl)
(2)某探究小组进行了“催化剂等因素对过氧化氢分解的影响”的系列探究,该小组分别取1 g不同的催化剂,再加入溶质质量分数5%的过氧化氢溶液20 mL,进行了如下实验:
序号 催化剂 温度 实验现象
甲 二氧化锰粉末 常温 持续产生气泡,速率适中,气流平稳
乙 红砖粉末 60 ℃ 持续产生气泡,速率适中,气流平稳
丙 红砖小颗粒 常温 缓慢,有少量气泡逸出
丁 块状红砖 常温 十分缓慢,几乎看不到气泡
①写出实验甲中发生反应文字表达式:
。
②二氧化锰粉末与红砖粉末对过氧化氢溶液分解具有相同的催化效果,你认为此结论是否科学
(填“是”或“否”)。理由是 。
③能说明催化剂的催化效果与其形态有关的实验组合是 (填实验序号)。
④在一定温度下,另取2 g红砖小颗粒,向其中加入8%的过氧化氢溶液20 mL,继续实验,发现产生气泡的速率明显比实验丙快。请分析可能的原因:
(至少写两条)。
5.“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁(化学式Fe2O3)能否作过氧化氢溶液分解的催化剂 如果能,其催化效果如何
【实验探究】
实验步骤 实验现象
① ,并分别在A、B两支试管中插入带火星的木条,观察现象 A试管中 ,带火星木条复燃。 B试管中无明显现象
②待A试管中没有现象发生时,重新加入 ,并把带火星的木条伸入试管内,如此反复多次试验,观察现象 试管内均产生大量气泡。 带火星木条均复燃
③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、 所得固体质量仍为a克
④取5 mL 5%过氧化氢溶液放入C试管中,向C试管中放入a克氧化铁粉末;向D试管中加入 和 克二氧化锰粉末,观察现象 现象略
【实验结论】
(1)实验②③证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(2)写出氧化铁催化过氧化氢发生反应的文字表达式: 。
【实验评论】实验设计④的目的是
。
【知识拓展】查阅资料得知,氧化铜、硫酸铜溶液、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法正确的是 (填字母)。
A.同一个化学反应可以有多种催化剂
B.MnO2 只能作为过氧化氢溶液分解的催化剂
C.催化剂只加快反应速率
D.作催化剂的物质不能是其他反应的反应物或生成物
【详解答案】
1.B 解析:根据控制变量法,甲和乙的变量是过氧化氢的浓度,则对比实验甲和乙,探究H2O2浓度对H2O2分解速率的影响;实验乙和丁的变量有浓度和二氧化锰,变量不唯一,则甲、乙不能探究MnO2对H2O2分解速率的影响;甲和丙的变量是温度不同,丙的温度高,反应速率快,则对比实验甲和丙,探究温度对H2O2分解速率的影响;根据C项的分析,对比甲和丙可以探究温度对H2O2分解速率的影响,对比实验甲、丁,变量是二氧化锰,则可以探究MnO2对H2O2分解速率的影响。
2.C 解析:甲、乙实验中唯一的不同点是乙实验将生成的氧气用冰水混合物对气体进行了冷却,由甲实验木条不复燃,而乙木条复燃对比可知,乙中冰水混合物的作用是将水蒸气冷凝;丙、丁中唯一的不同点是丁将反应容器放在了凉水中,温度低,反应平缓,丙是在常温下,反应剧烈,二者对比可知,温度会影响化学反应速率;甲、丁中反应物的温度不同,无法证明加入催化剂会影响化学反应速度;甲、乙实验中唯一的不同点是乙将生成的氧气用冰水混合物对气体进行了冷却,由甲实验木条不复燃,而乙木条复燃对比可知,甲中未复燃是因为加热后产生大量的水蒸气,冲淡了氧气浓度。
3.(1)猪肝块 (2)放热 30 (3)催化剂只改变化学反应速率,不改变生成物的质量
解析:(1)由图乙可知,相同时间内猪肝块作催化剂使装置内压强变化更大,说明相同时间内猪肝块作催化剂对过氧化氢分解产生的氧气更多,则两种催化剂中催化效率更高的是猪肝块。(2)由图乙可知,装置内压强先增大后减小,是因为反应产生气体使装置内压强增大,反应结束后温度降低使装置内压强减小,说明过氧化氢分解的反应是放热反应;由图乙可知,30 s时加猪肝块催化的过氧化氢使装置内压强达到最大,说明加猪肝块催化的过氧化氢完全反应所用的时间大约是30 s。(3)该实验为取大小相同的新鲜土豆块和新鲜猪肝块作催化剂,分别加入10 mL相同浓度的过氧化氢稀溶液,由图乙可知,曲线a、b最终达到相同的压强,说明最终生成氧气的体积相同,说明催化剂只改变化学反应速率,不改变生成物的质量。
4.(1)C (2)①过氧化氢水+氧气 ②否 实验温度不同,没有控制变量 ③丙、丁 ④在其他条件相同时,红砖小颗粒更多,催化效果更好;过氧化氢溶液浓度更高,反应更快(或温度更高,反应更快)
解析:(1)反应前后元素种类不变,制取氧气的试剂中应含有氧元素,氯化钠不含氧元素,所以不能用于氧气制取。(2)①实验甲发生的反应为过氧化氢在二氧化锰作催化剂的条件下分解生成水和氧气。②由表中甲乙实验数据可知,实验时除催化剂的种类不同,实验的温度也不同,没有控制变量,所以不能用于比较两种催化剂的催化效果,故实验结论不科学。③丙和丁只有催化剂的形态不同,可以用于探究催化剂的催化效果与催化剂的形态有关。④新增实验与实验丙对比变量为催化剂的质量和过氧化氢溶液的浓度不同,(温度也可能不同)所以造成产生气泡速率明显比实验丙快,可能是过氧化氢溶液浓度更高,使反应更快;也可能是温度更高,造成催化效果更好;或是红砖小颗粒的质量大,与过氧化氢溶液接触更充分,使催化效果更好。
5.【实验探究】①分别量取5 mL 5%过氧化氢溶液放入A、B两支试管中,向A试管加入a克氧化铁粉末 产生大量气泡
②过氧化氢溶液 ③称量 ④5 mL 5%过氧化氢溶液 a
【实验结论】(1)质量 化学性质 (2)过氧化氢水+氧气
【实验评论】比较二氧化锰与氧化铁对过氧化氢分解的催化效果
【知识拓展】A
解析:探究氧化铁能否作过氧化氢溶液分解的催化剂,需要设计对比实验,验证氧化铁是否改变过氧化氢分解的速率,所以分别量取5 mL 5%过氧化氢溶液放入A、B两支试管中,向A试管加入a克氧化铁粉末,在氧化铁的催化作用下,过氧化氢迅速分解产生了大量的氧气,所以观察到A试管中产生大量气泡,使带火星木条复燃;向A试管再次加入过氧化氢溶液,验证氧化铁是否还能改变反应速率,化学性质是否改变;实验设计④比较二氧化锰与氧化铁对过氧化氢分解的催化效果,所以C、D两个试管中过氧化氢溶液的质量、浓度一样,二氧化锰和氧化铁的质量一样,控制变量形成对比实验。MnO2不是只能作为过氧化氢溶液分解的催化剂,也可以作其他反应的催化剂;催化剂可以加快也可减慢反应的速率;作催化剂的物质可以是其他反应的反应物或生成物。
同课章节目录
