2.2氧气 第1课时 课件(共27张PPT内嵌视频)
文档属性
| 名称 | 2.2氧气 第1课时 课件(共27张PPT内嵌视频) |  | |
| 格式 | pptx | ||
| 文件大小 | 55.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-18 22:06:33 | ||
图片预览








文档简介
(共27张PPT)
教化学的花花老师
第二单元 空气和氧气
课题2 氧 气
第1课时
Learning aims
学习目标
1.
2.
了解氧气的物理性质和化学性质
学会描述实验现象的一般方法
阅读教材P38-40,解决相关问题:
1、氧气的性质有哪些?
2、怎样检验氧气?
3、木炭在空气中和在氧气中燃烧的实验现象是什么,生成了什么?
相关文字表达式是什么?
4、硫呢?铁呢?
一个“神秘访客”来地球签证中心
申请护照
作为“地球签证官”,我们需要核查“她”的身份信息(性质)。首先,
我们得认识“她”!
思考
物质的性质包括哪几个方面?
化学性质
物理性质
色、味
密度
溶解性
如何研究物质的性质?
颜色、气味、状态等
物质的外观性质
观 察
溶解性、可燃性等
物质的其他性质
实 验
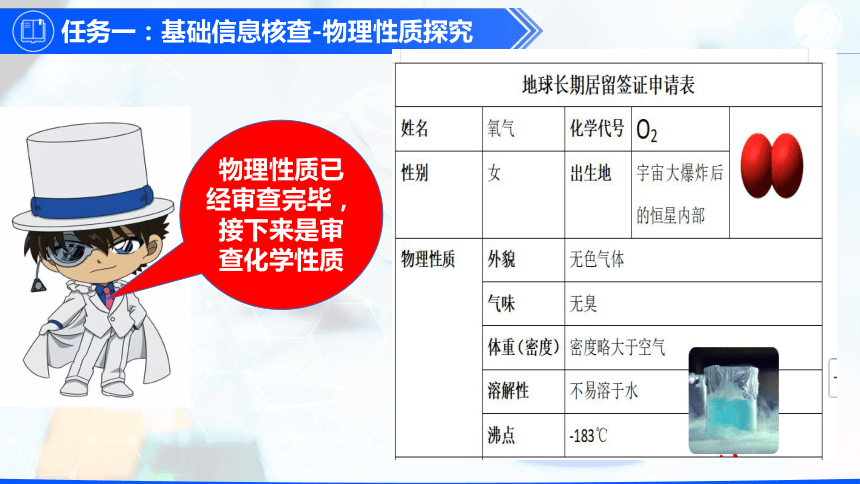
任务一:基础信息核查-物理性质探究
1、色、味、态:
2、密 度:
无色无臭气体
(标准状况下)
氧
气
密度比空气略大
不溶于水
3、溶 解 性:
不易溶于水
水中有溶解的氧气。
思考:鱼为什么能在水中自由呼吸呢?
在室温下,1 L水只能溶解约30 mL氧气
三态转化:
氧气
液态氧
101 kPa
-183 ℃
101 kPa
-219 ℃
物理变化
任务一:基础信息核查-物理性质探究
固态氧
液氧贮存在_____色钢瓶中。
蓝
任务一:基础信息核查-物理性质探究
物理性质已经审查完毕,接下来是审查化学性质
任务二:核心能力验证-化学性质大挑战
氧气女士最著名的能力是什么?如何用实验证明“她”有这种能力?
实验现象
实验结论
带火星的木条 。
氧气能 。
支持燃烧(助燃性)
复燃
挑战1
点燃木条
任务二:核心能力验证-化学性质大挑战
【思考1】如何检验氧气?
将带火星的木条伸入集气瓶中, 若小木条复燃 , 则为氧气 。
操作
现象
结论
检验一种物质的方法总结:
操作+现象+结论,缺一不可!
【思考2】如何检验二氧化碳?
倒入澄清石灰水,振荡,若澄清石灰水变浑浊,则为二氧化碳
任务二:核心能力验证-化学性质大挑战
【思考3】为什么带火星的木条在空气中不能复燃?
空气中氧气的含量相对较少,不足以使带火星木条复燃
【思考4】能使带火星的木条复燃的气体一定是纯净的氧气吗?
不一定,带火星的木条复燃,只能说明气体中氧气含量相对较多
注意:氧气本身是不能燃烧的,不能作燃料
任务二:核心能力验证-化学性质大挑战
实验内容 现 象 木炭在空气中燃烧
木炭在氧气中燃烧 发红光
发白光
放出热量,
产生能使澄清石灰水变浑浊气体
反应表达式:
碳 + 氧气 二氧化碳
点燃
C + O2 点燃 CO2
木炭由上向下缓慢伸入集气瓶的目的是什么?
目的:减少氧气的逸出,使其反应更充分
挑战2
与碳合作
任务二:核心能力验证-化学性质大挑战
挑战3
与硫“切磋”
实验内容 现 象 硫在空气中燃烧
硫在氧气中燃烧 先熔化,发出淡蓝色火焰
发出蓝紫色火焰
放出热量,
产生有刺激性气味气体
集气瓶底水的作用 :
吸收二氧化硫,防止污染空气
通风
反应表达式:
硫 + 氧气 二氧化硫
点燃
S + O2 点燃 SO2
任务二:核心能力验证-化学性质大挑战
挑战4
与铁丝共舞
实验内容 现 象
铁丝在空气中燃烧
铁丝在氧气中燃烧
铁丝在空气中红热
铁丝红热,不能燃烧
剧烈燃烧,火星四射,
放出热量,
生成黑色固体
反应表达式:
铁 +氧气 四氧化三铁
点燃
Fe + O2 点燃 Fe3O4
2.把铁丝绕成螺旋状是什么?
答:增大铁丝与氧气接触面积。增大铁丝的受热面积
3.火柴的作用是什么?为什么火柴即将燃尽时,再插入铁丝?
答:火柴的作用是引燃铁丝。防止火柴燃烧消耗瓶内氧气
4.在集气瓶底部留有少量水的作用分别是什么?能否用细沙代替?
答:防止高温熔化物溅落,炸裂瓶底。可以用细沙代替。
1.做实验前为什么要把铁丝打磨成光亮?
答:除去铁丝表面的铁锈
① 氧气化学性质 ,能和许多物质反应。
剧烈
比较活泼
① 有些在空气中不燃烧的物质,能在氧气中燃烧;
② 物质在氧气里燃烧的程度比在空气里 .
② 燃烧是物质和氧气反应,氧气的 越大,反应就越剧烈.
说明:
浓度
对比木炭、硫和铁丝在空气和氧气中燃烧的现象,我们能得到什么结论?
1.混淆“点燃”和“加热”。
硫 + 氧气 二氧化硫
点燃
2.混淆“点燃”和“燃烧”。
硫 + 氧气 二氧化硫
加热
硫 + 氧气 二氧化硫
燃烧
3.描述实验现象时不能用结论代替现象
(1)铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
(2)硫在氧气中燃烧,产生蓝紫色火焰,生成二氧化硫
(3)红磷燃烧,生成五氧化二磷。
黑色固体
刺激性气味的气体
大量白烟
镁条在空气里燃烧
铜在空气中加热
剧烈燃烧,发出耀眼白光,生成白色固体。
铜片表面变黑。
Cu + O2 CuO
铜 + 氧气 氧化铜
镁 + 氧气 氧化镁
Mg + O2 MgO
木炭
硫粉 铁丝
1.在“测定空气中氧气含量”的实验中,能否用木炭、硫粉或铁丝或镁条来代替红磷?铜呢?
均
不
能
生成物是气体,不能形成压强差
在空气中不能燃烧
镁条也不能,它不仅能与氧气反应,还会与空气中的二氧化碳、氮气反应,导致结果大于五分之一
铜可以,因为铜和空气中的氧气反应生成黑色固体氧化铜。
为什么木炭、铁丝在氧气中燃烧发光无火焰,而硫燃烧发出的是火焰?放热、发光和燃烧又有什么关系?
别着急,且听我娓娓道来
经过我们精密的调查和实验,氧气小姐的化学性质也终于审查完毕
任务二:核心能力验证-化学性质大挑战
1、下列对实验现象的描述不正确的是( )
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.蜡烛在空气中燃烧,生成二氧化碳和水
C.硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体
D.红磷在空气中燃烧,产生大量白烟
B
有三态变化
物理性质
助燃性
氧气的性质
化学性质
通常状况下是无色、无味的气体,密度比空气的略大,不易溶于水
硫 + 氧气 二氧化硫
点燃
铁 + 氧气 四氧化三铁
点燃
碳 + 氧气 二氧化碳
点燃
1.某物质在氧气中燃烧,发出明亮的蓝紫色火焰。该物质是
( )
A.铁丝 B.红磷 C.蜡烛 D.硫粉
2.下列各足量的物质分别在一充满空气的密闭容器中充分燃烧
后,容器中剩余的气体几乎都是氮气的是( )
A.红磷 B.硫粉 C.铁 D.木炭
D
A
3.观察、分析实验现象,可以帮助我们理解科学的本质。下列现象描述不正确的是( )
A.磷在氧气中燃烧,可看到产生大量的白烟
B.硫在氧气中燃烧,可看到产生淡蓝色的火焰
C.铁丝在氧气中燃烧,可看到火星四射
D.木炭在氧气中燃烧,可看到发白光
B
4.下列是化学实验小组的四位同学在实验室做有关氧气性质的实验操作,其中错误的是( )
A.小周将盛有红热木炭的燃烧匙从瓶口缓慢伸入集气瓶中
B.小郑在将细铁丝绕成螺旋状之前先用砂纸把铁丝打磨光亮
C.小吴准备做细铁丝在氧气中燃烧的实验,用排水法收集氧气时,他在集气瓶中留有一部分水
D.小王在酒精灯的火焰上引燃细铁丝底端的木条后立即将其伸入集气瓶中
D
Have a rest
教化学的花花老师
第二单元 空气和氧气
课题2 氧 气
第1课时
Learning aims
学习目标
1.
2.
了解氧气的物理性质和化学性质
学会描述实验现象的一般方法
阅读教材P38-40,解决相关问题:
1、氧气的性质有哪些?
2、怎样检验氧气?
3、木炭在空气中和在氧气中燃烧的实验现象是什么,生成了什么?
相关文字表达式是什么?
4、硫呢?铁呢?
一个“神秘访客”来地球签证中心
申请护照
作为“地球签证官”,我们需要核查“她”的身份信息(性质)。首先,
我们得认识“她”!
思考
物质的性质包括哪几个方面?
化学性质
物理性质
色、味
密度
溶解性
如何研究物质的性质?
颜色、气味、状态等
物质的外观性质
观 察
溶解性、可燃性等
物质的其他性质
实 验
任务一:基础信息核查-物理性质探究
1、色、味、态:
2、密 度:
无色无臭气体
(标准状况下)
氧
气
密度比空气略大
不溶于水
3、溶 解 性:
不易溶于水
水中有溶解的氧气。
思考:鱼为什么能在水中自由呼吸呢?
在室温下,1 L水只能溶解约30 mL氧气
三态转化:
氧气
液态氧
101 kPa
-183 ℃
101 kPa
-219 ℃
物理变化
任务一:基础信息核查-物理性质探究
固态氧
液氧贮存在_____色钢瓶中。
蓝
任务一:基础信息核查-物理性质探究
物理性质已经审查完毕,接下来是审查化学性质
任务二:核心能力验证-化学性质大挑战
氧气女士最著名的能力是什么?如何用实验证明“她”有这种能力?
实验现象
实验结论
带火星的木条 。
氧气能 。
支持燃烧(助燃性)
复燃
挑战1
点燃木条
任务二:核心能力验证-化学性质大挑战
【思考1】如何检验氧气?
将带火星的木条伸入集气瓶中, 若小木条复燃 , 则为氧气 。
操作
现象
结论
检验一种物质的方法总结:
操作+现象+结论,缺一不可!
【思考2】如何检验二氧化碳?
倒入澄清石灰水,振荡,若澄清石灰水变浑浊,则为二氧化碳
任务二:核心能力验证-化学性质大挑战
【思考3】为什么带火星的木条在空气中不能复燃?
空气中氧气的含量相对较少,不足以使带火星木条复燃
【思考4】能使带火星的木条复燃的气体一定是纯净的氧气吗?
不一定,带火星的木条复燃,只能说明气体中氧气含量相对较多
注意:氧气本身是不能燃烧的,不能作燃料
任务二:核心能力验证-化学性质大挑战
实验内容 现 象 木炭在空气中燃烧
木炭在氧气中燃烧 发红光
发白光
放出热量,
产生能使澄清石灰水变浑浊气体
反应表达式:
碳 + 氧气 二氧化碳
点燃
C + O2 点燃 CO2
木炭由上向下缓慢伸入集气瓶的目的是什么?
目的:减少氧气的逸出,使其反应更充分
挑战2
与碳合作
任务二:核心能力验证-化学性质大挑战
挑战3
与硫“切磋”
实验内容 现 象 硫在空气中燃烧
硫在氧气中燃烧 先熔化,发出淡蓝色火焰
发出蓝紫色火焰
放出热量,
产生有刺激性气味气体
集气瓶底水的作用 :
吸收二氧化硫,防止污染空气
通风
反应表达式:
硫 + 氧气 二氧化硫
点燃
S + O2 点燃 SO2
任务二:核心能力验证-化学性质大挑战
挑战4
与铁丝共舞
实验内容 现 象
铁丝在空气中燃烧
铁丝在氧气中燃烧
铁丝在空气中红热
铁丝红热,不能燃烧
剧烈燃烧,火星四射,
放出热量,
生成黑色固体
反应表达式:
铁 +氧气 四氧化三铁
点燃
Fe + O2 点燃 Fe3O4
2.把铁丝绕成螺旋状是什么?
答:增大铁丝与氧气接触面积。增大铁丝的受热面积
3.火柴的作用是什么?为什么火柴即将燃尽时,再插入铁丝?
答:火柴的作用是引燃铁丝。防止火柴燃烧消耗瓶内氧气
4.在集气瓶底部留有少量水的作用分别是什么?能否用细沙代替?
答:防止高温熔化物溅落,炸裂瓶底。可以用细沙代替。
1.做实验前为什么要把铁丝打磨成光亮?
答:除去铁丝表面的铁锈
① 氧气化学性质 ,能和许多物质反应。
剧烈
比较活泼
① 有些在空气中不燃烧的物质,能在氧气中燃烧;
② 物质在氧气里燃烧的程度比在空气里 .
② 燃烧是物质和氧气反应,氧气的 越大,反应就越剧烈.
说明:
浓度
对比木炭、硫和铁丝在空气和氧气中燃烧的现象,我们能得到什么结论?
1.混淆“点燃”和“加热”。
硫 + 氧气 二氧化硫
点燃
2.混淆“点燃”和“燃烧”。
硫 + 氧气 二氧化硫
加热
硫 + 氧气 二氧化硫
燃烧
3.描述实验现象时不能用结论代替现象
(1)铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
(2)硫在氧气中燃烧,产生蓝紫色火焰,生成二氧化硫
(3)红磷燃烧,生成五氧化二磷。
黑色固体
刺激性气味的气体
大量白烟
镁条在空气里燃烧
铜在空气中加热
剧烈燃烧,发出耀眼白光,生成白色固体。
铜片表面变黑。
Cu + O2 CuO
铜 + 氧气 氧化铜
镁 + 氧气 氧化镁
Mg + O2 MgO
木炭
硫粉 铁丝
1.在“测定空气中氧气含量”的实验中,能否用木炭、硫粉或铁丝或镁条来代替红磷?铜呢?
均
不
能
生成物是气体,不能形成压强差
在空气中不能燃烧
镁条也不能,它不仅能与氧气反应,还会与空气中的二氧化碳、氮气反应,导致结果大于五分之一
铜可以,因为铜和空气中的氧气反应生成黑色固体氧化铜。
为什么木炭、铁丝在氧气中燃烧发光无火焰,而硫燃烧发出的是火焰?放热、发光和燃烧又有什么关系?
别着急,且听我娓娓道来
经过我们精密的调查和实验,氧气小姐的化学性质也终于审查完毕
任务二:核心能力验证-化学性质大挑战
1、下列对实验现象的描述不正确的是( )
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.蜡烛在空气中燃烧,生成二氧化碳和水
C.硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体
D.红磷在空气中燃烧,产生大量白烟
B
有三态变化
物理性质
助燃性
氧气的性质
化学性质
通常状况下是无色、无味的气体,密度比空气的略大,不易溶于水
硫 + 氧气 二氧化硫
点燃
铁 + 氧气 四氧化三铁
点燃
碳 + 氧气 二氧化碳
点燃
1.某物质在氧气中燃烧,发出明亮的蓝紫色火焰。该物质是
( )
A.铁丝 B.红磷 C.蜡烛 D.硫粉
2.下列各足量的物质分别在一充满空气的密闭容器中充分燃烧
后,容器中剩余的气体几乎都是氮气的是( )
A.红磷 B.硫粉 C.铁 D.木炭
D
A
3.观察、分析实验现象,可以帮助我们理解科学的本质。下列现象描述不正确的是( )
A.磷在氧气中燃烧,可看到产生大量的白烟
B.硫在氧气中燃烧,可看到产生淡蓝色的火焰
C.铁丝在氧气中燃烧,可看到火星四射
D.木炭在氧气中燃烧,可看到发白光
B
4.下列是化学实验小组的四位同学在实验室做有关氧气性质的实验操作,其中错误的是( )
A.小周将盛有红热木炭的燃烧匙从瓶口缓慢伸入集气瓶中
B.小郑在将细铁丝绕成螺旋状之前先用砂纸把铁丝打磨光亮
C.小吴准备做细铁丝在氧气中燃烧的实验,用排水法收集氧气时,他在集气瓶中留有一部分水
D.小王在酒精灯的火焰上引燃细铁丝底端的木条后立即将其伸入集气瓶中
D
Have a rest
同课章节目录
