3.2.1 原子的构成 相对原子质量课件(共23张PPT) 2025-2026学年人教版(2024)初中化学九年级上册
文档属性
| 名称 | 3.2.1 原子的构成 相对原子质量课件(共23张PPT) 2025-2026学年人教版(2024)初中化学九年级上册 |  | |
| 格式 | pptx | ||
| 文件大小 | 28.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-23 15:01:01 | ||
图片预览







文档简介
(共23张PPT)
人教版九上
3.2 原子结构
(第一课时 原子的构成 相对原子质量)
1.知道原子的构成以及构成粒子间关系。
2.认识相对原子质量的含义及应用。
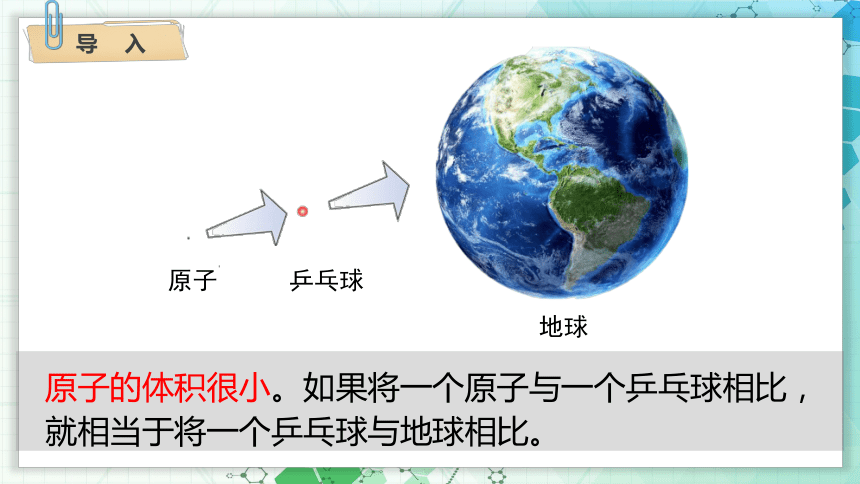
原子的体积很小。如果将一个原子与一个乒乓球相比,就相当于将一个乒乓球与地球相比。
原子
乒乓球
地球
这么小的原子人们是怎样认识它的?原子在化学变化中不可再分,但它也有自己的内部结构,人类探索原子结构经历了漫长的过程。
原子的构成
预习
准备
人类探索原子结构的过程:
1808年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
19世纪末,汤姆孙在原子内发现了电子,提出“枣糕模型”,人们抛弃了原子不可分割的观念。
实心球模型
枣糕模型
预习
准备
人类探索原子结构的过程:
1911年,卢瑟福通过α粒子散射实验证明在原子中心有一个极小的核,电子绕核运动,并提出了“行星模型”
行星模型
预习
准备
人类探索原子结构的过程:
原子内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
预习
准备
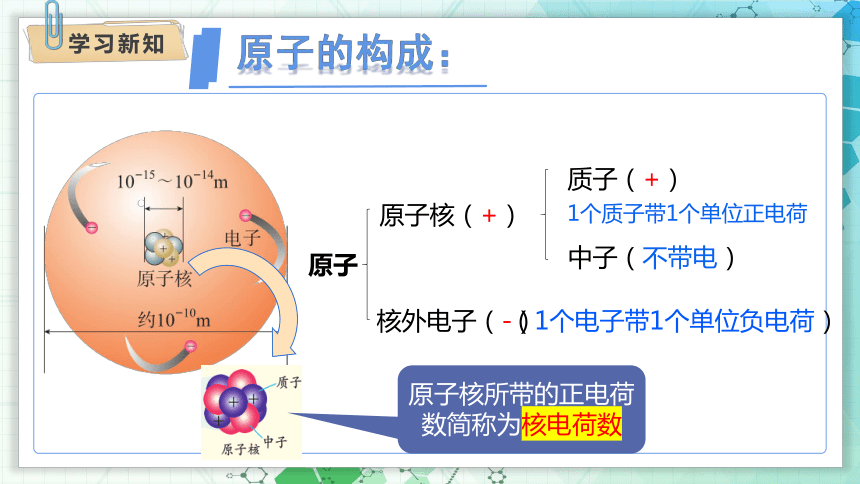
原子的构成:
原子内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子核(+)
中子(不带电)
1个质子带1个单位正电荷
(1个电子带1个单位负电荷)
核外电子(-)
质子(+)
原子
原子的构成:
原子核所带的正电荷数简称为核电荷数
预习
准备
思考与讨论
观察表中不同原子中各微观粒子的数目,你有什么发现?
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
不同种类的原子核内质子数不同。
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
并不是所有的原子中都含有中子(如氢原子)。
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
质子数与中子数不一定相等。
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
核电荷数=质子数=核外电子数。
原子不显电性
相对原子质量
预习
准备
思考与讨论
观察以下表格,你有什么发现?
粒子种类 质量
质子 1.6726×10-27kg
中子 1.6729×10-27kg
电子 质子质量的1/1836
构成原子的粒子的质量
2. 不同粒子的质量不同;
1. 电子质量很小,原子的质量主要集中在原子核上;
3. 如此小的数据书写、使用均不方便。
预习
准备
相对原子质量:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
定义:
以一种碳原子质量的1/12为标准,其他原子的质量与它相比,得到相对原子质量(符号Ar)。
公式:
某原子的相对原子质量=
该原子的质量
碳-12原子的质量×1/12
预习
准备
相对原子质量:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
注意:
相对原子质量不等于原子的实际质量,是个比值。
原子实际质量越大,它的相对原子质量数值越大。
相对原子质量的单位是“1”(书写时一般省略),原子实际质量的常用单位是:千克。
预习
准备
思考与讨论
观察以下表格,你有什么发现?
相对原子质量与质子数和中子数的关系
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
铁 26 30 26 56
预习
准备
相对原子质量:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
相对原子质量与质子数和中子数的关系
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
铁 26 30 26 56
在数值上,相对原子质量=质子数+中子数
原子结构(第一课时)
核外电子
原子的构成
相对原子质量
=质子数+中子数
原子核
质子
定义
中子
1.下列说法正确的是( )
A.任何原子都是由质子、中子和电子构成的
B.因为原子中质子带正电,中子不带电,故整个原子带正电
C.核电荷数=核外电子数
D.分子可分,原子不可分
C
2.已知某种锶原子核内中子数为50,核外电子数为38,则该种锶原子的相对原子质量可能为( )
A.12 B.38 C.50 D.88
D
3.钠、镁、铝、铁的相对原子质量分别为23、24、27、56,等质量的钠、镁、铝、铁四种金属,含原子数最多的是( )
A.钠 B.镁 C.铝 D.铁
A
人教版九上
3.2 原子结构
(第一课时 原子的构成 相对原子质量)
1.知道原子的构成以及构成粒子间关系。
2.认识相对原子质量的含义及应用。
原子的体积很小。如果将一个原子与一个乒乓球相比,就相当于将一个乒乓球与地球相比。
原子
乒乓球
地球
这么小的原子人们是怎样认识它的?原子在化学变化中不可再分,但它也有自己的内部结构,人类探索原子结构经历了漫长的过程。
原子的构成
预习
准备
人类探索原子结构的过程:
1808年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
19世纪末,汤姆孙在原子内发现了电子,提出“枣糕模型”,人们抛弃了原子不可分割的观念。
实心球模型
枣糕模型
预习
准备
人类探索原子结构的过程:
1911年,卢瑟福通过α粒子散射实验证明在原子中心有一个极小的核,电子绕核运动,并提出了“行星模型”
行星模型
预习
准备
人类探索原子结构的过程:
原子内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
预习
准备
原子的构成:
原子内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子核(+)
中子(不带电)
1个质子带1个单位正电荷
(1个电子带1个单位负电荷)
核外电子(-)
质子(+)
原子
原子的构成:
原子核所带的正电荷数简称为核电荷数
预习
准备
思考与讨论
观察表中不同原子中各微观粒子的数目,你有什么发现?
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
不同种类的原子核内质子数不同。
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
并不是所有的原子中都含有中子(如氢原子)。
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
质子数与中子数不一定相等。
预习
准备
原子的构成:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
核电荷数=质子数=核外电子数。
原子不显电性
相对原子质量
预习
准备
思考与讨论
观察以下表格,你有什么发现?
粒子种类 质量
质子 1.6726×10-27kg
中子 1.6729×10-27kg
电子 质子质量的1/1836
构成原子的粒子的质量
2. 不同粒子的质量不同;
1. 电子质量很小,原子的质量主要集中在原子核上;
3. 如此小的数据书写、使用均不方便。
预习
准备
相对原子质量:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
定义:
以一种碳原子质量的1/12为标准,其他原子的质量与它相比,得到相对原子质量(符号Ar)。
公式:
某原子的相对原子质量=
该原子的质量
碳-12原子的质量×1/12
预习
准备
相对原子质量:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
注意:
相对原子质量不等于原子的实际质量,是个比值。
原子实际质量越大,它的相对原子质量数值越大。
相对原子质量的单位是“1”(书写时一般省略),原子实际质量的常用单位是:千克。
预习
准备
思考与讨论
观察以下表格,你有什么发现?
相对原子质量与质子数和中子数的关系
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
铁 26 30 26 56
预习
准备
相对原子质量:
原内有相对很大的空间,在原子中心有一个体积小、质量大、带正电的原子核。
相对原子质量与质子数和中子数的关系
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
铁 26 30 26 56
在数值上,相对原子质量=质子数+中子数
原子结构(第一课时)
核外电子
原子的构成
相对原子质量
=质子数+中子数
原子核
质子
定义
中子
1.下列说法正确的是( )
A.任何原子都是由质子、中子和电子构成的
B.因为原子中质子带正电,中子不带电,故整个原子带正电
C.核电荷数=核外电子数
D.分子可分,原子不可分
C
2.已知某种锶原子核内中子数为50,核外电子数为38,则该种锶原子的相对原子质量可能为( )
A.12 B.38 C.50 D.88
D
3.钠、镁、铝、铁的相对原子质量分别为23、24、27、56,等质量的钠、镁、铝、铁四种金属,含原子数最多的是( )
A.钠 B.镁 C.铝 D.铁
A
同课章节目录
