第二单元认识物质的构成 单元测试(含答案) 2025-2026学年化学鲁教版(2024)九年级上册
文档属性
| 名称 | 第二单元认识物质的构成 单元测试(含答案) 2025-2026学年化学鲁教版(2024)九年级上册 |  | |
| 格式 | docx | ||
| 文件大小 | 169.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-29 23:28:15 | ||
图片预览


文档简介
第二单元 认识物质的构成
班级:______ 姓名:______ 学号:______ 得分:______
可能用到的相对原子质量:H—1 C—12 O—16 Fe—56
一、 选择题:共10题,每小题只有一个选项最符合题意。
1. (2025宿迁沭阳期中)化学用语是最简明、信息丰富、国际通用的语言。下列对化学用语解释不正确的是( )
A. 2H——2个氢元素 B. N2——氮气
C. 2H2O——2个水分子 D. Mg2+——镁离子
2. (2025无锡惠山阶段考)我国著名科学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕等几种元素的相对原子质量新值,其中他测定核电荷数为63的铕元素的相对原子质量的新值为152。则下列说法正确的是( )
A. 铕元素的原子核内的质子数为63
B. 铕元素的原子核内的中子数为63
C. 铕元素的原子核外电子数为89
D. 铕元素的原子的质量为152
3. (2025宿城期中)下列化学符号中,数字“2”表示的意义不正确的是( )
A. 2O:2个氧分子
B. H2O:1个水分子中有2个氢原子
C. :正二价的钙元素
D. Mg2+:1个镁离子带2个单位正电荷
4. (2025宿城期中)推理是初中化学常用的思维方法。下列推理正确的是( )
A. 氧化物中含有氧元素,所以含有氧元素的物质一定是氧化物
B. 同种元素的核内质子数都相同,所以核内质子数相同的微粒一定属于同种元素
C. 离子是带电荷的微粒,所以带电荷的微粒一定是离子
D. 单质中只含一种元素,所以由一种元素组成的纯净物一定是单质
5. (2025苏州外国语月考)目前大部分新能源汽车采用磷酸铁锂电池,已知Li元素在元素周期表中的信息如图1,生产该电池时,需添加适量的石墨烯(如图2)作导电剂,提高电池的性能。下列有关说法正确的是( )
图1 图2
A. 锂离子核外有3个电子 B. 锂元素的相对原子质量为6.94 g
C. 石墨烯属于化合物 D. 石墨烯具有导电性
6. (2025南通海安期末)铅存在多种原子:铅206,铅207,铅208。结合图中信息,下列说法正确的是( )
A. 铅原子的中子数为82
B. 在反应中,金属铅易得电子形成阴离子
C. 上述三种铅原子在周期表中占有相同的位置
D. 金属铅具有滑腻感,因此铅笔芯有助于打开生锈的铁锁
7. 在太空舱里,常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,NiFe2O4中Fe的化合价为+3,则Ni的化合价为( )
A. +4 B. +3 C. +2 D. +1
8. (2025宿迁沭阳期中)起云剂是一种合法的食品添加剂,黑心厂家用塑化剂替代,给人体健康带来危害。DEHP是塑化剂中的一种,其化学式为C24H38O4。下列关于塑化剂DEHP的说法不正确的是( )
A. DEHP由碳、氢、氧三种元素组成
B. DEHP中有4个氧原子
C. DEHP分子中碳、氢原子个数比为12∶19
D. DEHP的相对分子质量为390
9. (2025宿迁月考)化学观念是核心素养之一。下列有关化学观念的说法错误的是( )
A. 组成观:金刚石与石墨的组成元素相同
B. 变化观:铁在潮湿的空气中容易生锈,铁生锈属于化学变化
C. 微粒观:构成氧化镁的微粒是氧化镁离子
D. 结构观:二氧化碳和一氧化碳的分子构成不同,它们的化学性质不同
10. “归纳推理”是化学学习过程中常用的思维方法,以下类推结果正确的是( )
A. Na+、Cl-的最外层电子数均为8,则最外层电子数为8的粒子都是离子
B. 化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
C. 化学反应中通常伴随着发光放热现象,所以有发光放热现象的变化一定是化学变化
D. 氮气能使燃烧的木条熄灭,所以能使燃烧的木条熄灭的气体一定是氮气
二、 填空题:共3题。
11. (2025宿迁宿城月考)已知:相对原子质量是一个某原子的实际质量与一个碳12原子质量的的比值,一个碳12原子的质量为a kg。请根据相关信息进行计算。
(1) 已知镁的相对原子质量为24,则镁原子实际质量为________。
(2) 已知钾原子质量约等于一个碳12原子质量的3.25倍,则钾原子的相对原子质量为________。
(3) 若R原子的相对原子质量为23,核内质子数比中子数少一个,则R原子的质子数为________。
12. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式,请结合所学回答下列问题。
(1) 氦气是由________(填名称)构成的,氯化钠是由________(填离子符号,下同)和________构成的。保持过氧化氢的化学性质的最小粒子是____________(填名称)。
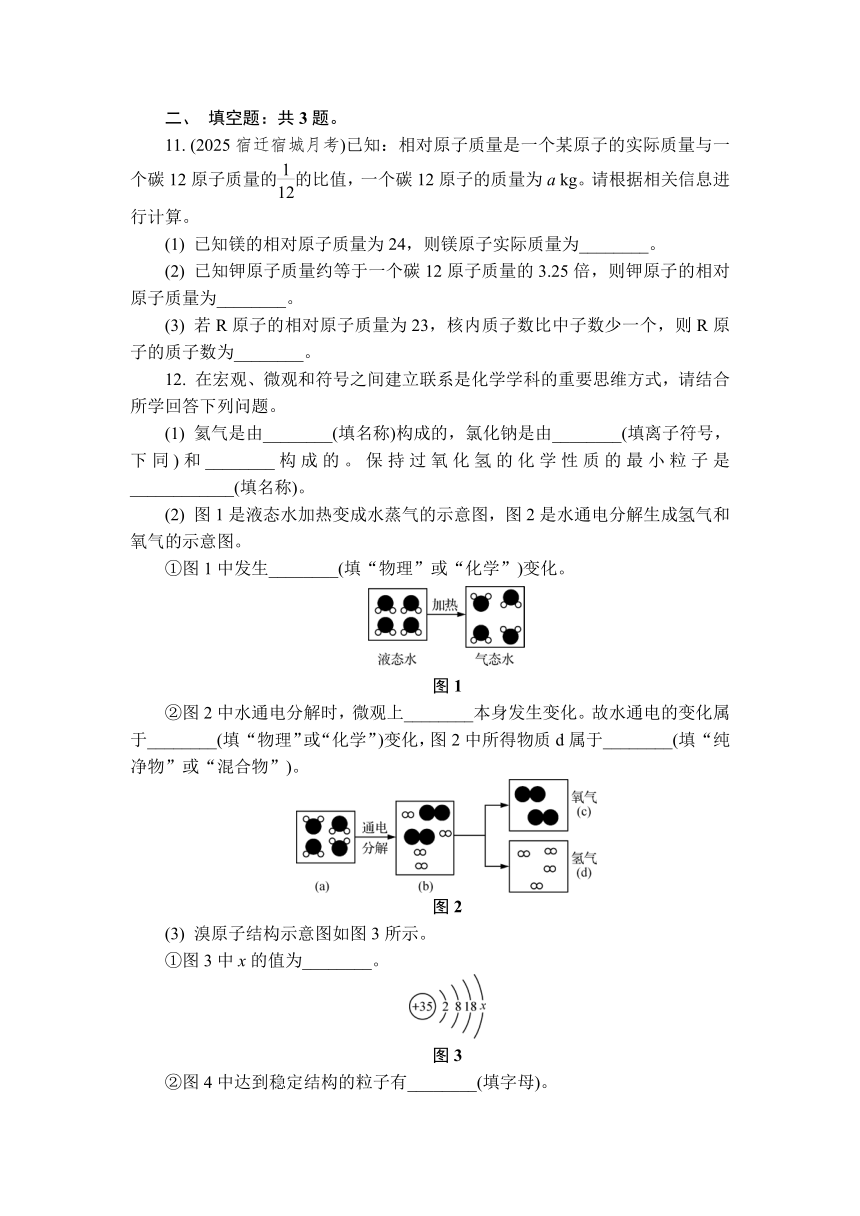
(2) 图1是液态水加热变成水蒸气的示意图,图2是水通电分解生成氢气和氧气的示意图。
①图1中发生________(填“物理”或“化学”)变化。
图1
②图2中水通电分解时,微观上________本身发生变化。故水通电的变化属于________(填“物理”或“化学”)变化,图2中所得物质d属于________(填“纯净物”或“混合物”)。
图2
(3) 溴原子结构示意图如图3所示。
①图3中x的值为________。
图3
②图4中达到稳定结构的粒子有________(填字母)。
A B C D
图4
③C在反应中容易________(填“得到”或“失去”)电子形成离子,所形成的离子符号为________。
13. 某品牌矿泉水外包装上部分文字说明如表所示,请回答下列问题。
天然矿泉水特征性指标:mg/L
锶(Sr) 偏硅酸(H2SiO3) 镁离子(Mg2+) 碳酸氢根离子(HCO) 氯离子(Cl-) 钙离子(Ca2+)
0.200~0.500 25.00~55.00 6.00~15.00 200.00~600.00 3.00~10.00 3.00~10.00
(1) 请用化学用语表示:氯离子________。
(2) Ca2+中“2+”的含义为____________________。
(3) 镁离子(Mg2+)表示镁原子________(填“失去”或“得到”)2个电子形成的________(填“阴”或“阳”)离子。
(4) 标出矿泉水中所含偏硅酸(H2SiO3)中硅元素的化合价:________。
(5) 结合表中信息请你写出碳酸氢钙的化学式:________。
三、 推理、计算题:共2题。
14. 已破损的维生素C(简写为Vc,其化学式为C6H8Ox)的说明书部分信息如图所示。
请回答下列问题。
(1) 维生素C中,碳原子与氢原子的个数比为________(填最简整数比,下同)。
(2) 维生素C中的碳元素与氢元素质量比为________。
(3) 维生素C中碳元素的质量分数为________(计算结果精确到0.1%)。
(4) 根据说明书可求出x,则维生素C的化学式为________。
(5) 小辉妈妈每天服用该维生素C片剂,小辉建议妈妈可食用西红柿来代替维生素C片,若100 g 西红柿含维生素C 30 mg,则小辉妈妈每天食用西红柿________g,即可达到服用上述维生素C片的效果。
15. 氧化铁的化学式为Fe2O3,请列式计算:
(1) 氧化铁的相对分子质量。
(2) 氧化铁中铁元素、氧元素的质量之比。
(3) 氧化铁中铁元素的质量分数。
1. A 2. A 3. A 4. D 5. D 6. C 7. C 8. B 9. C 10. B
11. (1) 2a kg (2) 39 (3) 11
12. (1) 氦原子 Na+ Cl- 过氧化氢分子
(2) ①物理 ②水分子 化学 纯净物
(3) ①7 ②AD ③得到 S2-
13. (1) Cl- (2) 1个钙离子带2个单位的正电荷 (3) 失去 阳 (4) H2O3
(5) Ca(HCO3)2
14. (1) 3∶4 (2) 9∶1 (3) 40.9% (4) C6H8O6 (5) 200
15. (1) 相对分子质量=(相对原子质量×原子个数)之和,氧化铁的相对分子质量=(56×2)+(16×3)=160
(2)氧化铁中铁元素、氧元素的质量之比=(56×2)∶(16×3)=7∶3
(3) 化合物中铁元素的质量分数=×100%=70%
班级:______ 姓名:______ 学号:______ 得分:______
可能用到的相对原子质量:H—1 C—12 O—16 Fe—56
一、 选择题:共10题,每小题只有一个选项最符合题意。
1. (2025宿迁沭阳期中)化学用语是最简明、信息丰富、国际通用的语言。下列对化学用语解释不正确的是( )
A. 2H——2个氢元素 B. N2——氮气
C. 2H2O——2个水分子 D. Mg2+——镁离子
2. (2025无锡惠山阶段考)我国著名科学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕等几种元素的相对原子质量新值,其中他测定核电荷数为63的铕元素的相对原子质量的新值为152。则下列说法正确的是( )
A. 铕元素的原子核内的质子数为63
B. 铕元素的原子核内的中子数为63
C. 铕元素的原子核外电子数为89
D. 铕元素的原子的质量为152
3. (2025宿城期中)下列化学符号中,数字“2”表示的意义不正确的是( )
A. 2O:2个氧分子
B. H2O:1个水分子中有2个氢原子
C. :正二价的钙元素
D. Mg2+:1个镁离子带2个单位正电荷
4. (2025宿城期中)推理是初中化学常用的思维方法。下列推理正确的是( )
A. 氧化物中含有氧元素,所以含有氧元素的物质一定是氧化物
B. 同种元素的核内质子数都相同,所以核内质子数相同的微粒一定属于同种元素
C. 离子是带电荷的微粒,所以带电荷的微粒一定是离子
D. 单质中只含一种元素,所以由一种元素组成的纯净物一定是单质
5. (2025苏州外国语月考)目前大部分新能源汽车采用磷酸铁锂电池,已知Li元素在元素周期表中的信息如图1,生产该电池时,需添加适量的石墨烯(如图2)作导电剂,提高电池的性能。下列有关说法正确的是( )
图1 图2
A. 锂离子核外有3个电子 B. 锂元素的相对原子质量为6.94 g
C. 石墨烯属于化合物 D. 石墨烯具有导电性
6. (2025南通海安期末)铅存在多种原子:铅206,铅207,铅208。结合图中信息,下列说法正确的是( )
A. 铅原子的中子数为82
B. 在反应中,金属铅易得电子形成阴离子
C. 上述三种铅原子在周期表中占有相同的位置
D. 金属铅具有滑腻感,因此铅笔芯有助于打开生锈的铁锁
7. 在太空舱里,常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,NiFe2O4中Fe的化合价为+3,则Ni的化合价为( )
A. +4 B. +3 C. +2 D. +1
8. (2025宿迁沭阳期中)起云剂是一种合法的食品添加剂,黑心厂家用塑化剂替代,给人体健康带来危害。DEHP是塑化剂中的一种,其化学式为C24H38O4。下列关于塑化剂DEHP的说法不正确的是( )
A. DEHP由碳、氢、氧三种元素组成
B. DEHP中有4个氧原子
C. DEHP分子中碳、氢原子个数比为12∶19
D. DEHP的相对分子质量为390
9. (2025宿迁月考)化学观念是核心素养之一。下列有关化学观念的说法错误的是( )
A. 组成观:金刚石与石墨的组成元素相同
B. 变化观:铁在潮湿的空气中容易生锈,铁生锈属于化学变化
C. 微粒观:构成氧化镁的微粒是氧化镁离子
D. 结构观:二氧化碳和一氧化碳的分子构成不同,它们的化学性质不同
10. “归纳推理”是化学学习过程中常用的思维方法,以下类推结果正确的是( )
A. Na+、Cl-的最外层电子数均为8,则最外层电子数为8的粒子都是离子
B. 化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
C. 化学反应中通常伴随着发光放热现象,所以有发光放热现象的变化一定是化学变化
D. 氮气能使燃烧的木条熄灭,所以能使燃烧的木条熄灭的气体一定是氮气
二、 填空题:共3题。
11. (2025宿迁宿城月考)已知:相对原子质量是一个某原子的实际质量与一个碳12原子质量的的比值,一个碳12原子的质量为a kg。请根据相关信息进行计算。
(1) 已知镁的相对原子质量为24,则镁原子实际质量为________。
(2) 已知钾原子质量约等于一个碳12原子质量的3.25倍,则钾原子的相对原子质量为________。
(3) 若R原子的相对原子质量为23,核内质子数比中子数少一个,则R原子的质子数为________。
12. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式,请结合所学回答下列问题。
(1) 氦气是由________(填名称)构成的,氯化钠是由________(填离子符号,下同)和________构成的。保持过氧化氢的化学性质的最小粒子是____________(填名称)。
(2) 图1是液态水加热变成水蒸气的示意图,图2是水通电分解生成氢气和氧气的示意图。
①图1中发生________(填“物理”或“化学”)变化。
图1
②图2中水通电分解时,微观上________本身发生变化。故水通电的变化属于________(填“物理”或“化学”)变化,图2中所得物质d属于________(填“纯净物”或“混合物”)。
图2
(3) 溴原子结构示意图如图3所示。
①图3中x的值为________。
图3
②图4中达到稳定结构的粒子有________(填字母)。
A B C D
图4
③C在反应中容易________(填“得到”或“失去”)电子形成离子,所形成的离子符号为________。
13. 某品牌矿泉水外包装上部分文字说明如表所示,请回答下列问题。
天然矿泉水特征性指标:mg/L
锶(Sr) 偏硅酸(H2SiO3) 镁离子(Mg2+) 碳酸氢根离子(HCO) 氯离子(Cl-) 钙离子(Ca2+)
0.200~0.500 25.00~55.00 6.00~15.00 200.00~600.00 3.00~10.00 3.00~10.00
(1) 请用化学用语表示:氯离子________。
(2) Ca2+中“2+”的含义为____________________。
(3) 镁离子(Mg2+)表示镁原子________(填“失去”或“得到”)2个电子形成的________(填“阴”或“阳”)离子。
(4) 标出矿泉水中所含偏硅酸(H2SiO3)中硅元素的化合价:________。
(5) 结合表中信息请你写出碳酸氢钙的化学式:________。
三、 推理、计算题:共2题。
14. 已破损的维生素C(简写为Vc,其化学式为C6H8Ox)的说明书部分信息如图所示。
请回答下列问题。
(1) 维生素C中,碳原子与氢原子的个数比为________(填最简整数比,下同)。
(2) 维生素C中的碳元素与氢元素质量比为________。
(3) 维生素C中碳元素的质量分数为________(计算结果精确到0.1%)。
(4) 根据说明书可求出x,则维生素C的化学式为________。
(5) 小辉妈妈每天服用该维生素C片剂,小辉建议妈妈可食用西红柿来代替维生素C片,若100 g 西红柿含维生素C 30 mg,则小辉妈妈每天食用西红柿________g,即可达到服用上述维生素C片的效果。
15. 氧化铁的化学式为Fe2O3,请列式计算:
(1) 氧化铁的相对分子质量。
(2) 氧化铁中铁元素、氧元素的质量之比。
(3) 氧化铁中铁元素的质量分数。
1. A 2. A 3. A 4. D 5. D 6. C 7. C 8. B 9. C 10. B
11. (1) 2a kg (2) 39 (3) 11
12. (1) 氦原子 Na+ Cl- 过氧化氢分子
(2) ①物理 ②水分子 化学 纯净物
(3) ①7 ②AD ③得到 S2-
13. (1) Cl- (2) 1个钙离子带2个单位的正电荷 (3) 失去 阳 (4) H2O3
(5) Ca(HCO3)2
14. (1) 3∶4 (2) 9∶1 (3) 40.9% (4) C6H8O6 (5) 200
15. (1) 相对分子质量=(相对原子质量×原子个数)之和,氧化铁的相对分子质量=(56×2)+(16×3)=160
(2)氧化铁中铁元素、氧元素的质量之比=(56×2)∶(16×3)=7∶3
(3) 化合物中铁元素的质量分数=×100%=70%
同课章节目录
