第五单元定量研究化学反应 单元测试 (含答案) 2025-2026学年化学鲁教版(2024)九年级上册
文档属性
| 名称 | 第五单元定量研究化学反应 单元测试 (含答案) 2025-2026学年化学鲁教版(2024)九年级上册 |  | |
| 格式 | docx | ||
| 文件大小 | 612.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-29 23:38:50 | ||
图片预览


文档简介
第五单元 定量研究化学反应
班级:______ 姓名:______ 学号:______ 得分:______
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5 K—39 Ca—40 Fe—56
一、 选择题:共10题,每小题只有一个选项最符合题意。
1. (2025扬州树人集团一模)下列物质燃烧不会生成水的是( )
A. C2H5OH B. CH4 C. CO D. H2
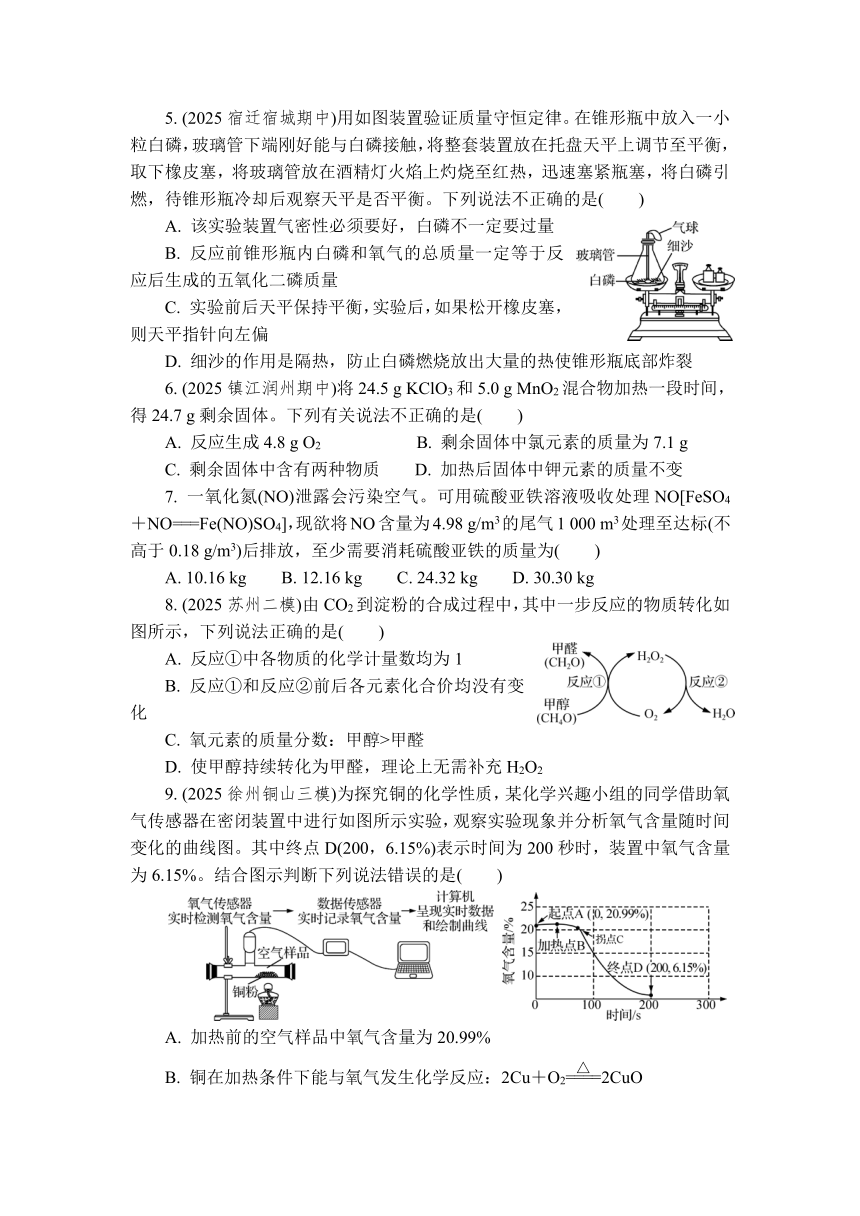
2. (2025南京秦淮二模)以下示意图描述了两种物质的变化过程,其中“”表示氧原子,“”表示氢原子。下列说法不正确的是( )
图1 图2
A. 图1所示过程属于物理变化
B. 图2是过氧化氢分解的示意图
C. 图1所示过程中,分子间的间隔增大
D. 图2所示过程中,原子的数目变多
3. (2025扬州广陵二模)呼吸面罩中的过氧化钠固体与人体呼出的二氧化碳反应产生碳酸钠和氧气,此反应涉及的化学用语表示正确的是( )
A. 2个碳酸根离子:2CO
B. 过氧化钠中氧元素化合价:Na22
C. CO2中数字“2”的意义:一个二氧化碳分子中含有2个氧原子
D. Na2O2+CO2===Na2CO3+O2
4. (2025南京秦淮一模)丙烷(化学式为C3H8)是液化石油气的主要成分之一。现有4.4 g丙烷与一定量氧气混合于密闭容器内,在一定条件下全部转化为一氧化碳、二氧化碳和水,恢复至室温,测得所得气体中氧元素质量分数为70%,则参加反应的氧气的质量为( )
A. 16 g B. 14.8 g C. 11.2 g D. 8.4 g
5. (2025宿迁宿城期中)用如图装置验证质量守恒定律。在锥形瓶中放入一小粒白磷,玻璃管下端刚好能与白磷接触,将整套装置放在托盘天平上调节至平衡,取下橡皮塞,将玻璃管放在酒精灯火焰上灼烧至红热,迅速塞紧瓶塞,将白磷引燃,待锥形瓶冷却后观察天平是否平衡。下列说法不正确的是( )
392747579375A. 该实验装置气密性必须要好,白磷不一定要过量
B. 反应前锥形瓶内白磷和氧气的总质量一定等于反应后生成的五氧化二磷质量
C. 实验前后天平保持平衡,实验后,如果松开橡皮塞,则天平指针向左偏
D. 细沙的作用是隔热,防止白磷燃烧放出大量的热使锥形瓶底部炸裂
6. (2025镇江润州期中)将24.5 g KClO3和5.0 g MnO2混合物加热一段时间,得24.7 g剩余固体。下列有关说法不正确的是( )
A. 反应生成4.8 g O2 B. 剩余固体中氯元素的质量为7.1 g
C. 剩余固体中含有两种物质 D. 加热后固体中钾元素的质量不变
7. 一氧化氮(NO)泄露会污染空气。可用硫酸亚铁溶液吸收处理NO[FeSO4+NO===Fe(NO)SO4],现欲将NO含量为4.98 g/m3的尾气1 000 m3处理至达标(不高于0.18 g/m3)后排放,至少需要消耗硫酸亚铁的质量为( )
A. 10.16 kg B. 12.16 kg C. 24.32 kg D. 30.30 kg
35814004521208. (2025苏州二模)由CO2到淀粉的合成过程中,其中一步反应的物质转化如图所示,下列说法正确的是( )
A. 反应①中各物质的化学计量数均为1
B. 反应①和反应②前后各元素化合价均没有变化
C. 氧元素的质量分数:甲醇>甲醛
D. 使甲醇持续转化为甲醛,理论上无需补充H2O2
9. (2025徐州铜山三模)为探究铜的化学性质,某化学兴趣小组的同学借助氧气传感器在密闭装置中进行如图所示实验,观察实验现象并分析氧气含量随时间变化的曲线图。其中终点D(200,6.15%)表示时间为200秒时,装置中氧气含量为6.15%。结合图示判断下列说法错误的是( )
A. 加热前的空气样品中氧气含量为20.99%
B. 铜在加热条件下能与氧气发生化学反应:2Cu+O22CuO
C. 拐点C至终点D所对应的时间范围内,装置内物质的总质量逐渐减少
D. 通过现象证据和数据证据,可以从定性和定量的视角分析得出合理解释
10. (2025宿迁宿城期中)某密闭容器中有M、氧气、二氧化碳和水四种物质,在一定条件下充分反应,测得各物质的质量如表所示。根据表中信息,判断下列说法正确的是( )
物质
M
氧气
二氧化碳
水
反应前的质量/g
23
64
8
5
反应后的质量/g
0
16
52
待测x
A. 待测x的值为27
B. M由碳、氢元素组成
C. 该反应属于化合反应
D. M中碳、氢元素质量比为4∶1
二、 填空、简答题:共2题。
11. (2025宿迁宿豫月考)近代化学史上对质量守恒定律、空气组成的研究都具有伟大意义。
图1 图2
(1) 图1装置探究空气中氧气的含量,硬质玻璃管内发生反应的化学方程式为________________,冷却至室温后,注射器内剩余气体的体积为6 mL,测得氧气的体积分数为________。该结果与空气中氧气的实际体积分数产生差异的原因是____________________(写出一点即可)。
(2) 图2是测定镁条燃烧前后质量的实验。镁条在空气中完全燃烧后,称量发现陶土网上燃烧产物的质量比反应前镁条质量小,其主要原因是________________________。为了正确验证质量守恒定律,改进了镁条燃烧的实验,成功并绘制了反应物和生成物各物质的质量关系图像,b物质应是________。
12. 某科学兴趣小组的同学设计了下图系列实验来探究化学反应前后的质量关系。
甲 乙
图1 图2
(1) 甲实验中,镁条剧烈燃烧,产生大量白烟,写出该反应的化学方程式:_______________________。某同学将两份m1 g的镁条和足量氧气分别置于密闭装置和开放装置中充分反应,实验过程中陶土网上盛接到的固体质量(m)随加热时间(t)变化如图2所示。下列有关分析错误的是 (填字母)。
A. 0B. m1与m2质量之差等于反应被消耗的氧气质量
C. m3D. m1与m3质量之差等于散逸走的氧化镁的质量
(2) 用乙装置改进实验甲,发现镁条燃烧除生成白色固体外,还有少量的淡黄色固体生成。这种淡黄色固体是什么呢?同学们在老师的指导下进行有关实验探究。
资料:镁能与氮气剧烈反应生成黄色的氮化镁固体;氮化镁可与水剧烈反应产生氨气和另一种化合物,氨气能使湿润的红色石蕊试纸变蓝。氨气极易溶于水,溶于水后形成氨水;当温度升高时,氨气又会从水中逸出。
为了确定氮化镁的化学式,将1.44 g镁在N2中充分燃烧,得到淡黄色固体2.00 g。氮化镁的化学式为 。
4297680432435(3) 小组同学通过交流反思得到启示:验证质量守恒定律时,有气体参与或生成的反应需要在 装置中进行。
三、 推理、计算题:共3题。
13. (2025宿迁如东实验月考)小林对某品牌牙膏样品中的碳酸钙含量进行测定。小林称取10.0 g牙膏样品,加入足量5%的稀盐酸,按如图装置实验,记录数据如下(牙膏中其他成分不与盐酸反应)。
时间/min
0
2
4
6
8
10
12
装置和药品总质量/g
261.0
260.0
259.3
259.0
258.8
n
258.8
请计算:
(1) 反应结束时,产生二氧化碳的质量是 。
(2) 牙膏样品中碳酸钙的质量分数是多少?(写出完整计算步骤)
(3) 经查实,上述方法所测得牙膏中碳酸钙含量偏小(实验操作规范),导致偏小的原因可能是 (填字母)。
A. 有水蒸气逸出 B. 盐酸挥发 C. 锥形瓶内残留二氧化碳
14. (2025南通通州期末)SCR催化剂(主要成分是WO3)在加热条件下能催化NH3脱除烟气中的NO,该反应机理为4NH3+O2+4NO4N2+6H2O,其中催化剂的活性受温度影响。
(1) 该反应中化合价降低的元素有 (填元素符号)。
(2) 将含4.0 t NO的混合气(NO、O2、NH3)匀速通过装有SCR催化剂的反应器,测得生成 2.8 t N2,计算NO的转化率。(NO的转化率=
×100%,写出计算过程)
15. (2025常州武进一模)生产、生活、科研等许多领域需要用到高浓度的氧气。
Ⅰ. 工业上常以空气为原料生产高浓度的氧气。
(1) 选择空气为原料的可能原因是 (答出一点即可)。
(2) 分离液态空气法获得氧气的过程可用图1所示实验进行模拟。将空石英大试管浸入液氮3 min后,试管内得到一定体积的无色液体(液态空气);取出试管,该液体立即沸腾,伸入燃着的木条,木条熄灭;1 min后再伸入带火星的木条,木条复燃。请从物质的物理性质和化学性质两个角度分析木条熄灭的原因:
;再过1 min后试管内“空空如也”,从微观角度分析试管变“空”的原因是_______________________________。
图1 图2
(3) 分子筛式制氧机是一种利用分子筛的吸附特性,从空气中分离制取高纯度氧气的设备。在一定条件下将N2、O2通过某种分子筛,测定其对N2、O2的吸附量,结果如图2。据图分析,25 ℃、吸附压为250 kPa时,将空气通过该分子筛,首先收集到的气体是 。
Ⅱ. 家庭常用制氧机获得高浓度的氧气。
(4) 某家庭制氧气原理如图3,将A(过碳酸钠白色固体)和B(二氧化锰黑色粉末)放入水中产生氧气。反应仓中过碳酸钠(2Na2CO3·3H2O2)溶于水时分解成Na2CO3和H2O2;反应时放出热量,反应仓里的黑色粉末上下翻腾。一段时间后,反应仓中质量和化学性质没有发生变化的物质是 (填化学式),过滤仓中水的作用是 。
图3 图4
Ⅲ. 空间站里也需要获得高浓度氧气。
(5) 早期空间站常用超氧化钾(KO2)分别与站内产生的CO2、H2O反应得到氧气,同时得到K2CO3、KOH。氧料比(产生氧气与消耗原料的质量比)可以表示原料生产氧气的效率高低,用超氧化钾供氧的氧料比是 %(精确到0.1%)。
(6) 目前空间站有多种供氧方式,其中一种方法是在300~400 ℃和催化剂作用下,利用萨巴蒂尔反应并配合水的电解来实现氧气的再生,大致流程如图4所示。萨巴蒂尔反应的化学方程式为 。当航天员乘组共需要有270 kg水在上述“电解水装置”中完全反应才能提供足够的氧气,则理论上通过该系统的循环,能回收利用的水质量是 。
1. C 2. D 3. C 4. B 5. B 6. C 7. C 8. A
9. C 10. D
11. (1) 2Cu+O22CuO 18% 铜粉的量不足(合理即可) (2) 部分氧化镁以白烟的形式逸散到空气中 镁
12. (1) 2Mg+O22MgO D (2) Mg3N2 (3) 密闭
13. (1) 2.2 g
(2) 解:设牙膏样品中碳酸钙的质量为x,则
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 44
x 2.2 g
=
x=5.0 g
牙膏样品中碳酸钙的质量分数=×100%=50%
答:牙膏样品中碳酸钙的质量分数为50%。
(3) C
14. (1) O、N
(2) 解:设消耗的NO的质量为x,则
4NH3+O2+4NO4N2+6H2O
120 112
x 2.8 t
=
x=3.0 t
NO的转化率=×100%=75%
答:NO的转化率为75%。
15. (1) 生产成本低 (2) 物理性质:氮气的沸点低于氧气,先发生汽化;化学性质:氮气不支持燃烧 气体分子会做无规则运动,并通过扩散迅速脱离液体表面,进入周围空气 (3) O2 (4) MnO2 通过产生气泡的速率来观察氧气的输出速率,湿润氧气 (5) 33.8 (6) 4H2+CO2CH4+2H2O 135 kg
班级:______ 姓名:______ 学号:______ 得分:______
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5 K—39 Ca—40 Fe—56
一、 选择题:共10题,每小题只有一个选项最符合题意。
1. (2025扬州树人集团一模)下列物质燃烧不会生成水的是( )
A. C2H5OH B. CH4 C. CO D. H2
2. (2025南京秦淮二模)以下示意图描述了两种物质的变化过程,其中“”表示氧原子,“”表示氢原子。下列说法不正确的是( )
图1 图2
A. 图1所示过程属于物理变化
B. 图2是过氧化氢分解的示意图
C. 图1所示过程中,分子间的间隔增大
D. 图2所示过程中,原子的数目变多
3. (2025扬州广陵二模)呼吸面罩中的过氧化钠固体与人体呼出的二氧化碳反应产生碳酸钠和氧气,此反应涉及的化学用语表示正确的是( )
A. 2个碳酸根离子:2CO
B. 过氧化钠中氧元素化合价:Na22
C. CO2中数字“2”的意义:一个二氧化碳分子中含有2个氧原子
D. Na2O2+CO2===Na2CO3+O2
4. (2025南京秦淮一模)丙烷(化学式为C3H8)是液化石油气的主要成分之一。现有4.4 g丙烷与一定量氧气混合于密闭容器内,在一定条件下全部转化为一氧化碳、二氧化碳和水,恢复至室温,测得所得气体中氧元素质量分数为70%,则参加反应的氧气的质量为( )
A. 16 g B. 14.8 g C. 11.2 g D. 8.4 g
5. (2025宿迁宿城期中)用如图装置验证质量守恒定律。在锥形瓶中放入一小粒白磷,玻璃管下端刚好能与白磷接触,将整套装置放在托盘天平上调节至平衡,取下橡皮塞,将玻璃管放在酒精灯火焰上灼烧至红热,迅速塞紧瓶塞,将白磷引燃,待锥形瓶冷却后观察天平是否平衡。下列说法不正确的是( )
392747579375A. 该实验装置气密性必须要好,白磷不一定要过量
B. 反应前锥形瓶内白磷和氧气的总质量一定等于反应后生成的五氧化二磷质量
C. 实验前后天平保持平衡,实验后,如果松开橡皮塞,则天平指针向左偏
D. 细沙的作用是隔热,防止白磷燃烧放出大量的热使锥形瓶底部炸裂
6. (2025镇江润州期中)将24.5 g KClO3和5.0 g MnO2混合物加热一段时间,得24.7 g剩余固体。下列有关说法不正确的是( )
A. 反应生成4.8 g O2 B. 剩余固体中氯元素的质量为7.1 g
C. 剩余固体中含有两种物质 D. 加热后固体中钾元素的质量不变
7. 一氧化氮(NO)泄露会污染空气。可用硫酸亚铁溶液吸收处理NO[FeSO4+NO===Fe(NO)SO4],现欲将NO含量为4.98 g/m3的尾气1 000 m3处理至达标(不高于0.18 g/m3)后排放,至少需要消耗硫酸亚铁的质量为( )
A. 10.16 kg B. 12.16 kg C. 24.32 kg D. 30.30 kg
35814004521208. (2025苏州二模)由CO2到淀粉的合成过程中,其中一步反应的物质转化如图所示,下列说法正确的是( )
A. 反应①中各物质的化学计量数均为1
B. 反应①和反应②前后各元素化合价均没有变化
C. 氧元素的质量分数:甲醇>甲醛
D. 使甲醇持续转化为甲醛,理论上无需补充H2O2
9. (2025徐州铜山三模)为探究铜的化学性质,某化学兴趣小组的同学借助氧气传感器在密闭装置中进行如图所示实验,观察实验现象并分析氧气含量随时间变化的曲线图。其中终点D(200,6.15%)表示时间为200秒时,装置中氧气含量为6.15%。结合图示判断下列说法错误的是( )
A. 加热前的空气样品中氧气含量为20.99%
B. 铜在加热条件下能与氧气发生化学反应:2Cu+O22CuO
C. 拐点C至终点D所对应的时间范围内,装置内物质的总质量逐渐减少
D. 通过现象证据和数据证据,可以从定性和定量的视角分析得出合理解释
10. (2025宿迁宿城期中)某密闭容器中有M、氧气、二氧化碳和水四种物质,在一定条件下充分反应,测得各物质的质量如表所示。根据表中信息,判断下列说法正确的是( )
物质
M
氧气
二氧化碳
水
反应前的质量/g
23
64
8
5
反应后的质量/g
0
16
52
待测x
A. 待测x的值为27
B. M由碳、氢元素组成
C. 该反应属于化合反应
D. M中碳、氢元素质量比为4∶1
二、 填空、简答题:共2题。
11. (2025宿迁宿豫月考)近代化学史上对质量守恒定律、空气组成的研究都具有伟大意义。
图1 图2
(1) 图1装置探究空气中氧气的含量,硬质玻璃管内发生反应的化学方程式为________________,冷却至室温后,注射器内剩余气体的体积为6 mL,测得氧气的体积分数为________。该结果与空气中氧气的实际体积分数产生差异的原因是____________________(写出一点即可)。
(2) 图2是测定镁条燃烧前后质量的实验。镁条在空气中完全燃烧后,称量发现陶土网上燃烧产物的质量比反应前镁条质量小,其主要原因是________________________。为了正确验证质量守恒定律,改进了镁条燃烧的实验,成功并绘制了反应物和生成物各物质的质量关系图像,b物质应是________。
12. 某科学兴趣小组的同学设计了下图系列实验来探究化学反应前后的质量关系。
甲 乙
图1 图2
(1) 甲实验中,镁条剧烈燃烧,产生大量白烟,写出该反应的化学方程式:_______________________。某同学将两份m1 g的镁条和足量氧气分别置于密闭装置和开放装置中充分反应,实验过程中陶土网上盛接到的固体质量(m)随加热时间(t)变化如图2所示。下列有关分析错误的是 (填字母)。
A. 0
C. m3
(2) 用乙装置改进实验甲,发现镁条燃烧除生成白色固体外,还有少量的淡黄色固体生成。这种淡黄色固体是什么呢?同学们在老师的指导下进行有关实验探究。
资料:镁能与氮气剧烈反应生成黄色的氮化镁固体;氮化镁可与水剧烈反应产生氨气和另一种化合物,氨气能使湿润的红色石蕊试纸变蓝。氨气极易溶于水,溶于水后形成氨水;当温度升高时,氨气又会从水中逸出。
为了确定氮化镁的化学式,将1.44 g镁在N2中充分燃烧,得到淡黄色固体2.00 g。氮化镁的化学式为 。
4297680432435(3) 小组同学通过交流反思得到启示:验证质量守恒定律时,有气体参与或生成的反应需要在 装置中进行。
三、 推理、计算题:共3题。
13. (2025宿迁如东实验月考)小林对某品牌牙膏样品中的碳酸钙含量进行测定。小林称取10.0 g牙膏样品,加入足量5%的稀盐酸,按如图装置实验,记录数据如下(牙膏中其他成分不与盐酸反应)。
时间/min
0
2
4
6
8
10
12
装置和药品总质量/g
261.0
260.0
259.3
259.0
258.8
n
258.8
请计算:
(1) 反应结束时,产生二氧化碳的质量是 。
(2) 牙膏样品中碳酸钙的质量分数是多少?(写出完整计算步骤)
(3) 经查实,上述方法所测得牙膏中碳酸钙含量偏小(实验操作规范),导致偏小的原因可能是 (填字母)。
A. 有水蒸气逸出 B. 盐酸挥发 C. 锥形瓶内残留二氧化碳
14. (2025南通通州期末)SCR催化剂(主要成分是WO3)在加热条件下能催化NH3脱除烟气中的NO,该反应机理为4NH3+O2+4NO4N2+6H2O,其中催化剂的活性受温度影响。
(1) 该反应中化合价降低的元素有 (填元素符号)。
(2) 将含4.0 t NO的混合气(NO、O2、NH3)匀速通过装有SCR催化剂的反应器,测得生成 2.8 t N2,计算NO的转化率。(NO的转化率=
×100%,写出计算过程)
15. (2025常州武进一模)生产、生活、科研等许多领域需要用到高浓度的氧气。
Ⅰ. 工业上常以空气为原料生产高浓度的氧气。
(1) 选择空气为原料的可能原因是 (答出一点即可)。
(2) 分离液态空气法获得氧气的过程可用图1所示实验进行模拟。将空石英大试管浸入液氮3 min后,试管内得到一定体积的无色液体(液态空气);取出试管,该液体立即沸腾,伸入燃着的木条,木条熄灭;1 min后再伸入带火星的木条,木条复燃。请从物质的物理性质和化学性质两个角度分析木条熄灭的原因:
;再过1 min后试管内“空空如也”,从微观角度分析试管变“空”的原因是_______________________________。
图1 图2
(3) 分子筛式制氧机是一种利用分子筛的吸附特性,从空气中分离制取高纯度氧气的设备。在一定条件下将N2、O2通过某种分子筛,测定其对N2、O2的吸附量,结果如图2。据图分析,25 ℃、吸附压为250 kPa时,将空气通过该分子筛,首先收集到的气体是 。
Ⅱ. 家庭常用制氧机获得高浓度的氧气。
(4) 某家庭制氧气原理如图3,将A(过碳酸钠白色固体)和B(二氧化锰黑色粉末)放入水中产生氧气。反应仓中过碳酸钠(2Na2CO3·3H2O2)溶于水时分解成Na2CO3和H2O2;反应时放出热量,反应仓里的黑色粉末上下翻腾。一段时间后,反应仓中质量和化学性质没有发生变化的物质是 (填化学式),过滤仓中水的作用是 。
图3 图4
Ⅲ. 空间站里也需要获得高浓度氧气。
(5) 早期空间站常用超氧化钾(KO2)分别与站内产生的CO2、H2O反应得到氧气,同时得到K2CO3、KOH。氧料比(产生氧气与消耗原料的质量比)可以表示原料生产氧气的效率高低,用超氧化钾供氧的氧料比是 %(精确到0.1%)。
(6) 目前空间站有多种供氧方式,其中一种方法是在300~400 ℃和催化剂作用下,利用萨巴蒂尔反应并配合水的电解来实现氧气的再生,大致流程如图4所示。萨巴蒂尔反应的化学方程式为 。当航天员乘组共需要有270 kg水在上述“电解水装置”中完全反应才能提供足够的氧气,则理论上通过该系统的循环,能回收利用的水质量是 。
1. C 2. D 3. C 4. B 5. B 6. C 7. C 8. A
9. C 10. D
11. (1) 2Cu+O22CuO 18% 铜粉的量不足(合理即可) (2) 部分氧化镁以白烟的形式逸散到空气中 镁
12. (1) 2Mg+O22MgO D (2) Mg3N2 (3) 密闭
13. (1) 2.2 g
(2) 解:设牙膏样品中碳酸钙的质量为x,则
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 44
x 2.2 g
=
x=5.0 g
牙膏样品中碳酸钙的质量分数=×100%=50%
答:牙膏样品中碳酸钙的质量分数为50%。
(3) C
14. (1) O、N
(2) 解:设消耗的NO的质量为x,则
4NH3+O2+4NO4N2+6H2O
120 112
x 2.8 t
=
x=3.0 t
NO的转化率=×100%=75%
答:NO的转化率为75%。
15. (1) 生产成本低 (2) 物理性质:氮气的沸点低于氧气,先发生汽化;化学性质:氮气不支持燃烧 气体分子会做无规则运动,并通过扩散迅速脱离液体表面,进入周围空气 (3) O2 (4) MnO2 通过产生气泡的速率来观察氧气的输出速率,湿润氧气 (5) 33.8 (6) 4H2+CO2CH4+2H2O 135 kg
同课章节目录
