期末检测卷 (含答案) 2025-2026学年化学鲁教版(2024)九年级上册
文档属性
| 名称 | 期末检测卷 (含答案) 2025-2026学年化学鲁教版(2024)九年级上册 |  | |
| 格式 | docx | ||
| 文件大小 | 516.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-29 22:25:29 | ||
图片预览

文档简介
期末检测卷
班级: 姓名: 学号: 得分:
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Ca—40
一、 选择题:共10题,每题2分,共20分。
1. (2025宿迁泗洪一模)火的利用促进人类文明进步,下列有关火的利用不利于人类文明进步的是( )
A. 驱赶野兽,开拓家园 B. 火攻水淹,夺城掠地
C. 取暖照明,改善生活 D. 冶炼金属,发展生产
2. (2025盐城大丰二模)2025年6月5日中国环境日主题为“美丽中国我先行”。下列做法不符合这一主题的是( )
A. 禁止使用化石燃料,防止污染空气
B. 多植树造林,促进达成“碳中和”
C. 煤炭脱硫处理,有效减少酸雨产生
D. 推广新能源汽车,降低尾气排放
3. (2025南通海门月考)分类是化学学习和研究的重要方法之一,下列分类正确的是( )
A. 化学性质包括:稳定性、挥发性、可燃性
B. 空气污染物包括:CO、NO2、SO2、CO2
C. 混合物:空气、海水、冰水混合物
D. 基本反应类型:化合反应、分解反应
4. (2025宿迁沭阳一模)利用催化剂将汽车尾气中部分气体进行转化,微观示意图如图。下列关于该转化的说法不正确的是( )
A. 反应物和生成物均由分子构成
B. 反应前后分子总数不发生改变
C. 反应前后共涉及3种化合物
D. 该转化减少了空气污染物的排放
5. (2025宿迁宿城期末)下列叙述或实验现象的描述中,正确的是( )
A. 在灭火中喷洒大量的水能冷却并能降低可燃物的着火点
B. 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
C. 红磷在氧气中燃烧剧烈,且产生大量白雾
D. 炒菜时油锅起火,可以用锅盖盖灭,该灭火原理是隔绝氧气
6. (2025宿迁沭阳期末)逻辑推理是化学常用的思维方法。下列推理正确的是( )
A. 单质由同种元素组成,所以由同种元素组成的物质一定是单质
B. 阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子
C. 化学变化中分子种类发生改变,所以分子种类改变的变化一定是化学变化
D. 有氧气参加的化合反应属于氧化反应,所以氧化反应一定是化合反应
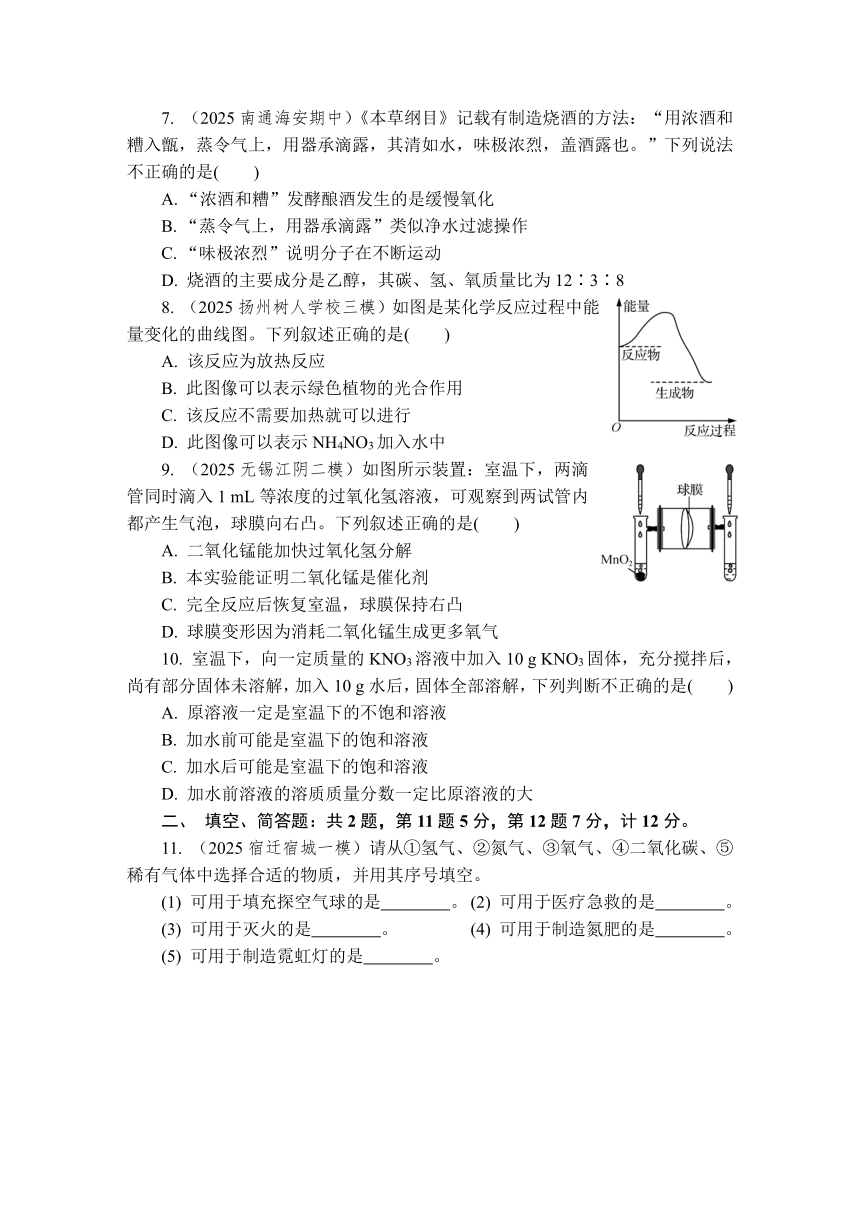
7. (2025南通海安期中)《本草纲目》记载有制造烧酒的方法:“用浓酒和糟入甑,蒸令气上,用器承滴露,其清如水,味极浓烈,盖酒露也。”下列说法不正确的是( )
A. “浓酒和糟”发酵酿酒发生的是缓慢氧化
B. “蒸令气上,用器承滴露”类似净水过滤操作
C. “味极浓烈”说明分子在不断运动
D. 烧酒的主要成分是乙醇,其碳、氢、氧质量比为12∶3∶8
8. (2025扬州树人学校三模)如图是某化学反应过程中能量变化的曲线图。下列叙述正确的是( )
A. 该反应为放热反应
B. 此图像可以表示绿色植物的光合作用
C. 该反应不需要加热就可以进行
D. 此图像可以表示NH4NO3加入水中
9. (2025无锡江阴二模)如图所示装置:室温下,两滴管同时滴入1 mL等浓度的过氧化氢溶液,可观察到两试管内都产生气泡,球膜向右凸。下列叙述正确的是( )
A. 二氧化锰能加快过氧化氢分解
B. 本实验能证明二氧化锰是催化剂
C. 完全反应后恢复室温,球膜保持右凸
D. 球膜变形因为消耗二氧化锰生成更多氧气
10. 室温下,向一定质量的KNO3溶液中加入10 g KNO3固体,充分搅拌后,尚有部分固体未溶解,加入10 g水后,固体全部溶解,下列判断不正确的是( )
A. 原溶液一定是室温下的不饱和溶液
B. 加水前可能是室温下的饱和溶液
C. 加水后可能是室温下的饱和溶液
D. 加水前溶液的溶质质量分数一定比原溶液的大
二、 填空、简答题:共2题,第11题5分,第12题7分,计12分。
11. (2025宿迁宿城一模)请从①氢气、②氮气、③氧气、④二氧化碳、⑤稀有气体中选择合适的物质,并用其序号填空。
(1) 可用于填充探空气球的是 。 (2) 可用于医疗急救的是 。
(3) 可用于灭火的是 。 (4) 可用于制造氮肥的是 。
(5) 可用于制造霓虹灯的是 。
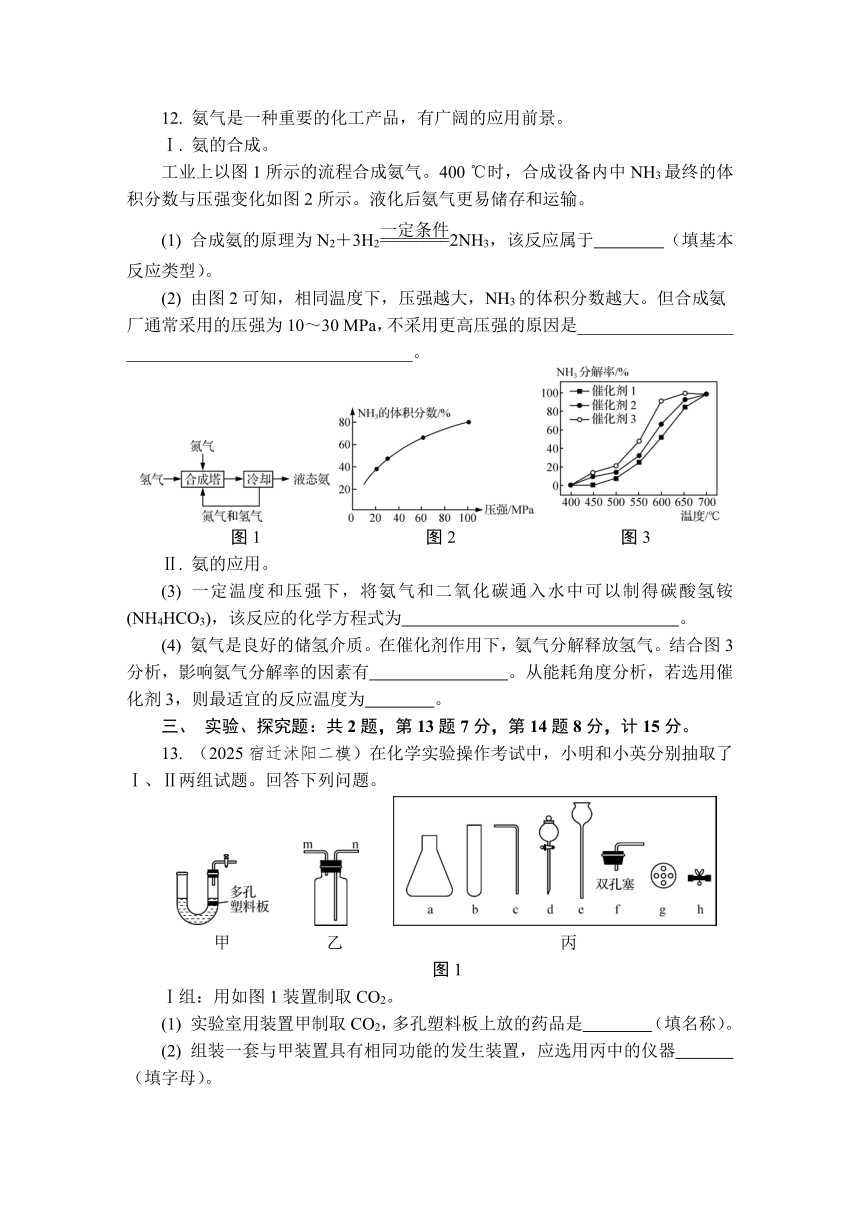
12. 氨气是一种重要的化工产品,有广阔的应用前景。
Ⅰ. 氨的合成。
工业上以图1所示的流程合成氨气。400 ℃时,合成设备内中NH3最终的体积分数与压强变化如图2所示。液化后氨气更易储存和运输。
(1) 合成氨的原理为N2+3H22NH3,该反应属于 (填基本反应类型)。
(2) 由图2可知,相同温度下,压强越大,NH3的体积分数越大。但合成氨厂通常采用的压强为10~30 MPa,不采用更高压强的原因是__________________
_________________________________。
图1 图2 图3
Ⅱ. 氨的应用。
(3) 一定温度和压强下,将氨气和二氧化碳通入水中可以制得碳酸氢铵(NH4HCO3),该反应的化学方程式为 。
(4) 氨气是良好的储氢介质。在催化剂作用下,氨气分解释放氢气。结合图3分析,影响氨气分解率的因素有 。从能耗角度分析,若选用催化剂3,则最适宜的反应温度为 。
三、 实验、探究题:共2题,第13题7分,第14题8分,计15分。
13. (2025宿迁沭阳二模)在化学实验操作考试中,小明和小英分别抽取了Ⅰ、Ⅱ两组试题。回答下列问题。
甲 乙 丙
图1
Ⅰ组:用如图1装置制取CO2。
(1) 实验室用装置甲制取CO2,多孔塑料板上放的药品是 (填名称)。
(2) 组装一套与甲装置具有相同功能的发生装置,应选用丙中的仪器 (填字母)。
(3) 用装置乙收集CO2,气体应从 (填“m”或“n”)端通入。
图2 图3
Ⅱ组:用如图2的自制“制氧机”制取O2。
【资料】过碳酸钠加水溶解会分解生成Na2CO3和H2O2;Na2CO3易溶于水。
【操作】在左瓶中依次加入适量水、过碳酸钠和二氧化锰。
【现象】左瓶中黑色粉末翻腾、液体浑浊,瓶壁温热;右瓶水中导管口有气泡冒出。
(4) 左瓶内产生气体的化学方程式为 ,左瓶中的二氧化锰可通过 、洗涤、干燥等操作回收;右瓶中水的作用除了观察气流快慢外还有 (写一个即可)。
【拓展反思】
(5) 某同学采用如图3所示的装置分离H2、CO2的混合气体。最后一步得到CO2的操作步骤是 。
14. (2025徐州新沂期中)小明同学在做家庭实验时,不小心将过氧化氢溶液溅到妈妈刚刚切好的土豆丝上,发现土豆丝上立即冒气泡,这种现象激发了小明的探究欲望,请你参与小明的探究。
(1) 请写出实验室用过氧化氢溶液制氧气的化学方程式:
。
【猜想】土豆丝可作过氧化氢分解的催化剂。
【实验】设计并完成表中所示的探究实验。
(2) 请你帮小明同学填写表中未填完的空格。
实验操作 实验现象 实验结论 总结
实验一 取5 mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 有气泡产生,木条不复燃 过氧化氢分解产生氧气,但是_____________ 土豆丝可作过氧化氢分解的催化剂
实验二 向盛水的试管中加入土豆丝,伸入带火星的木条 没有明显现象 水和土豆丝不能放出氧气
实验三 取5 mL 5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星的木条 __________________________ 土豆丝能加快过氧化氢的分解速率
(3) 在小明的探究实验中,“实验二”起的作用是 。
【反思】小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的。
(4) 第一补充实验:在实验三前后,各对土豆丝进行一次称量,其目的是证明:反应前后土豆丝的 没变。
第二补充实验:倾倒掉实验三反应后的液体,向试管中余下的土豆丝中重新加入 ,又有大量气泡产生,说明土豆丝的 没变。
【结论】通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂。
四、 计算、综合应用题:共2题,第15题5分,第16题8分,计13分。
15. 在地球上二氧化碳的含量比煤、石油和天然气的总和还多数倍。在一定条件下以二氧化碳和氨气合成尿素是固定和利用二氧化碳的成功范例,反应原理为CO2+2NH3CO(NH2)2+X。
(1) X的化学式为 。
(2) 按上述方法生产120万吨尿素,最多可固定二氧化碳多少万吨?(写出计算过程)
16. 化学反应需要一定的条件。燃烧是常见的化学反应,它与我们的生产生活密切相关。
[活动一]认识燃烧
(1) 下列属于石蜡、硫粉、铁丝燃烧共有的现象是 (填字母,下同)。
A. 发光 B. 产生有刺激性气味的气体
C. 放热 D. 产生使澄清石灰水变浑浊的气体
[活动二]探究燃烧
(2) 探究燃烧条件的实验装置如图1所示,能说明可燃物燃烧需要氧气的现象是 。
图1 图2 图3
[活动三]调控燃烧
(3) 西汉青铜雁鱼灯及其工作原理如图2所示。青铜雁鱼灯里面是空的,腹部用于贮水。使用时燃烧产生的烟气(含SO2)通过雁脖子进入腹部。
①雁鱼灯的灯罩可自由开合,以调节进风量的大小。看到大量黑烟产生时,应 (填“扩大”或“减小”)进风口从而促进燃料充分燃烧。
②雁鱼灯中盛放的清水的作用是 。
A. 主要目的是用于灭火 B. 减少油的挥发,以达到省油的目的
C. 可将燃烧产生的废气引入水中以减少对室内环境的污染
(4) 查阅文献:颗粒直径为20~30 nm的铁粉,在空气中会发生自燃生成氧化铁。该反应说明影响铁燃烧的因素有 (答出一点)。
[活动四]应用燃烧
(5) 戴维发明了一种安全灯,采用一种网眼很小的普通金属网罩住火焰,这种灯在矿井里点燃不会引起可燃性气体爆炸,为了纪念戴维,人们把这种安全灯称为“戴维灯”(如图3)。结合燃烧条件,分析这种灯在矿井里点燃不会引起可燃性气体爆炸的原因:____________________。
1. B 2. A 3. D 4. B 5. D 6. C 7. B 8. A
9. A 10. B
11. (1) ① (2) ③ (3) ④ (4) ② (5) ⑤
12. (1) 化合反应 (2) 压强过高,会影响催化剂的活性,且对设备要求较高,会提高成本 (3) NH3+CO2+H2ONH4HCO3
(4) 催化剂种类、温度 650 ℃
13. (1) 石灰石(或大理石) (2) befgh (3) n (4) 2H2O22H2O+O2↑ 过滤 湿润氧气(合理即可) (5) 关闭A,打开B
14. (1) 2H2O22H2O+O2↑ (2) 分解速率很慢 产生大量气泡,带火星的木条复燃 (3) 作对照实验 (4) 质量 5 mL 5%的过氧化氢溶液 化学性质
15. (1) H2O
(2) 解:设最多可固定二氧化碳质量为x,则
CO2+2NH3CO(NH2)2+H2O
44 60
x 120万吨
=
x=88万吨
答:按上述方法生产120万吨尿素,最多可固定二氧化碳88万吨。
16. (1) AC (2) Y形管中的白磷燃烧,水中的白磷不燃烧 (3) ①扩大 ②BC (4) 可燃物与氧气的接触面积 (5) 温度未达到着火点
班级: 姓名: 学号: 得分:
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Ca—40
一、 选择题:共10题,每题2分,共20分。
1. (2025宿迁泗洪一模)火的利用促进人类文明进步,下列有关火的利用不利于人类文明进步的是( )
A. 驱赶野兽,开拓家园 B. 火攻水淹,夺城掠地
C. 取暖照明,改善生活 D. 冶炼金属,发展生产
2. (2025盐城大丰二模)2025年6月5日中国环境日主题为“美丽中国我先行”。下列做法不符合这一主题的是( )
A. 禁止使用化石燃料,防止污染空气
B. 多植树造林,促进达成“碳中和”
C. 煤炭脱硫处理,有效减少酸雨产生
D. 推广新能源汽车,降低尾气排放
3. (2025南通海门月考)分类是化学学习和研究的重要方法之一,下列分类正确的是( )
A. 化学性质包括:稳定性、挥发性、可燃性
B. 空气污染物包括:CO、NO2、SO2、CO2
C. 混合物:空气、海水、冰水混合物
D. 基本反应类型:化合反应、分解反应
4. (2025宿迁沭阳一模)利用催化剂将汽车尾气中部分气体进行转化,微观示意图如图。下列关于该转化的说法不正确的是( )
A. 反应物和生成物均由分子构成
B. 反应前后分子总数不发生改变
C. 反应前后共涉及3种化合物
D. 该转化减少了空气污染物的排放
5. (2025宿迁宿城期末)下列叙述或实验现象的描述中,正确的是( )
A. 在灭火中喷洒大量的水能冷却并能降低可燃物的着火点
B. 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
C. 红磷在氧气中燃烧剧烈,且产生大量白雾
D. 炒菜时油锅起火,可以用锅盖盖灭,该灭火原理是隔绝氧气
6. (2025宿迁沭阳期末)逻辑推理是化学常用的思维方法。下列推理正确的是( )
A. 单质由同种元素组成,所以由同种元素组成的物质一定是单质
B. 阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子
C. 化学变化中分子种类发生改变,所以分子种类改变的变化一定是化学变化
D. 有氧气参加的化合反应属于氧化反应,所以氧化反应一定是化合反应
7. (2025南通海安期中)《本草纲目》记载有制造烧酒的方法:“用浓酒和糟入甑,蒸令气上,用器承滴露,其清如水,味极浓烈,盖酒露也。”下列说法不正确的是( )
A. “浓酒和糟”发酵酿酒发生的是缓慢氧化
B. “蒸令气上,用器承滴露”类似净水过滤操作
C. “味极浓烈”说明分子在不断运动
D. 烧酒的主要成分是乙醇,其碳、氢、氧质量比为12∶3∶8
8. (2025扬州树人学校三模)如图是某化学反应过程中能量变化的曲线图。下列叙述正确的是( )
A. 该反应为放热反应
B. 此图像可以表示绿色植物的光合作用
C. 该反应不需要加热就可以进行
D. 此图像可以表示NH4NO3加入水中
9. (2025无锡江阴二模)如图所示装置:室温下,两滴管同时滴入1 mL等浓度的过氧化氢溶液,可观察到两试管内都产生气泡,球膜向右凸。下列叙述正确的是( )
A. 二氧化锰能加快过氧化氢分解
B. 本实验能证明二氧化锰是催化剂
C. 完全反应后恢复室温,球膜保持右凸
D. 球膜变形因为消耗二氧化锰生成更多氧气
10. 室温下,向一定质量的KNO3溶液中加入10 g KNO3固体,充分搅拌后,尚有部分固体未溶解,加入10 g水后,固体全部溶解,下列判断不正确的是( )
A. 原溶液一定是室温下的不饱和溶液
B. 加水前可能是室温下的饱和溶液
C. 加水后可能是室温下的饱和溶液
D. 加水前溶液的溶质质量分数一定比原溶液的大
二、 填空、简答题:共2题,第11题5分,第12题7分,计12分。
11. (2025宿迁宿城一模)请从①氢气、②氮气、③氧气、④二氧化碳、⑤稀有气体中选择合适的物质,并用其序号填空。
(1) 可用于填充探空气球的是 。 (2) 可用于医疗急救的是 。
(3) 可用于灭火的是 。 (4) 可用于制造氮肥的是 。
(5) 可用于制造霓虹灯的是 。
12. 氨气是一种重要的化工产品,有广阔的应用前景。
Ⅰ. 氨的合成。
工业上以图1所示的流程合成氨气。400 ℃时,合成设备内中NH3最终的体积分数与压强变化如图2所示。液化后氨气更易储存和运输。
(1) 合成氨的原理为N2+3H22NH3,该反应属于 (填基本反应类型)。
(2) 由图2可知,相同温度下,压强越大,NH3的体积分数越大。但合成氨厂通常采用的压强为10~30 MPa,不采用更高压强的原因是__________________
_________________________________。
图1 图2 图3
Ⅱ. 氨的应用。
(3) 一定温度和压强下,将氨气和二氧化碳通入水中可以制得碳酸氢铵(NH4HCO3),该反应的化学方程式为 。
(4) 氨气是良好的储氢介质。在催化剂作用下,氨气分解释放氢气。结合图3分析,影响氨气分解率的因素有 。从能耗角度分析,若选用催化剂3,则最适宜的反应温度为 。
三、 实验、探究题:共2题,第13题7分,第14题8分,计15分。
13. (2025宿迁沭阳二模)在化学实验操作考试中,小明和小英分别抽取了Ⅰ、Ⅱ两组试题。回答下列问题。
甲 乙 丙
图1
Ⅰ组:用如图1装置制取CO2。
(1) 实验室用装置甲制取CO2,多孔塑料板上放的药品是 (填名称)。
(2) 组装一套与甲装置具有相同功能的发生装置,应选用丙中的仪器 (填字母)。
(3) 用装置乙收集CO2,气体应从 (填“m”或“n”)端通入。
图2 图3
Ⅱ组:用如图2的自制“制氧机”制取O2。
【资料】过碳酸钠加水溶解会分解生成Na2CO3和H2O2;Na2CO3易溶于水。
【操作】在左瓶中依次加入适量水、过碳酸钠和二氧化锰。
【现象】左瓶中黑色粉末翻腾、液体浑浊,瓶壁温热;右瓶水中导管口有气泡冒出。
(4) 左瓶内产生气体的化学方程式为 ,左瓶中的二氧化锰可通过 、洗涤、干燥等操作回收;右瓶中水的作用除了观察气流快慢外还有 (写一个即可)。
【拓展反思】
(5) 某同学采用如图3所示的装置分离H2、CO2的混合气体。最后一步得到CO2的操作步骤是 。
14. (2025徐州新沂期中)小明同学在做家庭实验时,不小心将过氧化氢溶液溅到妈妈刚刚切好的土豆丝上,发现土豆丝上立即冒气泡,这种现象激发了小明的探究欲望,请你参与小明的探究。
(1) 请写出实验室用过氧化氢溶液制氧气的化学方程式:
。
【猜想】土豆丝可作过氧化氢分解的催化剂。
【实验】设计并完成表中所示的探究实验。
(2) 请你帮小明同学填写表中未填完的空格。
实验操作 实验现象 实验结论 总结
实验一 取5 mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 有气泡产生,木条不复燃 过氧化氢分解产生氧气,但是_____________ 土豆丝可作过氧化氢分解的催化剂
实验二 向盛水的试管中加入土豆丝,伸入带火星的木条 没有明显现象 水和土豆丝不能放出氧气
实验三 取5 mL 5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星的木条 __________________________ 土豆丝能加快过氧化氢的分解速率
(3) 在小明的探究实验中,“实验二”起的作用是 。
【反思】小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的。
(4) 第一补充实验:在实验三前后,各对土豆丝进行一次称量,其目的是证明:反应前后土豆丝的 没变。
第二补充实验:倾倒掉实验三反应后的液体,向试管中余下的土豆丝中重新加入 ,又有大量气泡产生,说明土豆丝的 没变。
【结论】通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂。
四、 计算、综合应用题:共2题,第15题5分,第16题8分,计13分。
15. 在地球上二氧化碳的含量比煤、石油和天然气的总和还多数倍。在一定条件下以二氧化碳和氨气合成尿素是固定和利用二氧化碳的成功范例,反应原理为CO2+2NH3CO(NH2)2+X。
(1) X的化学式为 。
(2) 按上述方法生产120万吨尿素,最多可固定二氧化碳多少万吨?(写出计算过程)
16. 化学反应需要一定的条件。燃烧是常见的化学反应,它与我们的生产生活密切相关。
[活动一]认识燃烧
(1) 下列属于石蜡、硫粉、铁丝燃烧共有的现象是 (填字母,下同)。
A. 发光 B. 产生有刺激性气味的气体
C. 放热 D. 产生使澄清石灰水变浑浊的气体
[活动二]探究燃烧
(2) 探究燃烧条件的实验装置如图1所示,能说明可燃物燃烧需要氧气的现象是 。
图1 图2 图3
[活动三]调控燃烧
(3) 西汉青铜雁鱼灯及其工作原理如图2所示。青铜雁鱼灯里面是空的,腹部用于贮水。使用时燃烧产生的烟气(含SO2)通过雁脖子进入腹部。
①雁鱼灯的灯罩可自由开合,以调节进风量的大小。看到大量黑烟产生时,应 (填“扩大”或“减小”)进风口从而促进燃料充分燃烧。
②雁鱼灯中盛放的清水的作用是 。
A. 主要目的是用于灭火 B. 减少油的挥发,以达到省油的目的
C. 可将燃烧产生的废气引入水中以减少对室内环境的污染
(4) 查阅文献:颗粒直径为20~30 nm的铁粉,在空气中会发生自燃生成氧化铁。该反应说明影响铁燃烧的因素有 (答出一点)。
[活动四]应用燃烧
(5) 戴维发明了一种安全灯,采用一种网眼很小的普通金属网罩住火焰,这种灯在矿井里点燃不会引起可燃性气体爆炸,为了纪念戴维,人们把这种安全灯称为“戴维灯”(如图3)。结合燃烧条件,分析这种灯在矿井里点燃不会引起可燃性气体爆炸的原因:____________________。
1. B 2. A 3. D 4. B 5. D 6. C 7. B 8. A
9. A 10. B
11. (1) ① (2) ③ (3) ④ (4) ② (5) ⑤
12. (1) 化合反应 (2) 压强过高,会影响催化剂的活性,且对设备要求较高,会提高成本 (3) NH3+CO2+H2ONH4HCO3
(4) 催化剂种类、温度 650 ℃
13. (1) 石灰石(或大理石) (2) befgh (3) n (4) 2H2O22H2O+O2↑ 过滤 湿润氧气(合理即可) (5) 关闭A,打开B
14. (1) 2H2O22H2O+O2↑ (2) 分解速率很慢 产生大量气泡,带火星的木条复燃 (3) 作对照实验 (4) 质量 5 mL 5%的过氧化氢溶液 化学性质
15. (1) H2O
(2) 解:设最多可固定二氧化碳质量为x,则
CO2+2NH3CO(NH2)2+H2O
44 60
x 120万吨
=
x=88万吨
答:按上述方法生产120万吨尿素,最多可固定二氧化碳88万吨。
16. (1) AC (2) Y形管中的白磷燃烧,水中的白磷不燃烧 (3) ①扩大 ②BC (4) 可燃物与氧气的接触面积 (5) 温度未达到着火点
同课章节目录
