期中检测卷 (含答案) 2025-2026学年化学鲁教版(2024)九年级上册
文档属性
| 名称 | 期中检测卷 (含答案) 2025-2026学年化学鲁教版(2024)九年级上册 |  | |
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-29 22:26:45 | ||
图片预览

文档简介
期中检测卷
班级:______ 姓名:______ 学号:______ 得分:______
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Mg—24 Ca—40 Zn—65
一、 选择题:共10题,每题2分,共20分。
1. (2025宿迁沭阳月考)物质由微观粒子构成,下列物质是由原子直接构成的是( )
A. 水 B. 氧化镁 C. 金刚石 D. 氯化钾
2. (2025宿迁宿城一模)规范操作是实验成功和安全的重要保证。下列实验操作正确的是( )
A. 倾倒液体 B. 点燃酒精灯 C. 加热液体 D. 闻药品气味
3. (2025宿迁宿城二模)《天工开物》是我国古代科技发展的智慧结晶。书中记载的下列劳动生产过程,涉及化学变化的是( )
A. 楠木制舟 B. 轧蔗取浆 C. 粮食酿酒 D. 海水晒盐
4. (2025泰州泰兴二模)下列生活中的物质,属于溶液的是( )
A. 生理盐水 B. 玉米汁 C. 牛奶 D. 石灰浆
5. (2025无锡江阴月考)下列关于催化剂的说法正确的是( )
A. 生成物的质量与催化剂无关
B. 催化剂只能加快其他物质的化学反应速率
C. 二氧化锰是一切反应的催化剂
D. 没有二氧化锰的催化作用,过氧化氢在常温下就不能分解出氧气
6. (2025苏州昆山一模)下列有关化学用语表示正确的是( )
A. 3个氧原子:O3 B. 2个镁离子:2Mg2+
C. 氧化铝:AlO D. 硫酸钠:Na2S
7. (2025徐州第二十六中学期末)《清顶香茶》中记载:“日出卧龙日暮色,月生青顶月茶香。”从微观角度解释煮茶时闻到茶香的原因是( )
A. 分子可以分解为原子 B. 分子之间的间隔变大
C. 温度越高,分子能量增大,运动加快 D. 分子的总数增多
8. (2025苏州吴中一模)水是宝贵的自然资源。下列有关水的说法正确的是( )
A. 海水经滤纸过滤后可得到淡水 B. 工业污水必须经处理达标方可排放
C. 明矾可吸附水中所有杂质 D. 活性炭用于自来水杀菌消毒
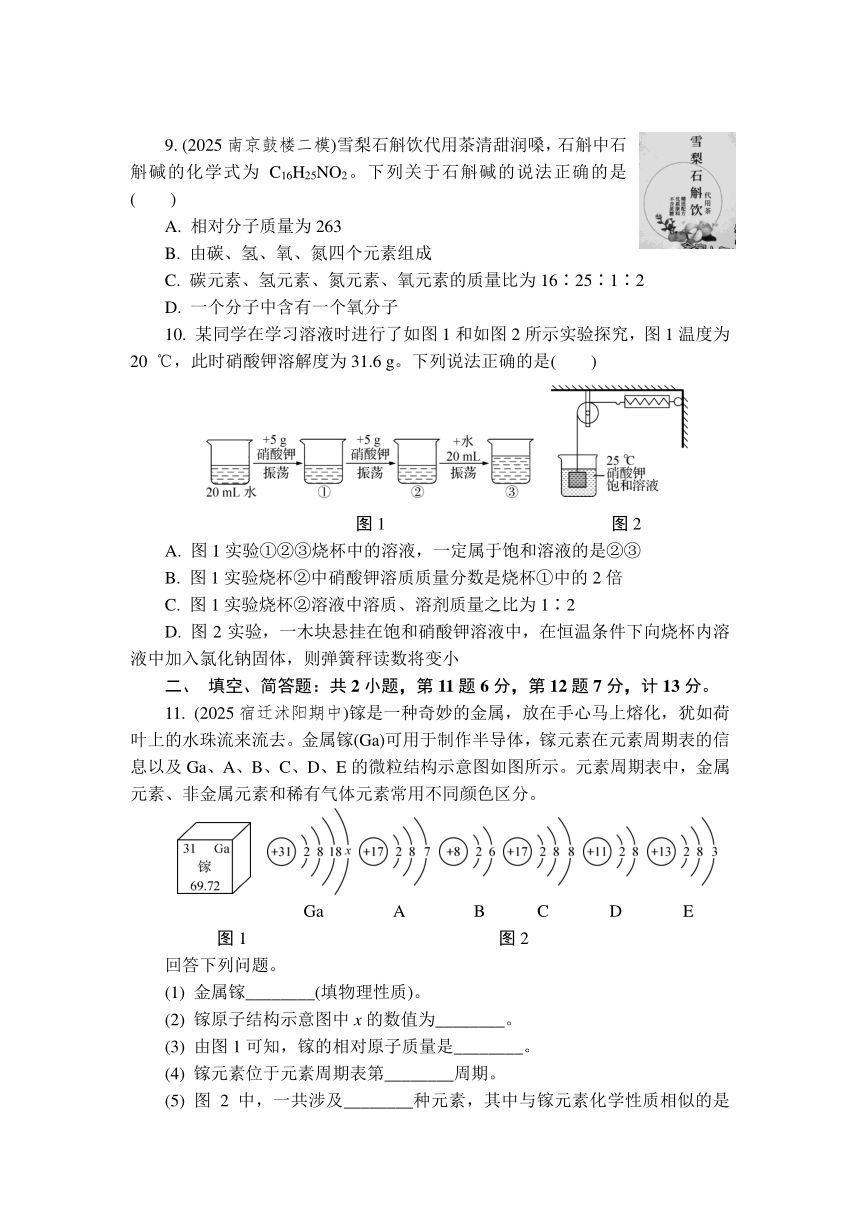
9. (2025南京鼓楼二模)雪梨石斛饮代用茶清甜润嗓,石斛中石斛碱的化学式为C16H25NO2。下列关于石斛碱的说法正确的是( )
A. 相对分子质量为263
B. 由碳、氢、氧、氮四个元素组成
C. 碳元素、氢元素、氮元素、氧元素的质量比为16∶25∶1∶2
D. 一个分子中含有一个氧分子
10. 某同学在学习溶液时进行了如图1和如图2所示实验探究,图1温度为20 ℃,此时硝酸钾溶解度为31.6 g。下列说法正确的是( )
图1 图2
A. 图1实验①②③烧杯中的溶液,一定属于饱和溶液的是②③
B. 图1实验烧杯②中硝酸钾溶质质量分数是烧杯①中的2倍
C. 图1实验烧杯②溶液中溶质、溶剂质量之比为1∶2
D. 图2实验,一木块悬挂在饱和硝酸钾溶液中,在恒温条件下向烧杯内溶液中加入氯化钠固体,则弹簧秤读数将变小
二、 填空、简答题:共2小题,第11题6分,第12题7分,计13分。
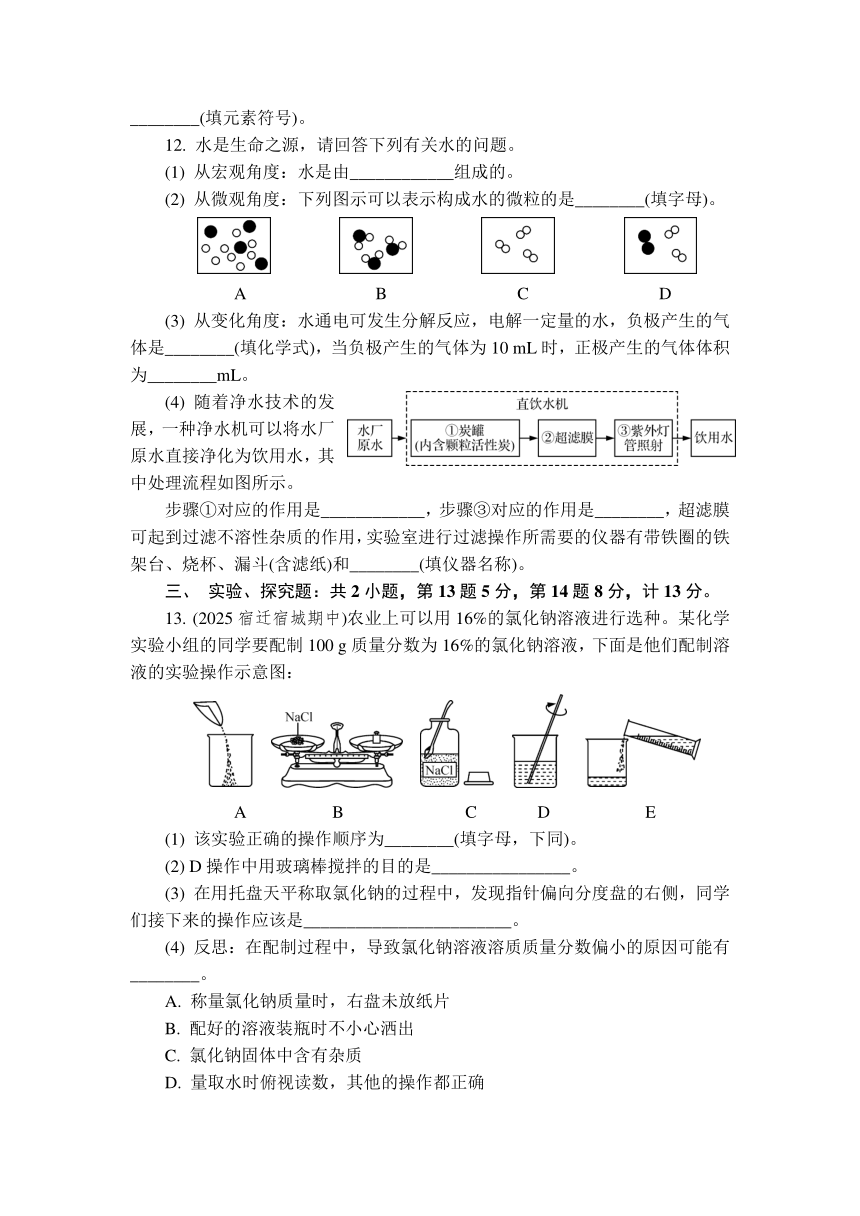
11. (2025宿迁沭阳期中)镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。金属镓(Ga)可用于制作半导体,镓元素在元素周期表的信息以及Ga、A、B、C、D、E的微粒结构示意图如图所示。元素周期表中,金属元素、非金属元素和稀有气体元素常用不同颜色区分。
Ga A B C D E
图1 图2
回答下列问题。
(1) 金属镓________(填物理性质)。
(2) 镓原子结构示意图中x的数值为________。
(3) 由图1可知,镓的相对原子质量是________。
(4) 镓元素位于元素周期表第________周期。
(5) 图2中,一共涉及________种元素,其中与镓元素化学性质相似的是________(填元素符号)。
12. 水是生命之源,请回答下列有关水的问题。
(1) 从宏观角度:水是由____________组成的。
(2) 从微观角度:下列图示可以表示构成水的微粒的是________(填字母)。
A B C D
(3) 从变化角度:水通电可发生分解反应,电解一定量的水,负极产生的气体是________(填化学式),当负极产生的气体为10 mL时,正极产生的气体体积为________mL。
(4) 随着净水技术的发展,一种净水机可以将水厂原水直接净化为饮用水,其中处理流程如图所示。
步骤①对应的作用是____________,步骤③对应的作用是________,超滤膜可起到过滤不溶性杂质的作用,实验室进行过滤操作所需要的仪器有带铁圈的铁架台、烧杯、漏斗(含滤纸)和________(填仪器名称)。
三、 实验、探究题:共2小题,第13题5分,第14题8分,计13分。
13. (2025宿迁宿城期中)农业上可以用16%的氯化钠溶液进行选种。某化学实验小组的同学要配制100 g质量分数为16%的氯化钠溶液,下面是他们配制溶液的实验操作示意图:
A B C D E
(1) 该实验正确的操作顺序为________(填字母,下同)。
(2) D操作中用玻璃棒搅拌的目的是________________。
(3) 在用托盘天平称取氯化钠的过程中,发现指针偏向分度盘的右侧,同学们接下来的操作应该是________________________。
(4) 反思:在配制过程中,导致氯化钠溶液溶质质量分数偏小的原因可能有________。
A. 称量氯化钠质量时,右盘未放纸片
B. 配好的溶液装瓶时不小心洒出
C. 氯化钠固体中含有杂质
D. 量取水时俯视读数,其他的操作都正确
14. (2025宿迁沭阳期中)某学习小组开展“测定空气里氧气含量”的探究活动。
【实验探究】
图1 图2
(1) 实验室用铜粉来测定空气中氧气的含量(装置如图1)。该实验装置中注射器的作用非常重要。在实验开始前,就需要推拉注射器活塞,观察松开手后气球恢复原状时,活塞是否能回到原来的位置。该操作目的是_____________________。实验过程中硬质玻璃管内的现象为________________________。铜粉加热反应时,也需要反复推拉注射器活塞,此时推拉活塞的目的是________________。
(2) 如果铜粉的量不足,会导致测定的空气中氧气含量结果________(填“偏大”“偏小”或“不变”)。
(3) 实验室还可以用红磷来测定空气中氧气的含量(装置如图2)主要步骤如下,正确的顺序为________(填序号)。
①弹簧夹夹紧胶皮管,在集气瓶中加入少量水,将水面上方空间分成5等份
②红磷熄灭并冷却后,打开弹簧夹
③点燃红磷后立即伸入瓶中并塞紧塞子
【优化改进】
同学们利用图2装置多次实验,水面均未上升到刻度“1”。查阅资料:颗粒非常细小的纳米铁粉由于比表面积很大,也能在空气中燃烧生成氧化铁。经讨论后,分别取足量纳米铁粉、红磷采用图3装置进行实验,记录并处理数据分别如图4、图5。
图3 图4 图5
(4) 温度传感器显示,实验过程中瓶内温度均________(填“升高”或“降低”)。
(5) 分析图4、图5可知,实验中消耗氧气更彻底的是________(填“纳米铁粉”或“红磷”)。
【交流反思】
(6) 铁丝在空气中不能燃烧,纳米铁粉却能在空气燃烧。你分析可能的原因是________________________。
四、 计算题:共2小题,第15题6分,第16题8分,计14分。
15. 钙是维持人体正常功能所必需的元素,有时需要服用补钙剂满足人体需求。下图分别为两种补钙剂说明书的一部分。
请根据图示中的信息回答下列问题。
(1) 每个葡萄糖酸钙分子中含________个原子,葡萄糖酸钙(C12H22O14Ca)的相对分子质量是________。
(2) 碳酸钙(化学式为CaCO3)中钙元素的质量分数为________。
(3) 按照金钙尔奇说明书补钙,若改服用葡萄糖酸钙片,一日3次,一次应服用几片(写出计算过程)。
16. 欲使50 g 10%的食盐溶液变成20%,可采用的方法是(要求列式计算):
(1) 蒸发水多少克?
(2) 加入多少克食盐?
(3) 加入30%的食盐溶液多少克?
(4) 若稀释到5%,应加水多少克?
期中检测卷
1. C 2. A 3. C 4. A 5. A 6. B 7. C 8. B 9. A 10. D
11. (1) 熔点低 (2) 3 (3) 69.72 (4) 四 (5) 5 Al
12. (1) 氢元素和氧元素 (2) B (3) H2 5 (4) 吸附水中的色素和异味 杀菌消毒 玻璃棒
13. (1) CBAED (2) 加快氯化钠溶解 (3) 继续向左盘加氯化钠直至天平平衡 (4) AC
14. (1) 检查装置的气密性 固体由红色变为黑色 使氧气与铜粉充分反应 (2) 偏小 (3) ①③② (4) 升高 (5) 纳米铁粉 (6) 纳米铁粉与氧气接触更充分(合理即可)
15. (1) 49 430 (2) 40%
(3) 解:金钙尔奇说明书中每日2次,一次1片,每片含钙280 mg,则每日的补钙量=280 mg×2=560 mg,每片葡萄糖酸钙片中,钙元素的质量=0.5 g××100%≈0.047 g=47 mg,则服用葡萄糖酸钙片,一日3次,每次应服的片数=≈4。
答:按照金钙尔奇说明书补钙,若改服用葡萄糖酸钙片,一日3次,一次应服用4片。
16. 解:(1) 设蒸发水的质量为x,则
50 g×10%=20%×(50 g-x)
x=25 g
答:蒸发水25 g。
(2) 设加入食盐的质量为y,则
×100%=20%
y=6.25 g
答:加入6.25 g食盐。
(3) 设加入30%的食盐溶液质量为z,则
50 g×10%+30%z=(50 g+z)×20%
z=50 g
答:加入30%的食盐溶液质量为50 g。
(4) 若稀释到5%,设应加水的质量为a,则
×100%=5%
a=50 g
答:若稀释到5%,应加水50 g。
班级:______ 姓名:______ 学号:______ 得分:______
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Mg—24 Ca—40 Zn—65
一、 选择题:共10题,每题2分,共20分。
1. (2025宿迁沭阳月考)物质由微观粒子构成,下列物质是由原子直接构成的是( )
A. 水 B. 氧化镁 C. 金刚石 D. 氯化钾
2. (2025宿迁宿城一模)规范操作是实验成功和安全的重要保证。下列实验操作正确的是( )
A. 倾倒液体 B. 点燃酒精灯 C. 加热液体 D. 闻药品气味
3. (2025宿迁宿城二模)《天工开物》是我国古代科技发展的智慧结晶。书中记载的下列劳动生产过程,涉及化学变化的是( )
A. 楠木制舟 B. 轧蔗取浆 C. 粮食酿酒 D. 海水晒盐
4. (2025泰州泰兴二模)下列生活中的物质,属于溶液的是( )
A. 生理盐水 B. 玉米汁 C. 牛奶 D. 石灰浆
5. (2025无锡江阴月考)下列关于催化剂的说法正确的是( )
A. 生成物的质量与催化剂无关
B. 催化剂只能加快其他物质的化学反应速率
C. 二氧化锰是一切反应的催化剂
D. 没有二氧化锰的催化作用,过氧化氢在常温下就不能分解出氧气
6. (2025苏州昆山一模)下列有关化学用语表示正确的是( )
A. 3个氧原子:O3 B. 2个镁离子:2Mg2+
C. 氧化铝:AlO D. 硫酸钠:Na2S
7. (2025徐州第二十六中学期末)《清顶香茶》中记载:“日出卧龙日暮色,月生青顶月茶香。”从微观角度解释煮茶时闻到茶香的原因是( )
A. 分子可以分解为原子 B. 分子之间的间隔变大
C. 温度越高,分子能量增大,运动加快 D. 分子的总数增多
8. (2025苏州吴中一模)水是宝贵的自然资源。下列有关水的说法正确的是( )
A. 海水经滤纸过滤后可得到淡水 B. 工业污水必须经处理达标方可排放
C. 明矾可吸附水中所有杂质 D. 活性炭用于自来水杀菌消毒
9. (2025南京鼓楼二模)雪梨石斛饮代用茶清甜润嗓,石斛中石斛碱的化学式为C16H25NO2。下列关于石斛碱的说法正确的是( )
A. 相对分子质量为263
B. 由碳、氢、氧、氮四个元素组成
C. 碳元素、氢元素、氮元素、氧元素的质量比为16∶25∶1∶2
D. 一个分子中含有一个氧分子
10. 某同学在学习溶液时进行了如图1和如图2所示实验探究,图1温度为20 ℃,此时硝酸钾溶解度为31.6 g。下列说法正确的是( )
图1 图2
A. 图1实验①②③烧杯中的溶液,一定属于饱和溶液的是②③
B. 图1实验烧杯②中硝酸钾溶质质量分数是烧杯①中的2倍
C. 图1实验烧杯②溶液中溶质、溶剂质量之比为1∶2
D. 图2实验,一木块悬挂在饱和硝酸钾溶液中,在恒温条件下向烧杯内溶液中加入氯化钠固体,则弹簧秤读数将变小
二、 填空、简答题:共2小题,第11题6分,第12题7分,计13分。
11. (2025宿迁沭阳期中)镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。金属镓(Ga)可用于制作半导体,镓元素在元素周期表的信息以及Ga、A、B、C、D、E的微粒结构示意图如图所示。元素周期表中,金属元素、非金属元素和稀有气体元素常用不同颜色区分。
Ga A B C D E
图1 图2
回答下列问题。
(1) 金属镓________(填物理性质)。
(2) 镓原子结构示意图中x的数值为________。
(3) 由图1可知,镓的相对原子质量是________。
(4) 镓元素位于元素周期表第________周期。
(5) 图2中,一共涉及________种元素,其中与镓元素化学性质相似的是________(填元素符号)。
12. 水是生命之源,请回答下列有关水的问题。
(1) 从宏观角度:水是由____________组成的。
(2) 从微观角度:下列图示可以表示构成水的微粒的是________(填字母)。
A B C D
(3) 从变化角度:水通电可发生分解反应,电解一定量的水,负极产生的气体是________(填化学式),当负极产生的气体为10 mL时,正极产生的气体体积为________mL。
(4) 随着净水技术的发展,一种净水机可以将水厂原水直接净化为饮用水,其中处理流程如图所示。
步骤①对应的作用是____________,步骤③对应的作用是________,超滤膜可起到过滤不溶性杂质的作用,实验室进行过滤操作所需要的仪器有带铁圈的铁架台、烧杯、漏斗(含滤纸)和________(填仪器名称)。
三、 实验、探究题:共2小题,第13题5分,第14题8分,计13分。
13. (2025宿迁宿城期中)农业上可以用16%的氯化钠溶液进行选种。某化学实验小组的同学要配制100 g质量分数为16%的氯化钠溶液,下面是他们配制溶液的实验操作示意图:
A B C D E
(1) 该实验正确的操作顺序为________(填字母,下同)。
(2) D操作中用玻璃棒搅拌的目的是________________。
(3) 在用托盘天平称取氯化钠的过程中,发现指针偏向分度盘的右侧,同学们接下来的操作应该是________________________。
(4) 反思:在配制过程中,导致氯化钠溶液溶质质量分数偏小的原因可能有________。
A. 称量氯化钠质量时,右盘未放纸片
B. 配好的溶液装瓶时不小心洒出
C. 氯化钠固体中含有杂质
D. 量取水时俯视读数,其他的操作都正确
14. (2025宿迁沭阳期中)某学习小组开展“测定空气里氧气含量”的探究活动。
【实验探究】
图1 图2
(1) 实验室用铜粉来测定空气中氧气的含量(装置如图1)。该实验装置中注射器的作用非常重要。在实验开始前,就需要推拉注射器活塞,观察松开手后气球恢复原状时,活塞是否能回到原来的位置。该操作目的是_____________________。实验过程中硬质玻璃管内的现象为________________________。铜粉加热反应时,也需要反复推拉注射器活塞,此时推拉活塞的目的是________________。
(2) 如果铜粉的量不足,会导致测定的空气中氧气含量结果________(填“偏大”“偏小”或“不变”)。
(3) 实验室还可以用红磷来测定空气中氧气的含量(装置如图2)主要步骤如下,正确的顺序为________(填序号)。
①弹簧夹夹紧胶皮管,在集气瓶中加入少量水,将水面上方空间分成5等份
②红磷熄灭并冷却后,打开弹簧夹
③点燃红磷后立即伸入瓶中并塞紧塞子
【优化改进】
同学们利用图2装置多次实验,水面均未上升到刻度“1”。查阅资料:颗粒非常细小的纳米铁粉由于比表面积很大,也能在空气中燃烧生成氧化铁。经讨论后,分别取足量纳米铁粉、红磷采用图3装置进行实验,记录并处理数据分别如图4、图5。
图3 图4 图5
(4) 温度传感器显示,实验过程中瓶内温度均________(填“升高”或“降低”)。
(5) 分析图4、图5可知,实验中消耗氧气更彻底的是________(填“纳米铁粉”或“红磷”)。
【交流反思】
(6) 铁丝在空气中不能燃烧,纳米铁粉却能在空气燃烧。你分析可能的原因是________________________。
四、 计算题:共2小题,第15题6分,第16题8分,计14分。
15. 钙是维持人体正常功能所必需的元素,有时需要服用补钙剂满足人体需求。下图分别为两种补钙剂说明书的一部分。
请根据图示中的信息回答下列问题。
(1) 每个葡萄糖酸钙分子中含________个原子,葡萄糖酸钙(C12H22O14Ca)的相对分子质量是________。
(2) 碳酸钙(化学式为CaCO3)中钙元素的质量分数为________。
(3) 按照金钙尔奇说明书补钙,若改服用葡萄糖酸钙片,一日3次,一次应服用几片(写出计算过程)。
16. 欲使50 g 10%的食盐溶液变成20%,可采用的方法是(要求列式计算):
(1) 蒸发水多少克?
(2) 加入多少克食盐?
(3) 加入30%的食盐溶液多少克?
(4) 若稀释到5%,应加水多少克?
期中检测卷
1. C 2. A 3. C 4. A 5. A 6. B 7. C 8. B 9. A 10. D
11. (1) 熔点低 (2) 3 (3) 69.72 (4) 四 (5) 5 Al
12. (1) 氢元素和氧元素 (2) B (3) H2 5 (4) 吸附水中的色素和异味 杀菌消毒 玻璃棒
13. (1) CBAED (2) 加快氯化钠溶解 (3) 继续向左盘加氯化钠直至天平平衡 (4) AC
14. (1) 检查装置的气密性 固体由红色变为黑色 使氧气与铜粉充分反应 (2) 偏小 (3) ①③② (4) 升高 (5) 纳米铁粉 (6) 纳米铁粉与氧气接触更充分(合理即可)
15. (1) 49 430 (2) 40%
(3) 解:金钙尔奇说明书中每日2次,一次1片,每片含钙280 mg,则每日的补钙量=280 mg×2=560 mg,每片葡萄糖酸钙片中,钙元素的质量=0.5 g××100%≈0.047 g=47 mg,则服用葡萄糖酸钙片,一日3次,每次应服的片数=≈4。
答:按照金钙尔奇说明书补钙,若改服用葡萄糖酸钙片,一日3次,一次应服用4片。
16. 解:(1) 设蒸发水的质量为x,则
50 g×10%=20%×(50 g-x)
x=25 g
答:蒸发水25 g。
(2) 设加入食盐的质量为y,则
×100%=20%
y=6.25 g
答:加入6.25 g食盐。
(3) 设加入30%的食盐溶液质量为z,则
50 g×10%+30%z=(50 g+z)×20%
z=50 g
答:加入30%的食盐溶液质量为50 g。
(4) 若稀释到5%,设应加水的质量为a,则
×100%=5%
a=50 g
答:若稀释到5%,应加水50 g。
同课章节目录
