苏教版化学选修五《有机化学基础》专题三 第二单元 芳香烃 苯的结构与性质 测试题 含答案 (1)
文档属性
| 名称 | 苏教版化学选修五《有机化学基础》专题三 第二单元 芳香烃 苯的结构与性质 测试题 含答案 (1) |  | |
| 格式 | zip | ||
| 文件大小 | 73.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-09-12 22:40:55 | ||
图片预览

文档简介
苏教版化学选修五《有机化学基础》专题三
第二单元
芳香烃
苯的结构与性质
测试题
一、选择题
1.下列物质分子中的氢原子不在同一平面上的有
(
)
A
C2H2
B.C2H4
C.C2H6
D.C6H6
2.比较下列化学键:①烷烃中的碳碳单键,②烯烃中的碳碳双键,③炔烃中的碳碳叁键,④苯环中碳碳键,其键长由长到短的顺序是
(
)
A.①②③④
B.①②④③
C.①④②③
D.④①③②
3.关于苯的下列说法中不正确的是
(
)
A.组成苯的12个原子在同一平面上
B.苯环中6个碳碳键键长完全相同
C.苯环中碳碳键的键能介于C-C和C=C之间
D.苯只能发生取代反应
4.能说明苯分子苯环的平面正六边形结构中,碳碳键不是单双键交替排布的事实是(
)
A.苯的一元取代物没有同分异构体
B.苯的邻位二元取代物只有一种
C.苯的间位二元取代物只有一种
D.苯的对位二元取代物只有一种
5.将下列各种液体分别与溴水混合并振荡,不能发生反应,静置后溶液分层,且溴水层几乎无色的是
(
)
A.CCl4
B.己烯
C.苯
D.酒精
6.在一定条件下,能和Br2起反应而且有HBr生成的是
(
)
A.丙烷
B.苯
C.乙烯
D.乙炔
7.用分液漏斗可以分离的一组液体混合物是
(
)
A.溴和CCl4
B.苯和溴苯
C.硝基苯和水
D.汽油和苯
8.已知二氯苯有3种同分异构体,则四氯苯的同分异构体有
(
)
A.2种
B.3种
C.4种
D.5种
9.某烃结构式如下:-C≡C-CH=CH-CH3,有关其结构说法正确的是
(
)
A.
所有原子可能在同一平面上
B.
所有原子可能在同一条直线上
C.
所有碳原子可能在同一平面上
D.
所有氢原子可能在同一平面上
10.实验室用溴和苯在FeBr3催化下制取溴苯,得到粗溴苯后,要用如下操作提纯:(1)蒸馏;(2)水洗;(3)用干燥剂干燥;(4)用10%的NaOH溶液洗涤。正确的操作顺序是
(
)
A、(1)
(2)
(3)
(4)
B、(4)
(2)
(3)
(1)
C、(4)
(1)
(2)
(3)
D、(2)
(4)
(3)
(1)
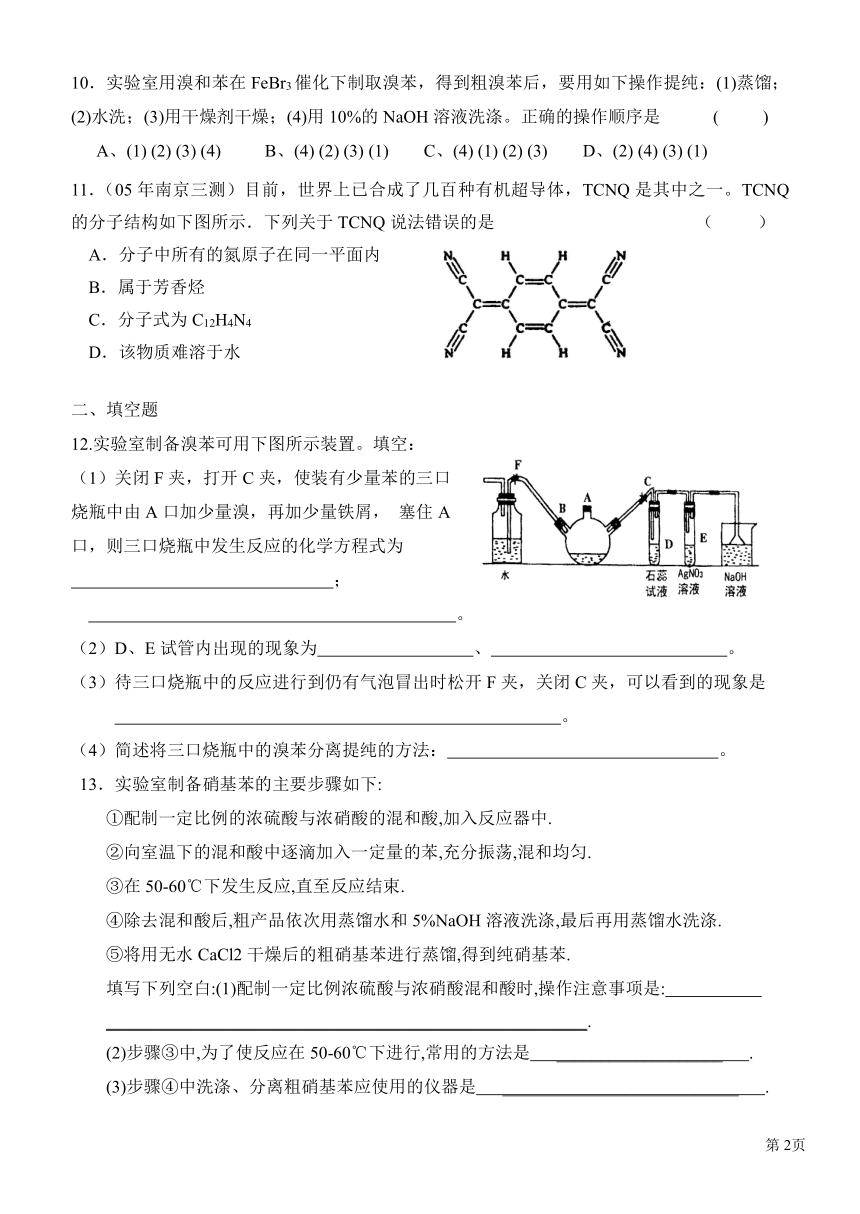
11.(05年南京三测)目前,世界上已合成了几百种有机超导体,TCNQ是其中之一。TCNQ的分子结构如下图所示.下列关于TCNQ说法错误的是
(
)
A.分子中所有的氮原子在同一平面内
B.属于芳香烃
C.分子式为C12H4N4
D.该物质难溶于水
二、填空题
12.实验室制备溴苯可用下图所示装置。填空:
(1)关闭F夹,打开C夹,使装有少量苯的三口
烧瓶中由A口加少量溴,再加少量铁屑,
塞住A
口,则三口烧瓶中发生反应的化学方程式为
;
。
(2)D、E试管内出现的现象为
、
。
(3)待三口烧瓶中的反应进行到仍有气泡冒出时松开F夹,关闭C夹,可以看到的现象是
。
(4)简述将三口烧瓶中的溴苯分离提纯的方法:
。
13.实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中.
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤.
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯.
填写下列空白:(1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是:
_______________________________________________________.
(2)步骤③中,为了使反应在50-60℃下进行,常用的方法是
___________________
.
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是
___________________________
.
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是
________________________
.
(5)纯硝基苯是无色,密度比水
____
(填"小"或"大"),具有
____
气味的油状液体.
三.计算
14.(5分)将一定量的CH4,O4和Na2O2放入一密闭容器中,用电火花不断引燃数量混合气体,使其充分反应,反应后容器内的压强趋于零。其残余固体溶于水无气体产生。则CH4、O2、Na2O2的物质的量之比为
。若CH4取0.1mol,则反应后残余固体中加入足量的盐酸,能放出气体
L(标准状况)。
苯的结构与性质
参考答案
( http: / / www.e- / shownews.asp id=59&title=本站%3cfont%20color=red%3e课时练习%3c / font%3e介绍 )
一、选择题
1.C
2.C
3.D
4.B
5.AC
6.AB
7.C
8.B
9.C
10.D
11.B
二、填空题
12.(1)2Fe
+
3Br2
=
2FeBr3
+
Br2
+
HBr
(2)D中有雾生成且石蕊试液变红;E中有浅黄色沉淀生成。
(3)水倒吸至三口烧瓶,并分层。
(4)倒入氢氧化钠溶液,振荡,静置,分液。
13.(1)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却.
(2)将反应器放在50~60℃(或回答60℃)的水浴中加热
(3)分液漏斗
(4)除去粗产品中残留的酸(或回答除去残留的硝酸,硫酸)
(5)大
苦杏仁
三.计算
14.答案:2∶l∶6
2.24L
析:反应后容器内无气体剩余,亦无Na202剩余,其固体只能是Na2CO3与NaOH的混合物。设Na2C03、NaOH物质的量分别为x、y,则可列出如下式子
根据C元素质量守恒,可知若CH4为0.1mol,Na2CO3亦为0.1mol
放出CO2气体亦为0.1mol,因此:标准状况可放出CO2
2.24L。
PAGE
第1页
第二单元
芳香烃
苯的结构与性质
测试题
一、选择题
1.下列物质分子中的氢原子不在同一平面上的有
(
)
A
C2H2
B.C2H4
C.C2H6
D.C6H6
2.比较下列化学键:①烷烃中的碳碳单键,②烯烃中的碳碳双键,③炔烃中的碳碳叁键,④苯环中碳碳键,其键长由长到短的顺序是
(
)
A.①②③④
B.①②④③
C.①④②③
D.④①③②
3.关于苯的下列说法中不正确的是
(
)
A.组成苯的12个原子在同一平面上
B.苯环中6个碳碳键键长完全相同
C.苯环中碳碳键的键能介于C-C和C=C之间
D.苯只能发生取代反应
4.能说明苯分子苯环的平面正六边形结构中,碳碳键不是单双键交替排布的事实是(
)
A.苯的一元取代物没有同分异构体
B.苯的邻位二元取代物只有一种
C.苯的间位二元取代物只有一种
D.苯的对位二元取代物只有一种
5.将下列各种液体分别与溴水混合并振荡,不能发生反应,静置后溶液分层,且溴水层几乎无色的是
(
)
A.CCl4
B.己烯
C.苯
D.酒精
6.在一定条件下,能和Br2起反应而且有HBr生成的是
(
)
A.丙烷
B.苯
C.乙烯
D.乙炔
7.用分液漏斗可以分离的一组液体混合物是
(
)
A.溴和CCl4
B.苯和溴苯
C.硝基苯和水
D.汽油和苯
8.已知二氯苯有3种同分异构体,则四氯苯的同分异构体有
(
)
A.2种
B.3种
C.4种
D.5种
9.某烃结构式如下:-C≡C-CH=CH-CH3,有关其结构说法正确的是
(
)
A.
所有原子可能在同一平面上
B.
所有原子可能在同一条直线上
C.
所有碳原子可能在同一平面上
D.
所有氢原子可能在同一平面上
10.实验室用溴和苯在FeBr3催化下制取溴苯,得到粗溴苯后,要用如下操作提纯:(1)蒸馏;(2)水洗;(3)用干燥剂干燥;(4)用10%的NaOH溶液洗涤。正确的操作顺序是
(
)
A、(1)
(2)
(3)
(4)
B、(4)
(2)
(3)
(1)
C、(4)
(1)
(2)
(3)
D、(2)
(4)
(3)
(1)
11.(05年南京三测)目前,世界上已合成了几百种有机超导体,TCNQ是其中之一。TCNQ的分子结构如下图所示.下列关于TCNQ说法错误的是
(
)
A.分子中所有的氮原子在同一平面内
B.属于芳香烃
C.分子式为C12H4N4
D.该物质难溶于水
二、填空题
12.实验室制备溴苯可用下图所示装置。填空:
(1)关闭F夹,打开C夹,使装有少量苯的三口
烧瓶中由A口加少量溴,再加少量铁屑,
塞住A
口,则三口烧瓶中发生反应的化学方程式为
;
。
(2)D、E试管内出现的现象为
、
。
(3)待三口烧瓶中的反应进行到仍有气泡冒出时松开F夹,关闭C夹,可以看到的现象是
。
(4)简述将三口烧瓶中的溴苯分离提纯的方法:
。
13.实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中.
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤.
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯.
填写下列空白:(1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是:
_______________________________________________________.
(2)步骤③中,为了使反应在50-60℃下进行,常用的方法是
___________________
.
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是
___________________________
.
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是
________________________
.
(5)纯硝基苯是无色,密度比水
____
(填"小"或"大"),具有
____
气味的油状液体.
三.计算
14.(5分)将一定量的CH4,O4和Na2O2放入一密闭容器中,用电火花不断引燃数量混合气体,使其充分反应,反应后容器内的压强趋于零。其残余固体溶于水无气体产生。则CH4、O2、Na2O2的物质的量之比为
。若CH4取0.1mol,则反应后残余固体中加入足量的盐酸,能放出气体
L(标准状况)。
苯的结构与性质
参考答案
( http: / / www.e- / shownews.asp id=59&title=本站%3cfont%20color=red%3e课时练习%3c / font%3e介绍 )
一、选择题
1.C
2.C
3.D
4.B
5.AC
6.AB
7.C
8.B
9.C
10.D
11.B
二、填空题
12.(1)2Fe
+
3Br2
=
2FeBr3
+
Br2
+
HBr
(2)D中有雾生成且石蕊试液变红;E中有浅黄色沉淀生成。
(3)水倒吸至三口烧瓶,并分层。
(4)倒入氢氧化钠溶液,振荡,静置,分液。
13.(1)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却.
(2)将反应器放在50~60℃(或回答60℃)的水浴中加热
(3)分液漏斗
(4)除去粗产品中残留的酸(或回答除去残留的硝酸,硫酸)
(5)大
苦杏仁
三.计算
14.答案:2∶l∶6
2.24L
析:反应后容器内无气体剩余,亦无Na202剩余,其固体只能是Na2CO3与NaOH的混合物。设Na2C03、NaOH物质的量分别为x、y,则可列出如下式子
根据C元素质量守恒,可知若CH4为0.1mol,Na2CO3亦为0.1mol
放出CO2气体亦为0.1mol,因此:标准状况可放出CO2
2.24L。
PAGE
第1页
