有机化学基础期中考试模拟
图片预览



文档简介
新课标化学选修5《有机化学基础》尖子生期中考试模拟试题
选择题(只有一个答案)
1.下列原子或原子团,不属于官能团的是
A. OH— B. —NO2 C. —SO3H D. —OH
2.乙醇(CH3CH2OH)和二甲醚(CH3—O—CH3)互为的同分异构体的类型为
A、位置异构 B、官能团异构 C、顺反异构 D、碳链异构
3.下列化学式只能表示一种物质的是
A、C3H8 B、C4H10 C、C4H8 D、C2H4Cl2
4.物质的量相等的戊烷、苯和苯酚完全燃烧,需要氧气的物质的量依次是x mol、y mol、z mol,则x、y、z的关系是
A、x>y>z B、 y>x>z C、 z>y>x D、 y>x>z
5.下列各组物质间的反应与反应类型不相符的是:
乙烯与溴水(加成反应) B、甲苯与浓硝酸(硝化反应)
C、氯乙烷与氢氧化钠醇溶液 (取代反应) D、乙稀与高锰酸钾(氧化反应)
6、相同质量的乙烷、乙烯、乙炔、乙醇在空气中充分燃烧后生成的二氧化碳在标准状况下体积最小的是:
乙醇 B、乙烯 C、乙炔 D、乙烷
7、与丙烯具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是
A.环丙烷 B.环丁烷 C.乙烯 D.丙烷
8、用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的种类数为:
A、3 B、 4 C、5 D、6
选择题(有一个或两个答案)
9、、两种烃混合,完全燃烧后生成的CO2 的物质的量大于生成的H2O 的物质的量,则这两种烃的组合可能是:
烷烃和烷烃 B、烯烃和烯烃C、烯烃和炔烃 D、烷烃和烯烃
10、有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实能说明上述观点的是
甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色
乙烯能发生加成反应,而乙烷不能发生加成反应
苯酚与溴水直接就可反应,而苯与溴水反应则需要铁作催化剂
D、 氯乙烷能与氢氧化钠水溶液发生取代反应,而乙烷不能
11、由烃转化为卤代烃的途径较多,下列能得到较纯氯乙烷的方法是
A. 乙烷与氯气发生取代反应 B.乙烯与氯化氢发生加成反应
C.乙烯与氯气发生加成反应 D.乙炔与氯化氢发生加成反应
12、某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是
A. C3H8 B. C4H10 C. C5H12 D. C6H14
13、丁烷催化裂化时碳链按两种方式断裂,生成两种烷烃和两种烯烃。如果丁烷的裂化率为60%,且裂化生成的两种烯烃的质量相等,则裂化后得到的分子量最小的气体占混合气体的体积分数为:
25% (B)30% (C)15% (D)20%
14、由两种气态烃组成的混合气体,其所含的碳元素和氢元素的质量之比为24:3,则混合气体的组成及其体积比可能是:
CH4和C3H4 ,体积比为1:1 B、C2H2和C2H6 ,体积比为3:1
C、C2H4和C2H6 ,体积比为2:1 D、C2H2 和C2H4 ,体积比为1:1
15、将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L<标况>CO2和3.6g水,对于组成判断正确的是( )
A.一定有甲烷 B.一定有乙烯 C.一定没有甲烷 D.一定没有乙烷
16、.某有机物CxHmOn完全燃烧,需O2的物质的量是有机物的x倍,则该有机物的化学式中x、m、n的关系不可能是( )
A.m≥2x+2 B.m∶n=2∶1 C.x∶m∶n=1∶2∶1 D.m<2x+2
17、某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体(
A( 2 B( 3 C( 4 D( 5
18、化学工作者把烷烃、烯烃、环烷烃……,转化为键数的通式,给研究有机物分子中键能大小的规律带来了很大的方便,设键数为I,则烷烃中碳原子与键数关系的通式为CnI3n+1,烯烃<视双键为的两个单键>,环烷烃中碳原子与键数关系的通式均为CnI3n?,则苯的同系物中碳原子与键数的关系通式为
A.CnI3n-1 B.CnI3n-2 C.CnI3n-3 D.CnI3n-4
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
三、实验题:
19、实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中.
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤.
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯.
填写下列空白:
(1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是: .
(2)步骤③中,为了使反应在50-60℃下进行,常用的方法是 .
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是 .
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是 .
(5)纯硝基苯是无色,密度比水 (填"小"或"大"),具有 气味的油状液体.
四、填空题:
20. 在沥青中有一系列稠环化合物,它们彼此并不是同系物,但其组成和结构都有规律性的变化
从萘开始这一系列化合物中第25个分子的分子式_________。该系列化合物碳元素质量分子的最大值____。
21.已知两结构式互为同分异构体a、b各为不同的原子
或原子团——顺反异构,试述具有这种异构的有机化合物在结构上必须具备的条件_______________现有组成为C4H7Cl的链状卤代烃的同分异构体(包括顺反异构)共有_____种。
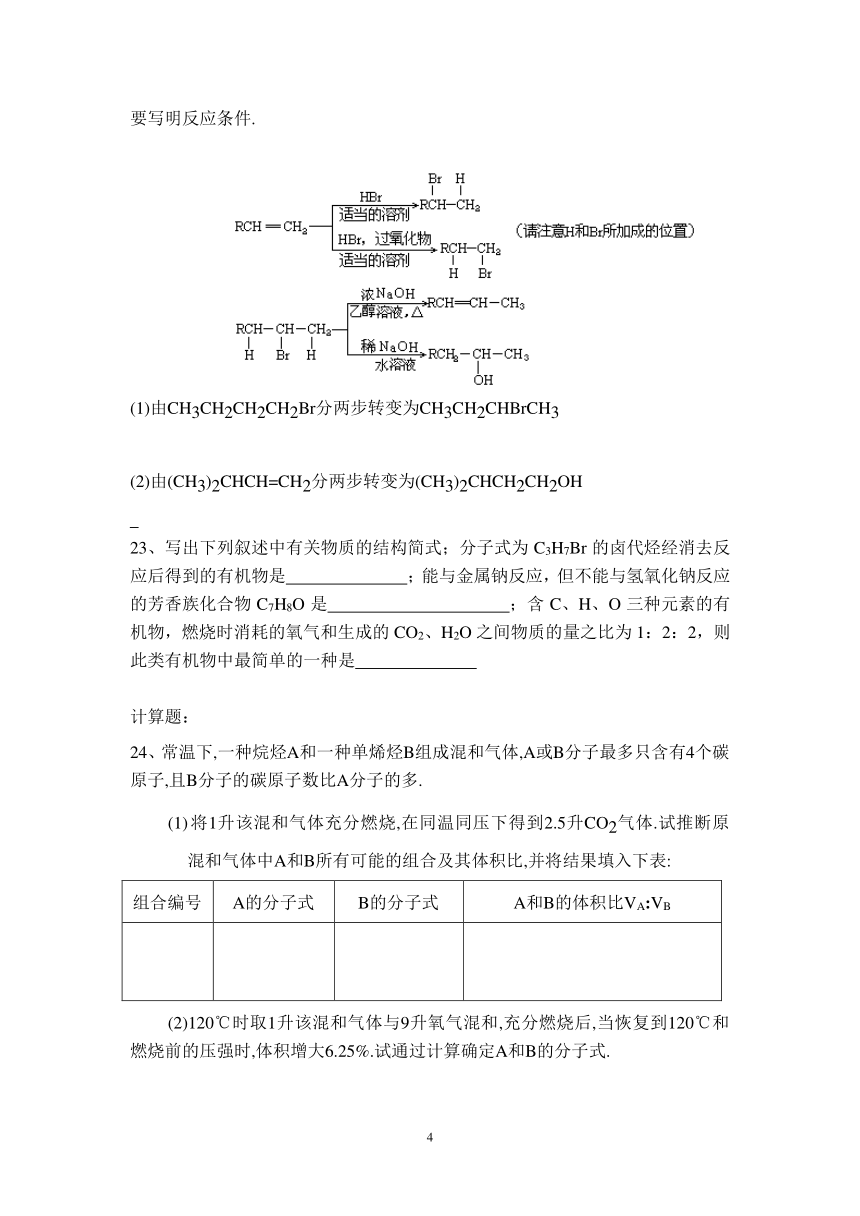
22、在有机反应中,反应物相同而条件不同,可得到不同的主产物.下式中R代表烃基,副产物均已略去.请写出实现下列转变的各步反应的化学方程式,特别注意要写明反应条件.
(1)由CH3CH2CH2CH2Br分两步转变为CH3CH2CHBrCH3
(2)由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH
23、写出下列叙述中有关物质的结构简式;分子式为C3H7Br的卤代烃经消去反应后得到的有机物是 ;能与金属钠反应,但不能与氢氧化钠反应的芳香族化合物C7H8O是 ;含C、H、O三种元素的有机物,燃烧时消耗的氧气和生成的CO2、H2O之间物质的量之比为1:2:2,则此类有机物中最简单的一种是
计算题:
24、常温下,一种烷烃A和一种单烯烃B组成混和气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多.
将1升该混和气体充分燃烧,在同温同压下得到2.5升CO2气体.试推断原混和气体中A和B所有可能的组合及其体积比,并将结果填入下表:
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
(2)120℃时取1升该混和气体与9升氧气混和,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%.试通过计算确定A和B的分子式.
25、(1)已知某混和气体的体积百分组成为80.0%CH4、15.0%C2H4和5.00%C2H6.请计算0.500摩该混和气体的质量和标准状况下的密度(克/升).
(2)CH4在一定条件下催化氧化可以生成C2H4、C2H6(水和其它反应产物忽略不计).取一定量CH4经催化氧化后得到一种混和气体,它在标准状况下的密度为0.780克/升.已知反应中CH4消耗了20.0%,计算混和气体中C2H4的体积百分含量.(本题计算过程中请保持3位有效数字)
答案:
19、(1)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却.
(3分)(注:浓硝酸和浓硫酸的加入次序写错,不给分;没回答"慢慢加入",扣1分;没回答"及时搅拌"扣1分.)
(2)将反应器放在50~60℃(或回答60℃)的水浴中加热.(2分)
[注:只回答"在水浴中加热",没回答50~60℃(或60℃)扣1分;回答"用酒精灯"直接加热,或只回答"加热"的不给分.]
(3)分液漏斗 (1分)
(4)除去粗产品中残留的酸(或回答除去残留的硝酸,硫酸)(1分)
(5)大 苦杏仁 (2分)
20、.通式 C6n+4H2n+6 n=25 C154H56 C%=97.3%
21.(1)必需具有键 (2)在键中的不饱和C必须都连有不同的原子或原子团 11种
22、
23、CH3-CH=CH2 HCOOH
24、(1)[解题思路]1升碳原子数为n的烷烃或烯烃充分燃烧后均得到n升CO2,由题意(1升混和气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多)可推断,混和气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成.它们有四种可能的组合.根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,可确定A和B的体积比.(以上内容不要求考生在卷面上回答.)
[说明:对于每种可能的组合,如果体积比不正确,或写出多于一种体积比,该组合不给分.]
(2)设1升气态烃与氧充分燃烧后体积变化为△V升,则
CH4+2O2=CO2+2H2O(气) △V1=0(升)
C4H8+6O2=4CO2+4H2O(气) △V4=1.0(升)
各种组合的1升混和气体与氧气充分燃烧,体积增大为:
(2分)
故组合④符合题意,即A:C2H6;B:C4H8.
(1分)
[说明:无论有无计算过程,结论正确,即给1分.给出正确判断的过程或以验算方式证实的,都给计算分2分.]
25、(1)0.500×(16×0.800+28×0.150+30×0.0500)=9.25(克)
(2分)
选择题(只有一个答案)
1.下列原子或原子团,不属于官能团的是
A. OH— B. —NO2 C. —SO3H D. —OH
2.乙醇(CH3CH2OH)和二甲醚(CH3—O—CH3)互为的同分异构体的类型为
A、位置异构 B、官能团异构 C、顺反异构 D、碳链异构
3.下列化学式只能表示一种物质的是
A、C3H8 B、C4H10 C、C4H8 D、C2H4Cl2
4.物质的量相等的戊烷、苯和苯酚完全燃烧,需要氧气的物质的量依次是x mol、y mol、z mol,则x、y、z的关系是
A、x>y>z B、 y>x>z C、 z>y>x D、 y>x>z
5.下列各组物质间的反应与反应类型不相符的是:
乙烯与溴水(加成反应) B、甲苯与浓硝酸(硝化反应)
C、氯乙烷与氢氧化钠醇溶液 (取代反应) D、乙稀与高锰酸钾(氧化反应)
6、相同质量的乙烷、乙烯、乙炔、乙醇在空气中充分燃烧后生成的二氧化碳在标准状况下体积最小的是:
乙醇 B、乙烯 C、乙炔 D、乙烷
7、与丙烯具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是
A.环丙烷 B.环丁烷 C.乙烯 D.丙烷
8、用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的种类数为:
A、3 B、 4 C、5 D、6
选择题(有一个或两个答案)
9、、两种烃混合,完全燃烧后生成的CO2 的物质的量大于生成的H2O 的物质的量,则这两种烃的组合可能是:
烷烃和烷烃 B、烯烃和烯烃C、烯烃和炔烃 D、烷烃和烯烃
10、有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实能说明上述观点的是
甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色
乙烯能发生加成反应,而乙烷不能发生加成反应
苯酚与溴水直接就可反应,而苯与溴水反应则需要铁作催化剂
D、 氯乙烷能与氢氧化钠水溶液发生取代反应,而乙烷不能
11、由烃转化为卤代烃的途径较多,下列能得到较纯氯乙烷的方法是
A. 乙烷与氯气发生取代反应 B.乙烯与氯化氢发生加成反应
C.乙烯与氯气发生加成反应 D.乙炔与氯化氢发生加成反应
12、某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是
A. C3H8 B. C4H10 C. C5H12 D. C6H14
13、丁烷催化裂化时碳链按两种方式断裂,生成两种烷烃和两种烯烃。如果丁烷的裂化率为60%,且裂化生成的两种烯烃的质量相等,则裂化后得到的分子量最小的气体占混合气体的体积分数为:
25% (B)30% (C)15% (D)20%
14、由两种气态烃组成的混合气体,其所含的碳元素和氢元素的质量之比为24:3,则混合气体的组成及其体积比可能是:
CH4和C3H4 ,体积比为1:1 B、C2H2和C2H6 ,体积比为3:1
C、C2H4和C2H6 ,体积比为2:1 D、C2H2 和C2H4 ,体积比为1:1
15、将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L<标况>CO2和3.6g水,对于组成判断正确的是( )
A.一定有甲烷 B.一定有乙烯 C.一定没有甲烷 D.一定没有乙烷
16、.某有机物CxHmOn完全燃烧,需O2的物质的量是有机物的x倍,则该有机物的化学式中x、m、n的关系不可能是( )
A.m≥2x+2 B.m∶n=2∶1 C.x∶m∶n=1∶2∶1 D.m<2x+2
17、某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体(
A( 2 B( 3 C( 4 D( 5
18、化学工作者把烷烃、烯烃、环烷烃……,转化为键数的通式,给研究有机物分子中键能大小的规律带来了很大的方便,设键数为I,则烷烃中碳原子与键数关系的通式为CnI3n+1,烯烃<视双键为的两个单键>,环烷烃中碳原子与键数关系的通式均为CnI3n?,则苯的同系物中碳原子与键数的关系通式为
A.CnI3n-1 B.CnI3n-2 C.CnI3n-3 D.CnI3n-4
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
三、实验题:
19、实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中.
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤.
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯.
填写下列空白:
(1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是: .
(2)步骤③中,为了使反应在50-60℃下进行,常用的方法是 .
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是 .
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是 .
(5)纯硝基苯是无色,密度比水 (填"小"或"大"),具有 气味的油状液体.
四、填空题:
20. 在沥青中有一系列稠环化合物,它们彼此并不是同系物,但其组成和结构都有规律性的变化
从萘开始这一系列化合物中第25个分子的分子式_________。该系列化合物碳元素质量分子的最大值____。
21.已知两结构式互为同分异构体a、b各为不同的原子
或原子团——顺反异构,试述具有这种异构的有机化合物在结构上必须具备的条件_______________现有组成为C4H7Cl的链状卤代烃的同分异构体(包括顺反异构)共有_____种。
22、在有机反应中,反应物相同而条件不同,可得到不同的主产物.下式中R代表烃基,副产物均已略去.请写出实现下列转变的各步反应的化学方程式,特别注意要写明反应条件.
(1)由CH3CH2CH2CH2Br分两步转变为CH3CH2CHBrCH3
(2)由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH
23、写出下列叙述中有关物质的结构简式;分子式为C3H7Br的卤代烃经消去反应后得到的有机物是 ;能与金属钠反应,但不能与氢氧化钠反应的芳香族化合物C7H8O是 ;含C、H、O三种元素的有机物,燃烧时消耗的氧气和生成的CO2、H2O之间物质的量之比为1:2:2,则此类有机物中最简单的一种是
计算题:
24、常温下,一种烷烃A和一种单烯烃B组成混和气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多.
将1升该混和气体充分燃烧,在同温同压下得到2.5升CO2气体.试推断原混和气体中A和B所有可能的组合及其体积比,并将结果填入下表:
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
(2)120℃时取1升该混和气体与9升氧气混和,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%.试通过计算确定A和B的分子式.
25、(1)已知某混和气体的体积百分组成为80.0%CH4、15.0%C2H4和5.00%C2H6.请计算0.500摩该混和气体的质量和标准状况下的密度(克/升).
(2)CH4在一定条件下催化氧化可以生成C2H4、C2H6(水和其它反应产物忽略不计).取一定量CH4经催化氧化后得到一种混和气体,它在标准状况下的密度为0.780克/升.已知反应中CH4消耗了20.0%,计算混和气体中C2H4的体积百分含量.(本题计算过程中请保持3位有效数字)
答案:
19、(1)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却.
(3分)(注:浓硝酸和浓硫酸的加入次序写错,不给分;没回答"慢慢加入",扣1分;没回答"及时搅拌"扣1分.)
(2)将反应器放在50~60℃(或回答60℃)的水浴中加热.(2分)
[注:只回答"在水浴中加热",没回答50~60℃(或60℃)扣1分;回答"用酒精灯"直接加热,或只回答"加热"的不给分.]
(3)分液漏斗 (1分)
(4)除去粗产品中残留的酸(或回答除去残留的硝酸,硫酸)(1分)
(5)大 苦杏仁 (2分)
20、.通式 C6n+4H2n+6 n=25 C154H56 C%=97.3%
21.(1)必需具有键 (2)在键中的不饱和C必须都连有不同的原子或原子团 11种
22、
23、CH3-CH=CH2 HCOOH
24、(1)[解题思路]1升碳原子数为n的烷烃或烯烃充分燃烧后均得到n升CO2,由题意(1升混和气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多)可推断,混和气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成.它们有四种可能的组合.根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,可确定A和B的体积比.(以上内容不要求考生在卷面上回答.)
[说明:对于每种可能的组合,如果体积比不正确,或写出多于一种体积比,该组合不给分.]
(2)设1升气态烃与氧充分燃烧后体积变化为△V升,则
CH4+2O2=CO2+2H2O(气) △V1=0(升)
C4H8+6O2=4CO2+4H2O(气) △V4=1.0(升)
各种组合的1升混和气体与氧气充分燃烧,体积增大为:
(2分)
故组合④符合题意,即A:C2H6;B:C4H8.
(1分)
[说明:无论有无计算过程,结论正确,即给1分.给出正确判断的过程或以验算方式证实的,都给计算分2分.]
25、(1)0.500×(16×0.800+28×0.150+30×0.0500)=9.25(克)
(2分)
