1.2.1《原子核外电子的排布》PPT课件(新人教版-必修2)
文档属性
| 名称 | 1.2.1《原子核外电子的排布》PPT课件(新人教版-必修2) |

|
|
| 格式 | zip | ||
| 文件大小 | 447.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-03 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
新课标人教版课件系列
《高中化学》
必修2
1.2.1《原子核外电子
的排布》
第一章 物质结构 元素周期律 第二节《元素周期律》 第1课时
教学目标
知识与技能:
1、以1-20号元素为例,了解元素原子核外电子排布规律。2、掌握元素化合价随原子序数的递增而呈现出的周期变化规律。
过程与方法:
1.归纳法、比较法。2.培养学生抽象思维能力。
情感、态度与价值观:
培养学生勤于思考、勇于探究的科学品质。
教学重点:元素化合价随原子序数的递增的变化规律。
教学难点:原子核外电子排布。
教具准备:实物投影仪、多媒体
一、核外电子排布
与元素周期表
现代周期表形成历程
门捷列夫式
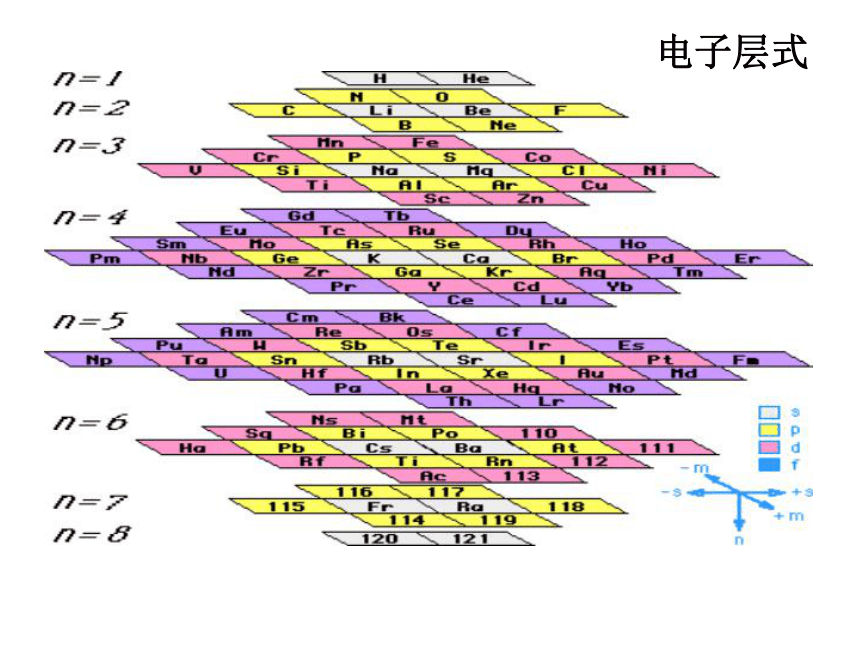
电子层式
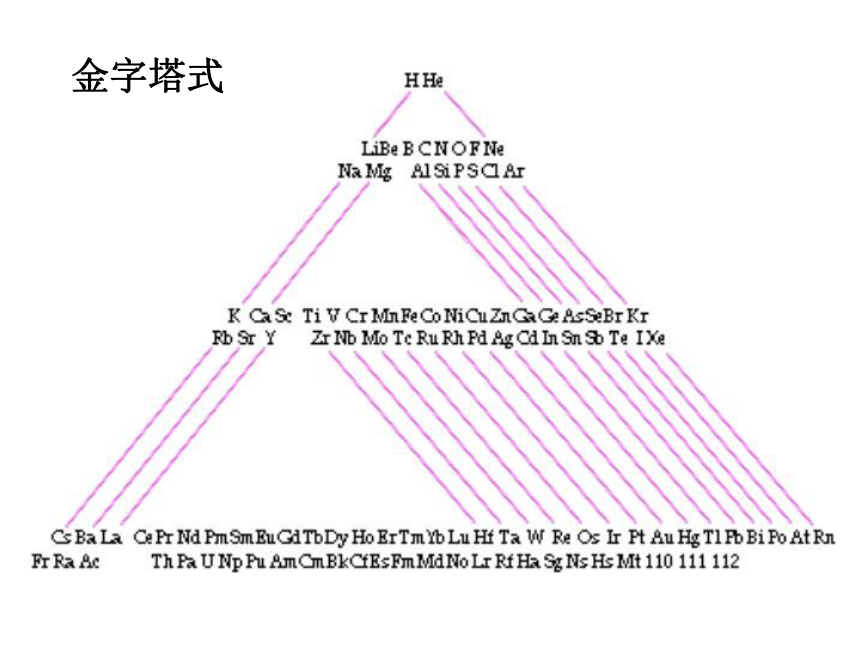
金字塔式
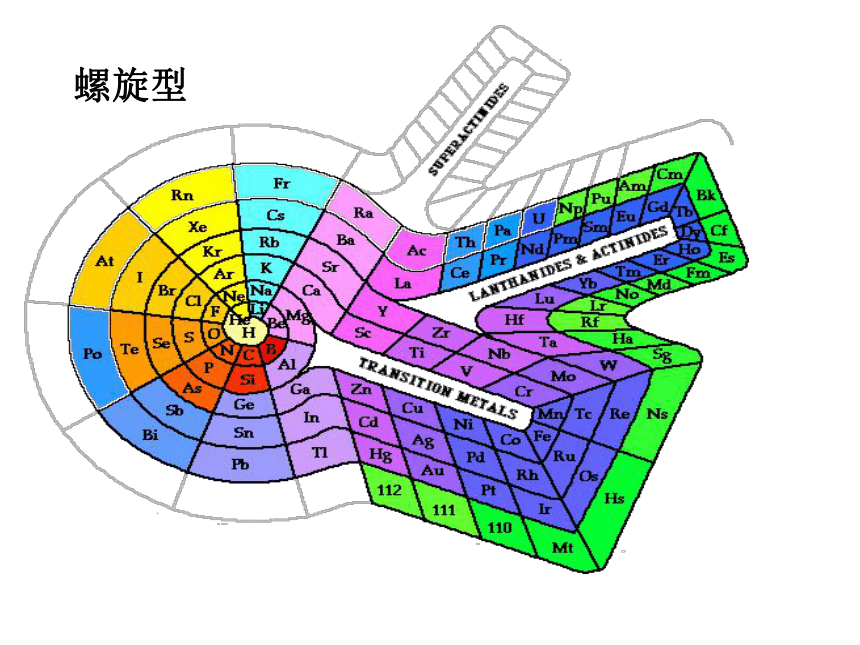
螺旋型
现代式
主 表
副 表
主 族\
主 族\
周 期
过 渡 元 素
镧 锕 系 元 素
零 族
教科书上的
元素周期表
1、核外电子排布
与周期的划分
1、周期的划分与什么有关?
2、每一周期中所能容纳的元素种
数与什么有关?
3、周期序数与什么有关?
美国化学家------鲍林
鲍林近似能级图
针对练习:
比较原子轨道的能级高低:
钾原子中 E3s___E3p E3d___E4s
铁原子中 E3s___E3p E3d___E4s
钡原子中 E3s___E3p E3d___E4s
<
>
<
>
<
<
1、周期的划分与能级组有关,七个
能级组对应七个周期。
2、每一周期中所能容纳的元素种
数与该能级所容纳的电子数相
等,即该能级组轨道数的两倍。
3、周期序数与主量子数有关,最
外层电子的主量子数为n,即
为第n周期。
请记下来呦!
能级
符号
能级组数(周期数) 能级组内最多电子数(周期中的元素数)
周期名称
1s 1 2 特短周期
2s,2p 2 8 短周期
3s,3p 3 8 短周期
4s,3d,4p 4 18 长周期
5s,4d,5p 5 18 长周期
6s,4f,5d,6p 6 32 特长周期
7s,5f,6d,7p 7 (32) 未满周期
2、核外电子排布
与族的划分
1.主族元素原子的价电子排布与过渡元素原子的价电子排布有什么区别?
2.同一主族元素原子的价电子排布有什么特点?主族序数与什么有关?
3.同一族过渡元素原子的价电子排布有什么特点?其族序数与什么有关?
族
价层电子构型
按近似能级最
后填入的电子
分区
IA 、IIA
IIIA~0
IIIB~VIII
IB、IIB
ns1~2
s电子
s
ns2np1~6
p电子
p
(n-1)d1~8ns1~2
d电子
d
(n-1)d10ns1~2
d10电子
ds
随堂练:
原子结构与元素周期表存在着内在的联系。
1.请写出基态原子的外层具有下列电子排
布的所有元素的名称与符号。
(1)ns2np3(n=2~4) (2)3d6~8 4s2(3)3d104s1(4)4s1
2.指出这些元素在周期表中的位置
3.外层具有4s电子排布的主族元素的基态原子容易失去1个电子,形成正一价的阳离子。写出该阳离子的电子排布式。
新课标人教版课件系列
《高中化学》
必修2
1.2.1《原子核外电子
的排布》
第一章 物质结构 元素周期律 第二节《元素周期律》 第1课时
教学目标
知识与技能:
1、以1-20号元素为例,了解元素原子核外电子排布规律。2、掌握元素化合价随原子序数的递增而呈现出的周期变化规律。
过程与方法:
1.归纳法、比较法。2.培养学生抽象思维能力。
情感、态度与价值观:
培养学生勤于思考、勇于探究的科学品质。
教学重点:元素化合价随原子序数的递增的变化规律。
教学难点:原子核外电子排布。
教具准备:实物投影仪、多媒体
一、核外电子排布
与元素周期表
现代周期表形成历程
门捷列夫式
电子层式
金字塔式
螺旋型
现代式
主 表
副 表
主 族\
主 族\
周 期
过 渡 元 素
镧 锕 系 元 素
零 族
教科书上的
元素周期表
1、核外电子排布
与周期的划分
1、周期的划分与什么有关?
2、每一周期中所能容纳的元素种
数与什么有关?
3、周期序数与什么有关?
美国化学家------鲍林
鲍林近似能级图
针对练习:
比较原子轨道的能级高低:
钾原子中 E3s___E3p E3d___E4s
铁原子中 E3s___E3p E3d___E4s
钡原子中 E3s___E3p E3d___E4s
<
>
<
>
<
<
1、周期的划分与能级组有关,七个
能级组对应七个周期。
2、每一周期中所能容纳的元素种
数与该能级所容纳的电子数相
等,即该能级组轨道数的两倍。
3、周期序数与主量子数有关,最
外层电子的主量子数为n,即
为第n周期。
请记下来呦!
能级
符号
能级组数(周期数) 能级组内最多电子数(周期中的元素数)
周期名称
1s 1 2 特短周期
2s,2p 2 8 短周期
3s,3p 3 8 短周期
4s,3d,4p 4 18 长周期
5s,4d,5p 5 18 长周期
6s,4f,5d,6p 6 32 特长周期
7s,5f,6d,7p 7 (32) 未满周期
2、核外电子排布
与族的划分
1.主族元素原子的价电子排布与过渡元素原子的价电子排布有什么区别?
2.同一主族元素原子的价电子排布有什么特点?主族序数与什么有关?
3.同一族过渡元素原子的价电子排布有什么特点?其族序数与什么有关?
族
价层电子构型
按近似能级最
后填入的电子
分区
IA 、IIA
IIIA~0
IIIB~VIII
IB、IIB
ns1~2
s电子
s
ns2np1~6
p电子
p
(n-1)d1~8ns1~2
d电子
d
(n-1)d10ns1~2
d10电子
ds
随堂练:
原子结构与元素周期表存在着内在的联系。
1.请写出基态原子的外层具有下列电子排
布的所有元素的名称与符号。
(1)ns2np3(n=2~4) (2)3d6~8 4s2(3)3d104s1(4)4s1
2.指出这些元素在周期表中的位置
3.外层具有4s电子排布的主族元素的基态原子容易失去1个电子,形成正一价的阳离子。写出该阳离子的电子排布式。
