高中化学苏教版(2019)必修第一册 专题1 第一单元 物质及其反应的分类(57张PPT)
文档属性
| 名称 | 高中化学苏教版(2019)必修第一册 专题1 第一单元 物质及其反应的分类(57张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-16 16:45:06 | ||
图片预览










文档简介
第一单元 物质及其反应的分类
1.能根据不同标准对物质进行分类。
2.能根据化合价变化判断氧化还原反应和非氧化还原反应。
3.初步认识研究物质通性及相关转化的思路和方法。
4.促进宏观辨识与微观探析核心素养发展。
核心素养发展目标
一、物质的分类
随堂演练 知识落实
课时对点练
二、物质的转化
内
容
索
引
三、化学反应的分类
1.分类法简介
分类是指按照_____、_____或_____分别归类。利用事物间的_______,把某些具有_______或_________的事物归为一类,通常可根据事物的_________或事物的_________来进行分类。
2.物质的分类方法
(1)根据物质的存在状态:分为_____物质、_____物质、_____物质。
(2)根据物质的导电性:分为_____、_______、_______。
(3)根据物质在水中的溶解性:分为_______物质、_______物质、______物质。
一、物质的分类
种类
等级
性质
相似性
共同点
相似特征
外部特征
本质特征
固态
液态
气态
导体
半导体
绝缘体
可溶性
微溶性
难溶性
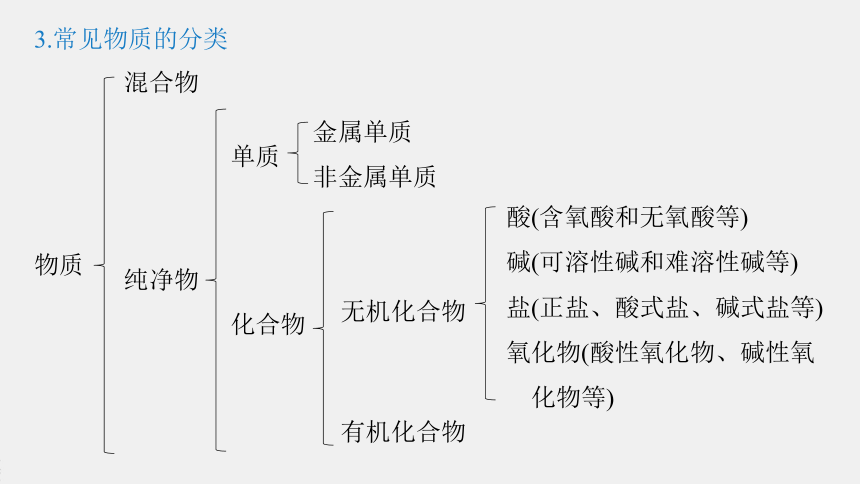
3.常见物质的分类
混合物
物质
纯净物
化合物
单质
金属单质
非金属单质
无机化合物
酸(含氧酸和无氧酸等)
碱(可溶性碱和难溶性碱等)
盐(正盐、酸式盐、碱式盐等)
氧化物(酸性氧化物、碱性氧
化物等)
有机化合物
(1)对于同一物质,分类标准不同,物质类别也不同。
如NaHSO4既属于盐、钠盐、酸式盐,又属于含氧酸盐等。
(2)依据组成和性质判断物质的类别时应注意:
①纯碱(Na2CO3)不属于碱,属于盐。
②结晶水合物如CuSO4·5H2O等为纯净物。
③只含有一种元素的物质可能是纯净物,也可能是混合物。
归纳总结
(1)K2CO3是钾盐,也是碳酸盐( )
(2)Na2CO3含有氧元素,所以属于氧化物( )
(3)SO3既是非金属氧化物,又是酸性氧化物( )
(4)相同种类元素可以形成不同的化合物( )
(5)非金属氧化物一定是酸性氧化物( )
(6)金属氧化物一定是碱性氧化物( )
判断正误
√
×
√
√
×
×
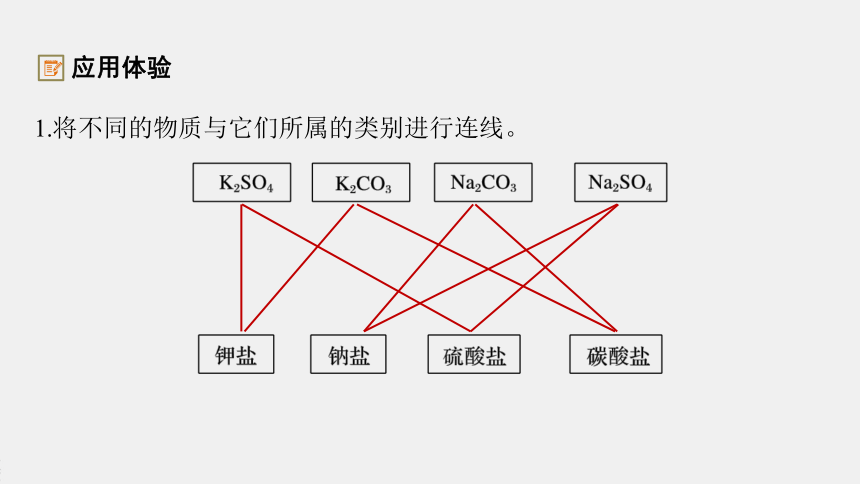
1.将不同的物质与它们所属的类别进行连线。
应用体验
2.下列每组中都有一种物质与其他物质在分类上不同,试分析每组物质的组成规律。将这种不同于其他物质的物质找出来(分类标准合理即可)。
(1)NaCl、KCl、NaClO、MgCl2________。
(2)HClO3、KClO3、Cl2、NaClO3_______。
(3)H3PO4、HNO3、HCl、H2SO4________。
(4)空气、N2、氯化氢气体、CuSO4·5H2O____________________。
(5)铜、金、汞、钠________。
NaClO
Cl2
HCl
空气(或CuSO4·5H2O)
钠(或汞)
返回
二、物质的转化
1.通过物质分类,可以建立物质间的从属关系,分析物质间的本质区别和联系,寻找各类物质之间的转化关系。
(1)以钙为例,用化学方程式表示钙及其化合物之间的转化关系。
①_________________;
②______________________;
③____________________;
④______________________________;
⑤______________________________;
⑥__________________________________。
2Ca+O2===2CaO
CaO+H2O===Ca(OH)2
CaO+CO2===CaCO3
Ca(OH)2+CO2===CaCO3↓+H2O
Ca(OH)2+2HCl===CaCl2+2H2O
CaCO3+2HCl===CaCl2+CO2↑+H2O
①_______________;
②___________________;
③___________________;
④_______________________________;
⑤__________________________________。
(2)碳及其化合物间的转化关系如图所示:
各步化学方程式:
CO2+H2O===H2CO3
CO2+CaO===CaCO3
CO2+Ca(OH)2===CaCO3↓+H2O
H2CO3+Ca(OH)2===CaCO3↓+2H2O
(1)可用Fe2O3与H2O反应制取Fe(OH)3( )
(2)只有利用酸碱中和反应才能生成盐( )
(3)根据酸的通性,酸能和所有的金属反应( )
(4)并不是所有的酸和盐都能发生反应( )
(5)CaCO3和H2SO4可以反应,因此实验室可以用大理石和稀硫酸制二氧化碳( )
判断正误
×
×
×
√
×
选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转化用化学方程式表示(所写化学方程式不得重复)。
应用体验
① ;
②CO2+H2O===H2CO3;
③______________________________;
④_______________________;
CO2+Ca(OH)2===CaCO3↓+H2O
Fe+2HCl===FeCl2+H2↑
⑤_________________________;
⑥______________________________;
⑦_____________________。
CaO+2HCl===CaCl2+H2O
Ca(OH)2+2HCl===CaCl2+2H2O
CaO+H2O===Ca(OH)2
解析 属于同一类的物质必定符合同一标准,就会有某一共同的性质,利用一类物质和另一类物质之间的关系,就可以找出物质之间转化的方法,一般有以下化学通性:
物质之间的转化关系
返回
归纳总结
单质、氧化物、酸、碱、盐之间的转化关系图示如下:
1.化学反应的分类及其依据
三、化学反应的分类
2.判断化学反应类型
(1)请指出下列各反应的四种基本反应类型:
①2NO+O2===2NO2 _________
②CO2+CaO===CaCO3 _________
③NH4HCO3 NH3↑+CO2↑+H2O _________
④2KClO3 2KCl+3O2↑ _________
⑤Fe+2HCl===FeCl2+H2↑ _________
⑥Zn+CuSO4===ZnSO4+Cu _________
⑦HCl+KOH===KCl+H2O ___________
⑧BaCl2+Na2SO4===BaSO4↓+2NaCl ___________
(2)上述各反应属于氧化还原反应的是__________(填序号)。
化合反应
化合反应
分解反应
分解反应
置换反应
置换反应
复分解反应
复分解反应
①④⑤⑥
(1)氧化还原反应中一定有氧元素的得失( )
(2)氧化还原反应中所有元素化合价都一定发生变化( )
(3)有单质参加的一定是氧化还原反应( )
(4)置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应
( )
(5)化合反应与分解反应可能是氧化还原反应,也可能是非氧化还原反应
( )
判断正误
×
×
×
√
√
化学反应按照不同的分类方法可以分为化合反应、分解反应、置换反应、复分解反应,也可以分为氧化还原反应和非氧化还原反应。回答下列问题:
应用体验
⑤Na2SO4+BaCl2===2NaCl+BaSO4↓ ⑥H2O2+H2S===S↓+2H2O
(1)既是氧化还原反应又是化合反应的为______(填序号,下同)。
(2)属于非氧化还原反应的为____。
(3)不属于四种基本反应类型的为____。
(4)属于置换反应的为____。
①②
⑤
⑥
③
氧化还原反应与四种基本反应类型之间的关系
返回
归纳总结
1
2
3
5
随堂演练 知识落实
4
1.对下列物质分类全部正确的是
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
A.碱:①④ B.纯净物:①③④⑤⑥
C.盐:①⑥ D.混合物:②③⑤
√
解析 纯碱是Na2CO3,属于盐,A项错误;
石灰水是混合物,B项错误;
液态氧是纯净物,D项错误。
6
2.国家质检部门检验出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种
A.氧化物 B.盐 C.碱 D.酸
1
2
3
5
4
解析 胆矾、绿矾等结晶水合物都属于盐,为纯净物。
√
6
解析 CO2、SO2属于酸性氧化物,CaCO3、KMnO4属于盐,CuO属于碱性氧化物。
3.根据某种共性,可将CO2、SO2归为一类氧化物,下列物质中与它们属于同一类的是
A.CaCO3 B.P2O5 C.CuO D.KMnO4
1
2
3
5
4
√
6
4.下列变化不能通过一步化学反应实现的是
A.BaCl2→BaSO4 B.CuO→Cu(OH)2
C.NaOH→Na2SO3 D.MgSO4→Mg(OH)2
1
2
3
5
4
解析 CuO难溶于水,不能与水反应。
√
6
5.下列反应既是化合反应又是氧化还原反应的是
A.2CO+O2 2CO2
B.CaO+H2O===Ca(OH)2
C.C+H2O(g) CO+H2
D.CO2+Ca(OH)2===CaCO3↓+H2O
1
2
3
5
4
√
6
解析 酸可以填写H2S、H2SO4、HNO3、H2CO3等,碱可以填写KOH或NaOH等;盐可填写K2CO3、Na2SO4、NaNO3、KNO3、K2SO4等。
6.(2020·天津调研)无机化合物可根据其组成和性质进行分类。
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表中。
1
2
3
5
4
6
物质类别
酸
碱
盐
氧化物
化学式
①HCl
②________
_________
③_________
_________
④Ba(OH)2
⑤Na2CO3
⑥_______________
___________________
⑦CO2
⑧Na2O
H2SO4(或
HNO3等)
NaOH(或
KOH等)
Na2SO4(或K2CO3
或Na2SO3或NaNO3等)
(2)写出⑦转化为⑤的化学方程式:_____________________________。
1
2
3
5
4
6
2NaOH+CO2===Na2CO3+H2O
(3)实验室制备⑦常用________和________反应,检验该气体的方法是______________________________________________。
稀盐酸
碳酸钙
将气体通入澄清石灰水中,若变浑浊,即证明是CO2
解析 CO2是酸性氧化物,可与NaOH反应生成Na2CO3和H2O。
解析 实验室常用CaCO3和稀盐酸反应制取CO2,产生的CO2气体可用澄清石灰水来检验。
返回
解析 煤是含有碳、硫等多种物质构成的混合物;生铁是由铁和碳组成的混合物;矿泉水中除含有水外,还有其他多种矿物质,是混合物。
课时对点练
1
2
3
4
5
6
7
8
9
题组一 物质的分类
1.(2019·河南龙泉中学月考)下列物质是生活中经常用到的物质,其中属于纯净物的是
A.煤 B.生铁 C.蒸馏水 D.矿泉水
√
A组 基础对点练
2.(2019·湖南株洲四中期末)分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可采取多种分类方法。下列各组归类不合理的是
1
2
3
4
5
6
7
8
9
选项
按某一分类标准分类的物质或变化
归类
A
FeSO4、NO2、MnO2、NaClO
H2SO3
B
CH3COOH、HClO、H2S、H2CO3
HF
C
氢气燃烧、氧化钙变质、食物腐烂
冰雪融化
D
(NH4)2SO4、NH4Cl、NH4NO3、NH3·H2O
NH4HCO3
√
解析 A项中物质均为含氧化合物;
B项中物质均属于酸;
C项中氢气燃烧、氧化钙变质、食物腐烂均为化学变化,而冰雪融化属于物理变化;
D项中物质均为含氮化合物。
1
2
3
4
5
6
7
8
9
3.(2019·福建厦门六中期中)下列关于物质分类的组合正确的是
1
2
3
4
5
6
7
8
9
选项
碱
酸
盐
碱性氧化物
酸性氧化物
A
Ca(OH)2
硫酸
小苏打
Mn2O7
干冰
B
烧碱
盐酸
氯化钠
氧化钠
一氧化碳
C
石灰水
冰醋酸(CH3COOH)
胆矾(CuSO4·5H2O)
氧化钠
二氧化硫
D
NaOH
HNO3
碳酸钙
氧化铁
SO3
√
解析 Mn2O7为酸性氧化物,A项错误;
盐酸是氯化氢的水溶液,为混合物,一氧化碳是不成盐氧化物,不属于酸性氧化物,B项错误;
石灰水是氢氧化钙与水的混合物,而碱为纯净物,C项错误。
1
2
3
4
5
6
7
8
9
解析 A项中Fe与盐酸反应生成FeCl2;
B项中H2O2分解生成H2O和O2;
C项中CaCl2和CO2不反应。
题组二 物质的转化
4.下列物质在给定条件下的转化均能一步实现的是
1
2
3
4
5
6
7
8
9
√
5.(2019·唐山高一检测)如图所示,“——”表示相连的物质间在一定条件下可以反应,“—→”表示丁在一定条件下可以转化为乙。下面四组选项中,符合图示要求的是
1
2
3
4
5
6
7
8
9
?
甲
乙
丙
丁
A
H2SO4
Na2SO4
NaOH
NaCl
B
KCl
K2CO3
KOH
HCl
C
O2
CO
C
CuO
D
Fe
CuCl2
Zn
HCl
√
解析 A中甲和乙、乙和丙、丙和丁、丁和甲均不能反应,丁也不能转化为乙;B中甲和乙、乙和丙、丁和甲之间均不能反应,丁也不能转化为乙,故A、B不符合题意;
1
2
3
4
5
6
7
8
9
D中反应依次为甲和乙:Fe+CuCl2===FeCl2+Cu;乙和丙:Zn+CuCl2===Cu+ZnCl2;丙和丁:Zn+2HCl===ZnCl2+H2↑;丁和甲:Fe+2HCl===FeCl2+H2↑;丁—→乙:CuO+2HCl===CuCl2+H2O,D符合题意。
1
2
3
4
5
6
7
8
9
解析 物质B与A发生中和反应,则B为酸或碱,又由于B与C可发生置换反应,可判断B为HCl(稀)。
1
2
3
4
5
6
7
8
9
6.现有A、B、C、D四种物质,它们分别是Fe、HCl(稀)、NaOH(溶液)、AgNO3(溶液)四种物质中的一种,它们之间的反应关系及所发生反应的反应类型如图:
则物质B为
A.Fe
B.HCl(稀)
C.NaOH(溶液)
D.AgNO3(溶液)
√
7.对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
1
2
3
4
5
6
7
8
9
?
X牙膏
Y牙膏
摩擦剂
碳酸钙
二氧化硅
摩擦剂的物质类别
(指酸、碱、盐、氧化物)
?
?
解析 碳酸钙属于盐,二氧化硅属于氧化物。
盐
氧化物
(2)根据你的推测,牙膏摩擦剂在水中的溶解性是______(填“易溶”或“难溶”)。
1
2
3
4
5
6
7
8
9
解析 摩擦剂的作用是除去牙齿上残留的食物,联系日常生活中用砂纸来摩擦金属以除去金属表面的锈迹的事实,可知摩擦剂应为坚硬难溶的物质。
难溶
1
2
3
4
5
6
7
8
9
(3)X牙膏中的摩擦剂——碳酸钙可以用石灰石来制备。某学生设计了一种实验室制备碳酸钙的实验方案,其流程如下图所示:
请写出上述方案中有关反应的化学方程式:
①__________________________;②_____________________;
③____________________________________。
CaO+H2O===Ca(OH)2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
解析 发生的反应依次为CaCO3 CaO+CO2↑,CaO+H2O===
Ca(OH)2,Ca(OH)2+Na2CO3===CaCO3↓+2NaOH。
解析 C选项是一个容易出错的选项,因为它貌似一个置换反应,实际却不是,从化合价变化来看,该反应为氧化还原反应。
题组三 化学反应的分类
8.对于下列反应的反应类型的判断不正确的是
A.CO2+H2O===H2CO3 化合反应;非氧化还原反应
B.Cu2(OH)2CO3 2CuO+CO2↑+H2O 分解反应;非氧化还原反应
C.CuO+CO Cu+CO2 置换反应;氧化还原反应
D.MgCO3+H2SO4===MgSO4+CO2↑+H2O 复分解反应;非氧化还原
反应
1
2
3
4
5
6
7
8
9
√
9.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是
1
2
3
4
5
6
7
8
9
A.Cl2+2KBr===Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O===4Fe(OH)3
D.2Na2O2+2CO2===2Na2CO3+O2(提示:Na2O2中的氧为-1价)
√
1
2
3
4
5
6
7
8
9
解析 由图可知,阴影部分所代表的化学反应不属于四种基本类型,属于氧化还原反应。
A、B、C三项分别属于置换反应、分解反应、化合反应,均不符合题意;
D项反应不属于四种基本类型中的任何一种而属于氧化还原反应(氧元素的化合价发生变化)。
1~4题是单项选择题,5~6题是不定项选择题
1.下列各组物质之间可以按下图所示关系直接转化的是
B组 综合强化练
1
2
3
4
5
6
7
8
A.Fe—→Fe2O3—→FeSO4—→Fe
B.CO—→CO2—→H2CO3—→CO
C.NaOH—→NaCl—→Na2CO3—→NaOH
D.HCl—→CuCl2—→BaCl2—→HCl
√
解析 选项A中,Fe2O3—→FeSO4不能一步实现;
选项B中,H2CO3—→CO不能一步实现;
选项C中,NaCl—→Na2CO3不能一步实现。
1
2
3
4
5
6
7
8
1
2
3
4
5
6
7
8
2.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是
A.化合、置换、分解、复分解 B.置换、复分解、化合、分解
C.置换、化合、分解、复分解 D.置换、化合、复分解、分解
√
3.下列变化,能通过加盐酸一步反应实现的是
①AgNO3→HNO3 ②Fe2O3→FeCl2 ③Cu→CuCl2 ④Cu(OH)2→CuCl2 ⑤Fe→FeCl3
A.①② B.②④ C.①④ D.③⑤
√
1
2
3
4
5
6
7
8
1
2
3
4
5
6
7
8
下列说法不正确的是
A.铜绿属于碱 B.乙为氧化铜
C.④为分解反应和非氧化还原反应 D.⑤为置换反应和氧化还原反应
4.铜器久置于空气中会和空气中的水蒸气、二氧化碳、氧气作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”(碱式碳酸铜),“铜绿”能跟酸反应生成铜盐、二氧化碳和水。某同学利用下述系列反应实现了“铜―→铜绿―→……―→铜”的转化。
√
1
2
3
4
5
6
7
8
解析 铜绿(碱式碳酸铜)属于盐而不是碱;反应④为Cu(OH)2 CuO
+H2O,属于分解反应同时属于非氧化还原反应,反应⑤为CuO+H2
Cu+H2O,属于置换反应同时属于氧化还原反应,选项 B、C、D正确。
1
2
3
4
5
6
7
8
5.将稀硫酸、硫酸铜溶液、氯化镁溶液、氢氧化钡溶液两两混合,最多能发生的反应个数及生成沉淀的种类数分别为
A.2、2 B.2、3 C.3、3 D.3、2
√
解析 稀硫酸与氢氧化钡溶液反应可生成硫酸钡沉淀;硫酸铜溶液与氢氧化钡溶液反应可生成氢氧化铜沉淀和硫酸钡沉淀;氯化镁溶液与氢氧化钡溶液反应可生成氢氧化镁沉淀,故这四种溶液两两混合最多能发生3个反应,并生成3种沉淀,C项符合题意。
6.将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是
A.银、二氧化硫、硫酸、烧碱、氯化钠
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
√
1
2
3
4
5
6
7
8
解析 选项B中的碘酒为混合物,硫酸氢钠属于盐而不属于酸;
选项D中的石灰水为混合物。
√
(2)B除了制取A之外的另一种用途是________________________________
__________。
(3)C和E反应的化学方程式为_____________________。
(4)这五种物质之间两两发生反应,其中没有涉及的基本反应类型是___________________。
1
2
3
4
5
6
7
8
7.如图五角星上排列的A、B、C、D、E五种物质均为中学化学中常见的化合物,相互之间的连线表示两种物质能发生化学反应。A、C、E均为氧化物,A是人体呼出的气体之一;在实验室中B可以用来制取A,而D可以用来检验A;C和E反应能生成D。
(1)写出下列物质的化学式:A_____,D________。
CO2
Ca(OH)2
用于金属表面除锈(制造药物、可帮
CaO+H2O===Ca(OH)2
助消化等)
分解反应和置换反应
1
2
3
4
5
6
7
8
8.如图,A、B、C、D、E各代表水、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请回答下列问题:
(1)写出下列物质的化学式:
A_____,B_______,D_____。
Fe
CuSO4
CO2
1
2
3
4
5
6
7
8
解析 题给五种物质中,常温下水只能与二氧化碳发生化合反应生成碳酸;铁只能与硫酸铜溶液发生置换反应生成铜和硫酸亚铁;二氧化碳与水和氢氧化钡溶液均能发生反应;硫酸铜溶液除能与铁反应外,还能与氢氧化钡发生复分解反应生成氢氧化铜和硫酸钡沉淀,故C为氢氧化钡,B的相对分子质量大于D,则B为硫酸铜,D为二氧化碳,A为铁,E为水。
(2)写出下列反应的化学方程式:
B+C:______________________________________。
(3)相连环物质间发生的反应中,置换反应共有____个。
1
2
3
4
5
6
7
8
返回
CuSO4+Ba(OH)2===Cu(OH)2↓+BaSO4↓
1
解析 根据以上分析可知,只有A与B的反应为置换反应。
本课结束
1.能根据不同标准对物质进行分类。
2.能根据化合价变化判断氧化还原反应和非氧化还原反应。
3.初步认识研究物质通性及相关转化的思路和方法。
4.促进宏观辨识与微观探析核心素养发展。
核心素养发展目标
一、物质的分类
随堂演练 知识落实
课时对点练
二、物质的转化
内
容
索
引
三、化学反应的分类
1.分类法简介
分类是指按照_____、_____或_____分别归类。利用事物间的_______,把某些具有_______或_________的事物归为一类,通常可根据事物的_________或事物的_________来进行分类。
2.物质的分类方法
(1)根据物质的存在状态:分为_____物质、_____物质、_____物质。
(2)根据物质的导电性:分为_____、_______、_______。
(3)根据物质在水中的溶解性:分为_______物质、_______物质、______物质。
一、物质的分类
种类
等级
性质
相似性
共同点
相似特征
外部特征
本质特征
固态
液态
气态
导体
半导体
绝缘体
可溶性
微溶性
难溶性
3.常见物质的分类
混合物
物质
纯净物
化合物
单质
金属单质
非金属单质
无机化合物
酸(含氧酸和无氧酸等)
碱(可溶性碱和难溶性碱等)
盐(正盐、酸式盐、碱式盐等)
氧化物(酸性氧化物、碱性氧
化物等)
有机化合物
(1)对于同一物质,分类标准不同,物质类别也不同。
如NaHSO4既属于盐、钠盐、酸式盐,又属于含氧酸盐等。
(2)依据组成和性质判断物质的类别时应注意:
①纯碱(Na2CO3)不属于碱,属于盐。
②结晶水合物如CuSO4·5H2O等为纯净物。
③只含有一种元素的物质可能是纯净物,也可能是混合物。
归纳总结
(1)K2CO3是钾盐,也是碳酸盐( )
(2)Na2CO3含有氧元素,所以属于氧化物( )
(3)SO3既是非金属氧化物,又是酸性氧化物( )
(4)相同种类元素可以形成不同的化合物( )
(5)非金属氧化物一定是酸性氧化物( )
(6)金属氧化物一定是碱性氧化物( )
判断正误
√
×
√
√
×
×
1.将不同的物质与它们所属的类别进行连线。
应用体验
2.下列每组中都有一种物质与其他物质在分类上不同,试分析每组物质的组成规律。将这种不同于其他物质的物质找出来(分类标准合理即可)。
(1)NaCl、KCl、NaClO、MgCl2________。
(2)HClO3、KClO3、Cl2、NaClO3_______。
(3)H3PO4、HNO3、HCl、H2SO4________。
(4)空气、N2、氯化氢气体、CuSO4·5H2O____________________。
(5)铜、金、汞、钠________。
NaClO
Cl2
HCl
空气(或CuSO4·5H2O)
钠(或汞)
返回
二、物质的转化
1.通过物质分类,可以建立物质间的从属关系,分析物质间的本质区别和联系,寻找各类物质之间的转化关系。
(1)以钙为例,用化学方程式表示钙及其化合物之间的转化关系。
①_________________;
②______________________;
③____________________;
④______________________________;
⑤______________________________;
⑥__________________________________。
2Ca+O2===2CaO
CaO+H2O===Ca(OH)2
CaO+CO2===CaCO3
Ca(OH)2+CO2===CaCO3↓+H2O
Ca(OH)2+2HCl===CaCl2+2H2O
CaCO3+2HCl===CaCl2+CO2↑+H2O
①_______________;
②___________________;
③___________________;
④_______________________________;
⑤__________________________________。
(2)碳及其化合物间的转化关系如图所示:
各步化学方程式:
CO2+H2O===H2CO3
CO2+CaO===CaCO3
CO2+Ca(OH)2===CaCO3↓+H2O
H2CO3+Ca(OH)2===CaCO3↓+2H2O
(1)可用Fe2O3与H2O反应制取Fe(OH)3( )
(2)只有利用酸碱中和反应才能生成盐( )
(3)根据酸的通性,酸能和所有的金属反应( )
(4)并不是所有的酸和盐都能发生反应( )
(5)CaCO3和H2SO4可以反应,因此实验室可以用大理石和稀硫酸制二氧化碳( )
判断正误
×
×
×
√
×
选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转化用化学方程式表示(所写化学方程式不得重复)。
应用体验
① ;
②CO2+H2O===H2CO3;
③______________________________;
④_______________________;
CO2+Ca(OH)2===CaCO3↓+H2O
Fe+2HCl===FeCl2+H2↑
⑤_________________________;
⑥______________________________;
⑦_____________________。
CaO+2HCl===CaCl2+H2O
Ca(OH)2+2HCl===CaCl2+2H2O
CaO+H2O===Ca(OH)2
解析 属于同一类的物质必定符合同一标准,就会有某一共同的性质,利用一类物质和另一类物质之间的关系,就可以找出物质之间转化的方法,一般有以下化学通性:
物质之间的转化关系
返回
归纳总结
单质、氧化物、酸、碱、盐之间的转化关系图示如下:
1.化学反应的分类及其依据
三、化学反应的分类
2.判断化学反应类型
(1)请指出下列各反应的四种基本反应类型:
①2NO+O2===2NO2 _________
②CO2+CaO===CaCO3 _________
③NH4HCO3 NH3↑+CO2↑+H2O _________
④2KClO3 2KCl+3O2↑ _________
⑤Fe+2HCl===FeCl2+H2↑ _________
⑥Zn+CuSO4===ZnSO4+Cu _________
⑦HCl+KOH===KCl+H2O ___________
⑧BaCl2+Na2SO4===BaSO4↓+2NaCl ___________
(2)上述各反应属于氧化还原反应的是__________(填序号)。
化合反应
化合反应
分解反应
分解反应
置换反应
置换反应
复分解反应
复分解反应
①④⑤⑥
(1)氧化还原反应中一定有氧元素的得失( )
(2)氧化还原反应中所有元素化合价都一定发生变化( )
(3)有单质参加的一定是氧化还原反应( )
(4)置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应
( )
(5)化合反应与分解反应可能是氧化还原反应,也可能是非氧化还原反应
( )
判断正误
×
×
×
√
√
化学反应按照不同的分类方法可以分为化合反应、分解反应、置换反应、复分解反应,也可以分为氧化还原反应和非氧化还原反应。回答下列问题:
应用体验
⑤Na2SO4+BaCl2===2NaCl+BaSO4↓ ⑥H2O2+H2S===S↓+2H2O
(1)既是氧化还原反应又是化合反应的为______(填序号,下同)。
(2)属于非氧化还原反应的为____。
(3)不属于四种基本反应类型的为____。
(4)属于置换反应的为____。
①②
⑤
⑥
③
氧化还原反应与四种基本反应类型之间的关系
返回
归纳总结
1
2
3
5
随堂演练 知识落实
4
1.对下列物质分类全部正确的是
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
A.碱:①④ B.纯净物:①③④⑤⑥
C.盐:①⑥ D.混合物:②③⑤
√
解析 纯碱是Na2CO3,属于盐,A项错误;
石灰水是混合物,B项错误;
液态氧是纯净物,D项错误。
6
2.国家质检部门检验出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种
A.氧化物 B.盐 C.碱 D.酸
1
2
3
5
4
解析 胆矾、绿矾等结晶水合物都属于盐,为纯净物。
√
6
解析 CO2、SO2属于酸性氧化物,CaCO3、KMnO4属于盐,CuO属于碱性氧化物。
3.根据某种共性,可将CO2、SO2归为一类氧化物,下列物质中与它们属于同一类的是
A.CaCO3 B.P2O5 C.CuO D.KMnO4
1
2
3
5
4
√
6
4.下列变化不能通过一步化学反应实现的是
A.BaCl2→BaSO4 B.CuO→Cu(OH)2
C.NaOH→Na2SO3 D.MgSO4→Mg(OH)2
1
2
3
5
4
解析 CuO难溶于水,不能与水反应。
√
6
5.下列反应既是化合反应又是氧化还原反应的是
A.2CO+O2 2CO2
B.CaO+H2O===Ca(OH)2
C.C+H2O(g) CO+H2
D.CO2+Ca(OH)2===CaCO3↓+H2O
1
2
3
5
4
√
6
解析 酸可以填写H2S、H2SO4、HNO3、H2CO3等,碱可以填写KOH或NaOH等;盐可填写K2CO3、Na2SO4、NaNO3、KNO3、K2SO4等。
6.(2020·天津调研)无机化合物可根据其组成和性质进行分类。
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表中。
1
2
3
5
4
6
物质类别
酸
碱
盐
氧化物
化学式
①HCl
②________
_________
③_________
_________
④Ba(OH)2
⑤Na2CO3
⑥_______________
___________________
⑦CO2
⑧Na2O
H2SO4(或
HNO3等)
NaOH(或
KOH等)
Na2SO4(或K2CO3
或Na2SO3或NaNO3等)
(2)写出⑦转化为⑤的化学方程式:_____________________________。
1
2
3
5
4
6
2NaOH+CO2===Na2CO3+H2O
(3)实验室制备⑦常用________和________反应,检验该气体的方法是______________________________________________。
稀盐酸
碳酸钙
将气体通入澄清石灰水中,若变浑浊,即证明是CO2
解析 CO2是酸性氧化物,可与NaOH反应生成Na2CO3和H2O。
解析 实验室常用CaCO3和稀盐酸反应制取CO2,产生的CO2气体可用澄清石灰水来检验。
返回
解析 煤是含有碳、硫等多种物质构成的混合物;生铁是由铁和碳组成的混合物;矿泉水中除含有水外,还有其他多种矿物质,是混合物。
课时对点练
1
2
3
4
5
6
7
8
9
题组一 物质的分类
1.(2019·河南龙泉中学月考)下列物质是生活中经常用到的物质,其中属于纯净物的是
A.煤 B.生铁 C.蒸馏水 D.矿泉水
√
A组 基础对点练
2.(2019·湖南株洲四中期末)分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可采取多种分类方法。下列各组归类不合理的是
1
2
3
4
5
6
7
8
9
选项
按某一分类标准分类的物质或变化
归类
A
FeSO4、NO2、MnO2、NaClO
H2SO3
B
CH3COOH、HClO、H2S、H2CO3
HF
C
氢气燃烧、氧化钙变质、食物腐烂
冰雪融化
D
(NH4)2SO4、NH4Cl、NH4NO3、NH3·H2O
NH4HCO3
√
解析 A项中物质均为含氧化合物;
B项中物质均属于酸;
C项中氢气燃烧、氧化钙变质、食物腐烂均为化学变化,而冰雪融化属于物理变化;
D项中物质均为含氮化合物。
1
2
3
4
5
6
7
8
9
3.(2019·福建厦门六中期中)下列关于物质分类的组合正确的是
1
2
3
4
5
6
7
8
9
选项
碱
酸
盐
碱性氧化物
酸性氧化物
A
Ca(OH)2
硫酸
小苏打
Mn2O7
干冰
B
烧碱
盐酸
氯化钠
氧化钠
一氧化碳
C
石灰水
冰醋酸(CH3COOH)
胆矾(CuSO4·5H2O)
氧化钠
二氧化硫
D
NaOH
HNO3
碳酸钙
氧化铁
SO3
√
解析 Mn2O7为酸性氧化物,A项错误;
盐酸是氯化氢的水溶液,为混合物,一氧化碳是不成盐氧化物,不属于酸性氧化物,B项错误;
石灰水是氢氧化钙与水的混合物,而碱为纯净物,C项错误。
1
2
3
4
5
6
7
8
9
解析 A项中Fe与盐酸反应生成FeCl2;
B项中H2O2分解生成H2O和O2;
C项中CaCl2和CO2不反应。
题组二 物质的转化
4.下列物质在给定条件下的转化均能一步实现的是
1
2
3
4
5
6
7
8
9
√
5.(2019·唐山高一检测)如图所示,“——”表示相连的物质间在一定条件下可以反应,“—→”表示丁在一定条件下可以转化为乙。下面四组选项中,符合图示要求的是
1
2
3
4
5
6
7
8
9
?
甲
乙
丙
丁
A
H2SO4
Na2SO4
NaOH
NaCl
B
KCl
K2CO3
KOH
HCl
C
O2
CO
C
CuO
D
Fe
CuCl2
Zn
HCl
√
解析 A中甲和乙、乙和丙、丙和丁、丁和甲均不能反应,丁也不能转化为乙;B中甲和乙、乙和丙、丁和甲之间均不能反应,丁也不能转化为乙,故A、B不符合题意;
1
2
3
4
5
6
7
8
9
D中反应依次为甲和乙:Fe+CuCl2===FeCl2+Cu;乙和丙:Zn+CuCl2===Cu+ZnCl2;丙和丁:Zn+2HCl===ZnCl2+H2↑;丁和甲:Fe+2HCl===FeCl2+H2↑;丁—→乙:CuO+2HCl===CuCl2+H2O,D符合题意。
1
2
3
4
5
6
7
8
9
解析 物质B与A发生中和反应,则B为酸或碱,又由于B与C可发生置换反应,可判断B为HCl(稀)。
1
2
3
4
5
6
7
8
9
6.现有A、B、C、D四种物质,它们分别是Fe、HCl(稀)、NaOH(溶液)、AgNO3(溶液)四种物质中的一种,它们之间的反应关系及所发生反应的反应类型如图:
则物质B为
A.Fe
B.HCl(稀)
C.NaOH(溶液)
D.AgNO3(溶液)
√
7.对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
1
2
3
4
5
6
7
8
9
?
X牙膏
Y牙膏
摩擦剂
碳酸钙
二氧化硅
摩擦剂的物质类别
(指酸、碱、盐、氧化物)
?
?
解析 碳酸钙属于盐,二氧化硅属于氧化物。
盐
氧化物
(2)根据你的推测,牙膏摩擦剂在水中的溶解性是______(填“易溶”或“难溶”)。
1
2
3
4
5
6
7
8
9
解析 摩擦剂的作用是除去牙齿上残留的食物,联系日常生活中用砂纸来摩擦金属以除去金属表面的锈迹的事实,可知摩擦剂应为坚硬难溶的物质。
难溶
1
2
3
4
5
6
7
8
9
(3)X牙膏中的摩擦剂——碳酸钙可以用石灰石来制备。某学生设计了一种实验室制备碳酸钙的实验方案,其流程如下图所示:
请写出上述方案中有关反应的化学方程式:
①__________________________;②_____________________;
③____________________________________。
CaO+H2O===Ca(OH)2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
解析 发生的反应依次为CaCO3 CaO+CO2↑,CaO+H2O===
Ca(OH)2,Ca(OH)2+Na2CO3===CaCO3↓+2NaOH。
解析 C选项是一个容易出错的选项,因为它貌似一个置换反应,实际却不是,从化合价变化来看,该反应为氧化还原反应。
题组三 化学反应的分类
8.对于下列反应的反应类型的判断不正确的是
A.CO2+H2O===H2CO3 化合反应;非氧化还原反应
B.Cu2(OH)2CO3 2CuO+CO2↑+H2O 分解反应;非氧化还原反应
C.CuO+CO Cu+CO2 置换反应;氧化还原反应
D.MgCO3+H2SO4===MgSO4+CO2↑+H2O 复分解反应;非氧化还原
反应
1
2
3
4
5
6
7
8
9
√
9.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是
1
2
3
4
5
6
7
8
9
A.Cl2+2KBr===Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O===4Fe(OH)3
D.2Na2O2+2CO2===2Na2CO3+O2(提示:Na2O2中的氧为-1价)
√
1
2
3
4
5
6
7
8
9
解析 由图可知,阴影部分所代表的化学反应不属于四种基本类型,属于氧化还原反应。
A、B、C三项分别属于置换反应、分解反应、化合反应,均不符合题意;
D项反应不属于四种基本类型中的任何一种而属于氧化还原反应(氧元素的化合价发生变化)。
1~4题是单项选择题,5~6题是不定项选择题
1.下列各组物质之间可以按下图所示关系直接转化的是
B组 综合强化练
1
2
3
4
5
6
7
8
A.Fe—→Fe2O3—→FeSO4—→Fe
B.CO—→CO2—→H2CO3—→CO
C.NaOH—→NaCl—→Na2CO3—→NaOH
D.HCl—→CuCl2—→BaCl2—→HCl
√
解析 选项A中,Fe2O3—→FeSO4不能一步实现;
选项B中,H2CO3—→CO不能一步实现;
选项C中,NaCl—→Na2CO3不能一步实现。
1
2
3
4
5
6
7
8
1
2
3
4
5
6
7
8
2.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是
A.化合、置换、分解、复分解 B.置换、复分解、化合、分解
C.置换、化合、分解、复分解 D.置换、化合、复分解、分解
√
3.下列变化,能通过加盐酸一步反应实现的是
①AgNO3→HNO3 ②Fe2O3→FeCl2 ③Cu→CuCl2 ④Cu(OH)2→CuCl2 ⑤Fe→FeCl3
A.①② B.②④ C.①④ D.③⑤
√
1
2
3
4
5
6
7
8
1
2
3
4
5
6
7
8
下列说法不正确的是
A.铜绿属于碱 B.乙为氧化铜
C.④为分解反应和非氧化还原反应 D.⑤为置换反应和氧化还原反应
4.铜器久置于空气中会和空气中的水蒸气、二氧化碳、氧气作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”(碱式碳酸铜),“铜绿”能跟酸反应生成铜盐、二氧化碳和水。某同学利用下述系列反应实现了“铜―→铜绿―→……―→铜”的转化。
√
1
2
3
4
5
6
7
8
解析 铜绿(碱式碳酸铜)属于盐而不是碱;反应④为Cu(OH)2 CuO
+H2O,属于分解反应同时属于非氧化还原反应,反应⑤为CuO+H2
Cu+H2O,属于置换反应同时属于氧化还原反应,选项 B、C、D正确。
1
2
3
4
5
6
7
8
5.将稀硫酸、硫酸铜溶液、氯化镁溶液、氢氧化钡溶液两两混合,最多能发生的反应个数及生成沉淀的种类数分别为
A.2、2 B.2、3 C.3、3 D.3、2
√
解析 稀硫酸与氢氧化钡溶液反应可生成硫酸钡沉淀;硫酸铜溶液与氢氧化钡溶液反应可生成氢氧化铜沉淀和硫酸钡沉淀;氯化镁溶液与氢氧化钡溶液反应可生成氢氧化镁沉淀,故这四种溶液两两混合最多能发生3个反应,并生成3种沉淀,C项符合题意。
6.将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是
A.银、二氧化硫、硫酸、烧碱、氯化钠
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
√
1
2
3
4
5
6
7
8
解析 选项B中的碘酒为混合物,硫酸氢钠属于盐而不属于酸;
选项D中的石灰水为混合物。
√
(2)B除了制取A之外的另一种用途是________________________________
__________。
(3)C和E反应的化学方程式为_____________________。
(4)这五种物质之间两两发生反应,其中没有涉及的基本反应类型是___________________。
1
2
3
4
5
6
7
8
7.如图五角星上排列的A、B、C、D、E五种物质均为中学化学中常见的化合物,相互之间的连线表示两种物质能发生化学反应。A、C、E均为氧化物,A是人体呼出的气体之一;在实验室中B可以用来制取A,而D可以用来检验A;C和E反应能生成D。
(1)写出下列物质的化学式:A_____,D________。
CO2
Ca(OH)2
用于金属表面除锈(制造药物、可帮
CaO+H2O===Ca(OH)2
助消化等)
分解反应和置换反应
1
2
3
4
5
6
7
8
8.如图,A、B、C、D、E各代表水、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请回答下列问题:
(1)写出下列物质的化学式:
A_____,B_______,D_____。
Fe
CuSO4
CO2
1
2
3
4
5
6
7
8
解析 题给五种物质中,常温下水只能与二氧化碳发生化合反应生成碳酸;铁只能与硫酸铜溶液发生置换反应生成铜和硫酸亚铁;二氧化碳与水和氢氧化钡溶液均能发生反应;硫酸铜溶液除能与铁反应外,还能与氢氧化钡发生复分解反应生成氢氧化铜和硫酸钡沉淀,故C为氢氧化钡,B的相对分子质量大于D,则B为硫酸铜,D为二氧化碳,A为铁,E为水。
(2)写出下列反应的化学方程式:
B+C:______________________________________。
(3)相连环物质间发生的反应中,置换反应共有____个。
1
2
3
4
5
6
7
8
返回
CuSO4+Ba(OH)2===Cu(OH)2↓+BaSO4↓
1
解析 根据以上分析可知,只有A与B的反应为置换反应。
本课结束
