2021-2022学年鲁教版(五四制)九年级上学期开学摸底考试化学试卷B卷(含解析)
文档属性
| 名称 | 2021-2022学年鲁教版(五四制)九年级上学期开学摸底考试化学试卷B卷(含解析) |  | |
| 格式 | zip | ||
| 文件大小 | 308.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-20 17:18:08 | ||
图片预览




文档简介
2021-2022学年鲁教版(五四制)
九年级上学期开学摸底考试化学试卷B卷
满分:100分
可能用到的相对原子质量:H—1
C—12
O—16
Ca—40
一、选择题(本大题共18小题,每小题2分,共36分)
1.下列各组物质中,都由分子构成的一组是(
)。
A.金和金刚石
B.水和氨气
C.汞和氯化钠
D.干冰和硫酸铜
2.臭氧()能杀死细菌,可用作消毒杀菌剂。臭氧属于(
)。
A.纯净物
B.混合物
C.氧气
D.稀有气体
3.下列图示实验操作中,正确的是( )
A.
B.
C.
D.
4.从《中国成语大会》到《中国诗词大会》,中国传统文化大放异彩,很多成语、诗词中蕴含着丰富的科学道理。下列叙述错误的是(
)
A.“百炼成钢”与“沙里淘金”所涉及的变化相同
B.“一畦春韭绿,十里稻花香”是因为分子在不断地运动
C.“真金不怕火炼”说明黄金的化学性质非常稳定
D.“釜底抽薪”与“钻木取火”都体现了燃烧的条件
5.下列事实不能作为相应观点的证据的是(
)
A.尘土飞扬,说明分子是运动的
B.电解水得到氢气和氧气,说明分子是可分的
C.气体被压缩后体积发生了较大变化,说明气体分子间的距离大
D.将两个干净平整的铅柱紧压在一起会结合起来,说明分子间存在引力
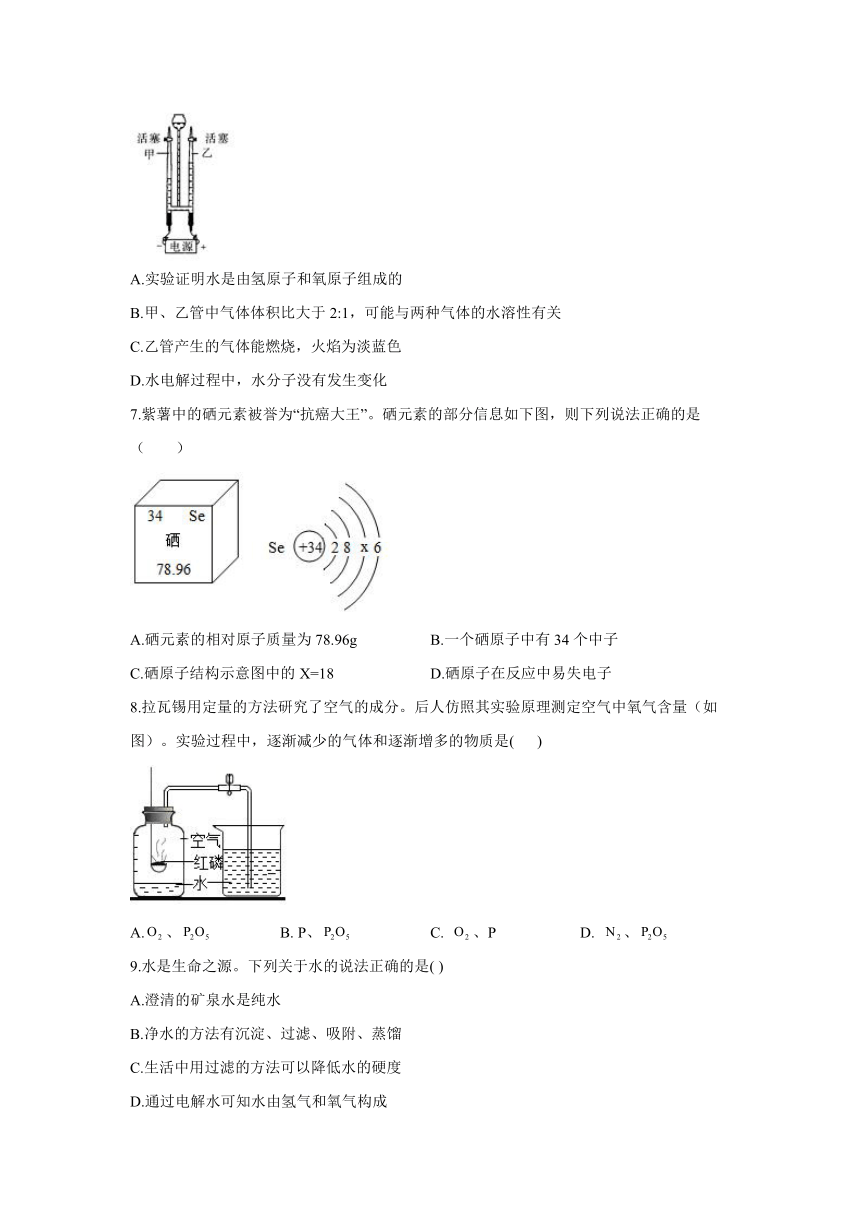
6.下列有关水电解实验的说法正确的是(
)。
A.实验证明水是由氢原子和氧原子组成的
B.甲、乙管中气体体积比大于2:1,可能与两种气体的水溶性有关
C.乙管产生的气体能燃烧,火焰为淡蓝色
D.水电解过程中,水分子没有发生变化
7.紫薯中的硒元素被誉为“抗癌大王”。硒元素的部分信息如下图,则下列说法正确的是( )
A.硒元素的相对原子质量为78.96g
B.一个硒原子中有34个中子
C.硒原子结构示意图中的X=18
D.硒原子在反应中易失电子
8.拉瓦锡用定量的方法研究了空气的成分。后人仿照其实验原理测定空气中氧气含量(如图)。实验过程中,逐渐减少的气体和逐渐增多的物质是(
)
A.、
B.
P、
C.
、P
D.
、
9.水是生命之源。下列关于水的说法正确的是(
)
A.澄清的矿泉水是纯水
B.净水的方法有沉淀、过滤、吸附、蒸馏
C.生活中用过滤的方法可以降低水的硬度
D.通过电解水可知水由氢气和氧气构成
10.空气是人类生产活动的重要资源。下列生活和生产中用到的气体不是来自空气的是(
)
A.炼钢过程用到的氧气
B.磁悬浮列车用到的氮气
C.用于生产氮肥的氨气
D.制作电光源的稀有气体
11.鱼能在水中生存的原因是(
)
A.水的组成中含有氧元素
B.常温下水是液体
C.水能分解放出氧气
D.水中溶解有一定量的氧气
12.生活中应用缓慢氧化的实例很多,下列反应中不属于缓慢氧化的是(
)
A.酒和醋的酿造
B.农家肥料的腐熟
C.酒精灯平稳燃烧
D.人在长跑时急促呼吸
13.下列说法中正确的是(
)
A.根据质量守恒定律,1L氢气和1L氧气反应能生成2L水
B.只有固体、液体间的反应遵循质量守恒定律,如果有气体参加,就不遵循了
C.镁条在空气中燃烧,生成物的总质量比原来镁条的质量大
D.水结冰后质量没有改变,由此说明化学变化遵循质量守恒定律
14.“火折子”被称为古代的打火机。火折子的主要材料为白薯蔓汁浸泡过的土纸,加以棉花、
苇絮等,晒干卷成长杆状,点燃后吹灭成暗火,装入竹筒内,需要时取出一吹就能复燃。下列关于火折子的说法错误的是
(
)
A.土纸棉花等都是可燃物
B.装入竹筒后火折子没有完全熄灭
C.竹筒不是完全密闭的
D.取出一吹即可复燃是因为降低了着火点
15.下列关于燃料的说法中,正确的是(
)
A.石油是纯净物
B.煤、石油、天然气和酒精都是化石燃料
C.煤和石油的燃烧会造成空气污染
D.只有通过燃料的燃烧才能获得热能
16.将充满下列气体的试管倒置于水槽中(如图),一段时间后试管内的水位上升最高的是(
)
A.氧气
B.氢气
C.氮气
D.二氧化碳
17.工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可用如图所示的模型表示。下列有关甲醇的叙述中,错误的是(
)。
A.甲醇的化学式为
B.甲醇的相对分子质量为32
C.甲醇中C、H、O三种元素的质量之比为1:4:1
D.甲醇中氧元素的质量分数为50%
18.在密闭容器内,有甲、乙、丙、丁四种物质,在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示,下列说法错误的是(
)
A.丁一定是化合物
B.生成的甲、丙两物质的质量比为8:1
C.乙可能是该反应的催化剂
D.参加反应的丁的质量一定是生成甲和丙的质量之和
二、填空题(本大题共5小题,共52分)
19.(9分)在2019年年底开始,我国爆发了新冠肺炎,给国家和人民的财产带来巨大的损失,给人民的生命带来严重的威胁,全国人民在党中央的领导下众志成城抗击新冠肺炎。抗疫中用到了许多消毒剂,“84”消毒液(有效成分为次氯酸钠)和二氧化氯()是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式,其反应原理:________。
(2)二氧化氯()中氯元素的化合价为_____,二氧化氯()属于______(填字母)。
A.酸
B.碱
C.盐
D.氧化物
(3)“84”消毒液不能与洁厕灵混合使用,原因是“84”消毒液中的次氯酸钠与洁厕灵中的盐酸会发生化学反应,生成氯化钠、水和有毒气体氯气,写出该反应的化学方程式:___________________。
20.(10分)分析硫、木炭、铁丝三种物质在氧气中燃烧的实验,回答问题。
(1)铁丝燃烧时,需在铁丝下端系一根火柴,火柴所起到的作用是________。
(2)木炭在空气中燃烧发红,在氧气中燃烧更旺,发白光。硫在空气里燃烧发出淡蓝色火焰,而在氧气里燃烧得更旺,发出___火焰。木炭和硫在空气里和氧气里燃烧的现象不同,原因是_______。
(3)铁丝燃烧瓶底的水可用细沙代替,而硫不能,由此推测,具有的物理性质是_____;硫、铁丝燃烧实验中用到的氧气,最好采用______法收集。
21.(8分)火的利用推动了人类文明的进程,观察图:
选择序号回答(1)~(3):①与氧气接触,②温度达到着火点,③有可燃物。
(1)图甲所示实验现象,说明燃烧应具备的条件是________;
(2)图乙烧杯中蜡烛渐渐熄灭,说明燃烧应具备的条件是_________________;
(3)图丙铜片上白磷燃烧,红磷不燃烧,说明燃烧应具备的条件是_____________;
(4)图丙实验中所用药品的保存方法正确的是___________(选填图丁中的序号)。
22.(12分)A~H是初中常见的8种物质,它们有如图所示的转化关系。
已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会增强温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
(1)请写出下列物质的化学符号:D__________,G__________,H__________。
(2)请写出下列变化的文字表达式:
①B→F_______________________________;
②C→B_______________________________。
23.(13分)下图A~H是实验室制取某些常见气体的装置示意图。请完成下列相关问题。
(1)写出图中仪器②的名称:__________。
(2)实验室要制取一瓶干燥的氧气所选择的装置是____________(填序号)。
(3)实验室制备的化学方程式为______________,若用装置H收集气体,产生的气体应从_________(填“a”或“b”)端通入;
(4)用石灰石和稀盐酸制取二氧化碳,选取装置C或D相对于装置B在操作方面的优势为______________;若选择装置D用双氧水和二氧化锰制备氧气,能否体现该优点_________(填“能”或“否”)。
(5)用排水法与排空气法收集及相关性质的比较(分别用体积相同的2个集气瓶收集)。
已知:向收集满的集气瓶内倒入等体积适量澄清石灰水,并振荡。二氧化碳纯度越高,澄清石灰水先变浑浊后变澄清的时间越短。
比较项目
排水法
向上排空气法
收集方法可行性分析
气体生成和从水面逸出的速率远大于其溶解和与水反应的速率
Ⅰ.___,且不与空气发生反应
收集过程分析
集满现象:Ⅱ.____
“验满”分析:因气体无色,是否集满难确定,即便用燃着的木条移近容器口熄灭,也难以证明空气完全排尽
石灰水变浑浊又变澄清所需时间分析
时间较短
时间较长
由上述实验可得结论:①二氧化碳可用排水法或向上排空气法收集;②与排空气法相比,排水法的优点是___________。
三、计算题(本大题共1小题,共12分)
24.张玲同学为了测定汉白玉中碳酸钙的质量分数,称取5.55g研碎的汉白玉粉末,进行四次高温加热,反应的化学方程式为(杂质不参加反应),冷却、称量剩余固体的重复操作,记录数据如下表所示:
操作次序
第一次
第二次
第三次
第四次
剩余固体质量/g
4.25
3.95
3.35
3.35
请计算:
(1)在碳酸钙中各元素的质量比为________(最简整数比)。
(2)完全反应后生成二氧化碳_________g。
(3)求汉白玉中碳酸钙的质量分数。(精确到0.1%)
答案以及解析
1.答案:B
2.答案:A
解析:臭氧为由氧元素组成的单质,属于纯净物,A项正确。
3.答案:D
解析:A、给试管内液体加热的注意事项:试管内液体量不能超过试管容积的三分之一,图中溶液过多,手握试管夹的长柄,不能握短柄,用酒精灯的外焰加热,故选项错误;
B、胶头滴管要垂悬在试管口上方,不能伸入试管内,或与试管壁接触,故选项错误;
C、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口;图中瓶口没有紧挨试管口、瓶塞没有倒放、标签没有向手心,故选项错误;
D、酒精灯的点燃方法:用火柴点燃,不能用酒精灯引燃,容易发生火灾,故选项正确。故选D。
4.答案:A
解析:本题考查物理变化和化学变化的判断、分子的性质、金的化学性质燃烧的条件。在古代,人们把烧红的生铁放在铁砧上反复捶打,目的是让碳和氧气反应生成二氧化碳,从而降低含碳量,属于化学变化;“沙里淘金”是从沙子中分离出金,属于物理变化,A项符合题意;“一畦春韭绿,十里稻花香”,是因为稻花中含有的分子在不断地运动,向四周扩散,使人们闻到稻花香,B项不符合题意;“真金不怕火炼”意思是金即使在高温时也不与氧气反应,说明金的化学性质不活泼,C项不符合题意;“釜底抽薪”是清除可燃物灭火,“钻木取火”是使温度达到物质的着火点使其燃烧,都体现了燃烧的条件,D项不符合题意。
5.答案:A
解析:尘土飞扬是固体小颗粒的运动,不是分子的运动。
6.答案:B
解析:A.水电解实验证明水是由氢元素和氧元素组成的,不能说实验证明水是由氢原子和氧原子构成的,故A错误;B.由于氧气与氢气的水溶性有差异,氧气是不易溶于水的,氢气是难溶于水的,所以甲、乙管中气体体积比大于2:1,可能与两种气体的水溶性有关,故B正确;C.乙管内电极与电源的正极相连,产生的气体是氧气,氧气具有助燃性,但不具有可燃性,故C错误;D.水电解过程中,水分子分裂成氢原子和氧原子,氢原子和氧原子再分别构成氢分子和氧分子,所以该过程中水分子发生改变,故D错误。
7.答案:C
解析:A、硒元素的相对原子质量为78.96,单位不是“g”;故选项错误;
B、一个硒原子中有34个质子;故选项错误;
C、硒原子结构示意图中,质子数=核外电子数,34=2+8+X+6,X=18;故选项正确;
D、硒原子最外层有6个电子,在反应中易得电子;故选项错误;
故选:C。
8.答案:A
解析:磷燃烧消耗了氧气生成五氧化二磷固体,装置中压强减小,水进入装置,进入装置中水的体积就是消耗氧气的体积;燃烧过程中氮气不参与反应,故实验过程中,逐渐减少的气体和逐渐增多的物质是氧气、五氧化二磷。
故选A。
9.答案:B
解析:A、矿泉水由水、矿物质等两种以上物质混合而成,属于混合物,不符合题意;
B、净水的方法有沉淀、过滤、吸附、消毒、蒸馏等,说法正确,符合题意;
C、过滤只能除去不溶性杂质,不能降低水的硬度,不符合题意;
D、水是由水分子构成,不是由氢气和氧气构成的,不符合题意。
故选B。
10.答案:C
解析:空气中的成分按体积计算,大约是氮气78%,氧气21%,稀有气体094%,不含有氨气,故选C。
11.答案:D
解析:鱼能在水中生存是因为水中溶有的少量氧气,氧气是由氧分子构成的;与水中含有氧元素、水是液态无关,且水常温无法分解生成氧气。
故选D。
12.答案:C
解析:酒精灯的平稳燃烧是较剧烈的氧化反应,而缓慢氧化进行得很慢,甚至不易被察觉,如A、B、D三项所述的氧化反应是缓慢氧化。
13.答案:C
解析:质量守恒定律解释的物理量是质量,不是体积,A错误;有气体参加的化学反应依然遵循质量守恒定律,B错误;镁条在空气中燃烧,生成物氧化镁的质量为参加反应的镁和氧气的质量总和,C正确;水结冰是物理变化,质量守恒定律只适用于化学变化,不适用于物理变化,D错误。
14.答案:D
15.答案:C
解析:石油是由多种物质组成的,属于混合物,A错误;煤、石油、天然气属于化石燃料,酒精不属于化石燃料,B错误;煤、石油等化石燃料的燃烧能生成大量的二氧化碳,造成温室效应,而产生氧化碳、二氧化硫、氮氧化物等会造成空气污乘,C正确;燃烧、摩擦等都可以产生热能,D错误。
16.答案:D
解析:氢气和氮气难溶于水,将充满氢气或氮气的试管倒置于水槽中时,试管内的水位几乎不上升;
氧气不易溶于水,将充满氧气的试管倒置于水槽中时,试管内的水位上升较少;
二氧化碳能够溶于水,将充满二氧化碳的试管倒置于水槽中时,试管内的水位上升较多;
由以上分析可知,一段时间后试管内的水位上升最高的是充满二氧化碳的试管。
故选:D。
17.答案:C
解析:根据图中的信息可知其化学式为,也可以写成,故A正确;相对分子质量等于相对原子质量与原子个数的乘积的总和。的相对分子质量=,故B正确;元素的质量比等于相对原子质量与原子个数的乘积的比值,中碳、氢、氧三种元素的质量比=,故C错误;物质中某种元素的质量分数=。所以甲醇中氧元素的质量分数=,故D正确。
18.答案:B
解析:反应前后容器中物质的总质量不变,反应后质量分数减小的物质是反应物,质量分数增大的物质是生成物,由图中物质的质量分数的变化可知,丁的质量分数减小,是反应物;甲、丙物质的质量分数增大,是生成物,而乙物质的质量分数不变,可能是催化剂。该反应为:丁→甲+丙,丁一定是化合物,A正确;生成的甲、丙两物质的质量比为2:16=1:8,B错误;乙物质的质量分数不变,可能是催化剂,C正确;参加反应的丁的质量一定是生成甲和丙的质量之和,D正确。
19.答案:(1)NaClO
(2)+4
;D
(3)
解析:(1)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式可知,反应前氯、钠、氧、氢的原子个数分别为2、2、2、2,反应后的生成物中氯、钠、氧、氢的原子个数分别为1、1、1、2,根据反应前后原子种类、数目不变,则每个分子由1个钠原子、1个氯原子和1个氧原子构成,则该物质的化学式为NaClO。
(2)氧元素显-2价,设氯元素的化合价是,根据在化合物中各元素的正负化合价代数和为零,可得:,则。二氧化氯是由两种元素组成的且有一种是氧元素的化合物,属于氧化物。
(3)次氯酸钠与洁厕灵中的盐酸会发生化学反应,生成氯化钠、水和有毒气体氯气,反应的化学方程式为。
20.答案:(1)引燃铁丝(2)蓝紫色;氧气浓度(或含量)不同(3)能(或可、易)溶于水;排水
解析:
(1)铁丝的一端系一根火柴并点燃可以给铁丝预热,提高铁丝温度,有利于铁丝燃烧,起引燃作用,故填引燃铁丝。
(2)硫在空气里燃烧发出淡蓝色火焰,而在氧气里燃烧得更旺,发出蓝紫色的火焰,故填蓝紫色;
木炭和硫分别在空气里和氧气里燃烧的现象不同,说明了可燃物燃烧时与氧气的浓度有关,浓度越大燃烧越剧烈,故填氧气浓度(或含量)不同。
(3)燃烧硫实验中,集气瓶底部只能装少量水不能装细沙,是因为二氧化硫易溶于水,用水吸收二氧化硫,可以防止空气污染,故填能(或可、易)溶于水。
用排水法收集到的氧气比较纯净,且瓶中还要留一些水,最好采用排水法收集氧气,故填排水。
21.答案:(1)③
(2)①
(3)②
(4)AB
解析:(1)图甲所示实验中小木块能燃烧,玻璃块不能燃烧,说明燃烧应具备的条件是有可燃物。
(2)图乙中,烧杯将蜡烛与外界氧气隔绝,所以烧杯中蜡烛渐渐熄灭,说明燃烧应具备的条件是与氧气接触。
(3)图丙铜片上白磷燃烧,红磷不燃烧,说明燃烧应具备的条件是温度达到着火点。
(4)由于白磷的着火点低易自燃,应保存在冷水中,红磷的着火点较高,可密封保存在广口瓶中,所以保存方法正确的是AB。
22.答案:(1)
(2)①②
解析:(1)A、C是无色液体,B、F、G是无色气体,D是黑色固体,其中大量排放F会增强温室效应,则F为二氧化碳;过氧化氢和水均为无色液体,过氧化氢在二氧化锰的催化作用下生成水和氧气,碳是一种黑色固体,在氧气中燃烧生成二氧化碳,则A为过氧化氢,B为氧气,C为水,D为碳;E在纯净的B中燃烧发出明亮的蓝紫色火焰,则E为硫,G为二氧化硫;水通电分解生成氢气和氧气,则H为氢气。(2)①B→F,即碳在氧气中燃烧生成二氧化碳;②C→B,即水通电分解生成氢气和氧气。
23.答案:(1)水槽
(2)AG(或AH)
(3);a
(4)可以控制反应的发生和停止(或随开随用,随关随停);否
(5)Ⅰ.密度比空气大;Ⅱ.集气瓶口有气泡冒出②收集到的气体更纯净
解析:(1)②为水槽。
(2)制取氧气可以选择固体加热型发生装置,也可以选择固液常温型发生装置,但是要制取干燥气体,只能选择固体加热型发生装置A;收集氧气可以用排水法或者向上排空气法,排水法收集的气体不干燥,所以选择G或H为收集装置。
(3)盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,化学方程式为;二氧化碳密度比空气大,所以从a端进气。
(4)C或D可通过控制固液接触和分离,从而控制反应的发生和停止;二氧化锰为固体粉末,实现不了固液分离,所以不能体现C或D的优点。
(5)二氧化碳密度比空气大,并且不与空气反应,故可采用向上排空气法收集;排水法收集气体时,集气瓶内集满气体后,气体逸出集气瓶,形成气泡;根据澄清石灰水变浑浊又变澄清所需的时间,可以推测出排水法收集的二氧化碳纯度高。
24.答案:(1)10:3:12(2)2.2(3)设汉白玉中碳酸钙的质量分数为x,则
解得x≈90.1%。
答:汉白玉中碳酸钙的质量分数为90.1%。
九年级上学期开学摸底考试化学试卷B卷
满分:100分
可能用到的相对原子质量:H—1
C—12
O—16
Ca—40
一、选择题(本大题共18小题,每小题2分,共36分)
1.下列各组物质中,都由分子构成的一组是(
)。
A.金和金刚石
B.水和氨气
C.汞和氯化钠
D.干冰和硫酸铜
2.臭氧()能杀死细菌,可用作消毒杀菌剂。臭氧属于(
)。
A.纯净物
B.混合物
C.氧气
D.稀有气体
3.下列图示实验操作中,正确的是( )
A.
B.
C.
D.
4.从《中国成语大会》到《中国诗词大会》,中国传统文化大放异彩,很多成语、诗词中蕴含着丰富的科学道理。下列叙述错误的是(
)
A.“百炼成钢”与“沙里淘金”所涉及的变化相同
B.“一畦春韭绿,十里稻花香”是因为分子在不断地运动
C.“真金不怕火炼”说明黄金的化学性质非常稳定
D.“釜底抽薪”与“钻木取火”都体现了燃烧的条件
5.下列事实不能作为相应观点的证据的是(
)
A.尘土飞扬,说明分子是运动的
B.电解水得到氢气和氧气,说明分子是可分的
C.气体被压缩后体积发生了较大变化,说明气体分子间的距离大
D.将两个干净平整的铅柱紧压在一起会结合起来,说明分子间存在引力
6.下列有关水电解实验的说法正确的是(
)。
A.实验证明水是由氢原子和氧原子组成的
B.甲、乙管中气体体积比大于2:1,可能与两种气体的水溶性有关
C.乙管产生的气体能燃烧,火焰为淡蓝色
D.水电解过程中,水分子没有发生变化
7.紫薯中的硒元素被誉为“抗癌大王”。硒元素的部分信息如下图,则下列说法正确的是( )
A.硒元素的相对原子质量为78.96g
B.一个硒原子中有34个中子
C.硒原子结构示意图中的X=18
D.硒原子在反应中易失电子
8.拉瓦锡用定量的方法研究了空气的成分。后人仿照其实验原理测定空气中氧气含量(如图)。实验过程中,逐渐减少的气体和逐渐增多的物质是(
)
A.、
B.
P、
C.
、P
D.
、
9.水是生命之源。下列关于水的说法正确的是(
)
A.澄清的矿泉水是纯水
B.净水的方法有沉淀、过滤、吸附、蒸馏
C.生活中用过滤的方法可以降低水的硬度
D.通过电解水可知水由氢气和氧气构成
10.空气是人类生产活动的重要资源。下列生活和生产中用到的气体不是来自空气的是(
)
A.炼钢过程用到的氧气
B.磁悬浮列车用到的氮气
C.用于生产氮肥的氨气
D.制作电光源的稀有气体
11.鱼能在水中生存的原因是(
)
A.水的组成中含有氧元素
B.常温下水是液体
C.水能分解放出氧气
D.水中溶解有一定量的氧气
12.生活中应用缓慢氧化的实例很多,下列反应中不属于缓慢氧化的是(
)
A.酒和醋的酿造
B.农家肥料的腐熟
C.酒精灯平稳燃烧
D.人在长跑时急促呼吸
13.下列说法中正确的是(
)
A.根据质量守恒定律,1L氢气和1L氧气反应能生成2L水
B.只有固体、液体间的反应遵循质量守恒定律,如果有气体参加,就不遵循了
C.镁条在空气中燃烧,生成物的总质量比原来镁条的质量大
D.水结冰后质量没有改变,由此说明化学变化遵循质量守恒定律
14.“火折子”被称为古代的打火机。火折子的主要材料为白薯蔓汁浸泡过的土纸,加以棉花、
苇絮等,晒干卷成长杆状,点燃后吹灭成暗火,装入竹筒内,需要时取出一吹就能复燃。下列关于火折子的说法错误的是
(
)
A.土纸棉花等都是可燃物
B.装入竹筒后火折子没有完全熄灭
C.竹筒不是完全密闭的
D.取出一吹即可复燃是因为降低了着火点
15.下列关于燃料的说法中,正确的是(
)
A.石油是纯净物
B.煤、石油、天然气和酒精都是化石燃料
C.煤和石油的燃烧会造成空气污染
D.只有通过燃料的燃烧才能获得热能
16.将充满下列气体的试管倒置于水槽中(如图),一段时间后试管内的水位上升最高的是(
)
A.氧气
B.氢气
C.氮气
D.二氧化碳
17.工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可用如图所示的模型表示。下列有关甲醇的叙述中,错误的是(
)。
A.甲醇的化学式为
B.甲醇的相对分子质量为32
C.甲醇中C、H、O三种元素的质量之比为1:4:1
D.甲醇中氧元素的质量分数为50%
18.在密闭容器内,有甲、乙、丙、丁四种物质,在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示,下列说法错误的是(
)
A.丁一定是化合物
B.生成的甲、丙两物质的质量比为8:1
C.乙可能是该反应的催化剂
D.参加反应的丁的质量一定是生成甲和丙的质量之和
二、填空题(本大题共5小题,共52分)
19.(9分)在2019年年底开始,我国爆发了新冠肺炎,给国家和人民的财产带来巨大的损失,给人民的生命带来严重的威胁,全国人民在党中央的领导下众志成城抗击新冠肺炎。抗疫中用到了许多消毒剂,“84”消毒液(有效成分为次氯酸钠)和二氧化氯()是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式,其反应原理:________。
(2)二氧化氯()中氯元素的化合价为_____,二氧化氯()属于______(填字母)。
A.酸
B.碱
C.盐
D.氧化物
(3)“84”消毒液不能与洁厕灵混合使用,原因是“84”消毒液中的次氯酸钠与洁厕灵中的盐酸会发生化学反应,生成氯化钠、水和有毒气体氯气,写出该反应的化学方程式:___________________。
20.(10分)分析硫、木炭、铁丝三种物质在氧气中燃烧的实验,回答问题。
(1)铁丝燃烧时,需在铁丝下端系一根火柴,火柴所起到的作用是________。
(2)木炭在空气中燃烧发红,在氧气中燃烧更旺,发白光。硫在空气里燃烧发出淡蓝色火焰,而在氧气里燃烧得更旺,发出___火焰。木炭和硫在空气里和氧气里燃烧的现象不同,原因是_______。
(3)铁丝燃烧瓶底的水可用细沙代替,而硫不能,由此推测,具有的物理性质是_____;硫、铁丝燃烧实验中用到的氧气,最好采用______法收集。
21.(8分)火的利用推动了人类文明的进程,观察图:
选择序号回答(1)~(3):①与氧气接触,②温度达到着火点,③有可燃物。
(1)图甲所示实验现象,说明燃烧应具备的条件是________;
(2)图乙烧杯中蜡烛渐渐熄灭,说明燃烧应具备的条件是_________________;
(3)图丙铜片上白磷燃烧,红磷不燃烧,说明燃烧应具备的条件是_____________;
(4)图丙实验中所用药品的保存方法正确的是___________(选填图丁中的序号)。
22.(12分)A~H是初中常见的8种物质,它们有如图所示的转化关系。
已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会增强温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
(1)请写出下列物质的化学符号:D__________,G__________,H__________。
(2)请写出下列变化的文字表达式:
①B→F_______________________________;
②C→B_______________________________。
23.(13分)下图A~H是实验室制取某些常见气体的装置示意图。请完成下列相关问题。
(1)写出图中仪器②的名称:__________。
(2)实验室要制取一瓶干燥的氧气所选择的装置是____________(填序号)。
(3)实验室制备的化学方程式为______________,若用装置H收集气体,产生的气体应从_________(填“a”或“b”)端通入;
(4)用石灰石和稀盐酸制取二氧化碳,选取装置C或D相对于装置B在操作方面的优势为______________;若选择装置D用双氧水和二氧化锰制备氧气,能否体现该优点_________(填“能”或“否”)。
(5)用排水法与排空气法收集及相关性质的比较(分别用体积相同的2个集气瓶收集)。
已知:向收集满的集气瓶内倒入等体积适量澄清石灰水,并振荡。二氧化碳纯度越高,澄清石灰水先变浑浊后变澄清的时间越短。
比较项目
排水法
向上排空气法
收集方法可行性分析
气体生成和从水面逸出的速率远大于其溶解和与水反应的速率
Ⅰ.___,且不与空气发生反应
收集过程分析
集满现象:Ⅱ.____
“验满”分析:因气体无色,是否集满难确定,即便用燃着的木条移近容器口熄灭,也难以证明空气完全排尽
石灰水变浑浊又变澄清所需时间分析
时间较短
时间较长
由上述实验可得结论:①二氧化碳可用排水法或向上排空气法收集;②与排空气法相比,排水法的优点是___________。
三、计算题(本大题共1小题,共12分)
24.张玲同学为了测定汉白玉中碳酸钙的质量分数,称取5.55g研碎的汉白玉粉末,进行四次高温加热,反应的化学方程式为(杂质不参加反应),冷却、称量剩余固体的重复操作,记录数据如下表所示:
操作次序
第一次
第二次
第三次
第四次
剩余固体质量/g
4.25
3.95
3.35
3.35
请计算:
(1)在碳酸钙中各元素的质量比为________(最简整数比)。
(2)完全反应后生成二氧化碳_________g。
(3)求汉白玉中碳酸钙的质量分数。(精确到0.1%)
答案以及解析
1.答案:B
2.答案:A
解析:臭氧为由氧元素组成的单质,属于纯净物,A项正确。
3.答案:D
解析:A、给试管内液体加热的注意事项:试管内液体量不能超过试管容积的三分之一,图中溶液过多,手握试管夹的长柄,不能握短柄,用酒精灯的外焰加热,故选项错误;
B、胶头滴管要垂悬在试管口上方,不能伸入试管内,或与试管壁接触,故选项错误;
C、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口;图中瓶口没有紧挨试管口、瓶塞没有倒放、标签没有向手心,故选项错误;
D、酒精灯的点燃方法:用火柴点燃,不能用酒精灯引燃,容易发生火灾,故选项正确。故选D。
4.答案:A
解析:本题考查物理变化和化学变化的判断、分子的性质、金的化学性质燃烧的条件。在古代,人们把烧红的生铁放在铁砧上反复捶打,目的是让碳和氧气反应生成二氧化碳,从而降低含碳量,属于化学变化;“沙里淘金”是从沙子中分离出金,属于物理变化,A项符合题意;“一畦春韭绿,十里稻花香”,是因为稻花中含有的分子在不断地运动,向四周扩散,使人们闻到稻花香,B项不符合题意;“真金不怕火炼”意思是金即使在高温时也不与氧气反应,说明金的化学性质不活泼,C项不符合题意;“釜底抽薪”是清除可燃物灭火,“钻木取火”是使温度达到物质的着火点使其燃烧,都体现了燃烧的条件,D项不符合题意。
5.答案:A
解析:尘土飞扬是固体小颗粒的运动,不是分子的运动。
6.答案:B
解析:A.水电解实验证明水是由氢元素和氧元素组成的,不能说实验证明水是由氢原子和氧原子构成的,故A错误;B.由于氧气与氢气的水溶性有差异,氧气是不易溶于水的,氢气是难溶于水的,所以甲、乙管中气体体积比大于2:1,可能与两种气体的水溶性有关,故B正确;C.乙管内电极与电源的正极相连,产生的气体是氧气,氧气具有助燃性,但不具有可燃性,故C错误;D.水电解过程中,水分子分裂成氢原子和氧原子,氢原子和氧原子再分别构成氢分子和氧分子,所以该过程中水分子发生改变,故D错误。
7.答案:C
解析:A、硒元素的相对原子质量为78.96,单位不是“g”;故选项错误;
B、一个硒原子中有34个质子;故选项错误;
C、硒原子结构示意图中,质子数=核外电子数,34=2+8+X+6,X=18;故选项正确;
D、硒原子最外层有6个电子,在反应中易得电子;故选项错误;
故选:C。
8.答案:A
解析:磷燃烧消耗了氧气生成五氧化二磷固体,装置中压强减小,水进入装置,进入装置中水的体积就是消耗氧气的体积;燃烧过程中氮气不参与反应,故实验过程中,逐渐减少的气体和逐渐增多的物质是氧气、五氧化二磷。
故选A。
9.答案:B
解析:A、矿泉水由水、矿物质等两种以上物质混合而成,属于混合物,不符合题意;
B、净水的方法有沉淀、过滤、吸附、消毒、蒸馏等,说法正确,符合题意;
C、过滤只能除去不溶性杂质,不能降低水的硬度,不符合题意;
D、水是由水分子构成,不是由氢气和氧气构成的,不符合题意。
故选B。
10.答案:C
解析:空气中的成分按体积计算,大约是氮气78%,氧气21%,稀有气体094%,不含有氨气,故选C。
11.答案:D
解析:鱼能在水中生存是因为水中溶有的少量氧气,氧气是由氧分子构成的;与水中含有氧元素、水是液态无关,且水常温无法分解生成氧气。
故选D。
12.答案:C
解析:酒精灯的平稳燃烧是较剧烈的氧化反应,而缓慢氧化进行得很慢,甚至不易被察觉,如A、B、D三项所述的氧化反应是缓慢氧化。
13.答案:C
解析:质量守恒定律解释的物理量是质量,不是体积,A错误;有气体参加的化学反应依然遵循质量守恒定律,B错误;镁条在空气中燃烧,生成物氧化镁的质量为参加反应的镁和氧气的质量总和,C正确;水结冰是物理变化,质量守恒定律只适用于化学变化,不适用于物理变化,D错误。
14.答案:D
15.答案:C
解析:石油是由多种物质组成的,属于混合物,A错误;煤、石油、天然气属于化石燃料,酒精不属于化石燃料,B错误;煤、石油等化石燃料的燃烧能生成大量的二氧化碳,造成温室效应,而产生氧化碳、二氧化硫、氮氧化物等会造成空气污乘,C正确;燃烧、摩擦等都可以产生热能,D错误。
16.答案:D
解析:氢气和氮气难溶于水,将充满氢气或氮气的试管倒置于水槽中时,试管内的水位几乎不上升;
氧气不易溶于水,将充满氧气的试管倒置于水槽中时,试管内的水位上升较少;
二氧化碳能够溶于水,将充满二氧化碳的试管倒置于水槽中时,试管内的水位上升较多;
由以上分析可知,一段时间后试管内的水位上升最高的是充满二氧化碳的试管。
故选:D。
17.答案:C
解析:根据图中的信息可知其化学式为,也可以写成,故A正确;相对分子质量等于相对原子质量与原子个数的乘积的总和。的相对分子质量=,故B正确;元素的质量比等于相对原子质量与原子个数的乘积的比值,中碳、氢、氧三种元素的质量比=,故C错误;物质中某种元素的质量分数=。所以甲醇中氧元素的质量分数=,故D正确。
18.答案:B
解析:反应前后容器中物质的总质量不变,反应后质量分数减小的物质是反应物,质量分数增大的物质是生成物,由图中物质的质量分数的变化可知,丁的质量分数减小,是反应物;甲、丙物质的质量分数增大,是生成物,而乙物质的质量分数不变,可能是催化剂。该反应为:丁→甲+丙,丁一定是化合物,A正确;生成的甲、丙两物质的质量比为2:16=1:8,B错误;乙物质的质量分数不变,可能是催化剂,C正确;参加反应的丁的质量一定是生成甲和丙的质量之和,D正确。
19.答案:(1)NaClO
(2)+4
;D
(3)
解析:(1)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式可知,反应前氯、钠、氧、氢的原子个数分别为2、2、2、2,反应后的生成物中氯、钠、氧、氢的原子个数分别为1、1、1、2,根据反应前后原子种类、数目不变,则每个分子由1个钠原子、1个氯原子和1个氧原子构成,则该物质的化学式为NaClO。
(2)氧元素显-2价,设氯元素的化合价是,根据在化合物中各元素的正负化合价代数和为零,可得:,则。二氧化氯是由两种元素组成的且有一种是氧元素的化合物,属于氧化物。
(3)次氯酸钠与洁厕灵中的盐酸会发生化学反应,生成氯化钠、水和有毒气体氯气,反应的化学方程式为。
20.答案:(1)引燃铁丝(2)蓝紫色;氧气浓度(或含量)不同(3)能(或可、易)溶于水;排水
解析:
(1)铁丝的一端系一根火柴并点燃可以给铁丝预热,提高铁丝温度,有利于铁丝燃烧,起引燃作用,故填引燃铁丝。
(2)硫在空气里燃烧发出淡蓝色火焰,而在氧气里燃烧得更旺,发出蓝紫色的火焰,故填蓝紫色;
木炭和硫分别在空气里和氧气里燃烧的现象不同,说明了可燃物燃烧时与氧气的浓度有关,浓度越大燃烧越剧烈,故填氧气浓度(或含量)不同。
(3)燃烧硫实验中,集气瓶底部只能装少量水不能装细沙,是因为二氧化硫易溶于水,用水吸收二氧化硫,可以防止空气污染,故填能(或可、易)溶于水。
用排水法收集到的氧气比较纯净,且瓶中还要留一些水,最好采用排水法收集氧气,故填排水。
21.答案:(1)③
(2)①
(3)②
(4)AB
解析:(1)图甲所示实验中小木块能燃烧,玻璃块不能燃烧,说明燃烧应具备的条件是有可燃物。
(2)图乙中,烧杯将蜡烛与外界氧气隔绝,所以烧杯中蜡烛渐渐熄灭,说明燃烧应具备的条件是与氧气接触。
(3)图丙铜片上白磷燃烧,红磷不燃烧,说明燃烧应具备的条件是温度达到着火点。
(4)由于白磷的着火点低易自燃,应保存在冷水中,红磷的着火点较高,可密封保存在广口瓶中,所以保存方法正确的是AB。
22.答案:(1)
(2)①②
解析:(1)A、C是无色液体,B、F、G是无色气体,D是黑色固体,其中大量排放F会增强温室效应,则F为二氧化碳;过氧化氢和水均为无色液体,过氧化氢在二氧化锰的催化作用下生成水和氧气,碳是一种黑色固体,在氧气中燃烧生成二氧化碳,则A为过氧化氢,B为氧气,C为水,D为碳;E在纯净的B中燃烧发出明亮的蓝紫色火焰,则E为硫,G为二氧化硫;水通电分解生成氢气和氧气,则H为氢气。(2)①B→F,即碳在氧气中燃烧生成二氧化碳;②C→B,即水通电分解生成氢气和氧气。
23.答案:(1)水槽
(2)AG(或AH)
(3);a
(4)可以控制反应的发生和停止(或随开随用,随关随停);否
(5)Ⅰ.密度比空气大;Ⅱ.集气瓶口有气泡冒出②收集到的气体更纯净
解析:(1)②为水槽。
(2)制取氧气可以选择固体加热型发生装置,也可以选择固液常温型发生装置,但是要制取干燥气体,只能选择固体加热型发生装置A;收集氧气可以用排水法或者向上排空气法,排水法收集的气体不干燥,所以选择G或H为收集装置。
(3)盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,化学方程式为;二氧化碳密度比空气大,所以从a端进气。
(4)C或D可通过控制固液接触和分离,从而控制反应的发生和停止;二氧化锰为固体粉末,实现不了固液分离,所以不能体现C或D的优点。
(5)二氧化碳密度比空气大,并且不与空气反应,故可采用向上排空气法收集;排水法收集气体时,集气瓶内集满气体后,气体逸出集气瓶,形成气泡;根据澄清石灰水变浑浊又变澄清所需的时间,可以推测出排水法收集的二氧化碳纯度高。
24.答案:(1)10:3:12(2)2.2(3)设汉白玉中碳酸钙的质量分数为x,则
解得x≈90.1%。
答:汉白玉中碳酸钙的质量分数为90.1%。
同课章节目录
