第四章 化学与可持续发展 第一节 开发利用金属矿产和海水资源
文档属性
| 名称 | 第四章 化学与可持续发展 第一节 开发利用金属矿产和海水资源 |

|
|
| 格式 | zip | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-07 00:00:00 | ||
图片预览









文档简介
(共35张PPT)
海洋生物资源
海洋能源
具有商业开发价值的:潮汐发电和波浪发电
大陆架的浅海海底:
石油、天然气、煤、硫、磷等
近岸带的滨海砂矿:
砂、贝壳等建筑材料和金属矿产
多数海盆中:
深海锰结核
海底矿产资源
海洋资源的分类
水资源
矿产资源
生物资源
能源
……
海水资源的开发利用
第一节 开发利用金属矿物和海水资源
第二课时
我们面临的问题
地球表面虽然有71%被水覆盖,
但其中97.2%是海水,
在2.8%的淡水中,又有69%是人类难以利用的两极冰盖。
人类可用淡水只占全球水总量的0.77%
2、海水的淡化
(1)使海水淡化的途径
通过从海水中提取淡水或从海水中把盐分离
出去,都可以达到淡化海水的目的。
(2)海水淡化的方法及其特点
海水淡化的方法主要有蒸馏法、电渗析法、
离子交换法等。
其中蒸馏法的历史最久,技术和工艺也比较
完善,但成本较高。
1、海水中水资源利用的项目
主要包括海水的淡化和直接利用海水的循环冷却等。
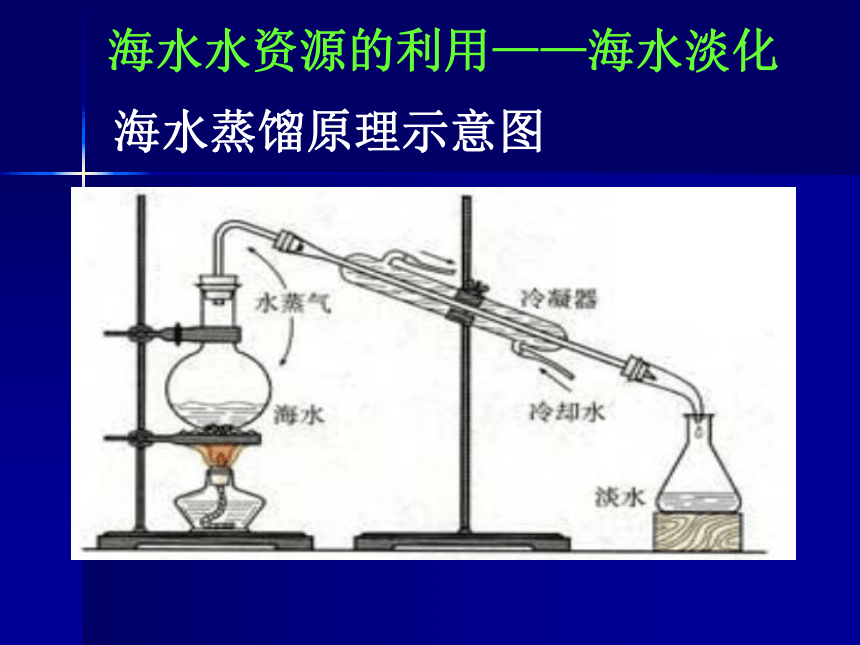
海水蒸馏原理示意图
海水水资源的利用——海水淡化
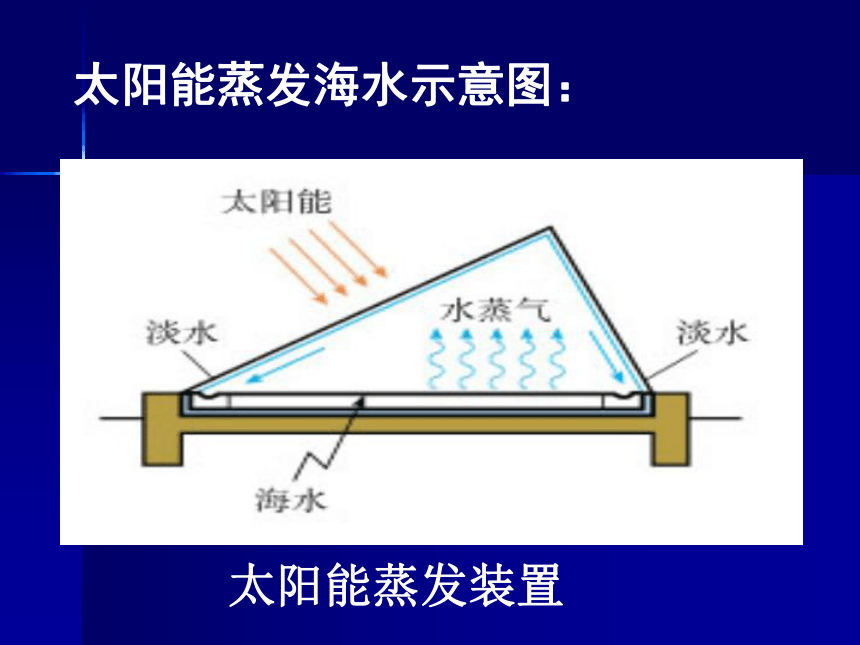
太阳能蒸发海水示意图:
太阳能蒸发装置
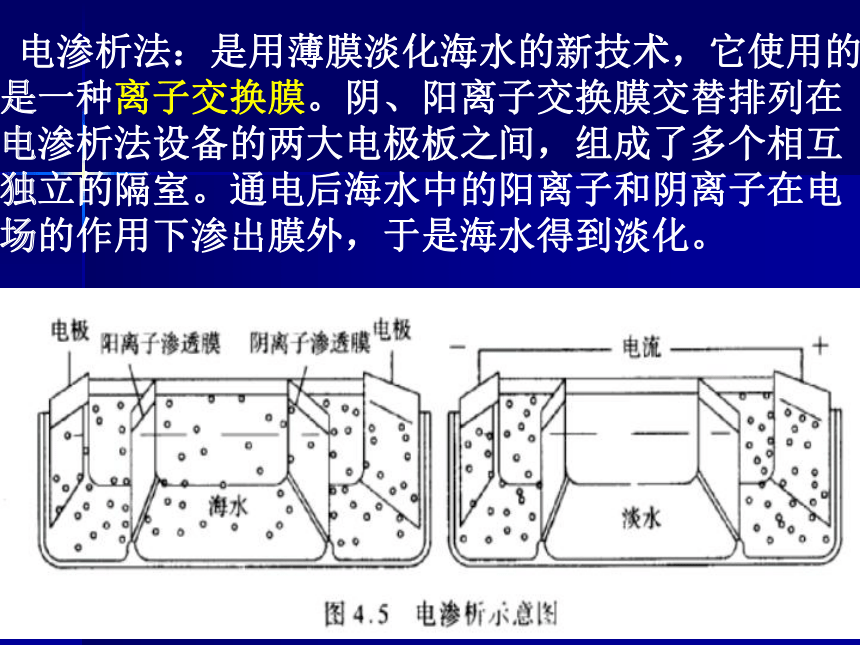
电渗析法:是用薄膜淡化海水的新技术,它使用的是一种离子交换膜。阴、阳离子交换膜交替排列在电渗析法设备的两大电极板之间,组成了多个相互独立的隔室。通电后海水中的阳离子和阴离子在电场的作用下渗出膜外,于是海水得到淡化。
离子交换法:
现代人工合成的离子交换树脂能吸附
溶液中的离子,使咸水变成淡水.离子
交换树脂的结构中带有许多H+和OH-
利用离子交换树脂进行离子交换时,
阴离子能和海水中的氯离子交换,
阳离子和海水中的钠离子交换,这样
水里的盐分就少了。
如何提取海水中的氯化钠?
海水提取 NaCl
海水化学资源的开发利用
海水晒盐
粗盐中的杂质:泥沙、Ca2+、Mg2+、SO42-
除杂试剂:
①Na2CO3
②NaOH
③BaCl2
试剂加入顺序:
②③①
③②①
③①②
基本原则:
先加BaCl2,后加Na2CO3
海水
粗盐
滤液
沉淀
NaCl
苦卤(Mg2+、Br-、I- …)
BaCl2、NaOH、Na2CO3
过滤
蒸发结晶
适量盐酸
蒸发
结晶
Na
氯碱工业
纯碱工业
氯碱工业简介
盐酸
漂白液
2NaCl+2H2O = 2NaOH+Cl2↑+H2↑
电解
原理:
原料:
产品:
用途:
苦卤(Mg2+…)
Mg
海水提镁
?
海水提取镁的工艺流程图
Mg2++2OH-=Mg(OH)2
海水
(含Mg2+)
试剂①
溶液
Mg(OH)2
沉淀
试剂②
MgCl2
溶液
Mg
无水MgCl2
熔融电解
海水中溴的提取
将Br - 转变为Br2是海水提溴中关键的化学反应,你能否设计一个实验方案模拟这一生产过程?写出有关反应的化学方程式
工业上如何将海水中的溴离子变成溴单质?阅读P91资料卡片—海水提溴
浓缩海水
溴单质
氢溴酸
溴单质
通Cl2
①
通空气、水蒸气, SO2吸收
②
通氯气
③
2HBr + Cl2= Br2+2HCl
2NaBr + Cl2= Br2+2NaCl
2H2O + Br2+SO2= H2SO4+2HBr
海带中碘元素的检验
相关资料:
1.海水中碘的含量
2.碘元素的存在的形式
3.碘是人体必需的微量元素,与人体智力发育密切
相关,缺碘易导致智力低下和甲状腺肿大
0.06%毫克/升
主要是 I-,富集在海带中
如何证明海带中有碘离子?
阅读P91实验4-2
海带中碘元素的检验
1、用剪刀剪碎海带,用酒精润湿,放入坩埚中
2、灼烧海带至完全生成灰,停止加热,冷却
3、将海带灰移至小烧杯中,加蒸馏水,搅拌,煮沸,过滤
4、在滤液中滴加稀H2SO4及H2O2,然后加几滴淀粉溶液。
方程式为:
2KI+H2O2+H2SO4 = I2+2H2O+K2SO4
实验现象:
加入H2O2溶液后,溶液由无色变为深黄
色;加入淀粉溶液后,溶液又变为深蓝色。
实验说明:
海带如果用水浸泡,碘化物会部分溶解而损耗,因此干海带不要用水冲洗。
将海带剪碎后,再用酒精润湿,可使海带易于灼烧完全,灼烧时产生的烟也较少,并缩短灼烧时间(湿海带不易燃烧)
海带灼烧若不完全,其灰的滤液会呈浅褐色,所以应将海带灼烧完全。
海水资源的综合利用——海水综合利用联合工业体系
1、医生建议因缺少某种元素而患甲状腺肿大的病人多食海带,这是由于海带中含有较丰富的( )
A.碘元素 B.铁元素
C.钾元素 D.锌元素
A
课堂练习:
2、一位海上遇难的水手,随着木排在海上漂流。他用完了淡水,感到异常口渴,但他不喝海水,因为他知道海水会致命,主要原因是 ( )
A、海水有苦涩味,根本喝不下去
B、海水中含有多种盐,能使肠胃腐烂致人死亡
C、海水中有许多微生物,有些微生物能致人死亡
D、海水会造成人体水分从血液和组织内脱离出来,进入肠胃中,使人脱水死亡
D
3、海水中含有MgCl2,从海水中提取Mg,最适宜的方法是( )
A、海水 Mg(OH)2 Mg
B、海水 MgCl2溶液 MgCl2(熔融) Mg
C、海水 Mg(OH)2 MgO Mg
D、海水 Mg(OH)2 MgCl2溶液 MgCl2(熔融) Mg
NaOH
电解
电解
HCl
电解
石灰乳
灼烧
石灰乳
HCl
电解
D
4、在检验海带中碘元素的实验中,有以下步骤:
①灼烧海带至完全生成灰,停止加热,冷却;
②在滤液中滴加稀H2SO4及H2O2,然后加入几滴淀粉溶液;
③用剪刀剪碎海带,用酒精润湿,放入坩埚中;
④海带灰转移到小烧杯,加蒸馏水,搅拌、煮沸、过滤。
(1)合理的步骤是__________________;
(2)证明含碘的步骤是_____________,
现象是__________________________,
反应的离子方程式是 __________________________。
③①④②
②
滴入淀粉溶液,溶液变蓝
2I- + 2H+ +H2O2 I2+2H2O
作业:
P93: 4
海洋生物资源
海洋能源
具有商业开发价值的:潮汐发电和波浪发电
大陆架的浅海海底:
石油、天然气、煤、硫、磷等
近岸带的滨海砂矿:
砂、贝壳等建筑材料和金属矿产
多数海盆中:
深海锰结核
海底矿产资源
海洋资源的分类
水资源
矿产资源
生物资源
能源
……
海水资源的开发利用
第一节 开发利用金属矿物和海水资源
第二课时
我们面临的问题
地球表面虽然有71%被水覆盖,
但其中97.2%是海水,
在2.8%的淡水中,又有69%是人类难以利用的两极冰盖。
人类可用淡水只占全球水总量的0.77%
2、海水的淡化
(1)使海水淡化的途径
通过从海水中提取淡水或从海水中把盐分离
出去,都可以达到淡化海水的目的。
(2)海水淡化的方法及其特点
海水淡化的方法主要有蒸馏法、电渗析法、
离子交换法等。
其中蒸馏法的历史最久,技术和工艺也比较
完善,但成本较高。
1、海水中水资源利用的项目
主要包括海水的淡化和直接利用海水的循环冷却等。
海水蒸馏原理示意图
海水水资源的利用——海水淡化
太阳能蒸发海水示意图:
太阳能蒸发装置
电渗析法:是用薄膜淡化海水的新技术,它使用的是一种离子交换膜。阴、阳离子交换膜交替排列在电渗析法设备的两大电极板之间,组成了多个相互独立的隔室。通电后海水中的阳离子和阴离子在电场的作用下渗出膜外,于是海水得到淡化。
离子交换法:
现代人工合成的离子交换树脂能吸附
溶液中的离子,使咸水变成淡水.离子
交换树脂的结构中带有许多H+和OH-
利用离子交换树脂进行离子交换时,
阴离子能和海水中的氯离子交换,
阳离子和海水中的钠离子交换,这样
水里的盐分就少了。
如何提取海水中的氯化钠?
海水提取 NaCl
海水化学资源的开发利用
海水晒盐
粗盐中的杂质:泥沙、Ca2+、Mg2+、SO42-
除杂试剂:
①Na2CO3
②NaOH
③BaCl2
试剂加入顺序:
②③①
③②①
③①②
基本原则:
先加BaCl2,后加Na2CO3
海水
粗盐
滤液
沉淀
NaCl
苦卤(Mg2+、Br-、I- …)
BaCl2、NaOH、Na2CO3
过滤
蒸发结晶
适量盐酸
蒸发
结晶
Na
氯碱工业
纯碱工业
氯碱工业简介
盐酸
漂白液
2NaCl+2H2O = 2NaOH+Cl2↑+H2↑
电解
原理:
原料:
产品:
用途:
苦卤(Mg2+…)
Mg
海水提镁
?
海水提取镁的工艺流程图
Mg2++2OH-=Mg(OH)2
海水
(含Mg2+)
试剂①
溶液
Mg(OH)2
沉淀
试剂②
MgCl2
溶液
Mg
无水MgCl2
熔融电解
海水中溴的提取
将Br - 转变为Br2是海水提溴中关键的化学反应,你能否设计一个实验方案模拟这一生产过程?写出有关反应的化学方程式
工业上如何将海水中的溴离子变成溴单质?阅读P91资料卡片—海水提溴
浓缩海水
溴单质
氢溴酸
溴单质
通Cl2
①
通空气、水蒸气, SO2吸收
②
通氯气
③
2HBr + Cl2= Br2+2HCl
2NaBr + Cl2= Br2+2NaCl
2H2O + Br2+SO2= H2SO4+2HBr
海带中碘元素的检验
相关资料:
1.海水中碘的含量
2.碘元素的存在的形式
3.碘是人体必需的微量元素,与人体智力发育密切
相关,缺碘易导致智力低下和甲状腺肿大
0.06%毫克/升
主要是 I-,富集在海带中
如何证明海带中有碘离子?
阅读P91实验4-2
海带中碘元素的检验
1、用剪刀剪碎海带,用酒精润湿,放入坩埚中
2、灼烧海带至完全生成灰,停止加热,冷却
3、将海带灰移至小烧杯中,加蒸馏水,搅拌,煮沸,过滤
4、在滤液中滴加稀H2SO4及H2O2,然后加几滴淀粉溶液。
方程式为:
2KI+H2O2+H2SO4 = I2+2H2O+K2SO4
实验现象:
加入H2O2溶液后,溶液由无色变为深黄
色;加入淀粉溶液后,溶液又变为深蓝色。
实验说明:
海带如果用水浸泡,碘化物会部分溶解而损耗,因此干海带不要用水冲洗。
将海带剪碎后,再用酒精润湿,可使海带易于灼烧完全,灼烧时产生的烟也较少,并缩短灼烧时间(湿海带不易燃烧)
海带灼烧若不完全,其灰的滤液会呈浅褐色,所以应将海带灼烧完全。
海水资源的综合利用——海水综合利用联合工业体系
1、医生建议因缺少某种元素而患甲状腺肿大的病人多食海带,这是由于海带中含有较丰富的( )
A.碘元素 B.铁元素
C.钾元素 D.锌元素
A
课堂练习:
2、一位海上遇难的水手,随着木排在海上漂流。他用完了淡水,感到异常口渴,但他不喝海水,因为他知道海水会致命,主要原因是 ( )
A、海水有苦涩味,根本喝不下去
B、海水中含有多种盐,能使肠胃腐烂致人死亡
C、海水中有许多微生物,有些微生物能致人死亡
D、海水会造成人体水分从血液和组织内脱离出来,进入肠胃中,使人脱水死亡
D
3、海水中含有MgCl2,从海水中提取Mg,最适宜的方法是( )
A、海水 Mg(OH)2 Mg
B、海水 MgCl2溶液 MgCl2(熔融) Mg
C、海水 Mg(OH)2 MgO Mg
D、海水 Mg(OH)2 MgCl2溶液 MgCl2(熔融) Mg
NaOH
电解
电解
HCl
电解
石灰乳
灼烧
石灰乳
HCl
电解
D
4、在检验海带中碘元素的实验中,有以下步骤:
①灼烧海带至完全生成灰,停止加热,冷却;
②在滤液中滴加稀H2SO4及H2O2,然后加入几滴淀粉溶液;
③用剪刀剪碎海带,用酒精润湿,放入坩埚中;
④海带灰转移到小烧杯,加蒸馏水,搅拌、煮沸、过滤。
(1)合理的步骤是__________________;
(2)证明含碘的步骤是_____________,
现象是__________________________,
反应的离子方程式是 __________________________。
③①④②
②
滴入淀粉溶液,溶液变蓝
2I- + 2H+ +H2O2 I2+2H2O
作业:
P93: 4
