阿司匹林
图片预览











文档简介
(共37张PPT)
关于阿司匹林的合成
课标基本要求:
1.了解阿司匹林制备的反应原理和实验方法。
2.通过阿司匹林制备实验,初步熟悉有机化合物的分离、提纯等方法。
3.巩固称量、溶解、加热、结晶、洗涤、重结晶等基本操作。
课标发展要求:
能根据水杨酸分子结构中含有的官能团,分析水杨酸可能具有的化学性质。
能根据乙酰水杨酸分子结构中含有的官能团,分析乙酰水杨酸可能具有的化学性质。
让学生
领略有机合成的无穷魅力!
切不可让学生 “照方抓药”
1、明确阿司匹林的合成原理及方案:
如何对参考的合成路线进行理解?
为什么要选择这条路线?
这条路线的优缺点有哪些?
还有哪些反应可以达到制备目标?
哪种路线更好?
2、指导学生对反应条件进行讨论。
3、要重视产品纯度分析,介绍除杂、验纯的方法 。
4、重在制备实验的经历和体验
使学生经历和体验制备实验方案的设计以及实验实施的过程,形成解决制备问题的一般思路,以及从哪些角度考虑要注意的问题。
课题2
课时建议:2课时(或2小时)
第一课时:合成方案的设计及问题讨论。
第二课时:学生根据方案认真完成实验。
第一课时:
合成方案的设计及问题讨论。
【创设情景】:展示几幅唯美的柳树图片,引出有关“阿司匹林”古老的故事。
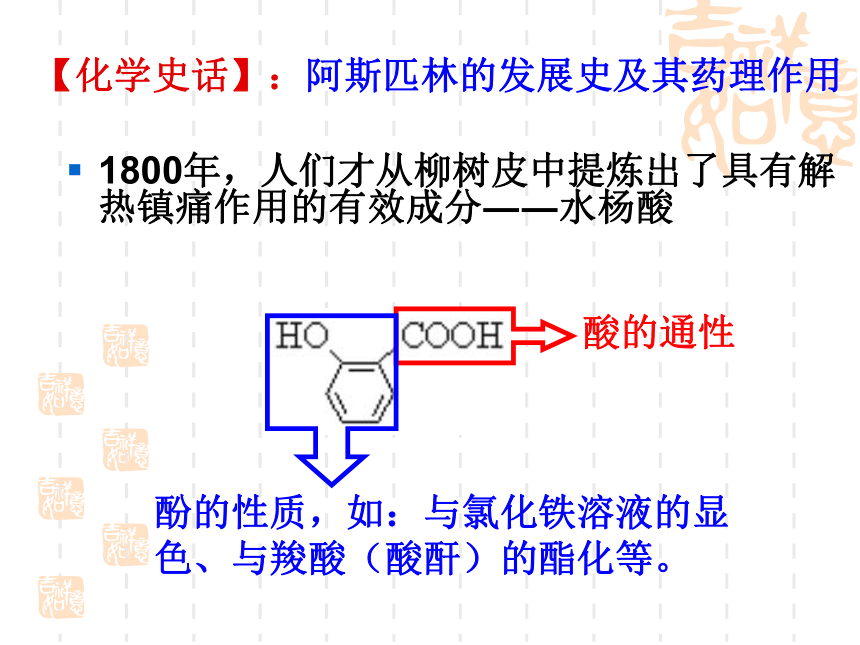
【化学史话】:阿斯匹林的发展史及其药理作用
1800年,人们才从柳树皮中提炼出了具有解热镇痛作用的有效成分――水杨酸
酸的通性
酚的性质,如:与氯化铁溶液的显色、与羧酸(酸酐)的酯化等。
1898年,德国化学家霍夫曼用水杨酸与醋酐反应,合成了乙酰水杨酸
1899年,德国拜仁药厂正式生产这种药品,取商品名为Aspirin
阿斯匹林的药理作用
阿司匹林为解镇痛药,用于治疗伤风、感冒、头痛、发烧、神经痛、关节痛及风湿病等。近年来,又证明它具有抑制血小板凝聚的作用,其治疗范围又进一步扩大到预防血栓形成,治疗心血管疾患。
【展示样品】:
阿司匹林肠溶片使用说明书(部分)
[药品名称] 通用名称:阿司匹林肠溶片 汉语拼音:Asipilin Changrong Pian 英文名称:Aspirin Enteric-coated Tablets 结构式:
分子式:C9H8O4 分子量:180.16 [药物组成]本品每片含主要成分阿司匹林0.3克。辅料为 。 [性状]本品为 色肠溶包衣片,除去包衣后显白色。 [作用类别]、[药理作用]、[适应症] 同片剂。 [用法与用量] 整片吞服 成人 一次1片,若发热或疼痛持续不缓解,间隔4-6小时重复用药一次。24小时内不超过4片。儿童用量请咨询医师或药师。 [注意事项]、[药物相互作用]同片剂。 [不良反应]
认识阿斯匹林的组成与结构:
阿司匹林的分子式、官能团名称。
C9H8O4 羧基、酯基
分析阿斯匹林的重要化学性质:
分析合成阿斯匹林的原料:
水杨酸(来源于天然植物)、
乙酸(提示:实验中实际是用乙酸酐代
替乙酸)
水解
酸性
分析合成阿斯匹林所需要的条件:
浓硫酸(作催化剂)
加热(85℃-90 ℃ ,水浴加热法)
设计合成阿斯匹林的方案:
1.主反应是:
2.副反应是
3.乙酰水杨酸微溶于冷水,如何获得粗产品?
(冰水溶解、过滤。)
4.粗产品中主要含有哪些杂质?
(水杨酸聚合物、水杨酸)
5.副产物聚合物能溶于NaHCO3溶液吗?
(不能)
能用NaHCO3溶液除去副产物聚合物吗?
(可以。因为乙酰水杨酸中含羧基,能与NaHCO3 溶液反应生成可溶性盐。)
如何操作?
(加NaHCO3 溶液、搅拌、过滤、洗涤;滤液中加足量盐酸、冷却结晶、过滤、洗涤。)
C
O
O
H
O
O
C
H
3
+
N
a
H
C
O
3
C
O
O
N
a
O
O
C
H
3
+
H
2
O
+
C
O
2
6.水杨酸可以在各步纯化过程和产物的重结晶过程中被除去,如何检验水杨酸已被除尽?
(取乙酰水杨酸晶体少许,溶解,向其中滴加两滴1%的氯化铁溶液,观察颜色。)
具体方案及步骤:
1)2g水杨酸+5mL乙酸酐+5滴浓硫酸,振摇
溶解
2)85~90 ℃水浴加热5~10min,冷却
3)加水50mL析出晶体,抽滤,洗涤得粗品。
4)粗品加25mL饱和碳酸氢钠,搅拌至无CO2
放出
5)布氏漏斗过滤,用水冲洗
6) 15mL4mol·L-1 +10mLH2O+滤液,冰水浴,
析出晶体
7)吸滤,冷水洗2次,干燥,得精品。
8)几粒结晶+5mL水+1%的FeCl3溶液。
9)干燥、称量,计算产率。
本课题实际实施过程中可能存在的问题:
1、乙酸酐的贮备。
2、仪器:抽滤设备没有或数量不足。
电子天平没有。
3、耗时太长。
第二课时
学生根据方案认真完成实验
实际操作:
1)2g水杨酸+5mL乙酸酐+5滴浓硫酸,振摇
溶解
0.5mL左右
实际操作:
2)85~90 ℃水浴加热5~10min,冷却
十分钟或更长些
如果冷却后发现底部是一层红棕色油状物,此实验即已失败。整个实验这一步最难。
而正常的应该是乳白色悬浊液。
实际操作:
3)加水50mL析出
晶体,抽滤,洗涤
得粗品。
(如果无抽滤设备,
就用简易抽滤法吧)
实际操作:
4)粗品加25mL饱和碳酸氢钠溶液,搅拌至无CO2放出
5)布氏漏斗过滤,用水冲洗
实际操作:
6)15mL4mol·L-1盐酸+滤液,冰水浴,析出晶体
实际操作:
7)抽滤,冷水洗2次,干燥,得精品。
实际操作:
8)几粒结晶+5mL水+1%的FeCl3溶液。
9)干燥、称量,计算产率。
(理论产量2.6g,实际产量1.1g,
产率42.31%)
注意事项:
1、要按照书上的顺序加样。否则,如果先加水杨酸和浓硫酸,水杨酸就会被氧化。
2、本实验的几次结晶都比较困难,要有耐心。在冰水冷却下,用玻棒充分磨擦器皿壁,才能结晶出来。
3、由于产品微溶于水,所以水洗时,要用少量冷水洗涤,用水不能太多。
4、第一次的粗产品不用干燥,即可进行下步纯化。
5、开始实验时,仪器药品要干燥。
关于阿司匹林的合成
课标基本要求:
1.了解阿司匹林制备的反应原理和实验方法。
2.通过阿司匹林制备实验,初步熟悉有机化合物的分离、提纯等方法。
3.巩固称量、溶解、加热、结晶、洗涤、重结晶等基本操作。
课标发展要求:
能根据水杨酸分子结构中含有的官能团,分析水杨酸可能具有的化学性质。
能根据乙酰水杨酸分子结构中含有的官能团,分析乙酰水杨酸可能具有的化学性质。
让学生
领略有机合成的无穷魅力!
切不可让学生 “照方抓药”
1、明确阿司匹林的合成原理及方案:
如何对参考的合成路线进行理解?
为什么要选择这条路线?
这条路线的优缺点有哪些?
还有哪些反应可以达到制备目标?
哪种路线更好?
2、指导学生对反应条件进行讨论。
3、要重视产品纯度分析,介绍除杂、验纯的方法 。
4、重在制备实验的经历和体验
使学生经历和体验制备实验方案的设计以及实验实施的过程,形成解决制备问题的一般思路,以及从哪些角度考虑要注意的问题。
课题2
课时建议:2课时(或2小时)
第一课时:合成方案的设计及问题讨论。
第二课时:学生根据方案认真完成实验。
第一课时:
合成方案的设计及问题讨论。
【创设情景】:展示几幅唯美的柳树图片,引出有关“阿司匹林”古老的故事。
【化学史话】:阿斯匹林的发展史及其药理作用
1800年,人们才从柳树皮中提炼出了具有解热镇痛作用的有效成分――水杨酸
酸的通性
酚的性质,如:与氯化铁溶液的显色、与羧酸(酸酐)的酯化等。
1898年,德国化学家霍夫曼用水杨酸与醋酐反应,合成了乙酰水杨酸
1899年,德国拜仁药厂正式生产这种药品,取商品名为Aspirin
阿斯匹林的药理作用
阿司匹林为解镇痛药,用于治疗伤风、感冒、头痛、发烧、神经痛、关节痛及风湿病等。近年来,又证明它具有抑制血小板凝聚的作用,其治疗范围又进一步扩大到预防血栓形成,治疗心血管疾患。
【展示样品】:
阿司匹林肠溶片使用说明书(部分)
[药品名称] 通用名称:阿司匹林肠溶片 汉语拼音:Asipilin Changrong Pian 英文名称:Aspirin Enteric-coated Tablets 结构式:
分子式:C9H8O4 分子量:180.16 [药物组成]本品每片含主要成分阿司匹林0.3克。辅料为 。 [性状]本品为 色肠溶包衣片,除去包衣后显白色。 [作用类别]、[药理作用]、[适应症] 同片剂。 [用法与用量] 整片吞服 成人 一次1片,若发热或疼痛持续不缓解,间隔4-6小时重复用药一次。24小时内不超过4片。儿童用量请咨询医师或药师。 [注意事项]、[药物相互作用]同片剂。 [不良反应]
认识阿斯匹林的组成与结构:
阿司匹林的分子式、官能团名称。
C9H8O4 羧基、酯基
分析阿斯匹林的重要化学性质:
分析合成阿斯匹林的原料:
水杨酸(来源于天然植物)、
乙酸(提示:实验中实际是用乙酸酐代
替乙酸)
水解
酸性
分析合成阿斯匹林所需要的条件:
浓硫酸(作催化剂)
加热(85℃-90 ℃ ,水浴加热法)
设计合成阿斯匹林的方案:
1.主反应是:
2.副反应是
3.乙酰水杨酸微溶于冷水,如何获得粗产品?
(冰水溶解、过滤。)
4.粗产品中主要含有哪些杂质?
(水杨酸聚合物、水杨酸)
5.副产物聚合物能溶于NaHCO3溶液吗?
(不能)
能用NaHCO3溶液除去副产物聚合物吗?
(可以。因为乙酰水杨酸中含羧基,能与NaHCO3 溶液反应生成可溶性盐。)
如何操作?
(加NaHCO3 溶液、搅拌、过滤、洗涤;滤液中加足量盐酸、冷却结晶、过滤、洗涤。)
C
O
O
H
O
O
C
H
3
+
N
a
H
C
O
3
C
O
O
N
a
O
O
C
H
3
+
H
2
O
+
C
O
2
6.水杨酸可以在各步纯化过程和产物的重结晶过程中被除去,如何检验水杨酸已被除尽?
(取乙酰水杨酸晶体少许,溶解,向其中滴加两滴1%的氯化铁溶液,观察颜色。)
具体方案及步骤:
1)2g水杨酸+5mL乙酸酐+5滴浓硫酸,振摇
溶解
2)85~90 ℃水浴加热5~10min,冷却
3)加水50mL析出晶体,抽滤,洗涤得粗品。
4)粗品加25mL饱和碳酸氢钠,搅拌至无CO2
放出
5)布氏漏斗过滤,用水冲洗
6) 15mL4mol·L-1 +10mLH2O+滤液,冰水浴,
析出晶体
7)吸滤,冷水洗2次,干燥,得精品。
8)几粒结晶+5mL水+1%的FeCl3溶液。
9)干燥、称量,计算产率。
本课题实际实施过程中可能存在的问题:
1、乙酸酐的贮备。
2、仪器:抽滤设备没有或数量不足。
电子天平没有。
3、耗时太长。
第二课时
学生根据方案认真完成实验
实际操作:
1)2g水杨酸+5mL乙酸酐+5滴浓硫酸,振摇
溶解
0.5mL左右
实际操作:
2)85~90 ℃水浴加热5~10min,冷却
十分钟或更长些
如果冷却后发现底部是一层红棕色油状物,此实验即已失败。整个实验这一步最难。
而正常的应该是乳白色悬浊液。
实际操作:
3)加水50mL析出
晶体,抽滤,洗涤
得粗品。
(如果无抽滤设备,
就用简易抽滤法吧)
实际操作:
4)粗品加25mL饱和碳酸氢钠溶液,搅拌至无CO2放出
5)布氏漏斗过滤,用水冲洗
实际操作:
6)15mL4mol·L-1盐酸+滤液,冰水浴,析出晶体
实际操作:
7)抽滤,冷水洗2次,干燥,得精品。
实际操作:
8)几粒结晶+5mL水+1%的FeCl3溶液。
9)干燥、称量,计算产率。
(理论产量2.6g,实际产量1.1g,
产率42.31%)
注意事项:
1、要按照书上的顺序加样。否则,如果先加水杨酸和浓硫酸,水杨酸就会被氧化。
2、本实验的几次结晶都比较困难,要有耐心。在冰水冷却下,用玻棒充分磨擦器皿壁,才能结晶出来。
3、由于产品微溶于水,所以水洗时,要用少量冷水洗涤,用水不能太多。
4、第一次的粗产品不用干燥,即可进行下步纯化。
5、开始实验时,仪器药品要干燥。
