3.1《醇酚》PPT课件(新人教版-选修5)
文档属性
| 名称 | 3.1《醇酚》PPT课件(新人教版-选修5) |

|
|
| 格式 | zip | ||
| 文件大小 | 208.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-12 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
新课标人教版课件系列
《高中化学》
选修5
3.1《醇酚》
教学目标
知识与技能
在分析醇的结构了解性质的过程中使学生获得物质的结构与性质之间关系的科学观点,学会由事物的表象分析事物的本质、变化,进一步培养学生综合运用知识、解决问题的能力。使学生掌握苯酚的分子结构特征、重要性质、了解苯酚的用途;掌握苯酚的检验方法。培养学生操作、观察、分析能力,加深对分子中原子团相互影响的认识,培养学生辩证唯物主义观点。
过程与方法
通过分析表格的数据,使学生学会利用曲线图表分析有关数据并且得出正确的结论找出相关的规律,培养学生分析数据和处理数据的能力。利用假说的方法引导学生开拓思维,进行科学探究。
情感态度和价值观
对学生进行辩证唯物主义教,即内因是事物变化的根据,外因是事物变化的条件,从而使学生了解学习和研究化学问题的一般方法和思维过程,进一步激发学生学习的兴趣和求知欲 。逐渐树立学生透过现象看本质的化学学科思想,激发学生学习兴趣,培养学生求实进取的品质。
教学重点:苯酚的化学性质和结构特征。
教学难点:苯酚的化学性质。
1.教法:(1)教师设计课型,以探究性实验为先导,探究性质(2)引导学生分析、讨论、对比,练习固所学知识。(3)多媒体辅助教学
2.学法:(1)实验探究、讨论、练习巩固。(2)积极使用手、眼、脑,培养语言表达能力,提高思维分析能力。
教学目标:
1.掌握乙醇的主要化学性质
2.掌握乙醇 的工业制法和用途
3.了解醇的分类和命名
4.了解醇类的一般通性和典型醇的用途
重点: 乙醇的化学性质
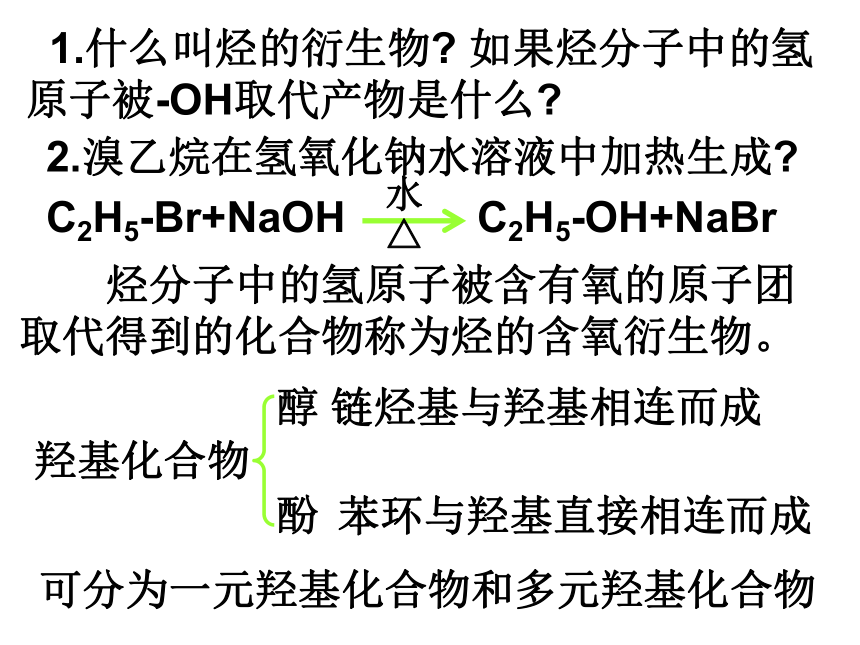
1.什么叫烃的衍生物 如果烃分子中的氢原子被-OH取代产物是什么
2.溴乙烷在氢氧化钠水溶液中加热生成
C2H5-Br+NaOH C2H5-OH+NaBr
水
△
烃分子中的氢原子被含有氧的原子团取代得到的化合物称为烃的含氧衍生物。
羟基化合物
醇
酚
链烃基与羟基相连而成
苯环与羟基直接相连而成
可分为一元羟基化合物和多元羟基化合物
一、醇
1、醇的分类:
醇
一元醇
多元醇
饱和一元醇:
不饱和一元醇
CnH2n+1OH
:如乙二醇、丙三醇等
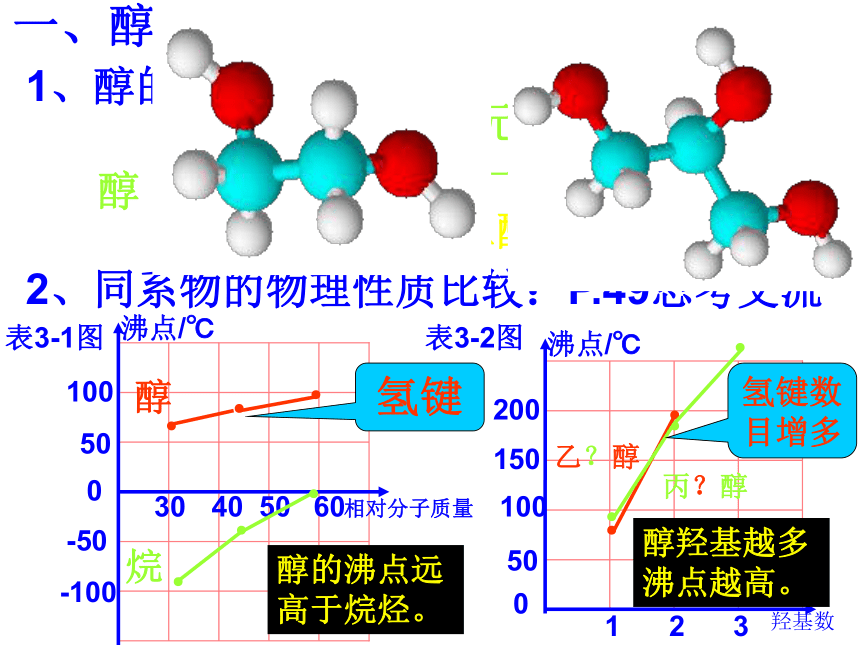
2、同系物的物理性质比较:P.49思考交流
相对分子质量
沸点/℃
表3-1图
0
50
100
-50
-100
30
40
50
60
表3-2图
羟基数
沸点/℃
0
150
200
100
50
1
2
3
●
●
●
●
●
●
●
●
●
●
●
醇
烷
乙?醇
丙?醇
醇的沸点远高于烷烃。
醇羟基越多沸点越高。
氢键
氢键数目增多
3、乙醇
1)乙醇的物理性质和分子结构
a.乙醇的物理性质
乙醇(酒精)是无色透明、具有特殊香味的液体,密度比水小,沸点比水低,易挥发,任意比溶于水,能溶解多种无机物和有机物。
b.乙醇的分子结构
化学式:C2H6O
结构简式:CH3CH2OH
或C2H5OH
结构式:
乙醇是极性分子
2、乙醇的化学性质
2CH3CH2-OH +2Na →2CH3CH2ONa +H2↑
2)乙醇的消去反应
1) 乙醇与钠反应
现象:缓慢产生气泡,金属钠沉于底部或上下浮动。
产物乙醇钠在水中强烈水解
CH3CH2-ONa +H2O→CH3CH2OH +NaOH
练习:写出乙醇与K、Ca分别反应的化学方程式
P.49思考与交流
②
①
③
④
实验装置及注意事项
实验3-1
1)反应温度:170℃ 2)加碎瓷片
3)V乙醇:V浓硫酸=1:3 4)检查气密性
注意事项:
可能产生的现象分析
题外话:分子间脱水
3)乙醇与氢卤酸的取代反应
2CH3CH2-OH CH3CH2-O-CH2CH3+H2O
140℃
浓H2SO4
②
①
③
④
2CH3CH2-OH+HBr CH3CH2Br+H2O
△
4)乙醇的氧化反应
乙醇能不能被其他氧化剂氧化?
实验3-2
怎样制备无水乙醇
CH3CH2-OH
CH3CHO
CH3COOH
[O]
[O]
CH3CH2-ONa
乙醇的氧化反应
CH3CH2-Br
CH2=CH2
CH3CH2-O-CH2CH3
乙醇的化学性质小结
Na
H2O
HBr
NaOH水溶液
浓H2SO4
170℃
浓H2SO4
140℃
CH3C-O-CH2CH3
O
4、乙醇的工业制法?
5、醇的化学性质——与乙醇相似
1.什么是酚
羟基与芳香烃侧链上的碳原子相连,其化合物是芳香醇。
练习:判断下列物质哪种是酚类?
羟基与苯环上的碳原子直接相连,其化合物则是酚。
思考:相同碳原子个数的芳香醇与酚类是什么关系?
2、试推导饱和一元酚的通式,并思考符合此通式的还有什么物质?
(同分异构体)
CnH2n-6O
二、酚
1、苯酚的结构和物理性质
无色晶体,有特殊气味,在空气中易被氧化而呈粉红色,熔点低(43℃) 。常温下在水中溶解度不大(9.3g),加热时易溶(>65℃时任意比溶)于水,易溶于乙醇等有机溶剂,有毒,有腐蚀性 。
如不慎沾到皮肤上应立即用酒精洗涤。
2、苯酚的化学性质:
1)苯酚的酸性:(实验探究3-3)
填表P.53
OH
OH
ONa
+NaOH
+H2O
为什么?
图3-7现象有误
2)苯酚与浓溴水的反应——取代反应
实验探究:实验3-4
苯酚的酸性比碳酸的还弱,但比HCO3-强。
(石炭酸)
结论:苯环影响了-OH的活性
结论:-OH影响了苯环的活性
用于苯酚的检验和测定
P.54 学与问
现象P.54图3-9
4)加成反应——与H2加成
1、为什么苯和苯酚发生溴代反应的条件和产物有很大的不同?
2、实验表明,苯酚的酸性比乙醇强。
3)苯酚的显色反应:
+Fe3+
OH
6
[Fe(C6H5O)6]3-
+6H+
5)氧化反应
OH
(易燃)
=O
=
O
在与醇相似的条件下,苯酚不能发生酯化反应。
注意:
苯酚的用途:
化工原料,制酚醛树脂、医药、染料等,稀溶液用作防腐剂和消毒剂
小结:
新课标人教版课件系列
《高中化学》
选修5
3.1《醇酚》
教学目标
知识与技能
在分析醇的结构了解性质的过程中使学生获得物质的结构与性质之间关系的科学观点,学会由事物的表象分析事物的本质、变化,进一步培养学生综合运用知识、解决问题的能力。使学生掌握苯酚的分子结构特征、重要性质、了解苯酚的用途;掌握苯酚的检验方法。培养学生操作、观察、分析能力,加深对分子中原子团相互影响的认识,培养学生辩证唯物主义观点。
过程与方法
通过分析表格的数据,使学生学会利用曲线图表分析有关数据并且得出正确的结论找出相关的规律,培养学生分析数据和处理数据的能力。利用假说的方法引导学生开拓思维,进行科学探究。
情感态度和价值观
对学生进行辩证唯物主义教,即内因是事物变化的根据,外因是事物变化的条件,从而使学生了解学习和研究化学问题的一般方法和思维过程,进一步激发学生学习的兴趣和求知欲 。逐渐树立学生透过现象看本质的化学学科思想,激发学生学习兴趣,培养学生求实进取的品质。
教学重点:苯酚的化学性质和结构特征。
教学难点:苯酚的化学性质。
1.教法:(1)教师设计课型,以探究性实验为先导,探究性质(2)引导学生分析、讨论、对比,练习固所学知识。(3)多媒体辅助教学
2.学法:(1)实验探究、讨论、练习巩固。(2)积极使用手、眼、脑,培养语言表达能力,提高思维分析能力。
教学目标:
1.掌握乙醇的主要化学性质
2.掌握乙醇 的工业制法和用途
3.了解醇的分类和命名
4.了解醇类的一般通性和典型醇的用途
重点: 乙醇的化学性质
1.什么叫烃的衍生物 如果烃分子中的氢原子被-OH取代产物是什么
2.溴乙烷在氢氧化钠水溶液中加热生成
C2H5-Br+NaOH C2H5-OH+NaBr
水
△
烃分子中的氢原子被含有氧的原子团取代得到的化合物称为烃的含氧衍生物。
羟基化合物
醇
酚
链烃基与羟基相连而成
苯环与羟基直接相连而成
可分为一元羟基化合物和多元羟基化合物
一、醇
1、醇的分类:
醇
一元醇
多元醇
饱和一元醇:
不饱和一元醇
CnH2n+1OH
:如乙二醇、丙三醇等
2、同系物的物理性质比较:P.49思考交流
相对分子质量
沸点/℃
表3-1图
0
50
100
-50
-100
30
40
50
60
表3-2图
羟基数
沸点/℃
0
150
200
100
50
1
2
3
●
●
●
●
●
●
●
●
●
●
●
醇
烷
乙?醇
丙?醇
醇的沸点远高于烷烃。
醇羟基越多沸点越高。
氢键
氢键数目增多
3、乙醇
1)乙醇的物理性质和分子结构
a.乙醇的物理性质
乙醇(酒精)是无色透明、具有特殊香味的液体,密度比水小,沸点比水低,易挥发,任意比溶于水,能溶解多种无机物和有机物。
b.乙醇的分子结构
化学式:C2H6O
结构简式:CH3CH2OH
或C2H5OH
结构式:
乙醇是极性分子
2、乙醇的化学性质
2CH3CH2-OH +2Na →2CH3CH2ONa +H2↑
2)乙醇的消去反应
1) 乙醇与钠反应
现象:缓慢产生气泡,金属钠沉于底部或上下浮动。
产物乙醇钠在水中强烈水解
CH3CH2-ONa +H2O→CH3CH2OH +NaOH
练习:写出乙醇与K、Ca分别反应的化学方程式
P.49思考与交流
②
①
③
④
实验装置及注意事项
实验3-1
1)反应温度:170℃ 2)加碎瓷片
3)V乙醇:V浓硫酸=1:3 4)检查气密性
注意事项:
可能产生的现象分析
题外话:分子间脱水
3)乙醇与氢卤酸的取代反应
2CH3CH2-OH CH3CH2-O-CH2CH3+H2O
140℃
浓H2SO4
②
①
③
④
2CH3CH2-OH+HBr CH3CH2Br+H2O
△
4)乙醇的氧化反应
乙醇能不能被其他氧化剂氧化?
实验3-2
怎样制备无水乙醇
CH3CH2-OH
CH3CHO
CH3COOH
[O]
[O]
CH3CH2-ONa
乙醇的氧化反应
CH3CH2-Br
CH2=CH2
CH3CH2-O-CH2CH3
乙醇的化学性质小结
Na
H2O
HBr
NaOH水溶液
浓H2SO4
170℃
浓H2SO4
140℃
CH3C-O-CH2CH3
O
4、乙醇的工业制法?
5、醇的化学性质——与乙醇相似
1.什么是酚
羟基与芳香烃侧链上的碳原子相连,其化合物是芳香醇。
练习:判断下列物质哪种是酚类?
羟基与苯环上的碳原子直接相连,其化合物则是酚。
思考:相同碳原子个数的芳香醇与酚类是什么关系?
2、试推导饱和一元酚的通式,并思考符合此通式的还有什么物质?
(同分异构体)
CnH2n-6O
二、酚
1、苯酚的结构和物理性质
无色晶体,有特殊气味,在空气中易被氧化而呈粉红色,熔点低(43℃) 。常温下在水中溶解度不大(9.3g),加热时易溶(>65℃时任意比溶)于水,易溶于乙醇等有机溶剂,有毒,有腐蚀性 。
如不慎沾到皮肤上应立即用酒精洗涤。
2、苯酚的化学性质:
1)苯酚的酸性:(实验探究3-3)
填表P.53
OH
OH
ONa
+NaOH
+H2O
为什么?
图3-7现象有误
2)苯酚与浓溴水的反应——取代反应
实验探究:实验3-4
苯酚的酸性比碳酸的还弱,但比HCO3-强。
(石炭酸)
结论:苯环影响了-OH的活性
结论:-OH影响了苯环的活性
用于苯酚的检验和测定
P.54 学与问
现象P.54图3-9
4)加成反应——与H2加成
1、为什么苯和苯酚发生溴代反应的条件和产物有很大的不同?
2、实验表明,苯酚的酸性比乙醇强。
3)苯酚的显色反应:
+Fe3+
OH
6
[Fe(C6H5O)6]3-
+6H+
5)氧化反应
OH
(易燃)
=O
=
O
在与醇相似的条件下,苯酚不能发生酯化反应。
注意:
苯酚的用途:
化工原料,制酚醛树脂、医药、染料等,稀溶液用作防腐剂和消毒剂
小结:
