3.5《归纳与整理-第三章全章知识复习》PPT课件(新人教版-选修5)
文档属性
| 名称 | 3.5《归纳与整理-第三章全章知识复习》PPT课件(新人教版-选修5) |

|
|
| 格式 | zip | ||
| 文件大小 | 198.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-12 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
新课标人教版课件系列
《高中化学》
选修5
2.5《归纳与整理-
第三章全章知识复习》
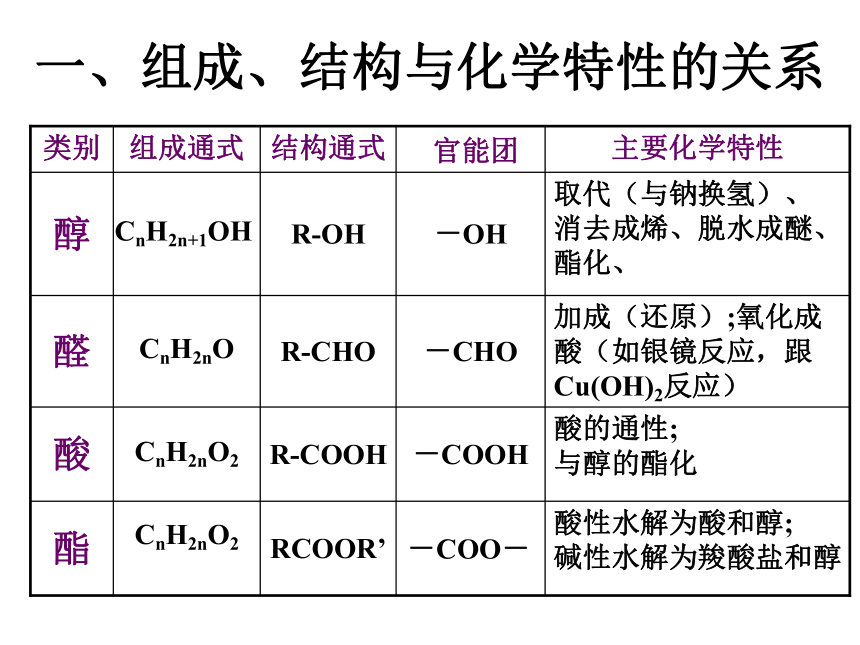
一、组成、结构与化学特性的关系
酸的通性;
与醇的酯化
-COOH
R-COOH
CnH2nO2
酸
酸性水解为酸和醇;
碱性水解为羧酸盐和醇
-COO-
RCOOR’
CnH2nO2
酯
加成(还原);氧化成酸(如银镜反应,跟Cu(OH)2反应)
-CHO
R-CHO
CnH2nO
醛
取代(与钠换氢)、
消去成烯、脱水成醚、酯化、
-OH
R-OH
CnH2n+1OH
醇
主要化学特性
官能团
结构通式
组成通式
类别
二、有机物的几点特性:
1、能使酸性KMnO4褪色的有机物:
2、因化学反应能使溴水褪色的有机物:
3、互为类别异构的物质:
烯烃、炔烃、苯的同系物、 苯酚、 醇、醛、裂化汽油。
烯烃、炔烃、苯酚、醛 裂化汽油。
单烯烃与环烷烃(CnH2n) 二烯烃与炔烃(CnH2n-2)
醇与醚(CnH2n+2O) 苯酚与芳香醇、
醛与酮(CnH2nO) 羧酸与酯(CnH2nO2)
5、能发生银镜反应的有机物:
醛、甲酸、甲酸盐、甲酸酯等。
4、实验中用到浓硫酸的反应及其作用:
实验室制乙烯——催化剂、脱水剂
硝化反应——催化剂、吸水剂
磺化反应——反应物、吸水剂
酯化反应——催化剂、吸水剂
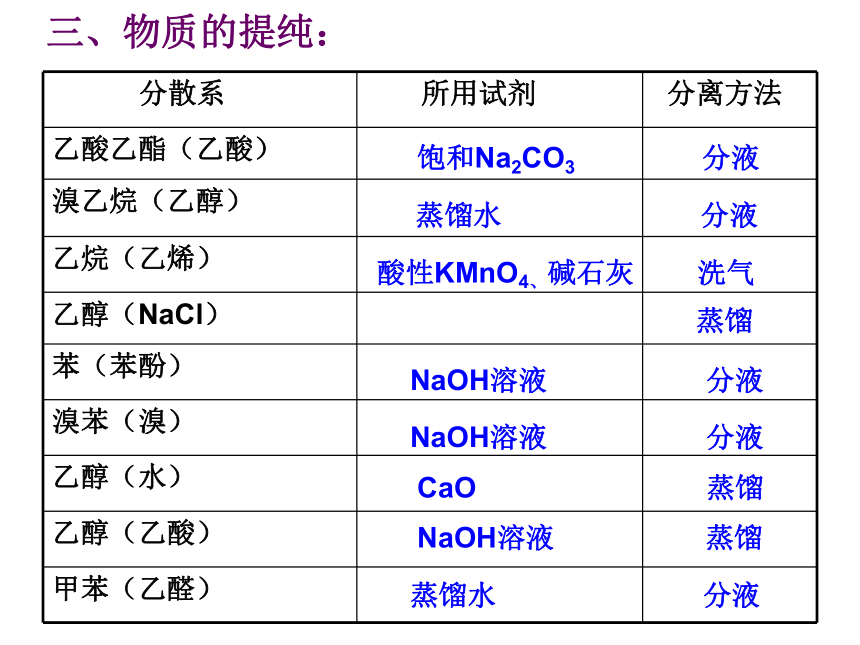
分散系 所用试剂 分离方法
乙酸乙酯(乙酸)
溴乙烷(乙醇)
乙烷(乙烯)
乙醇(NaCl)
苯(苯酚)
溴苯(溴)
乙醇(水)
乙醇(乙酸)
甲苯(乙醛)
三、物质的提纯:
饱和Na2CO3 分液
蒸馏水 分液
酸性KMnO4、碱石灰 洗气
蒸馏
NaOH溶液 分液
NaOH溶液 分液
CaO 蒸馏
蒸馏水 分液
NaOH溶液 蒸馏
7. (1)先分别加入Cu(OH)2,加热,有红色沉淀生成的为甲醛溶液;取另四种物质,通入或加入溴水,褪色的为乙烯,出现白色沉淀的为苯酚;余下的加入重铬酸钾酸性溶液,振荡后变色的为乙醇,不变的为苯。
(2)方程式略。
复习题参考答案
1.D 2.B 3.A、B 4.A 5.B 6.C
8.CH2=CH-COOH
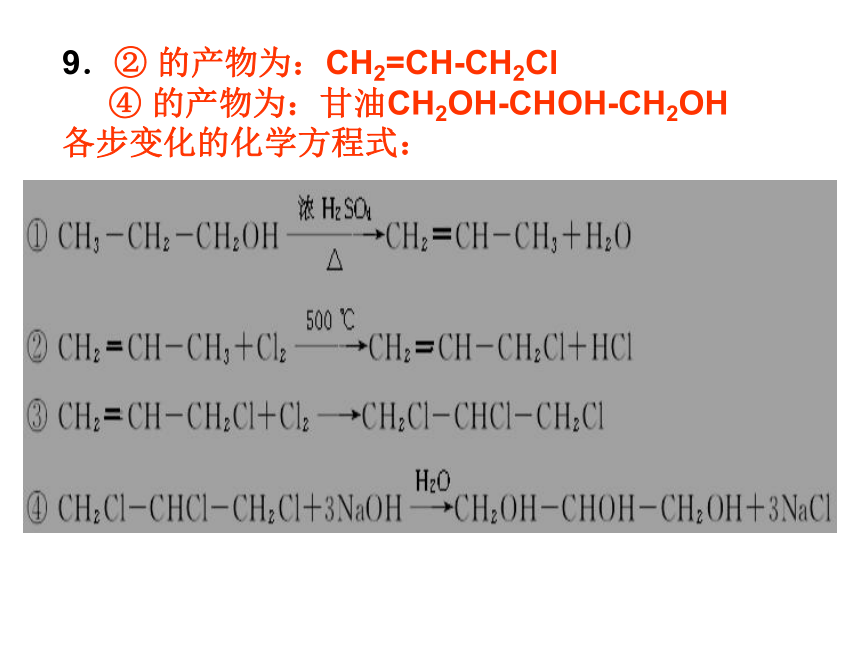
9.② 的产物为:CH2=CH-CH2Cl
④ 的产物为:甘油CH2OH-CHOH-CH2OH
各步变化的化学方程式:
如果在制取丙烯时所用的1-丙醇中混有2-丙醇,对所制丙烯的纯度没有影响。因为二者在发生消去反应时的产物都是丙烯。
10.A:CH3CH2OH 乙醇 B:CH2=CH2 乙烯
C:CH3CH2Br 溴乙烷
催化剂
复习课
第三章 烃的含氧衍生物
一、烃的各类衍生物的重要性质
类别 通式 官能团 代表性物质 分子结构特点 主要化学性质
卤代烃 R—X
—X
卤原子 溴乙烷
C2H5Br C—Br
易断裂 1、取代反应:与NaOH水溶液反应生成醇。
2、消去反应:与强碱的乙醇溶液共热,脱去卤代氢,生成烯烃。
醇 R—OH —OH
羟基 乙醇C2H5OH —OH与链烃基相连, C—O键和O—H键易断裂 1、跟金属钠反应。
2、跟氢卤酸反应。
3、分子间脱水。
4、分子内脱水。
5、氧化反应。
6、酯化反应。
类别 通式 官能团 代表性物质 分子结构特点 主要化学性质
酚 —OH —OH直接跟苯环相连 1、弱酸性:与强碱溶液反应,生成苯酚盐和水。
2、取代反应:跟浓溴水反应。
3、显色反应:跟铁盐反应,生成紫色物质。
醛 R—CHO —CHO
醛基 乙醛CH3—CHO —CHO具有不饱和性和还原性 1、加成反应:加氢生成乙醇。
2、具有还原性:能被弱氧化剂氧化成羧酸(如:银镜反应)
OH
类别 通式 官能团 代表性物质 分子结构特点 主要化学性质
羧酸 R—COOH —COOH
羧基 乙酸 受C=O双键影响,O—H能够电离,产生H+ 1、具有酸类通性。
2、能起酯化反应。
酯 R—COOR —COOR
酯基 乙酸乙酯 分子中RCO和OR 之间的键容易断裂 发生水解反应,生成羧酸和醇
二、有机反应的主要类型
1、取代反应:有机物分子中某些原子或原子团
被其它原子或原子团所代替的反应。
取代反应包括卤代、硝化、磺化、水解、酯化等反应类型。
①是原子或原子团与另一原子或原子团的交换;
②两种物质反应,生成两种物质,有进有出的;
③该反应前后的有机物的空间结构没有发生变化;
④取代反应总是发生在单键上;
⑤这是饱和化合物的特有反应。
2、加成反应:有机物分子中未饱和的碳原子跟其它原子或原子团直接结合生成别的物质的反应。
加成反应试剂包括H2、X2(卤素)、HX、HCN等。
①加成反应发生在不饱和 碳 原子上;
②该反应中加进原子或原子团,只生成一种有机物 相当于化合反应),只进不出。
③加成前后的有机物的结构将发生变化,烯烃变烷烃,结构由平面形变立体形;炔烃变烯烃,结构由直线形变平面形;
④加成反应是不饱和化合物的较特有反应,另外,芳香族化合物也有可能发生加成反应。
3、消去反应:有机物在一定条件下,从一个分子中脱去一个小分子(如:H2O、HX、NH3等)生成不饱和化合物的反应(消去小分子)。
①消去反应发生在分子内;
②发生在相邻的两个碳原子上;
③消去反应会脱去小分子,即生成小分子;
④消去后生成的有机物会产生双键或叁键;
⑤消去前后的有机物的分子结构变发生变化,它与加成反应相反,因此,分子结构的变化正好与加成反应的情况相反。
4、氧化反应:有机物得氧或失氢的反应。
氧化反应包括:
(1)烃和烃的衍生物的燃烧反应;
(2)烯烃、炔烃、二烯烃、苯的同系物、醇、醛等与酸性高锰酸钾反应;
(3)醇氧化为醛和酮;
(4)醛氧化为羧酸等反应。
5、还原反应:有机物加氢或去氧的反应。
6、加聚反应:通过加成反应聚合成高分子化合物的反应(加成聚合)。主要为含双键的单体聚合。
7、缩合(聚)反应:单体间通过缩合反应生成高分子化合物,同时生成小分子(H2O、NH3、HX等)的反应。
缩聚反应主要包括:醇酸缩聚、羟酸缩聚、氨基酸缩聚等。
8、酯化反应(属于取代反应):酸(有机羧酸、无机含氧酸)与醇作用生成酯和水的反应。
9、水解反应:有机物在一定条件下跟水作用
生成两种或多种物质的反应。
水解反应包括卤代烃水解、酯水解、糖(除单糖外)水解、蛋白质水解等。
10、裂化反应:在一定温度下,把相对分子质量大、沸点高的长链烃断裂为相对分子质量小、沸点低的短链烃的反应。
三、有机反应的官能团
有机物
无机物/有机物
反应名称
烷,芳烃,酚
X2
卤代反应
苯的同系物
HNO3
硝化反应
苯的同系物
H2SO4
磺化反应
醇
醇
脱水反应
醇
HX
取代反应
酸
醇
酯化反应
酯
醇
酯交换反应
酯/卤代烃
酸溶液或碱溶液
水解反应
二糖多糖
H2O
水解反应
蛋白质
H2O
水解反应
羧 酸 盐
碱石灰
脱羧反应
1、发生取代反应的基/官能团
结构变化形式 —— 等 价 替 换
2、发生加成反应的官能团
官能团 C=C C C -CHO -C=O C6H5-
有 机 物
反应条件
C
O
-OH
C
O
-H
C
O
-O-
C
O
-
-
3、发生氧化反应的官能团
C=C C C C-OH CHO C6H5-R CH3CH2CH2CH3
试剂
条件
产物
-CH2OH -CHO为脱氢重键式
-CHO -COOH为氧原子插入式
反应条件 常 见 反 应
催化剂
加热加压 乙烯水化、乙烯氧化、丁烷氧化、
氯苯水解、油脂氢化
催化剂
加热 烯炔醛酮加氢、乙醇消去、
乙醇氧化、酯化反应
水浴加热 C6H5NO2制备、银镜反应、树脂制备、纤维素水解、CH3COOC2H5水解
只用催化剂 苯的溴代、乙醛被空气氧化
只需加热 制CH4、苯的磺化、 R-OH的卤代
R-X水解和消去
不需外加
条件 烯与炔加溴、苯酚的取代
烯炔与苯的同系物氧化、
四、有机反应的条件
五、主要有机物之间的转化关系
还原
水
解
酯
化
酯
羧酸
醛
醇
卤代烃
氧化
氧化
水解
烯
烷
炔
加成
加成
加成
消去
取代
加成
消去
氧化
—CH2—CH2—
n
CH3—CH3
CH2==CH2
CH≡CH
CH3CH2Cl
CH3COOH
CH3CH2OH
CH3CHO
CH3COONa
CH2—CH2
—
—
Cl
Cl
CH2==CH
—
Cl
CH==CH
—
—
Cl
Cl
HC—CH
—
—
Cl
Cl
—
—
Cl
Cl
Br
OH
ONa
OH
Br
Br
Br
CH3COOCH2CH3
(1)
(2)
(3)
(4)
(5)
(6)
(8)
(7)
(9)
(10)
(11)
(12)
(13)
(14)
(15)
(16)
(17)
(18)
(19)
(20)
(21)
(22)
(23)
(24)
(25)
新课标人教版课件系列
《高中化学》
选修5
2.5《归纳与整理-
第三章全章知识复习》
一、组成、结构与化学特性的关系
酸的通性;
与醇的酯化
-COOH
R-COOH
CnH2nO2
酸
酸性水解为酸和醇;
碱性水解为羧酸盐和醇
-COO-
RCOOR’
CnH2nO2
酯
加成(还原);氧化成酸(如银镜反应,跟Cu(OH)2反应)
-CHO
R-CHO
CnH2nO
醛
取代(与钠换氢)、
消去成烯、脱水成醚、酯化、
-OH
R-OH
CnH2n+1OH
醇
主要化学特性
官能团
结构通式
组成通式
类别
二、有机物的几点特性:
1、能使酸性KMnO4褪色的有机物:
2、因化学反应能使溴水褪色的有机物:
3、互为类别异构的物质:
烯烃、炔烃、苯的同系物、 苯酚、 醇、醛、裂化汽油。
烯烃、炔烃、苯酚、醛 裂化汽油。
单烯烃与环烷烃(CnH2n) 二烯烃与炔烃(CnH2n-2)
醇与醚(CnH2n+2O) 苯酚与芳香醇、
醛与酮(CnH2nO) 羧酸与酯(CnH2nO2)
5、能发生银镜反应的有机物:
醛、甲酸、甲酸盐、甲酸酯等。
4、实验中用到浓硫酸的反应及其作用:
实验室制乙烯——催化剂、脱水剂
硝化反应——催化剂、吸水剂
磺化反应——反应物、吸水剂
酯化反应——催化剂、吸水剂
分散系 所用试剂 分离方法
乙酸乙酯(乙酸)
溴乙烷(乙醇)
乙烷(乙烯)
乙醇(NaCl)
苯(苯酚)
溴苯(溴)
乙醇(水)
乙醇(乙酸)
甲苯(乙醛)
三、物质的提纯:
饱和Na2CO3 分液
蒸馏水 分液
酸性KMnO4、碱石灰 洗气
蒸馏
NaOH溶液 分液
NaOH溶液 分液
CaO 蒸馏
蒸馏水 分液
NaOH溶液 蒸馏
7. (1)先分别加入Cu(OH)2,加热,有红色沉淀生成的为甲醛溶液;取另四种物质,通入或加入溴水,褪色的为乙烯,出现白色沉淀的为苯酚;余下的加入重铬酸钾酸性溶液,振荡后变色的为乙醇,不变的为苯。
(2)方程式略。
复习题参考答案
1.D 2.B 3.A、B 4.A 5.B 6.C
8.CH2=CH-COOH
9.② 的产物为:CH2=CH-CH2Cl
④ 的产物为:甘油CH2OH-CHOH-CH2OH
各步变化的化学方程式:
如果在制取丙烯时所用的1-丙醇中混有2-丙醇,对所制丙烯的纯度没有影响。因为二者在发生消去反应时的产物都是丙烯。
10.A:CH3CH2OH 乙醇 B:CH2=CH2 乙烯
C:CH3CH2Br 溴乙烷
催化剂
复习课
第三章 烃的含氧衍生物
一、烃的各类衍生物的重要性质
类别 通式 官能团 代表性物质 分子结构特点 主要化学性质
卤代烃 R—X
—X
卤原子 溴乙烷
C2H5Br C—Br
易断裂 1、取代反应:与NaOH水溶液反应生成醇。
2、消去反应:与强碱的乙醇溶液共热,脱去卤代氢,生成烯烃。
醇 R—OH —OH
羟基 乙醇C2H5OH —OH与链烃基相连, C—O键和O—H键易断裂 1、跟金属钠反应。
2、跟氢卤酸反应。
3、分子间脱水。
4、分子内脱水。
5、氧化反应。
6、酯化反应。
类别 通式 官能团 代表性物质 分子结构特点 主要化学性质
酚 —OH —OH直接跟苯环相连 1、弱酸性:与强碱溶液反应,生成苯酚盐和水。
2、取代反应:跟浓溴水反应。
3、显色反应:跟铁盐反应,生成紫色物质。
醛 R—CHO —CHO
醛基 乙醛CH3—CHO —CHO具有不饱和性和还原性 1、加成反应:加氢生成乙醇。
2、具有还原性:能被弱氧化剂氧化成羧酸(如:银镜反应)
OH
类别 通式 官能团 代表性物质 分子结构特点 主要化学性质
羧酸 R—COOH —COOH
羧基 乙酸 受C=O双键影响,O—H能够电离,产生H+ 1、具有酸类通性。
2、能起酯化反应。
酯 R—COOR —COOR
酯基 乙酸乙酯 分子中RCO和OR 之间的键容易断裂 发生水解反应,生成羧酸和醇
二、有机反应的主要类型
1、取代反应:有机物分子中某些原子或原子团
被其它原子或原子团所代替的反应。
取代反应包括卤代、硝化、磺化、水解、酯化等反应类型。
①是原子或原子团与另一原子或原子团的交换;
②两种物质反应,生成两种物质,有进有出的;
③该反应前后的有机物的空间结构没有发生变化;
④取代反应总是发生在单键上;
⑤这是饱和化合物的特有反应。
2、加成反应:有机物分子中未饱和的碳原子跟其它原子或原子团直接结合生成别的物质的反应。
加成反应试剂包括H2、X2(卤素)、HX、HCN等。
①加成反应发生在不饱和 碳 原子上;
②该反应中加进原子或原子团,只生成一种有机物 相当于化合反应),只进不出。
③加成前后的有机物的结构将发生变化,烯烃变烷烃,结构由平面形变立体形;炔烃变烯烃,结构由直线形变平面形;
④加成反应是不饱和化合物的较特有反应,另外,芳香族化合物也有可能发生加成反应。
3、消去反应:有机物在一定条件下,从一个分子中脱去一个小分子(如:H2O、HX、NH3等)生成不饱和化合物的反应(消去小分子)。
①消去反应发生在分子内;
②发生在相邻的两个碳原子上;
③消去反应会脱去小分子,即生成小分子;
④消去后生成的有机物会产生双键或叁键;
⑤消去前后的有机物的分子结构变发生变化,它与加成反应相反,因此,分子结构的变化正好与加成反应的情况相反。
4、氧化反应:有机物得氧或失氢的反应。
氧化反应包括:
(1)烃和烃的衍生物的燃烧反应;
(2)烯烃、炔烃、二烯烃、苯的同系物、醇、醛等与酸性高锰酸钾反应;
(3)醇氧化为醛和酮;
(4)醛氧化为羧酸等反应。
5、还原反应:有机物加氢或去氧的反应。
6、加聚反应:通过加成反应聚合成高分子化合物的反应(加成聚合)。主要为含双键的单体聚合。
7、缩合(聚)反应:单体间通过缩合反应生成高分子化合物,同时生成小分子(H2O、NH3、HX等)的反应。
缩聚反应主要包括:醇酸缩聚、羟酸缩聚、氨基酸缩聚等。
8、酯化反应(属于取代反应):酸(有机羧酸、无机含氧酸)与醇作用生成酯和水的反应。
9、水解反应:有机物在一定条件下跟水作用
生成两种或多种物质的反应。
水解反应包括卤代烃水解、酯水解、糖(除单糖外)水解、蛋白质水解等。
10、裂化反应:在一定温度下,把相对分子质量大、沸点高的长链烃断裂为相对分子质量小、沸点低的短链烃的反应。
三、有机反应的官能团
有机物
无机物/有机物
反应名称
烷,芳烃,酚
X2
卤代反应
苯的同系物
HNO3
硝化反应
苯的同系物
H2SO4
磺化反应
醇
醇
脱水反应
醇
HX
取代反应
酸
醇
酯化反应
酯
醇
酯交换反应
酯/卤代烃
酸溶液或碱溶液
水解反应
二糖多糖
H2O
水解反应
蛋白质
H2O
水解反应
羧 酸 盐
碱石灰
脱羧反应
1、发生取代反应的基/官能团
结构变化形式 —— 等 价 替 换
2、发生加成反应的官能团
官能团 C=C C C -CHO -C=O C6H5-
有 机 物
反应条件
C
O
-OH
C
O
-H
C
O
-O-
C
O
-
-
3、发生氧化反应的官能团
C=C C C C-OH CHO C6H5-R CH3CH2CH2CH3
试剂
条件
产物
-CH2OH -CHO为脱氢重键式
-CHO -COOH为氧原子插入式
反应条件 常 见 反 应
催化剂
加热加压 乙烯水化、乙烯氧化、丁烷氧化、
氯苯水解、油脂氢化
催化剂
加热 烯炔醛酮加氢、乙醇消去、
乙醇氧化、酯化反应
水浴加热 C6H5NO2制备、银镜反应、树脂制备、纤维素水解、CH3COOC2H5水解
只用催化剂 苯的溴代、乙醛被空气氧化
只需加热 制CH4、苯的磺化、 R-OH的卤代
R-X水解和消去
不需外加
条件 烯与炔加溴、苯酚的取代
烯炔与苯的同系物氧化、
四、有机反应的条件
五、主要有机物之间的转化关系
还原
水
解
酯
化
酯
羧酸
醛
醇
卤代烃
氧化
氧化
水解
烯
烷
炔
加成
加成
加成
消去
取代
加成
消去
氧化
—CH2—CH2—
n
CH3—CH3
CH2==CH2
CH≡CH
CH3CH2Cl
CH3COOH
CH3CH2OH
CH3CHO
CH3COONa
CH2—CH2
—
—
Cl
Cl
CH2==CH
—
Cl
CH==CH
—
—
Cl
Cl
HC—CH
—
—
Cl
Cl
—
—
Cl
Cl
Br
OH
ONa
OH
Br
Br
Br
CH3COOCH2CH3
(1)
(2)
(3)
(4)
(5)
(6)
(8)
(7)
(9)
(10)
(11)
(12)
(13)
(14)
(15)
(16)
(17)
(18)
(19)
(20)
(21)
(22)
(23)
(24)
(25)
