4.0《生命中的基础有机化学物质》PPT课件(新人教版-选修5)
文档属性
| 名称 | 4.0《生命中的基础有机化学物质》PPT课件(新人教版-选修5) |

|
|
| 格式 | zip | ||
| 文件大小 | 1023.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-12 00:00:00 | ||
图片预览







文档简介
(共75张PPT)
新课标人教版课件系列
《高中化学》
选修5
第四章
《生命中的基础有机
化学物质》
第二章 分子结构与性质
第一节
《油脂》
第四章 生命中的基础有机化学物质
一、油脂的组成和结构:
油脂是由多种高级脂肪酸如硬脂酸、软脂酸或油酸等跟甘油生成的甘油酯。
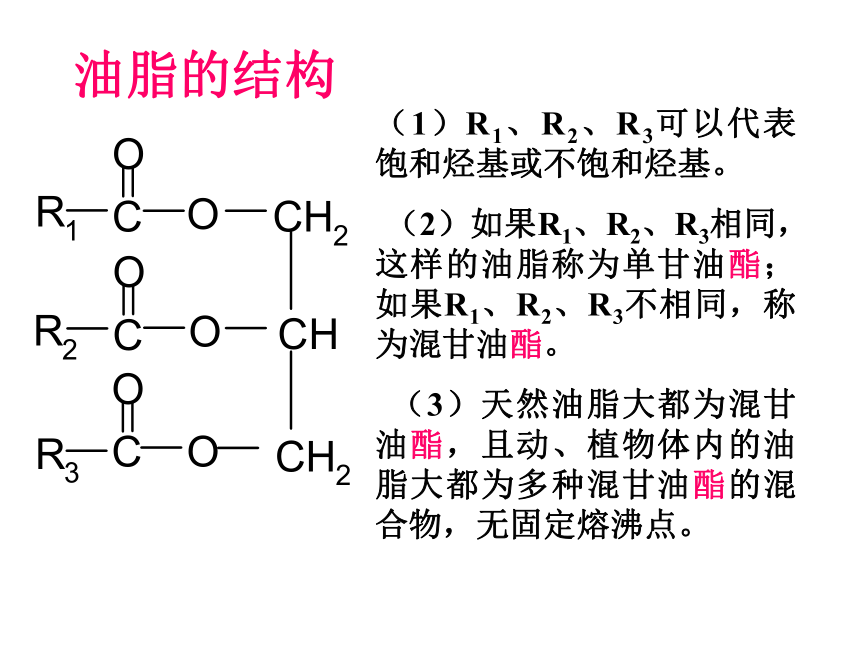
油脂的结构
(1)R1、R2、R3可以代表饱和烃基或不饱和烃基。
(2)如果R1、R2、R3相同,这样的油脂称为单甘油酯;如果R1、R2、R3不相同,称为混甘油酯。
(3)天然油脂大都为混甘油酯,且动、植物体内的油脂大都为多种混甘油酯的混合物,无固定熔沸点。
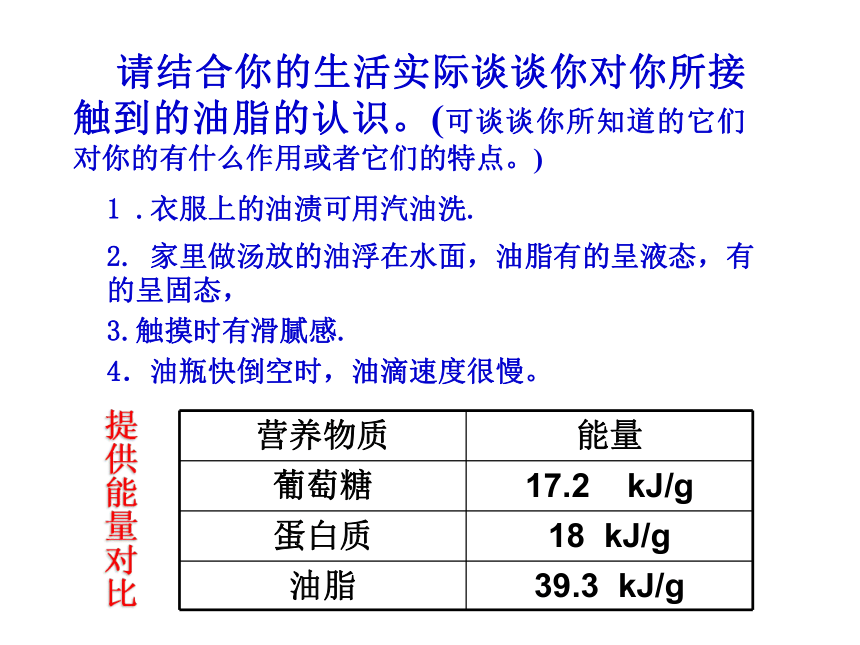
营养物质 能量
葡萄糖 17.2 kJ/g
蛋白质 18 kJ/g
油脂 39.3 kJ/g
1 .衣服上的油渍可用汽油洗.
2. 家里做汤放的油浮在水面,油脂有的呈液态,有的呈固态,
3.触摸时有滑腻感.
4.油瓶快倒空时,油滴速度很慢。
提供能量对比
请结合你的生活实际谈谈你对你所接触到的油脂的认识。(可谈谈你所知道的它们对你的有什么作用或者它们的特点。)
二、油脂的物理性质
1.密度比水的密度小,为0.9~0.95g/cm3
2.有明显的油腻感
3.不溶于水,易溶于有机溶剂
4.是一种良好的有机溶剂
5.当高级脂肪酸中烯烃基多时大多为液态的油;当高级脂肪酸中烷烃基多时,大多为固态的脂肪。
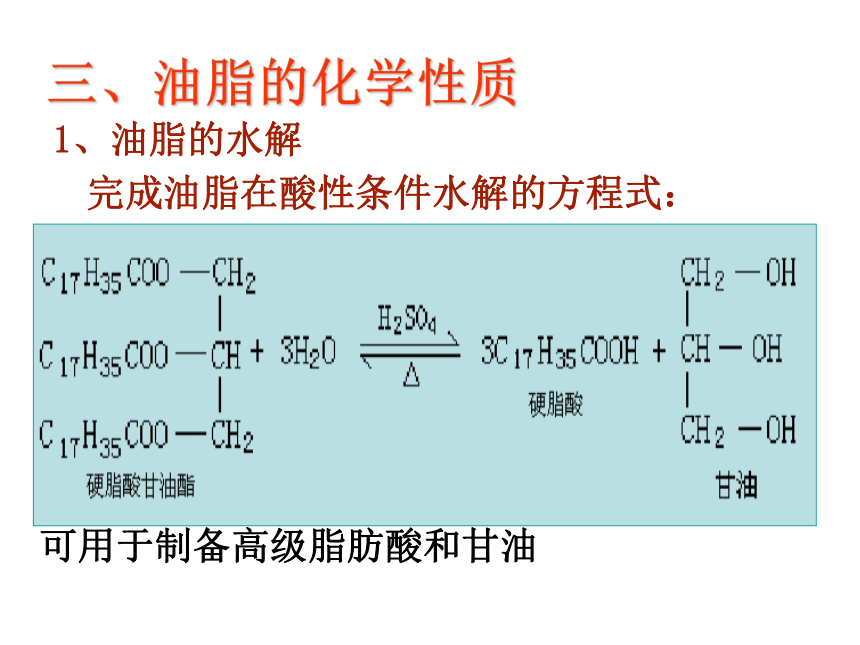
1、油脂的水解
完成油脂在酸性条件水解的方程式:
可用于制备高级脂肪酸和甘油
三、油脂的化学性质
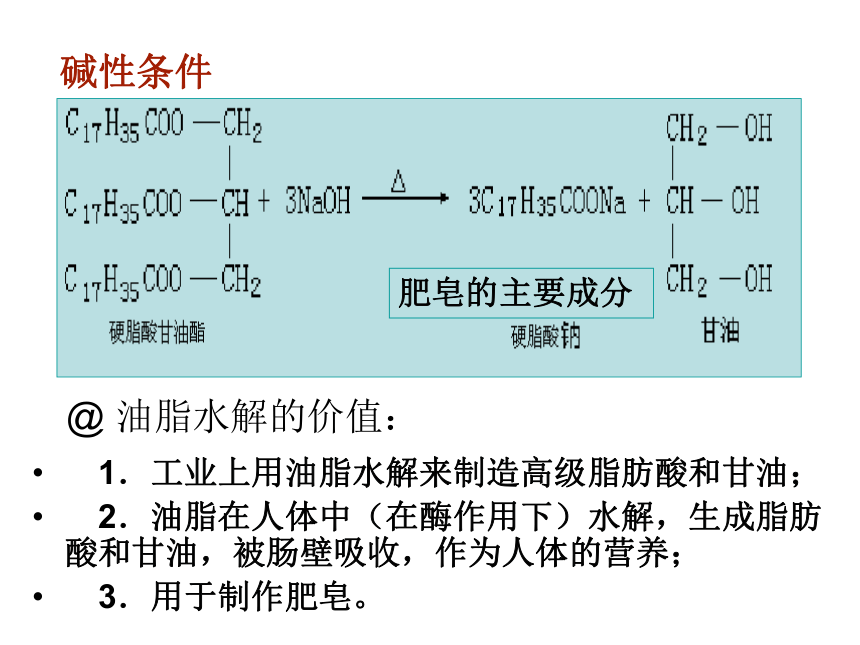
碱性条件
肥皂的主要成分
@ 油脂水解的价值:
1.工业上用油脂水解来制造高级脂肪酸和甘油;
2.油脂在人体中(在酶作用下)水解,生成脂肪酸和甘油,被肠壁吸收,作为人体的营养;
3.用于制作肥皂。
1.肥皂的制取
把动物脂肪或植物油NaOH溶液按一定比例放在皂化锅内,加热、搅拌使之发生皂化反应;
往锅内加入食盐,使生成物高级脂肪酸钠从甘油和水的混合物中分离析出(盐析);
集取浮在液面的高级脂肪酸钠,加入填充剂,进行压滤、干燥、成型,就制成成品肥皂;
下层液体经分离提纯后,便得到甘油。
肥皂和洗涤剂
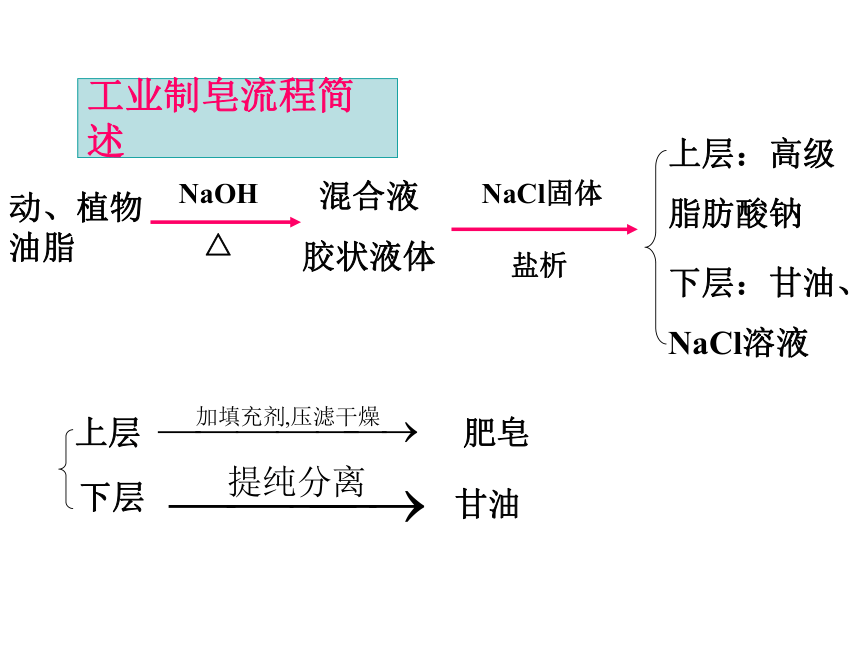
工业制皂流程简述
动、植物油脂
混合液
胶状液体
上层:高级
脂肪酸钠
下层:甘油、
NaCl溶液
上层
肥皂
下层
甘油
NaOH
△
NaCl固体
盐析
练习
(1)在硬水中滴加少量肥皂水,为什么会有白色沉淀产生?
答:硬水中的Ca2+或Mg2+跟肥皂的主要成分硬脂酸钠起反应生成硬脂酸钙[Ca (c17H35COO)2]或硬脂酸镁[Mg (C17H35COO)2]沉淀。
(2)在日常生活中为什么常用热的纯碱溶液洗涤沾有油脂的器皿?
答:热的纯碱溶液呈碱性,油脂在碱性溶液中能水解生成溶于水的高级脂肪酸钠盐和甘油。
2.肥皂的去污原理
(1)亲水基--肥皂结构中-COONa或-COO-是极性基团,极易溶于水,具有亲水性;
(2)憎水基--肥皂结构中的烃基-R,不溶于,但极易溶于有机溶剂,具有亲油性质;
(3)肥皂的去污过程
①. 合成洗涤剂的组成:由憎水基和亲水基组成,如:
烷基苯磺酸钠
烷基磺酸钠
3.合成洗涤剂
②.合成洗涤剂与肥皂的比较
(1)肥皂不适合在硬水中使用,而合成洗涤剂使用不受限制;
(2)合成洗涤剂洗涤能力强,可以用于洗衣机使用;
(3)合成洗涤剂的原料便宜。
(4)合成洗涤剂的危害:由于其稳定性,在自然界中不易被细菌分解,造成水体污染。尤其含磷洗涤剂造成水体富营养。
油脂的结构决定其性质: 1.油脂是高级脂肪酸的甘油酯,所以具有酯的性质——能在催化剂存在条件下水解;由不饱和高级脂肪酸所生成的油脂还具有烯烃的性质。 2.油脂中高级脂肪酸的饱和程度越大,其熔点越高,影响着油脂的存在状态
性质决定用途:
1、氢化:制人造奶油
2、酸性水解:甘油、高级脂肪酸
3、碱性水解: 肥皂等。
课堂小结:
三、油脂的化学性质
2.油脂的氢化
(油脂的硬化)
2、与H2加成—油脂的氢化
工业应用:把多种植物油转变成硬化油。
油脂的硬化
1.硬化油的特性:
(1)油脂氢化得到的硬化油,就是人造脂肪,也叫硬化油;
(2)硬化油性质稳定,不易变质(为什么?);
(3)硬化油便于运输;
(4)用于制肥皂、脂肪酸、甘油、人造奶油等的原料。
(油)
(脂肪)
[课堂小结]
油脂
油
脂肪
结构
性质
水解
氢化
用途
酯
碳碳双键
食物、制肥皂、甘油、人造奶油等
练习:
1、下列物质不属于酯类的是( )
A.花生油 B.硝化甘油
C.酚醛树脂 D.醋酸纤维
2、下列各组中属于同系物的是( )
A.乙二醇、丙三醇 B.油酸、丙烯酸
C.三乙酸甘油酯、硬脂酸甘油酯
D.甲酸乙酯、乙酸甲酯
C
BC
练 习
3、在日常生活中为什么常用热的老碱溶液洗涤沾有油脂的器皿?
(1999年广东高考题)
4、下列叙述中正确的是( )
A.牛油是纯净物
B.牛油是高级脂肪酸的高级醇酯
C.牛油可以在碱性条件下加热水解
D.工业上将牛油加氢制造硬化油
C
5、可以判断油脂皂化反应基本完成的现象是( )
A.反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D. 反应后静置,反应液不分层
(2000年广东高考题)
练 习
D
练习:
2、“花生油属于纯净物”这种说法对不对?
3、工业上如何从植物的种子中提取油和分离油的?
1、请写出硬脂酸、软脂酸与甘油反应的化学方程式。
第二章 分子结构与性质
第二节
《糖 类》
第四章 生命中的基础有机化学物质
糖 类
一、糖类具有怎样的特征?
绿色植物光合反应的产物
由C、H、O元素组成
常用通式Cn(H2O)m来表示
二、糖类如何分类?
单糖(不能水解成更简单的糖)
二糖(1mol水解产生2mol单糖)
多糖(1mol水解产生多摩单糖)
-葡萄糖、果糖
-麦芽糖、蔗糖
-淀粉、纤维素
[阅读课本]思考下列问题:
一、葡萄糖与果糖
根据下列信息推出葡萄糖的分子组成
葡萄糖的相对分子质量为180,其中
含碳40%,氢6.7%,其余是氧。求分子
式。
葡萄糖分子式:C6H12O6
1、葡萄糖
白色晶体、有甜味、能溶于水
(1)物理性质
根据下列信息推出葡萄糖的分子结构:
1、在一定条件下,1mol葡萄糖与1molH2反应,还原成己六醇
2、 葡萄糖能发生酯化反应生成五乙酸葡萄糖(提示:同一个C原子上连接2个羟基不稳定)
3、 葡萄糖分子被氧化,碳链并不断裂,而是生含6个C原子的葡萄糖酸
说明分子中有双键,也说明是直链化合物
说明葡萄糖分子中有5个—OH,且分别连在5个C原子上
说明葡萄糖分子中含有一个—CHO
科学推理:
分子式:C6H12O6
(2)结构
结构简式:
CH2 CH CH CH CH CHO
OH
OH
OH
OH
OH
预测:葡萄糖的化学性质
1、葡萄糖
(3)化学性质:
银镜反应
与新制Cu(OH)2反应
与H2加成
② 羟基的性质:
③ 人体内氧化反应-人体能量主要来源:
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
①醛基的性质:
(4)用途
制药、制镜、制糖果
酯化
葡萄糖的性质
CH2OH(CHOH)4CHO + H2
CH2OH(CHOH)4CH2OH
催化剂
CH2OH(CHOH)4CHO+2 Ag(NH3)2OH
2Ag +CH2OH(CHOH)4COOH+4NH3 +H2O
CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O +2H2O
2、果糖:
分子式:C6H12O6
结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH
多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的影响有很强的还原性,所以果糖能被银氨溶液和新制氢氧化铜氧化。
在酸性条件下,果糖不被溴水氧化,可用溴水区分葡萄糖和果糖。
分子的手性
碳原子上连有四个不相同的原子或原子团,这样的碳原子叫做“不对称碳原子”,也叫做“手性分子”。
二、蔗糖 麦芽糖:
演示对比实验:
银氨溶液
银氨溶液
热水浴
热水浴
无现象
产生
银镜
热水浴
热水浴
20%蔗
糖溶液
20%麦芽糖溶液
无还原性
有还原性
蔗糖:
麦芽糖:
化学性质:
同分异构
演示对比实验:
热水浴
20%蔗
糖溶液
银氨溶液
热水浴
无现象
蔗糖 +
稀硫酸
热水浴
NaOH
中和酸
银氨溶液
热水浴
产生
银镜
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
二、蔗糖 麦芽糖:
二、蔗糖 麦芽糖:
葡萄糖 还原性糖
(有-CHO) 不能水解 单糖
蔗糖 非还原性糖
(无-CHO) 水解成一分子葡萄糖一分子果糖 二糖
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
●蔗糖与葡萄糖的比较:
二、蔗糖 麦芽糖:
●蔗糖与麦芽糖的比较:
蔗糖 C12H22O11
同分异构 非还原性糖
(无-CHO) 水解成一分子葡萄糖,一分子果糖 二糖
麦芽糖 还原性糖
(有-CHO) 水解成二分子葡萄糖 二糖
C12H22O11 + H2O 2 C6H12O6
(麦芽糖) (葡萄糖)
催化剂
三.淀粉与纤维素
1.淀粉
存在:存在于植物的种子和块根里。
结构:含有几百到几千个单糖单元(C6H10O5)。每个结构单元式量:162。相对分子质量从几万到几十万;属于天然有机高分子化合物
物质性质:白色、无气味、无味道的粉末状物质,不溶于冷水,在热水中产生糊化作用(即食物由生变熟的过程)
淀粉的化学性质
①通常淀粉不显还原性
②遇碘变蓝色
③淀粉在催化剂(如酸)存在和加热下可以逐步水解,生成一系列比淀粉分子小的化合物,最终生成还原性糖:葡萄糖。
(C6H10O5)n + n H2O n C6H12O6
淀粉 葡萄糖
催化剂
思考:解释为什么在吃馒头或米饭时,多加咀嚼就会感到有甜味?
答:淀粉在人体内进行水解。人在咀嚼馒头时,淀粉受唾液所含淀粉酶(一种蛋白质)的催化作用,开始水解,生成了一部分葡萄糖。
(淀粉在小肠里,在胰脏分泌出的淀粉酶的作用下,继续进行水解。生成的葡萄糖经过肠壁的吸收,进入血液,供人体组织的营养需要。)
淀粉的用途
(1)淀粉是食物的重要成分,是人体的重要能源;
(2)可用于制葡萄糖和酒精等;
(3)淀粉在淀粉酶的作用下,先转化为麦芽糖,再转化为葡萄糖,在酒化酶的作用下,转化为乙醇:
C6H12O6 2C2H5OH +2 CO2
催化剂
三.淀粉和纤维素
2.纤维素
存在:纤维素存在于一切植物中。是构成植物细胞壁的基础物质。
结构:分子中含有约几千个单糖单元(C6H10O5)n ;n为几千;属于天然高分子化合物;纤维素结构与淀粉不同,所以性质有差异。
纤维素的化学性质
不显还原性
可发生水解,但比淀粉水解困难
(C6H10H5)n + nH2O nC6H12O6(葡萄糖)
酯化反应
催化剂
△
纤维素的酯化反应
(C6H7O2)
O—NO2
O—NO2
O—NO2
n
(C6H7O2)
OH
OH
OH
n
3n HNO3
浓硫酸
3nH2O
+
+
纤维素硝酸酯
(硝酸纤维)
思考:如何设计实验检验纤维素水解已经开始?
答案:
取少量反应液,滴加几滴硫酸铜溶液,再加入过量的NaOH溶液,中和作催化剂的硫酸,一直加到出现Cu(OH)2沉淀,最后,加热煮沸,观察现象。如果出现红色沉淀,表明已经开始水解。
5.纤维素的用途
1、棉麻纤维大量用于纺织工业
2、木材、稻草、麦秸、蔗渣等用于造纸
3、制造纤维素硝酸酯(硝酸纤维)。根据含N量分为火棉(含N量较高,用于制造无烟火药)、胶棉(含N量较低,用于制赛璐璐和油漆)
4、制造纤维素乙酸酯(醋酸纤维),不易着火,用于制胶片
5、制造粘胶纤维(NaOH、CS2处理后所得,其中的长纤维称人造丝,短纤维称人造棉)
6、食物中的纤维素有利于人的消化。
糖的概念
具有多羟基醛或多羟基酮结构,以及能够水解生成它们的一类有机化合物叫做糖类,旧称碳水化合物,通式为Cm(H2O)n
分类及相互转化
低聚糖
单糖
多糖
水解
缩合
水解
缩聚
水解
缩合
(2~10)
( >10)
练一练:
1、下列物质具有相同的最简式的组是( )
A、乙醛 葡萄糖 B、乙酸 乙醛
C、乙醇 葡萄糖 D、甲酸甲酯 葡萄糖
2、葡萄糖所不具有的性质是( )
A、和H2发生加成反应
B、和银氨溶液发生氧化反应
C、和酸发生酯化反应
D、和NaOH溶液反应
D
D
第二章 分子结构与性质
第三节
蛋白质和核酸
第四章 生命中的基础有机化学物质
SARS病的凶手——冠状病毒, 有自己的核酸和蛋白质。它进入人体后,借助人体内的原料合成病毒。当我们人体发病时,就是它的蛋白质对我们起了作用。
SARS病毒的电子图片
蛋白质是最重要的营养物质
思考讨论:
1、蛋白质在人体内起什么作用?
(1)对生物反应起催化作用的:
(2)运输作用的:
(3)保护作用的:
(4)抵抗病毒、细菌作用的高度特异性蛋白:
(5)构成动物大部分结构的纤维物质:
酶
血红蛋白
毛发、皮肤、甲、壳等;
抗体
软骨、肌肉
“生命是蛋白质存在的方式”——恩格斯
思考讨论:
2、蛋白质在人体内是如何代谢的?
食物中的蛋白质→ 氨基酸→ 人体内多种蛋白质
3、蛋白质种类为何如此丰富(从结构方面)
蛋白质的基石——氨基酸
1、几种常见的氨基酸:
(1) 甘氨酸
(2) 丙氨酸
(3) 谷氨酸
CH2—COOH
NH2
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
一、氨基酸
羧酸分子里烃基上的氢原子被氨基取代后的生成物叫氨基酸。
什么是氨基酸?
天然蛋白质都是由多种α-氨基酸组成,天然蛋白质水解生成α-氨基酸。
2、氨基酸的性质
(1)既能与酸反应又能与碱反应
与氢氧化钠的反应:
NH2CH2COOH+NaOH→NH2CH2COO-Na++H2O
试写出与盐酸反应的化学方程式
NH2CH2COOH+HCl→Cl-+NH3CH2COOH
(2)成肽反应
2NH2CH2COOH→NH2CH2CONHCH2COOH+H2O
1.书写出乙酸与乙醇发生酯化反应的化学方程式。
2.书写出氨基乙酸与氨基乙酸脱水的方程式。
成肽反应
2NH2CH2COOH→
肽键
两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另一分子的羧基间脱去一分子水,缩合形成含有肽键的化合物,成为成肽反应。
二、蛋白质的结构与性质
蛋白质分子中含有C、O、H、N、S等元素。1965年我国科技工作者成功合成了具有生物活性的——结晶牛胰岛素。这是科学史上的一大成就,可以说是科学史上又一“丰碑”。
蛋白质是含氮生物高分子化合物,有C、H、0、N、S等元素,还有一些微量元素,构成的种类有10万种以上。
天然蛋白质的结构独特而稳定,按照氨基酸的连接方式分为:一级结构、二级结构、三级结构、四级结构。
蛋白质的一级、二级、三级结构
蛋白质的分子图象
蛋白质的空间结构
滴加 (NH4)2SO4
?
再加水
?
?
再加水
?
第一组
滴加乙醇溶液
?
再加水
?
第二组
滴加浓HNO3,微热
?
第三组
加热
?
再加水
?
灼烧 两样品(丝、棉),对比燃烧后产物状态及气味
滴加(CH3COO)2Pb溶液
溶液
滴加(NH4)2SO4
?
再加水
?
?
再加水
?
第一组
盐析 变性
涵义
可逆性
生理活性
一定条件下使蛋白质凝结为固体析出
一定条件下,蛋白质失去生理活性、溶解性降低
保持生理活性
失去生理活性
白色↓
白色↓
溶解
不溶解
加盐析出、加水溶解
——可逆
变性后、加水不溶解
——不可逆
滴加(CH3COO)2Pb溶液
溶液
滴加乙醇溶液
?
再加水
?
第二组
加热
?
再加水
?
白色↓
白色↓
不溶解
不溶解
思考讨论:
(1)你提倡用直发器加热的方法拉直头发吗?
加热使蛋白质变性在生活中最常见,试举例说明。
(2)为什么动物的皮经过药剂鞣制后,才能够成为加工皮革的原料。
第三组
灼烧 两样品(丝和棉),对比燃烧后产物状态及气味
黄色↓
滴加浓HNO3,微热
⑴ 为什么医院用高温蒸煮,照射紫外线,喷洒苯酚溶液,在伤口处涂抹酒精的方法来杀菌
⑵ 为什么生物实验室用甲醛溶液保存标本
⑶ 为什么在农业上用波尔多液(由硫酸铜,生石灰和水制成)来消灭害虫
⑷怎样鉴别丝织品和棉织品
请回答下列问题:
归纳蛋白质的性质:
3. 盐析:
1. 水溶性:有些可溶,有些难溶。
2. 水解:水解生成氨基酸。
4. 变性
5. 颜色反应
6. 灼烧产生烧焦羽毛的气味
CH2 C
NH2
O
N
CH2 COOH
H
三、酶
生物体、植物无时无刻都在进行着化学反应,并且这些反应在生物体存在的条件下进行,而且会随着环境、身体的情况而随时自动、精确的改变,是什么让这些反应可以实现的?
酶的催化特点:
1.条件温和,不需加热
2.具有高度的专一性
3.具有高效催化作用
四、核酸
核酸是一类含磷的高分子化合物,DNA就是其中组成,还有一种是RNA(核糖核酸),DNA和RNA互相作用合成蛋白质。
【练习】
1、下列过程中,不可逆的是( )
A.蛋白质的盐析 B.酯的水解
C.蛋白质白变性 D.氯化铁的水解
2、欲将蛋白质从水中析出而又不改变它的性 质应加入( )
A.甲醛溶液 B.CuSO4溶液
C.饱和Na2SO4溶液 D.浓硫酸
C
C
3、下图表示蛋白质分子结构的一部分,图中A、B、C、D标出了分子中不同的键,当蛋白质发生水解时,断裂的键是( )
C
4、为鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可选用的方法是( )
A、滴加浓硝酸 B、滴加浓硫酸
C、滴加酒精 D、灼烧
A、D
5、误食重金属盐会使人中毒,可以
用以解毒急救的措施是( )
A、服大量食盐水 B、服葡萄糖水
C、服鸡蛋清 D、服新鲜牛奶
C、D
6、蛋白质、淀粉、脂肪是三种重要的营养物质,其中______不是高分子化合物,这三种物质水解的最终产物分别是 蛋白质→________淀粉→_________; 脂肪→_________;在蛋白质水解的最终产物分子中,含有_________官能团。
*7、若将氨基乙酸和丙氨酸混合反应(在一定条件下)最多可得 种二肽。
新课标人教版课件系列
《高中化学》
选修5
第四章
《生命中的基础有机
化学物质》
第二章 分子结构与性质
第一节
《油脂》
第四章 生命中的基础有机化学物质
一、油脂的组成和结构:
油脂是由多种高级脂肪酸如硬脂酸、软脂酸或油酸等跟甘油生成的甘油酯。
油脂的结构
(1)R1、R2、R3可以代表饱和烃基或不饱和烃基。
(2)如果R1、R2、R3相同,这样的油脂称为单甘油酯;如果R1、R2、R3不相同,称为混甘油酯。
(3)天然油脂大都为混甘油酯,且动、植物体内的油脂大都为多种混甘油酯的混合物,无固定熔沸点。
营养物质 能量
葡萄糖 17.2 kJ/g
蛋白质 18 kJ/g
油脂 39.3 kJ/g
1 .衣服上的油渍可用汽油洗.
2. 家里做汤放的油浮在水面,油脂有的呈液态,有的呈固态,
3.触摸时有滑腻感.
4.油瓶快倒空时,油滴速度很慢。
提供能量对比
请结合你的生活实际谈谈你对你所接触到的油脂的认识。(可谈谈你所知道的它们对你的有什么作用或者它们的特点。)
二、油脂的物理性质
1.密度比水的密度小,为0.9~0.95g/cm3
2.有明显的油腻感
3.不溶于水,易溶于有机溶剂
4.是一种良好的有机溶剂
5.当高级脂肪酸中烯烃基多时大多为液态的油;当高级脂肪酸中烷烃基多时,大多为固态的脂肪。
1、油脂的水解
完成油脂在酸性条件水解的方程式:
可用于制备高级脂肪酸和甘油
三、油脂的化学性质
碱性条件
肥皂的主要成分
@ 油脂水解的价值:
1.工业上用油脂水解来制造高级脂肪酸和甘油;
2.油脂在人体中(在酶作用下)水解,生成脂肪酸和甘油,被肠壁吸收,作为人体的营养;
3.用于制作肥皂。
1.肥皂的制取
把动物脂肪或植物油NaOH溶液按一定比例放在皂化锅内,加热、搅拌使之发生皂化反应;
往锅内加入食盐,使生成物高级脂肪酸钠从甘油和水的混合物中分离析出(盐析);
集取浮在液面的高级脂肪酸钠,加入填充剂,进行压滤、干燥、成型,就制成成品肥皂;
下层液体经分离提纯后,便得到甘油。
肥皂和洗涤剂
工业制皂流程简述
动、植物油脂
混合液
胶状液体
上层:高级
脂肪酸钠
下层:甘油、
NaCl溶液
上层
肥皂
下层
甘油
NaOH
△
NaCl固体
盐析
练习
(1)在硬水中滴加少量肥皂水,为什么会有白色沉淀产生?
答:硬水中的Ca2+或Mg2+跟肥皂的主要成分硬脂酸钠起反应生成硬脂酸钙[Ca (c17H35COO)2]或硬脂酸镁[Mg (C17H35COO)2]沉淀。
(2)在日常生活中为什么常用热的纯碱溶液洗涤沾有油脂的器皿?
答:热的纯碱溶液呈碱性,油脂在碱性溶液中能水解生成溶于水的高级脂肪酸钠盐和甘油。
2.肥皂的去污原理
(1)亲水基--肥皂结构中-COONa或-COO-是极性基团,极易溶于水,具有亲水性;
(2)憎水基--肥皂结构中的烃基-R,不溶于,但极易溶于有机溶剂,具有亲油性质;
(3)肥皂的去污过程
①. 合成洗涤剂的组成:由憎水基和亲水基组成,如:
烷基苯磺酸钠
烷基磺酸钠
3.合成洗涤剂
②.合成洗涤剂与肥皂的比较
(1)肥皂不适合在硬水中使用,而合成洗涤剂使用不受限制;
(2)合成洗涤剂洗涤能力强,可以用于洗衣机使用;
(3)合成洗涤剂的原料便宜。
(4)合成洗涤剂的危害:由于其稳定性,在自然界中不易被细菌分解,造成水体污染。尤其含磷洗涤剂造成水体富营养。
油脂的结构决定其性质: 1.油脂是高级脂肪酸的甘油酯,所以具有酯的性质——能在催化剂存在条件下水解;由不饱和高级脂肪酸所生成的油脂还具有烯烃的性质。 2.油脂中高级脂肪酸的饱和程度越大,其熔点越高,影响着油脂的存在状态
性质决定用途:
1、氢化:制人造奶油
2、酸性水解:甘油、高级脂肪酸
3、碱性水解: 肥皂等。
课堂小结:
三、油脂的化学性质
2.油脂的氢化
(油脂的硬化)
2、与H2加成—油脂的氢化
工业应用:把多种植物油转变成硬化油。
油脂的硬化
1.硬化油的特性:
(1)油脂氢化得到的硬化油,就是人造脂肪,也叫硬化油;
(2)硬化油性质稳定,不易变质(为什么?);
(3)硬化油便于运输;
(4)用于制肥皂、脂肪酸、甘油、人造奶油等的原料。
(油)
(脂肪)
[课堂小结]
油脂
油
脂肪
结构
性质
水解
氢化
用途
酯
碳碳双键
食物、制肥皂、甘油、人造奶油等
练习:
1、下列物质不属于酯类的是( )
A.花生油 B.硝化甘油
C.酚醛树脂 D.醋酸纤维
2、下列各组中属于同系物的是( )
A.乙二醇、丙三醇 B.油酸、丙烯酸
C.三乙酸甘油酯、硬脂酸甘油酯
D.甲酸乙酯、乙酸甲酯
C
BC
练 习
3、在日常生活中为什么常用热的老碱溶液洗涤沾有油脂的器皿?
(1999年广东高考题)
4、下列叙述中正确的是( )
A.牛油是纯净物
B.牛油是高级脂肪酸的高级醇酯
C.牛油可以在碱性条件下加热水解
D.工业上将牛油加氢制造硬化油
C
5、可以判断油脂皂化反应基本完成的现象是( )
A.反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D. 反应后静置,反应液不分层
(2000年广东高考题)
练 习
D
练习:
2、“花生油属于纯净物”这种说法对不对?
3、工业上如何从植物的种子中提取油和分离油的?
1、请写出硬脂酸、软脂酸与甘油反应的化学方程式。
第二章 分子结构与性质
第二节
《糖 类》
第四章 生命中的基础有机化学物质
糖 类
一、糖类具有怎样的特征?
绿色植物光合反应的产物
由C、H、O元素组成
常用通式Cn(H2O)m来表示
二、糖类如何分类?
单糖(不能水解成更简单的糖)
二糖(1mol水解产生2mol单糖)
多糖(1mol水解产生多摩单糖)
-葡萄糖、果糖
-麦芽糖、蔗糖
-淀粉、纤维素
[阅读课本]思考下列问题:
一、葡萄糖与果糖
根据下列信息推出葡萄糖的分子组成
葡萄糖的相对分子质量为180,其中
含碳40%,氢6.7%,其余是氧。求分子
式。
葡萄糖分子式:C6H12O6
1、葡萄糖
白色晶体、有甜味、能溶于水
(1)物理性质
根据下列信息推出葡萄糖的分子结构:
1、在一定条件下,1mol葡萄糖与1molH2反应,还原成己六醇
2、 葡萄糖能发生酯化反应生成五乙酸葡萄糖(提示:同一个C原子上连接2个羟基不稳定)
3、 葡萄糖分子被氧化,碳链并不断裂,而是生含6个C原子的葡萄糖酸
说明分子中有双键,也说明是直链化合物
说明葡萄糖分子中有5个—OH,且分别连在5个C原子上
说明葡萄糖分子中含有一个—CHO
科学推理:
分子式:C6H12O6
(2)结构
结构简式:
CH2 CH CH CH CH CHO
OH
OH
OH
OH
OH
预测:葡萄糖的化学性质
1、葡萄糖
(3)化学性质:
银镜反应
与新制Cu(OH)2反应
与H2加成
② 羟基的性质:
③ 人体内氧化反应-人体能量主要来源:
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
①醛基的性质:
(4)用途
制药、制镜、制糖果
酯化
葡萄糖的性质
CH2OH(CHOH)4CHO + H2
CH2OH(CHOH)4CH2OH
催化剂
CH2OH(CHOH)4CHO+2 Ag(NH3)2OH
2Ag +CH2OH(CHOH)4COOH+4NH3 +H2O
CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O +2H2O
2、果糖:
分子式:C6H12O6
结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH
多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的影响有很强的还原性,所以果糖能被银氨溶液和新制氢氧化铜氧化。
在酸性条件下,果糖不被溴水氧化,可用溴水区分葡萄糖和果糖。
分子的手性
碳原子上连有四个不相同的原子或原子团,这样的碳原子叫做“不对称碳原子”,也叫做“手性分子”。
二、蔗糖 麦芽糖:
演示对比实验:
银氨溶液
银氨溶液
热水浴
热水浴
无现象
产生
银镜
热水浴
热水浴
20%蔗
糖溶液
20%麦芽糖溶液
无还原性
有还原性
蔗糖:
麦芽糖:
化学性质:
同分异构
演示对比实验:
热水浴
20%蔗
糖溶液
银氨溶液
热水浴
无现象
蔗糖 +
稀硫酸
热水浴
NaOH
中和酸
银氨溶液
热水浴
产生
银镜
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
二、蔗糖 麦芽糖:
二、蔗糖 麦芽糖:
葡萄糖 还原性糖
(有-CHO) 不能水解 单糖
蔗糖 非还原性糖
(无-CHO) 水解成一分子葡萄糖一分子果糖 二糖
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
●蔗糖与葡萄糖的比较:
二、蔗糖 麦芽糖:
●蔗糖与麦芽糖的比较:
蔗糖 C12H22O11
同分异构 非还原性糖
(无-CHO) 水解成一分子葡萄糖,一分子果糖 二糖
麦芽糖 还原性糖
(有-CHO) 水解成二分子葡萄糖 二糖
C12H22O11 + H2O 2 C6H12O6
(麦芽糖) (葡萄糖)
催化剂
三.淀粉与纤维素
1.淀粉
存在:存在于植物的种子和块根里。
结构:含有几百到几千个单糖单元(C6H10O5)。每个结构单元式量:162。相对分子质量从几万到几十万;属于天然有机高分子化合物
物质性质:白色、无气味、无味道的粉末状物质,不溶于冷水,在热水中产生糊化作用(即食物由生变熟的过程)
淀粉的化学性质
①通常淀粉不显还原性
②遇碘变蓝色
③淀粉在催化剂(如酸)存在和加热下可以逐步水解,生成一系列比淀粉分子小的化合物,最终生成还原性糖:葡萄糖。
(C6H10O5)n + n H2O n C6H12O6
淀粉 葡萄糖
催化剂
思考:解释为什么在吃馒头或米饭时,多加咀嚼就会感到有甜味?
答:淀粉在人体内进行水解。人在咀嚼馒头时,淀粉受唾液所含淀粉酶(一种蛋白质)的催化作用,开始水解,生成了一部分葡萄糖。
(淀粉在小肠里,在胰脏分泌出的淀粉酶的作用下,继续进行水解。生成的葡萄糖经过肠壁的吸收,进入血液,供人体组织的营养需要。)
淀粉的用途
(1)淀粉是食物的重要成分,是人体的重要能源;
(2)可用于制葡萄糖和酒精等;
(3)淀粉在淀粉酶的作用下,先转化为麦芽糖,再转化为葡萄糖,在酒化酶的作用下,转化为乙醇:
C6H12O6 2C2H5OH +2 CO2
催化剂
三.淀粉和纤维素
2.纤维素
存在:纤维素存在于一切植物中。是构成植物细胞壁的基础物质。
结构:分子中含有约几千个单糖单元(C6H10O5)n ;n为几千;属于天然高分子化合物;纤维素结构与淀粉不同,所以性质有差异。
纤维素的化学性质
不显还原性
可发生水解,但比淀粉水解困难
(C6H10H5)n + nH2O nC6H12O6(葡萄糖)
酯化反应
催化剂
△
纤维素的酯化反应
(C6H7O2)
O—NO2
O—NO2
O—NO2
n
(C6H7O2)
OH
OH
OH
n
3n HNO3
浓硫酸
3nH2O
+
+
纤维素硝酸酯
(硝酸纤维)
思考:如何设计实验检验纤维素水解已经开始?
答案:
取少量反应液,滴加几滴硫酸铜溶液,再加入过量的NaOH溶液,中和作催化剂的硫酸,一直加到出现Cu(OH)2沉淀,最后,加热煮沸,观察现象。如果出现红色沉淀,表明已经开始水解。
5.纤维素的用途
1、棉麻纤维大量用于纺织工业
2、木材、稻草、麦秸、蔗渣等用于造纸
3、制造纤维素硝酸酯(硝酸纤维)。根据含N量分为火棉(含N量较高,用于制造无烟火药)、胶棉(含N量较低,用于制赛璐璐和油漆)
4、制造纤维素乙酸酯(醋酸纤维),不易着火,用于制胶片
5、制造粘胶纤维(NaOH、CS2处理后所得,其中的长纤维称人造丝,短纤维称人造棉)
6、食物中的纤维素有利于人的消化。
糖的概念
具有多羟基醛或多羟基酮结构,以及能够水解生成它们的一类有机化合物叫做糖类,旧称碳水化合物,通式为Cm(H2O)n
分类及相互转化
低聚糖
单糖
多糖
水解
缩合
水解
缩聚
水解
缩合
(2~10)
( >10)
练一练:
1、下列物质具有相同的最简式的组是( )
A、乙醛 葡萄糖 B、乙酸 乙醛
C、乙醇 葡萄糖 D、甲酸甲酯 葡萄糖
2、葡萄糖所不具有的性质是( )
A、和H2发生加成反应
B、和银氨溶液发生氧化反应
C、和酸发生酯化反应
D、和NaOH溶液反应
D
D
第二章 分子结构与性质
第三节
蛋白质和核酸
第四章 生命中的基础有机化学物质
SARS病的凶手——冠状病毒, 有自己的核酸和蛋白质。它进入人体后,借助人体内的原料合成病毒。当我们人体发病时,就是它的蛋白质对我们起了作用。
SARS病毒的电子图片
蛋白质是最重要的营养物质
思考讨论:
1、蛋白质在人体内起什么作用?
(1)对生物反应起催化作用的:
(2)运输作用的:
(3)保护作用的:
(4)抵抗病毒、细菌作用的高度特异性蛋白:
(5)构成动物大部分结构的纤维物质:
酶
血红蛋白
毛发、皮肤、甲、壳等;
抗体
软骨、肌肉
“生命是蛋白质存在的方式”——恩格斯
思考讨论:
2、蛋白质在人体内是如何代谢的?
食物中的蛋白质→ 氨基酸→ 人体内多种蛋白质
3、蛋白质种类为何如此丰富(从结构方面)
蛋白质的基石——氨基酸
1、几种常见的氨基酸:
(1) 甘氨酸
(2) 丙氨酸
(3) 谷氨酸
CH2—COOH
NH2
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
一、氨基酸
羧酸分子里烃基上的氢原子被氨基取代后的生成物叫氨基酸。
什么是氨基酸?
天然蛋白质都是由多种α-氨基酸组成,天然蛋白质水解生成α-氨基酸。
2、氨基酸的性质
(1)既能与酸反应又能与碱反应
与氢氧化钠的反应:
NH2CH2COOH+NaOH→NH2CH2COO-Na++H2O
试写出与盐酸反应的化学方程式
NH2CH2COOH+HCl→Cl-+NH3CH2COOH
(2)成肽反应
2NH2CH2COOH→NH2CH2CONHCH2COOH+H2O
1.书写出乙酸与乙醇发生酯化反应的化学方程式。
2.书写出氨基乙酸与氨基乙酸脱水的方程式。
成肽反应
2NH2CH2COOH→
肽键
两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另一分子的羧基间脱去一分子水,缩合形成含有肽键的化合物,成为成肽反应。
二、蛋白质的结构与性质
蛋白质分子中含有C、O、H、N、S等元素。1965年我国科技工作者成功合成了具有生物活性的——结晶牛胰岛素。这是科学史上的一大成就,可以说是科学史上又一“丰碑”。
蛋白质是含氮生物高分子化合物,有C、H、0、N、S等元素,还有一些微量元素,构成的种类有10万种以上。
天然蛋白质的结构独特而稳定,按照氨基酸的连接方式分为:一级结构、二级结构、三级结构、四级结构。
蛋白质的一级、二级、三级结构
蛋白质的分子图象
蛋白质的空间结构
滴加 (NH4)2SO4
?
再加水
?
?
再加水
?
第一组
滴加乙醇溶液
?
再加水
?
第二组
滴加浓HNO3,微热
?
第三组
加热
?
再加水
?
灼烧 两样品(丝、棉),对比燃烧后产物状态及气味
滴加(CH3COO)2Pb溶液
溶液
滴加(NH4)2SO4
?
再加水
?
?
再加水
?
第一组
盐析 变性
涵义
可逆性
生理活性
一定条件下使蛋白质凝结为固体析出
一定条件下,蛋白质失去生理活性、溶解性降低
保持生理活性
失去生理活性
白色↓
白色↓
溶解
不溶解
加盐析出、加水溶解
——可逆
变性后、加水不溶解
——不可逆
滴加(CH3COO)2Pb溶液
溶液
滴加乙醇溶液
?
再加水
?
第二组
加热
?
再加水
?
白色↓
白色↓
不溶解
不溶解
思考讨论:
(1)你提倡用直发器加热的方法拉直头发吗?
加热使蛋白质变性在生活中最常见,试举例说明。
(2)为什么动物的皮经过药剂鞣制后,才能够成为加工皮革的原料。
第三组
灼烧 两样品(丝和棉),对比燃烧后产物状态及气味
黄色↓
滴加浓HNO3,微热
⑴ 为什么医院用高温蒸煮,照射紫外线,喷洒苯酚溶液,在伤口处涂抹酒精的方法来杀菌
⑵ 为什么生物实验室用甲醛溶液保存标本
⑶ 为什么在农业上用波尔多液(由硫酸铜,生石灰和水制成)来消灭害虫
⑷怎样鉴别丝织品和棉织品
请回答下列问题:
归纳蛋白质的性质:
3. 盐析:
1. 水溶性:有些可溶,有些难溶。
2. 水解:水解生成氨基酸。
4. 变性
5. 颜色反应
6. 灼烧产生烧焦羽毛的气味
CH2 C
NH2
O
N
CH2 COOH
H
三、酶
生物体、植物无时无刻都在进行着化学反应,并且这些反应在生物体存在的条件下进行,而且会随着环境、身体的情况而随时自动、精确的改变,是什么让这些反应可以实现的?
酶的催化特点:
1.条件温和,不需加热
2.具有高度的专一性
3.具有高效催化作用
四、核酸
核酸是一类含磷的高分子化合物,DNA就是其中组成,还有一种是RNA(核糖核酸),DNA和RNA互相作用合成蛋白质。
【练习】
1、下列过程中,不可逆的是( )
A.蛋白质的盐析 B.酯的水解
C.蛋白质白变性 D.氯化铁的水解
2、欲将蛋白质从水中析出而又不改变它的性 质应加入( )
A.甲醛溶液 B.CuSO4溶液
C.饱和Na2SO4溶液 D.浓硫酸
C
C
3、下图表示蛋白质分子结构的一部分,图中A、B、C、D标出了分子中不同的键,当蛋白质发生水解时,断裂的键是( )
C
4、为鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可选用的方法是( )
A、滴加浓硝酸 B、滴加浓硫酸
C、滴加酒精 D、灼烧
A、D
5、误食重金属盐会使人中毒,可以
用以解毒急救的措施是( )
A、服大量食盐水 B、服葡萄糖水
C、服鸡蛋清 D、服新鲜牛奶
C、D
6、蛋白质、淀粉、脂肪是三种重要的营养物质,其中______不是高分子化合物,这三种物质水解的最终产物分别是 蛋白质→________淀粉→_________; 脂肪→_________;在蛋白质水解的最终产物分子中,含有_________官能团。
*7、若将氨基乙酸和丙氨酸混合反应(在一定条件下)最多可得 种二肽。
