4.2.1《糖类(1)糖类》PPT课件(新人教版-选修5)
文档属性
| 名称 | 4.2.1《糖类(1)糖类》PPT课件(新人教版-选修5) |

|
|
| 格式 | zip | ||
| 文件大小 | 166.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-12 00:00:00 | ||
图片预览









文档简介
(共30张PPT)
新课标人教版课件系列
《高中化学》
选修5
4.2.1
《糖类(1)糖类》
第二节 糖类
第1课时
糖类
糖类在生命活动过程中起着重要的作用,是一切生物体维持生命活动所需要的主要能量来源。
一、糖类
1、糖的的定义:具有多羟基醛或多羟基酮
结构,以及能够水解生成
它们的一类有机化合物旧
称碳水化合物.
2、 组成元素:C、H、O Cn(H2O)m
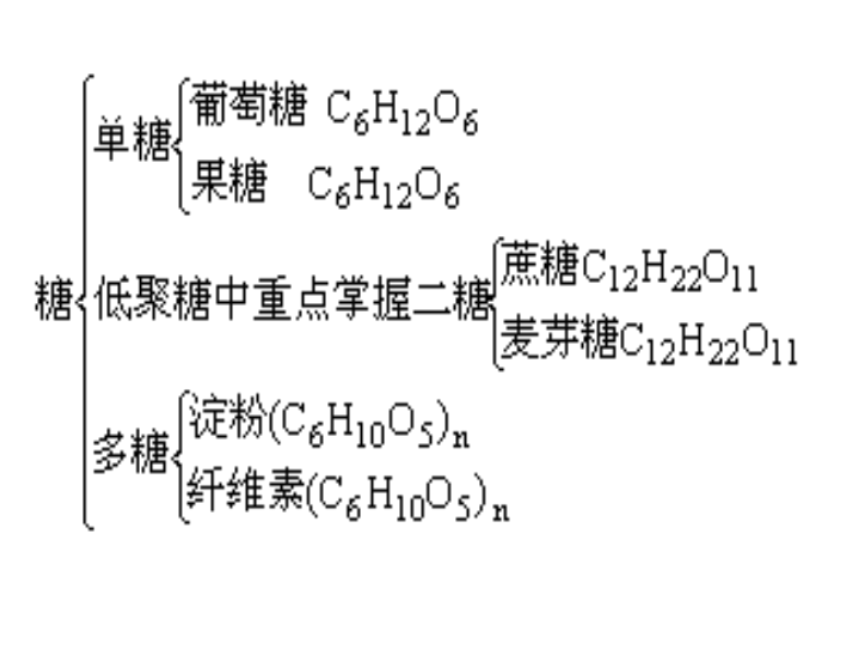
3、分类
单糖
低聚糖
多糖
糖
不能再发生水解的糖
能水解成较少分子单糖的糖(≤10)
能水解成多分子单糖的糖(>10)
4、多糖属于天然高分子化合物
能否水解以及水解产物的多少
淀粉、纤维素
蔗糖、麦芽糖、纤维二糖和乳糖
葡萄糖、果糖、半乳糖、山梨糖
说明:(1)糖类不都是甜的。我们食用的蔗糖是甜的,它只是糖类中的一种。淀粉、纤维素均不甜,它们属于糖类。有些有甜味的物质,如糖精,不属于糖类。 (2)糖类是由C、H、O三种元素组成的有机化合物,通式为______________。所以糖类又称碳水化合物。实际上这种叫法不科学,在学习中对通式的理解应注意:
Cn(H2O)m
① 糖分子中的H、O原子并不是结合成水分子形式存在,它只能说明糖类由____、_____、_____三种元素组成。 ②此通式适用于大多数糖类化合物,而对少数糖类物质不适合,如鼠李糖化学式为_____________。有些符合此通式的物质并不是糖类,如_____________,____________,______________等。
C
H
O
C6H12O5
甲醛 CH2O , 乙酸 C2H4O2
乳酸 C3H6O3
______糖是糖类中最简单的一类糖,它不能水解生成其它糖。葡萄糖和果糖是______糖中的两种,它们互为____________。 一、葡萄糖
(一)、葡萄糖的物理性质
_____色晶体、熔点为________℃,有_____味,但甜度_______蔗糖,_____溶于水,_______溶于乙醇,________溶于乙醚。
单
单
同分异构体
无
146
甜
不如
易
稍
不
(二)、葡萄糖的结构
⑴ 葡萄糖的相对分子质量为180,其中含碳40%,氢6.7%,其余是氧。
分子式_________________
⑵ 1 mol 葡萄糖最多可以和 5 mol 醋酸发生酯化(提示:同一个C原子上连接2个羟基不稳定)
说明分子中有______个醇羟基
⑶ 现代物理方法测定得知:葡萄糖分子中的碳原子最多与两个碳原子相连。
说明:葡萄糖分子中六个碳原子为______结构。
葡萄糖具有多羟基醛的结构式为:_________________________________________
C6H12O6
五
直链
CH2OH–(CHOH)4 -CHO
C C C C C C
O
H
OH OH OH H OH
H
H H H OH H
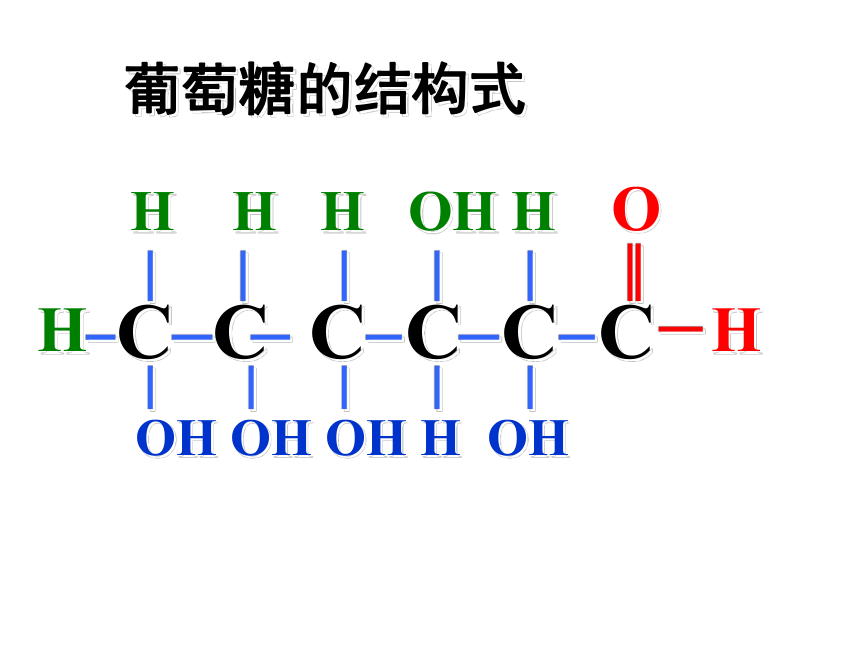
葡萄糖的结构式
结构简式:
CH2OH–(CHOH)4 -CHO
或
CHO
(CHOH)4
CH2OH
结构特点:是多羟基醛
分子式:
C6H12O6
(三)、葡萄糖的化学性质
因分子中有醛基,使葡萄糖既有氧化性又有还原性。
1.银镜反应(被氧化为葡萄糖酸):
点击实验:在一支洁净的试管里,加入2%硝酸银溶液2mL,振荡试管,同时加入2%稀氨水,直到析出的沉淀恰好溶解为止。所得澄清溶液就是银氨溶液。在盛着银氨溶液的试管里,加入10%葡萄糖溶液1mL,把试管放入热水浴里加热,观察现象。
CH 2OH—(CHOH)4 —COO NH4 + Ag + H2O + NH3
1、银镜反应
2
2
3
CH2OH—(CHOH)4—CHO
+ [Ag(NH3)2]OH
加热
(三)、葡萄糖的化学性质
[实验2] :向试管里加入10%NaOH溶液2mL,再滴加5%CuSO4溶液4~5滴。可以观察到淡蓝色Cu(OH)2沉淀生成。在新制Cu(OH)2悬浊液试管里,立即加入10%葡萄糖溶液2mL,振荡后观察现象; 然后再加热观察现象。
葡萄糖结构的测定
实 验 或 论 述 现 象 结 论
葡萄糖
+
新制 Cu(OH)2
不加热
加热
绛蓝色
砖红色
沉淀
分子中有多羟基
分子中有醛基
(官能团的测定)
2、与新制Cu(OH)2反应
CH2OH –(CHOH)4- CHO + Cu(OH)2
加热
CH2OH –(CHOH)4-COOH +
Cu2O + H2O
2
2
3、还原反应
CH2OH -(CHOH)4-CHO + H2
催化剂
加热
己六醇
CH2OH –(CHOH)4 - CH2OH
5
5
五乙酸葡萄糖酯
+
CHO
(CHOOCCH 3) 4
CH2OOCCH3
H2O
+
CH3COOH
浓H2SO4
CHO
(CHOH )4
CH2OH
4.酯化反应(有多元醇的性质):
(能与酸发生酯化反应)
5、氧化反应(与氧气)
葡萄糖是人体内的重要能源物质:
C6H12O6 (s)+ 6O2(g) →6CO2(g) + 6H2O(l) + 2804kJ
营养物质 ——动物需要的能量来源。
体弱和血糖过低的患者可利用静脉注射葡萄糖溶液的方式来迅速补充营养.
(四)、葡萄糖的用途
葡萄糖
生活中——糖果
工业上——制镜
医药上——迅速补充营养
1. 关于葡萄糖的下列说法中,错误的是 ( )
A. 葡萄糖具有醇羟基,能和酸发
生酯化反应
B. 葡萄糖能使溴水褪色
C. 葡萄糖能被硝酸氧化
D. 葡萄糖可被还原为1-己醇
练习
D
2. 在一定的条件下,既可以发生氧化反应,又可以发生还原反应,又可以和酸发生酯化反应的是( )
A、乙醇 B、乙醛
C、乙酸 D、葡萄糖
D
3.思考题:
患有糖尿病的人的尿液中含有葡萄糖,设想怎样去检验一个病人是否患有糖尿病?
1、银镜反应
2、与新制Cu(OH)2悬浊液反应
5、氧化反应
小结:葡萄糖的化学性质
3、酯化反应
4、加氢还原
2.果糖
单糖跟葡萄糖是同分异构体—果糖,它是最甜的糖,广泛分布于植物中,在_____和_______中含量较高。纯净的果糖是_____色晶体,熔点为_______________℃,它_____易结晶,通常为_______________,易溶于_____、_______和__________。
水果
蜂蜜
无
103 ~ 105
不
黏稠性液体
水
乙醇
乙醚
果糖分子不像葡萄糖分子那样含有醛基,果糖是一种多羟基酮,结构简式为:
CH2OH-CHOH-CHOH-CHOH-CO-CH2OH
[探究]
果糖是否也像葡萄糖一样具有还原性,能发生银镜反应呢?
怎样鉴别葡萄糖和果糖?
实践活动:P.81
分子的手性——有机物的空间异构现象
自然界的葡萄糖和果糖都是D-型结构
HO— C —H
CHO
CH2—OH
H— C —OH
CHO
CH2—OH
D-甘油醛
L-甘油醛
H— C —OH
CHO
CH2—OH
HO— C —H
H— C —OH
H— C —OH
HO— C —H
C=O
CH2—OH
H— C —OH
H— C —OH
CH2—OH
D-葡萄糖
D-果糖
HO
HO
CH2
H2N
H
COOH
药物多巴结构简式
在两种构型的药物中,一种对人体无效,而另一种却被广泛用于治疗中枢神经系统的慢性病——帕金森氏症。
葡萄糖 果糖
分子式
结构特点
存在
物理性质
化学性质
用途
制法
多羟基醛
多羟基醛酮
C6H12O6(同分异构体)
自然界分布最广,葡萄及甜味水果中
水果、蜂蜜
无色晶体,溶于水
不易结晶,常为粘稠状液体、纯净的为白色晶体,溶于水
羟基性质:酯化反应
醛基性质:还原性(新制Cu(OH)2
悬浊液、银镜反应、溴水)、
氧化性
生物作用:氧化反应
可发生银镜反应及与新制
Cu(OH)2悬浊液的反应,(碱性条件下异构化)
不与溴水反应
制药、制糖果、制镜
食物
淀粉水解
新课标人教版课件系列
《高中化学》
选修5
4.2.1
《糖类(1)糖类》
第二节 糖类
第1课时
糖类
糖类在生命活动过程中起着重要的作用,是一切生物体维持生命活动所需要的主要能量来源。
一、糖类
1、糖的的定义:具有多羟基醛或多羟基酮
结构,以及能够水解生成
它们的一类有机化合物旧
称碳水化合物.
2、 组成元素:C、H、O Cn(H2O)m
3、分类
单糖
低聚糖
多糖
糖
不能再发生水解的糖
能水解成较少分子单糖的糖(≤10)
能水解成多分子单糖的糖(>10)
4、多糖属于天然高分子化合物
能否水解以及水解产物的多少
淀粉、纤维素
蔗糖、麦芽糖、纤维二糖和乳糖
葡萄糖、果糖、半乳糖、山梨糖
说明:(1)糖类不都是甜的。我们食用的蔗糖是甜的,它只是糖类中的一种。淀粉、纤维素均不甜,它们属于糖类。有些有甜味的物质,如糖精,不属于糖类。 (2)糖类是由C、H、O三种元素组成的有机化合物,通式为______________。所以糖类又称碳水化合物。实际上这种叫法不科学,在学习中对通式的理解应注意:
Cn(H2O)m
① 糖分子中的H、O原子并不是结合成水分子形式存在,它只能说明糖类由____、_____、_____三种元素组成。 ②此通式适用于大多数糖类化合物,而对少数糖类物质不适合,如鼠李糖化学式为_____________。有些符合此通式的物质并不是糖类,如_____________,____________,______________等。
C
H
O
C6H12O5
甲醛 CH2O , 乙酸 C2H4O2
乳酸 C3H6O3
______糖是糖类中最简单的一类糖,它不能水解生成其它糖。葡萄糖和果糖是______糖中的两种,它们互为____________。 一、葡萄糖
(一)、葡萄糖的物理性质
_____色晶体、熔点为________℃,有_____味,但甜度_______蔗糖,_____溶于水,_______溶于乙醇,________溶于乙醚。
单
单
同分异构体
无
146
甜
不如
易
稍
不
(二)、葡萄糖的结构
⑴ 葡萄糖的相对分子质量为180,其中含碳40%,氢6.7%,其余是氧。
分子式_________________
⑵ 1 mol 葡萄糖最多可以和 5 mol 醋酸发生酯化(提示:同一个C原子上连接2个羟基不稳定)
说明分子中有______个醇羟基
⑶ 现代物理方法测定得知:葡萄糖分子中的碳原子最多与两个碳原子相连。
说明:葡萄糖分子中六个碳原子为______结构。
葡萄糖具有多羟基醛的结构式为:_________________________________________
C6H12O6
五
直链
CH2OH–(CHOH)4 -CHO
C C C C C C
O
H
OH OH OH H OH
H
H H H OH H
葡萄糖的结构式
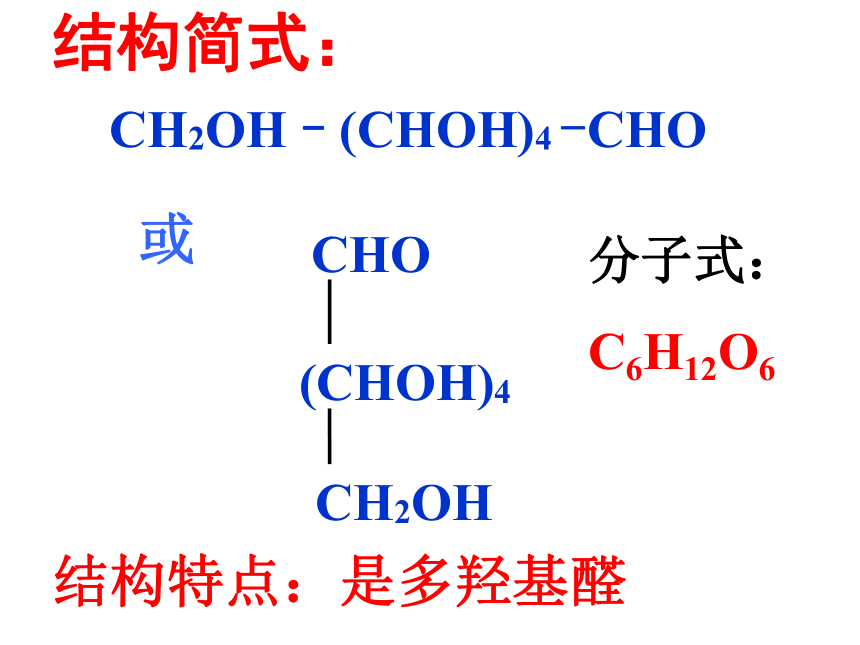
结构简式:
CH2OH–(CHOH)4 -CHO
或
CHO
(CHOH)4
CH2OH
结构特点:是多羟基醛
分子式:
C6H12O6
(三)、葡萄糖的化学性质
因分子中有醛基,使葡萄糖既有氧化性又有还原性。
1.银镜反应(被氧化为葡萄糖酸):
点击实验:在一支洁净的试管里,加入2%硝酸银溶液2mL,振荡试管,同时加入2%稀氨水,直到析出的沉淀恰好溶解为止。所得澄清溶液就是银氨溶液。在盛着银氨溶液的试管里,加入10%葡萄糖溶液1mL,把试管放入热水浴里加热,观察现象。
CH 2OH—(CHOH)4 —COO NH4 + Ag + H2O + NH3
1、银镜反应
2
2
3
CH2OH—(CHOH)4—CHO
+ [Ag(NH3)2]OH
加热
(三)、葡萄糖的化学性质
[实验2] :向试管里加入10%NaOH溶液2mL,再滴加5%CuSO4溶液4~5滴。可以观察到淡蓝色Cu(OH)2沉淀生成。在新制Cu(OH)2悬浊液试管里,立即加入10%葡萄糖溶液2mL,振荡后观察现象; 然后再加热观察现象。
葡萄糖结构的测定
实 验 或 论 述 现 象 结 论
葡萄糖
+
新制 Cu(OH)2
不加热
加热
绛蓝色
砖红色
沉淀
分子中有多羟基
分子中有醛基
(官能团的测定)
2、与新制Cu(OH)2反应
CH2OH –(CHOH)4- CHO + Cu(OH)2
加热
CH2OH –(CHOH)4-COOH +
Cu2O + H2O
2
2
3、还原反应
CH2OH -(CHOH)4-CHO + H2
催化剂
加热
己六醇
CH2OH –(CHOH)4 - CH2OH
5
5
五乙酸葡萄糖酯
+
CHO
(CHOOCCH 3) 4
CH2OOCCH3
H2O
+
CH3COOH
浓H2SO4
CHO
(CHOH )4
CH2OH
4.酯化反应(有多元醇的性质):
(能与酸发生酯化反应)
5、氧化反应(与氧气)
葡萄糖是人体内的重要能源物质:
C6H12O6 (s)+ 6O2(g) →6CO2(g) + 6H2O(l) + 2804kJ
营养物质 ——动物需要的能量来源。
体弱和血糖过低的患者可利用静脉注射葡萄糖溶液的方式来迅速补充营养.
(四)、葡萄糖的用途
葡萄糖
生活中——糖果
工业上——制镜
医药上——迅速补充营养
1. 关于葡萄糖的下列说法中,错误的是 ( )
A. 葡萄糖具有醇羟基,能和酸发
生酯化反应
B. 葡萄糖能使溴水褪色
C. 葡萄糖能被硝酸氧化
D. 葡萄糖可被还原为1-己醇
练习
D
2. 在一定的条件下,既可以发生氧化反应,又可以发生还原反应,又可以和酸发生酯化反应的是( )
A、乙醇 B、乙醛
C、乙酸 D、葡萄糖
D
3.思考题:
患有糖尿病的人的尿液中含有葡萄糖,设想怎样去检验一个病人是否患有糖尿病?
1、银镜反应
2、与新制Cu(OH)2悬浊液反应
5、氧化反应
小结:葡萄糖的化学性质
3、酯化反应
4、加氢还原
2.果糖
单糖跟葡萄糖是同分异构体—果糖,它是最甜的糖,广泛分布于植物中,在_____和_______中含量较高。纯净的果糖是_____色晶体,熔点为_______________℃,它_____易结晶,通常为_______________,易溶于_____、_______和__________。
水果
蜂蜜
无
103 ~ 105
不
黏稠性液体
水
乙醇
乙醚
果糖分子不像葡萄糖分子那样含有醛基,果糖是一种多羟基酮,结构简式为:
CH2OH-CHOH-CHOH-CHOH-CO-CH2OH
[探究]
果糖是否也像葡萄糖一样具有还原性,能发生银镜反应呢?
怎样鉴别葡萄糖和果糖?
实践活动:P.81
分子的手性——有机物的空间异构现象
自然界的葡萄糖和果糖都是D-型结构
HO— C —H
CHO
CH2—OH
H— C —OH
CHO
CH2—OH
D-甘油醛
L-甘油醛
H— C —OH
CHO
CH2—OH
HO— C —H
H— C —OH
H— C —OH
HO— C —H
C=O
CH2—OH
H— C —OH
H— C —OH
CH2—OH
D-葡萄糖
D-果糖
HO
HO
CH2
H2N
H
COOH
药物多巴结构简式
在两种构型的药物中,一种对人体无效,而另一种却被广泛用于治疗中枢神经系统的慢性病——帕金森氏症。
葡萄糖 果糖
分子式
结构特点
存在
物理性质
化学性质
用途
制法
多羟基醛
多羟基醛酮
C6H12O6(同分异构体)
自然界分布最广,葡萄及甜味水果中
水果、蜂蜜
无色晶体,溶于水
不易结晶,常为粘稠状液体、纯净的为白色晶体,溶于水
羟基性质:酯化反应
醛基性质:还原性(新制Cu(OH)2
悬浊液、银镜反应、溴水)、
氧化性
生物作用:氧化反应
可发生银镜反应及与新制
Cu(OH)2悬浊液的反应,(碱性条件下异构化)
不与溴水反应
制药、制糖果、制镜
食物
淀粉水解
