9.0《物态和物态变化》PPT课件(新人教版 选修3-3)
文档属性
| 名称 | 9.0《物态和物态变化》PPT课件(新人教版 选修3-3) |

|
|
| 格式 | zip | ||
| 文件大小 | 360.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2012-06-13 00:00:00 | ||
图片预览











文档简介
(共49张PPT)
新课标人教版课件系列
《高中物理》
选修3-3
第九章
《物态和物态变化》
9.1《固体》
教学目标
知识与能力
1.知道固体可分为晶体和非晶体两大类,了解它们在物理性质上的差别。
2.知道晶体分子或离子按一定的空间点阵排列。知道晶体可分为单晶体和多晶体,通常说的晶体及性质是指单晶体,多晶体的性质与非晶体类似。
3.能用晶体的空间点阵说明其物理性质的各向异性。
重点、难点
1.晶体与非晶体的区别;晶体与多晶体的区别
2.晶体的微观结构
一、晶体和非晶体
1.晶体:具有规则的几何形状.
点击下图观看动画
几种晶体的形状.swf
由此可知:
( 1 )常见的晶体有:石英、云母、明矾、食盐、硫酸铜、糖、味精等.
(2)几种常见晶体的规则外形:
食盐的晶体呈立方体形;
明矾的晶体呈八面体形;
石英的晶体中间是一个六棱柱,两端呈六棱锥;
雪花是水蒸气在空气中凝华时形成的晶体,一般为六角形的规则图案.
2.非晶体:没有规则的几何形状.
常见的非晶体有:玻璃、蜂蜡、松香、沥青、橡胶等.
松香
沥青
3.晶体和非晶体的差异
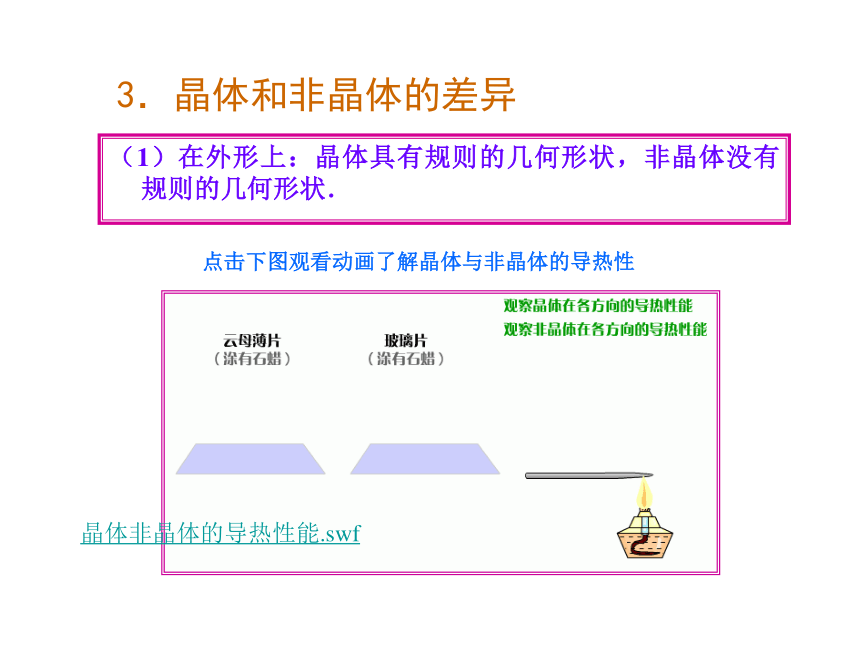
(1)在外形上:晶体具有规则的几何形状,非晶体没有规则的几何形状.
点击下图观看动画了解晶体与非晶体的导热性
晶体非晶体的导热性能.swf
由此可知:
(2)在物理性质上,晶体的物理性质与方向有关(这种特性叫各向异性),非晶体的物理性质在各个方向是相同的(这种特性叫各向同性).
注意:
①晶体具有各向异性,并不是每种晶体在各种物理性质上都表现出各向异性.云母导热性上表现出显著的各向异性,而有些晶体在导电性上表现出显著的各向异性,如方铝矿,有些晶体在光的折射上表现出显著的各向异性,如方解石.
②晶体有一定的熔点,非晶体没有一定的熔点.
4.晶体和非晶体间的转化
1.一种物质可能以晶体和非晶体两种不同的形态出现,例如水晶.天然水晶是晶体,熔化后再凝结的水晶(石英玻璃)就是非晶体,即一种物质是晶体还是非晶体并不是绝对的.
2.许多非晶体在一定的条件下可以转化为晶体.
3.在冷却得足够快和冷却到足够低的温度时,几乎所有的材料都能成为非晶体.
二、单晶体和多晶体
1.单晶体:如果一个物体就是一个完整的晶体,这样的晶体叫做单晶体.
例如:雪花、食盐小颗粒、单晶硅、单晶锗等.
2.多晶体:如果整个物体是由许多杂乱无章地排列着的小晶体组成的,这样的物体叫做多晶体.其中的小晶体叫做晶粒.
(1)多晶体没有规则的几何形状.
(2)多晶体 ①不显示各向异性.(每一晶粒内部都是各向异性的). ②有确定的熔点.
固体是否有确定的熔点,可作为区分晶体非晶体的标志.
3.多晶体和非晶体比较
(1)多晶体和非晶体都没有规则的几何形状.
(2)多晶体有一定的熔点,非晶体没有一定的熔点.
(3)多晶体和非晶体的一些物理性质都表现为各向同性.
例题:
下列说法中正确的是( )
A.常见的金属材料都是多晶体
B.只有非晶体才显示各向同性
C.凡是具有规则天然几何形状的物体必定是单晶体
D.多晶体不显示各向异性
解析:
常见的金属:金、银、铜、铁、铝、锡、铅等都是多晶体,选项A正确.因为非晶体和多晶体的物理性质都表现为各向同性,所以选项B错误,这项D正确.有天然规则的几何形状的物体一定是单晶体,选项C正确.
该题的正确答案为A、C、D.
小结:
晶体和非晶体.
单晶体和多晶体.
9.2《液体》
教学目标
知识与技能
1、知道液体的宏观性质(具有一定的体积,不易压缩,有流动性); 2、了解液体的微观结构:液体的微观粒子也在平衡位置附近做微小的振动,但液体分子没有固定不变的平衡位置;3、能用分子动理论的观点初步说明液体表面张力现象;4、了解表面张力现象在实际中的应用,并能解释一些简单的自然现象.
过程与方法
1.运用能用分子动理论的观点初步说明液体表面张力现象.
2.理论联系实际,学习运用表面张力解释自然现象
情感、态度与价值观
通过对表面张力现象在实际中的应用,感受成功的喜悦,培养学生对科学研究的兴趣.
教学重点难点:
液体的微观结构及其宏观解释
教学方法:探究法
教具:多媒体课件
分子在不停的做无规则的运动,
分子之间的的相互作用力使得分子
聚集在一起,而分子的无规则运动
又使它们分散开来,我们看到自然
界中物质的三种状态:液态、气态
和固态,便是由于分子的这两种作
用而产生的三种不同的聚集状态。
1、对比液态、气态、固态 研究液体的性质
(1)液体和气体没有一定的形状,是流动的。
(2)液体和固体具有一定的体积;
而气体的体积可以变化千万倍;
(3)液体和固体都很难被压缩;
而气体可以很容易的被压缩;
结论:液体的性质介于气体和固体之间,
它与固体一样具有一定的体积,不易压缩,
同时,又像气体一样没有固定的形状,具有流动性。
这些性质是由它的微观结构决定的。
2、液体的微观结构
①液体分子间距介于气体分子间距和固体分子间距之间;
②液体分子的排列更接近于固体;
③液体分子间的相互作用力比固体分子间的作用力要小
【例】下面关于液体的说法正确的是( )
A.非晶体的结构跟液体非常类似,
可以看作是粘滞性极大的液体
B.液体的物理性质一般表现为各向同性
C.液体的密度总是小于固体的密度
D.所有的金属在常温下都是固体
⑴液体的表面张力
表面层
液体
汽
3、液体的特殊现象
液体的表面张力具有使液体表面收缩的趋势
请学生们分析下面这些现象,并解释产生的原因?
(1)雨伞的伞面有细小的孔,为什么水不会从孔里漏下去?
(2)将分币轻轻地放在一碗水的水面上,为什么分币
会浮在水面上不沉下去?
因为水将纱线浸湿后,在纱线孔隙中形成水膜,
水膜的表面张力使得雨水不致漏下.
这是由于表面张力使得液体表面形成一个张紧的薄膜,
当分币放置上后,使得液体表面发生形变,产生弹力,
这样受力平衡,所以分币会浮在水面上不沉下去。
⑵浸润和不浸润
⑴液体的表面张力
3、液体的特殊现象
⑶毛细现象
化学上如何检查试管是否刷的干净?
【例】人造卫星中有一个盛液体的容器
如果液体浸润容器壁,会发生什么现象?
如果液体不浸润器壁,又将出现什么现象?
【例】在水中浸入两个同样细的毛细管,
一个是直的,另一个是弯的,如图,水在直管
中上升的高度比弯管的最高点还要高,那么
弯管中的水能否流出 为什么
4、液晶
像液体一样具有流动性,
而其光学性质与某些晶体相似,具有各向异性
的一些化合物取名为液晶
液晶分子结构
液晶的应用:电子表显示窗
笔记本彩色显示器
人造生物膜
1、液体的微观结构
⑵浸润和不浸润
⑴液体的表面张力
2、液体的特殊现象
⑶毛细现象
3、液晶
9.3《饱和汽和
饱和气压》
教学目标
知识与能力
1.知道汽化及汽化的两种方式和其特点。
2.理解饱和汽与饱和汽压,能从分子动理论的角度解释有关现象。
3.理解空气的绝对湿度和相对湿度,并能进行简单计算。
4.了解湿度计的原理。
重点、难点:
1、理解饱和汽与饱和汽压,能从分子动理论的角度解释有关现象。
2、理解空气的绝对湿度和相对湿度,并能进行简单计算。
一、蒸发与沸腾
1.汽化:
物质从液态变成气态的过程
2.蒸发:
发生在液体表面,即液体分子由液体表面跑出去的过程
3.影响蒸发的因素:
表面积
温度
通风
液面气压高低
蒸发可使液体降温
4.沸腾:
在一定大气压下,加热液体到某一温度时,在液体表面和内部同时发生的剧烈的汽化现象,相应的温度叫沸点
t/0C
p/kPa
100
200
300
50
100
150
沸点与液面上气体的压强有关
蒸发 沸腾
相同点
不
同
点 发生部位
温度条件
剧烈程度
温度变化
影响因素
方式
项目
都是汽化现象,都能使液体变为气体,都吸收热量
液面
内部、液面同时进行
任何温度
一定温度(沸点)
缓慢
剧烈
降低
不变
1.液体温度的高低
2.液体表面积的大小
3.液体表面空气流动的快慢
4.液体汽压的高低
液面气压的高低
现象:减小瓶中的气压,水会沸腾。
表明:气压减小,水的沸点降低。
二、饱和汽和饱和汽压
1.饱和汽
在密闭容器中的液体不断的蒸发,液面上的蒸气也不断地凝结,当这两个同时存在的过程达到动态平衡时,宏观的蒸发也停止了,这种与液体处于动态平衡的蒸气叫做饱和汽。
2.未饱和汽:
没有达到饱和状态的蒸气
3.饱和汽压:
在一定温度下,饱和汽的分子数密度是一定的,
因而饱和汽的压强也是一定的,这个压强叫做
这种液体的饱和汽压。
说明:
(1)饱和汽压随温度的升高而增大。
(2)饱和汽压与蒸气所占的体积无关,也和这种体积中有无其他气体无关。
a.往一个真空容器中注入液体,表面的上方形成饱和蒸汽时,表面的上方空间的气压就是饱和汽压.
b.往一个密闭的原来有空气的容器中注入液体,表面的上方形成饱和蒸汽时,表面的上方空间的气压不等于饱和汽压,而是饱和汽压与空气压强的总和.
c.液体的饱和汽压只指这种气体的分气压.
温度升高时,分子平均动能增大,单位时间内逸出液面的分子数增多,于是原来的动态平衡状态被破坏,空间气态分子密度逐渐增大,导致单位时间内返回的分子数增多,从而达到新的条件下的动态平衡.
(3)液体沸腾的条件就是饱和汽压和外部压强相等
三、空气的湿度
1.绝对湿度:
空气里所含水汽的压强
2.相对湿度:
在某一温度下,水蒸汽的压强与同温度下饱和汽压的比,称为空气的相对湿度。
相对湿度
=
水蒸汽的实际压强
同温度下的饱和汽压
即B=
p
ps
X100%
3.影响蒸发快慢以及影响人们对干爽与潮湿感受的因素,不是空气中水蒸气的绝对数量,而是空气中水蒸气的压强与同一温度下水的饱和汽压的差距.
四、空气的湿度
1.空气的相对湿度常用湿度计来测量。
2.常用的湿度计有干湿泡湿度计、毛发湿度计和湿度传感器等
水蒸气的压强离饱和汽压越远,越有利于水的蒸发,人们感觉干爽.
9.4《物态变化中的
能量交换》
教学目标
知识与能力
1.知道熔化和熔化热、汽化和汽化热的概念。
2.会用熔化热和汽化热处理有关问题。
3.体会能的转化与守恒在物态变化中的应用。
重点、难点:
知道熔化和熔化热、汽化和汽化热的概念
会用熔化热和汽化热处理有关问题。
固态
液态
气态
熔化吸热
汽化吸热
凝固放热
液化放热
一、熔化热
物质从固态变成液态的过程。
物质从液态变成固态的过程。
熔化是凝固的逆过程。
1. 熔化与凝固
熔化:
凝固:
一、熔化热
由于固体分子间的强大作用,固体分子只能在各自的平衡位置附近振动,对固体加热,在其熔解之前,获得的能量主要转化为分子的动能,使物体温度升高,当温度升高到一定程度,一部分分子的能量足以克服其他分子的束缚,从而可以在其他分子间移动,固体开始熔解。
为什么熔化会吸热?
一、熔化热
2.熔化热:
某种晶体熔化过程中所需的能量与其
质量之比,称做这种晶体的熔化热
一定质量的晶体,熔化时吸收的热量与凝固时
放出的热量相等
一、熔化热
为什么晶体有确定的熔点和熔化热,非晶体却没有?
晶体熔化过程中,当温度达到熔点时,吸收的热量全部用
来破坏空间点阵,增加分子势能,而分子平均动能却保持不变,
所以晶体有固定的熔点。非晶体没有空间点阵,熔化时不需要
去破坏空间点阵,吸收的热量主要转化为分子的动能,不断吸
热,温度就不断上升。
由于在不同温度下物质由固态变成液态时吸收的热量不同,
而晶体有固定的熔点,因此有固定的熔化热,非晶体没有固定的
熔点,也就没有固定的熔化热。
一、熔化热
3.熔化热的计算
熔化时吸收的热量:Q=λm
二、汽化热
1.汽化与液化
汽化:
物质从液态变成气态的过程
液化:
物质从气态变成液态的过程
液体汽化时,为何要吸热?
二、汽化热
2.汽化热
某种液体汽化成同温度的气体时所需的能量与其质量之比,称做这种物质在这个温度下的汽化热。
汽化热跟温度和压强有关
t /0C
100
Q/(J.g-1)
500
1000
1500
2000
2500
0
200
300
400
水在大气压强为
1.01x105Pa下汽
化热与温度的关系
二、汽化热
一定质量的物质,在一定温度和压强下,汽化时吸收的热量与液化时放出的热量
相等
新课标人教版课件系列
《高中物理》
选修3-3
第九章
《物态和物态变化》
9.1《固体》
教学目标
知识与能力
1.知道固体可分为晶体和非晶体两大类,了解它们在物理性质上的差别。
2.知道晶体分子或离子按一定的空间点阵排列。知道晶体可分为单晶体和多晶体,通常说的晶体及性质是指单晶体,多晶体的性质与非晶体类似。
3.能用晶体的空间点阵说明其物理性质的各向异性。
重点、难点
1.晶体与非晶体的区别;晶体与多晶体的区别
2.晶体的微观结构
一、晶体和非晶体
1.晶体:具有规则的几何形状.
点击下图观看动画
几种晶体的形状.swf
由此可知:
( 1 )常见的晶体有:石英、云母、明矾、食盐、硫酸铜、糖、味精等.
(2)几种常见晶体的规则外形:
食盐的晶体呈立方体形;
明矾的晶体呈八面体形;
石英的晶体中间是一个六棱柱,两端呈六棱锥;
雪花是水蒸气在空气中凝华时形成的晶体,一般为六角形的规则图案.
2.非晶体:没有规则的几何形状.
常见的非晶体有:玻璃、蜂蜡、松香、沥青、橡胶等.
松香
沥青
3.晶体和非晶体的差异
(1)在外形上:晶体具有规则的几何形状,非晶体没有规则的几何形状.
点击下图观看动画了解晶体与非晶体的导热性
晶体非晶体的导热性能.swf
由此可知:
(2)在物理性质上,晶体的物理性质与方向有关(这种特性叫各向异性),非晶体的物理性质在各个方向是相同的(这种特性叫各向同性).
注意:
①晶体具有各向异性,并不是每种晶体在各种物理性质上都表现出各向异性.云母导热性上表现出显著的各向异性,而有些晶体在导电性上表现出显著的各向异性,如方铝矿,有些晶体在光的折射上表现出显著的各向异性,如方解石.
②晶体有一定的熔点,非晶体没有一定的熔点.
4.晶体和非晶体间的转化
1.一种物质可能以晶体和非晶体两种不同的形态出现,例如水晶.天然水晶是晶体,熔化后再凝结的水晶(石英玻璃)就是非晶体,即一种物质是晶体还是非晶体并不是绝对的.
2.许多非晶体在一定的条件下可以转化为晶体.
3.在冷却得足够快和冷却到足够低的温度时,几乎所有的材料都能成为非晶体.
二、单晶体和多晶体
1.单晶体:如果一个物体就是一个完整的晶体,这样的晶体叫做单晶体.
例如:雪花、食盐小颗粒、单晶硅、单晶锗等.
2.多晶体:如果整个物体是由许多杂乱无章地排列着的小晶体组成的,这样的物体叫做多晶体.其中的小晶体叫做晶粒.
(1)多晶体没有规则的几何形状.
(2)多晶体 ①不显示各向异性.(每一晶粒内部都是各向异性的). ②有确定的熔点.
固体是否有确定的熔点,可作为区分晶体非晶体的标志.
3.多晶体和非晶体比较
(1)多晶体和非晶体都没有规则的几何形状.
(2)多晶体有一定的熔点,非晶体没有一定的熔点.
(3)多晶体和非晶体的一些物理性质都表现为各向同性.
例题:
下列说法中正确的是( )
A.常见的金属材料都是多晶体
B.只有非晶体才显示各向同性
C.凡是具有规则天然几何形状的物体必定是单晶体
D.多晶体不显示各向异性
解析:
常见的金属:金、银、铜、铁、铝、锡、铅等都是多晶体,选项A正确.因为非晶体和多晶体的物理性质都表现为各向同性,所以选项B错误,这项D正确.有天然规则的几何形状的物体一定是单晶体,选项C正确.
该题的正确答案为A、C、D.
小结:
晶体和非晶体.
单晶体和多晶体.
9.2《液体》
教学目标
知识与技能
1、知道液体的宏观性质(具有一定的体积,不易压缩,有流动性); 2、了解液体的微观结构:液体的微观粒子也在平衡位置附近做微小的振动,但液体分子没有固定不变的平衡位置;3、能用分子动理论的观点初步说明液体表面张力现象;4、了解表面张力现象在实际中的应用,并能解释一些简单的自然现象.
过程与方法
1.运用能用分子动理论的观点初步说明液体表面张力现象.
2.理论联系实际,学习运用表面张力解释自然现象
情感、态度与价值观
通过对表面张力现象在实际中的应用,感受成功的喜悦,培养学生对科学研究的兴趣.
教学重点难点:
液体的微观结构及其宏观解释
教学方法:探究法
教具:多媒体课件
分子在不停的做无规则的运动,
分子之间的的相互作用力使得分子
聚集在一起,而分子的无规则运动
又使它们分散开来,我们看到自然
界中物质的三种状态:液态、气态
和固态,便是由于分子的这两种作
用而产生的三种不同的聚集状态。
1、对比液态、气态、固态 研究液体的性质
(1)液体和气体没有一定的形状,是流动的。
(2)液体和固体具有一定的体积;
而气体的体积可以变化千万倍;
(3)液体和固体都很难被压缩;
而气体可以很容易的被压缩;
结论:液体的性质介于气体和固体之间,
它与固体一样具有一定的体积,不易压缩,
同时,又像气体一样没有固定的形状,具有流动性。
这些性质是由它的微观结构决定的。
2、液体的微观结构
①液体分子间距介于气体分子间距和固体分子间距之间;
②液体分子的排列更接近于固体;
③液体分子间的相互作用力比固体分子间的作用力要小
【例】下面关于液体的说法正确的是( )
A.非晶体的结构跟液体非常类似,
可以看作是粘滞性极大的液体
B.液体的物理性质一般表现为各向同性
C.液体的密度总是小于固体的密度
D.所有的金属在常温下都是固体
⑴液体的表面张力
表面层
液体
汽
3、液体的特殊现象
液体的表面张力具有使液体表面收缩的趋势
请学生们分析下面这些现象,并解释产生的原因?
(1)雨伞的伞面有细小的孔,为什么水不会从孔里漏下去?
(2)将分币轻轻地放在一碗水的水面上,为什么分币
会浮在水面上不沉下去?
因为水将纱线浸湿后,在纱线孔隙中形成水膜,
水膜的表面张力使得雨水不致漏下.
这是由于表面张力使得液体表面形成一个张紧的薄膜,
当分币放置上后,使得液体表面发生形变,产生弹力,
这样受力平衡,所以分币会浮在水面上不沉下去。
⑵浸润和不浸润
⑴液体的表面张力
3、液体的特殊现象
⑶毛细现象
化学上如何检查试管是否刷的干净?
【例】人造卫星中有一个盛液体的容器
如果液体浸润容器壁,会发生什么现象?
如果液体不浸润器壁,又将出现什么现象?
【例】在水中浸入两个同样细的毛细管,
一个是直的,另一个是弯的,如图,水在直管
中上升的高度比弯管的最高点还要高,那么
弯管中的水能否流出 为什么
4、液晶
像液体一样具有流动性,
而其光学性质与某些晶体相似,具有各向异性
的一些化合物取名为液晶
液晶分子结构
液晶的应用:电子表显示窗
笔记本彩色显示器
人造生物膜
1、液体的微观结构
⑵浸润和不浸润
⑴液体的表面张力
2、液体的特殊现象
⑶毛细现象
3、液晶
9.3《饱和汽和
饱和气压》
教学目标
知识与能力
1.知道汽化及汽化的两种方式和其特点。
2.理解饱和汽与饱和汽压,能从分子动理论的角度解释有关现象。
3.理解空气的绝对湿度和相对湿度,并能进行简单计算。
4.了解湿度计的原理。
重点、难点:
1、理解饱和汽与饱和汽压,能从分子动理论的角度解释有关现象。
2、理解空气的绝对湿度和相对湿度,并能进行简单计算。
一、蒸发与沸腾
1.汽化:
物质从液态变成气态的过程
2.蒸发:
发生在液体表面,即液体分子由液体表面跑出去的过程
3.影响蒸发的因素:
表面积
温度
通风
液面气压高低
蒸发可使液体降温
4.沸腾:
在一定大气压下,加热液体到某一温度时,在液体表面和内部同时发生的剧烈的汽化现象,相应的温度叫沸点
t/0C
p/kPa
100
200
300
50
100
150
沸点与液面上气体的压强有关
蒸发 沸腾
相同点
不
同
点 发生部位
温度条件
剧烈程度
温度变化
影响因素
方式
项目
都是汽化现象,都能使液体变为气体,都吸收热量
液面
内部、液面同时进行
任何温度
一定温度(沸点)
缓慢
剧烈
降低
不变
1.液体温度的高低
2.液体表面积的大小
3.液体表面空气流动的快慢
4.液体汽压的高低
液面气压的高低
现象:减小瓶中的气压,水会沸腾。
表明:气压减小,水的沸点降低。
二、饱和汽和饱和汽压
1.饱和汽
在密闭容器中的液体不断的蒸发,液面上的蒸气也不断地凝结,当这两个同时存在的过程达到动态平衡时,宏观的蒸发也停止了,这种与液体处于动态平衡的蒸气叫做饱和汽。
2.未饱和汽:
没有达到饱和状态的蒸气
3.饱和汽压:
在一定温度下,饱和汽的分子数密度是一定的,
因而饱和汽的压强也是一定的,这个压强叫做
这种液体的饱和汽压。
说明:
(1)饱和汽压随温度的升高而增大。
(2)饱和汽压与蒸气所占的体积无关,也和这种体积中有无其他气体无关。
a.往一个真空容器中注入液体,表面的上方形成饱和蒸汽时,表面的上方空间的气压就是饱和汽压.
b.往一个密闭的原来有空气的容器中注入液体,表面的上方形成饱和蒸汽时,表面的上方空间的气压不等于饱和汽压,而是饱和汽压与空气压强的总和.
c.液体的饱和汽压只指这种气体的分气压.
温度升高时,分子平均动能增大,单位时间内逸出液面的分子数增多,于是原来的动态平衡状态被破坏,空间气态分子密度逐渐增大,导致单位时间内返回的分子数增多,从而达到新的条件下的动态平衡.
(3)液体沸腾的条件就是饱和汽压和外部压强相等
三、空气的湿度
1.绝对湿度:
空气里所含水汽的压强
2.相对湿度:
在某一温度下,水蒸汽的压强与同温度下饱和汽压的比,称为空气的相对湿度。
相对湿度
=
水蒸汽的实际压强
同温度下的饱和汽压
即B=
p
ps
X100%
3.影响蒸发快慢以及影响人们对干爽与潮湿感受的因素,不是空气中水蒸气的绝对数量,而是空气中水蒸气的压强与同一温度下水的饱和汽压的差距.
四、空气的湿度
1.空气的相对湿度常用湿度计来测量。
2.常用的湿度计有干湿泡湿度计、毛发湿度计和湿度传感器等
水蒸气的压强离饱和汽压越远,越有利于水的蒸发,人们感觉干爽.
9.4《物态变化中的
能量交换》
教学目标
知识与能力
1.知道熔化和熔化热、汽化和汽化热的概念。
2.会用熔化热和汽化热处理有关问题。
3.体会能的转化与守恒在物态变化中的应用。
重点、难点:
知道熔化和熔化热、汽化和汽化热的概念
会用熔化热和汽化热处理有关问题。
固态
液态
气态
熔化吸热
汽化吸热
凝固放热
液化放热
一、熔化热
物质从固态变成液态的过程。
物质从液态变成固态的过程。
熔化是凝固的逆过程。
1. 熔化与凝固
熔化:
凝固:
一、熔化热
由于固体分子间的强大作用,固体分子只能在各自的平衡位置附近振动,对固体加热,在其熔解之前,获得的能量主要转化为分子的动能,使物体温度升高,当温度升高到一定程度,一部分分子的能量足以克服其他分子的束缚,从而可以在其他分子间移动,固体开始熔解。
为什么熔化会吸热?
一、熔化热
2.熔化热:
某种晶体熔化过程中所需的能量与其
质量之比,称做这种晶体的熔化热
一定质量的晶体,熔化时吸收的热量与凝固时
放出的热量相等
一、熔化热
为什么晶体有确定的熔点和熔化热,非晶体却没有?
晶体熔化过程中,当温度达到熔点时,吸收的热量全部用
来破坏空间点阵,增加分子势能,而分子平均动能却保持不变,
所以晶体有固定的熔点。非晶体没有空间点阵,熔化时不需要
去破坏空间点阵,吸收的热量主要转化为分子的动能,不断吸
热,温度就不断上升。
由于在不同温度下物质由固态变成液态时吸收的热量不同,
而晶体有固定的熔点,因此有固定的熔化热,非晶体没有固定的
熔点,也就没有固定的熔化热。
一、熔化热
3.熔化热的计算
熔化时吸收的热量:Q=λm
二、汽化热
1.汽化与液化
汽化:
物质从液态变成气态的过程
液化:
物质从气态变成液态的过程
液体汽化时,为何要吸热?
二、汽化热
2.汽化热
某种液体汽化成同温度的气体时所需的能量与其质量之比,称做这种物质在这个温度下的汽化热。
汽化热跟温度和压强有关
t /0C
100
Q/(J.g-1)
500
1000
1500
2000
2500
0
200
300
400
水在大气压强为
1.01x105Pa下汽
化热与温度的关系
二、汽化热
一定质量的物质,在一定温度和压强下,汽化时吸收的热量与液化时放出的热量
相等
