第四单元 我们周围的空气 能力提升—2021-2022学年鲁教版九年级上册化学单元测试卷(word版 含解析)
文档属性
| 名称 | 第四单元 我们周围的空气 能力提升—2021-2022学年鲁教版九年级上册化学单元测试卷(word版 含解析) |  | |
| 格式 | doc | ||
| 文件大小 | 932.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-28 15:07:10 | ||
图片预览



文档简介
第四单元
我们周围的空气
B卷
能力提升
—2021-2022学年鲁教版九年级上册化学单元测试AB卷
(时间:
45分钟
满分:100分)
一、选择题:本大题共15小题,每小题4分,共60分
1.空气是一种重要的资源。下列有关空气的说法正确的是(
)
A.食品包装袋中充入氧气可延长食品的保质期
B.空气污染指数越高,空气质量越好
C.氧循环对维持自然界中物质、能量及生态的平衡有重要意义
D.分离液态空气得到氧气和氮气的过程中发生了化学变化
2.下列有关氧气的组成、结构、性质和用途的说法中,正确的是(
)
A.氧气极易溶于水
B.氧气是一种化学性质非常活泼的气体
C.氧气由氧元素组成,氧气由2个氧原子构成
D.炼钢、气焊以及化工生产和航空航天等都要用到氧气
3.下列选项不属于氧气在自然界中消耗途径的是(
)
A.生物的呼吸作用
B.绿色植物的光合作用
C.物质在空气中的燃烧
D.物质在空气中的缓慢氧化
4.地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成的化合物是(
)
A.
B.
C.
D.
5.如图是铁元素和氧元素常见化合价的坐标图,试判断点上形成化合物的化学式为(
)
A.
B.
C.
D.
6.下列化学符号所表示的含义正确的是(
)
A.He可表示氦气
B.表示2个氮原子
C.NaCl可表示1个氯化钠分子
D.只表示二氧化硫由硫、氧两种元素组成
7.景德镇的高岭土[主要成分:]是制造陶瓷器的优良原料。经分析,其中铝、氧元素质量比为3:8,则(
)
A.
B.
C.
D.
8.乙烯()是石油炼制的重要产物之一,常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是(
)
A.
B.
C.
D.
9.下列化学符号中数字“2”表示的意义不正确的是(
)。
A.:2个铵根离子
B.:一个水分子中含有一个氢分子
C.:1个镁离子带2个单位的正电荷
D.:氧化铜中铜元素的化合价为+2
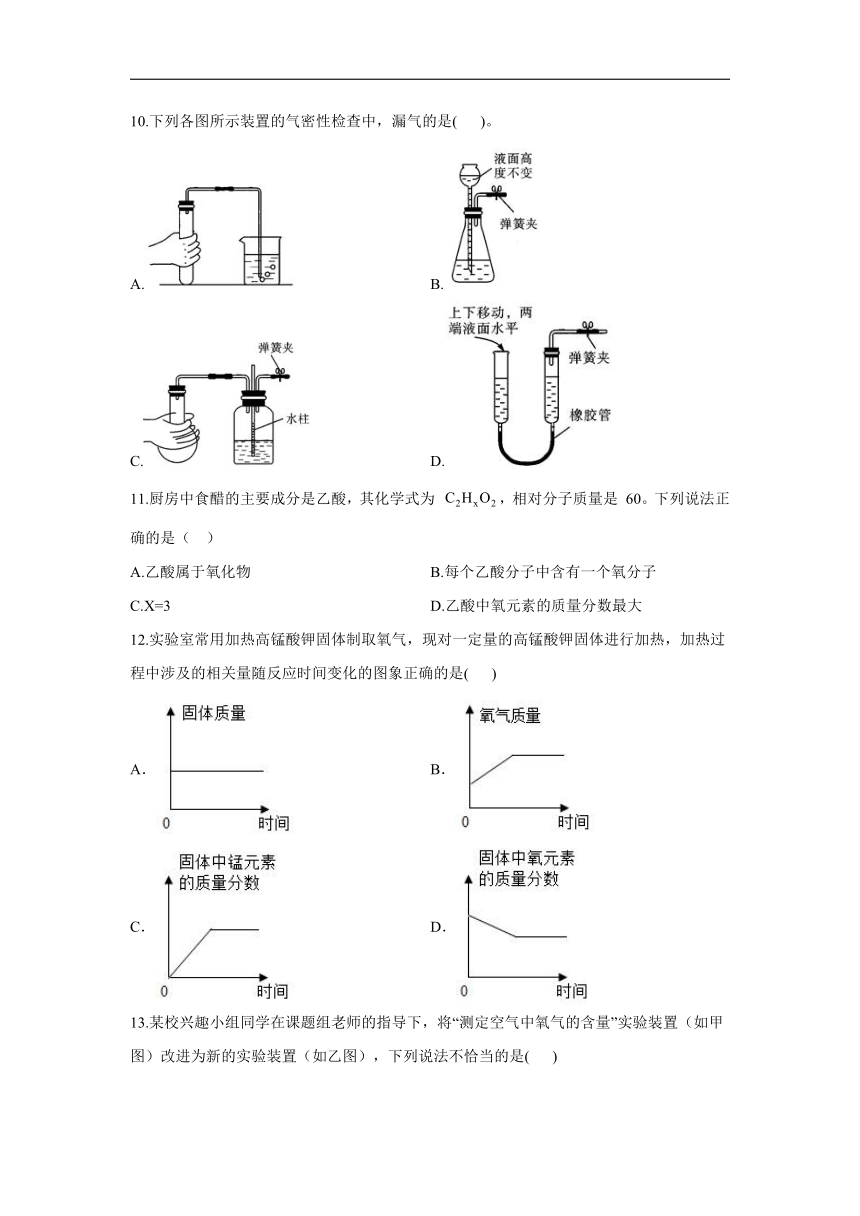
10.下列各图所示装置的气密性检查中,漏气的是(
)。
A.
B.
C.
D.
11.厨房中食醋的主要成分是乙酸,其化学式为
,相对分子质量是
60。下列说法正确的是(
)
A.乙酸属于氧化物
B.每个乙酸分子中含有一个氧分子
C.X=3
D.乙酸中氧元素的质量分数最大
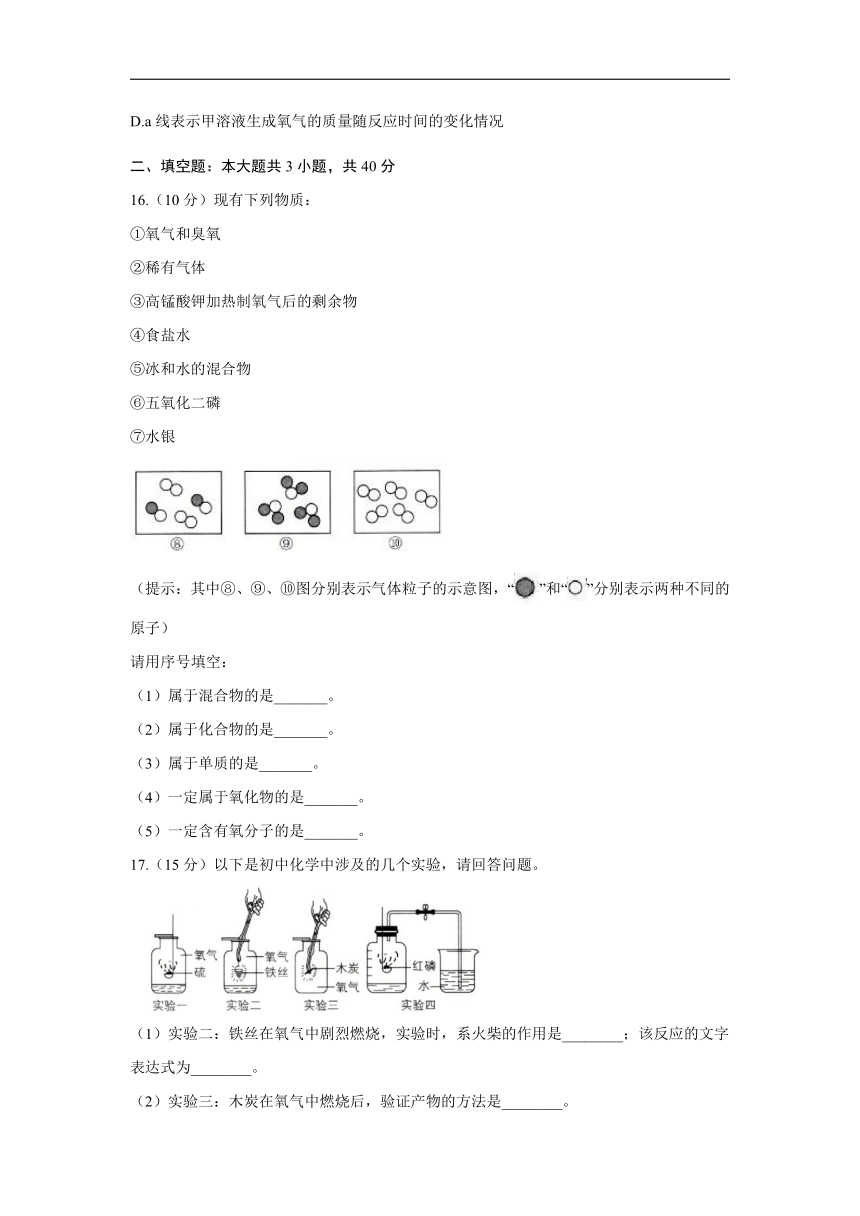
12.实验室常用加热高锰酸钾固体制取氧气,现对一定量的高锰酸钾固体进行加热,加热过程中涉及的相关量随反应时间变化的图象正确的是(
)
A.
B.
C.
D.
13.某校兴趣小组同学在课题组老师的指导下,将“测定空气中氧气的含量”实验装置(如甲图)改进为新的实验装置(如乙图),下列说法不恰当的是(
)
A.乙反应容器与甲相比体积更小,药品消耗更少
B.乙反应容器装置简洁,减少了甲装置中导管引起的误差
C.甲装置中反应前若止水夹未夹紧,则进入集气瓶中的水量偏大
D.乙反应容器中点燃白磷,胶塞会先向左后向右移动
14.小乐利用图甲所示装置测定空气中氧气的含量,其中燃烧匙内的白磷用电加热装置点燃,瓶内气压用气体压强传感器测定,其变化如图乙所示,则下列分析合理的是(
)
A.s后的一段时间内瓶内气压显著增加,其原因是白磷燃烧产生大量白雾
B.从瓶内气压达到最高点直至s,瓶内温度始终保持不变
C.通过s瓶内的气压值,可以计算得出氧气约占空气质量的五分之一
D.s后的一段时间内瓶内气压又显著增加,其原因是气体的体积减小
15.取甲、乙两份质量和浓度均相同的过氧化氢溶液,向甲中加入适量的二氧化锰,反应生成氧气的质量与反应时间的关系如图所示。从图中不能获取的信息是(
)
A.二氧化锰可改变过氧化氢的分解速率
B.甲、乙两份溶液最终生成氧气的质量相同
C.反应前后二氧化锰的质量和化学性质均不变
D.a线表示甲溶液生成氧气的质量随反应时间的变化情况
二、填空题:本大题共3小题,共40分
16.(10分)现有下列物质:
①氧气和臭氧
②稀有气体
③高锰酸钾加热制氧气后的剩余物
④食盐水
⑤冰和水的混合物
⑥五氧化二磷
⑦水银
(提示:其中⑧、⑨、⑩图分别表示气体粒子的示意图,“”和“”分别表示两种不同的原子)
请用序号填空:
(1)属于混合物的是_______。
(2)属于化合物的是_______。
(3)属于单质的是_______。
(4)一定属于氧化物的是_______。
(5)一定含有氧分子的是_______。
17.(15分)以下是初中化学中涉及的几个实验,请回答问题。
(1)实验二:铁丝在氧气中剧烈燃烧,实验时,系火柴的作用是________;该反应的文字表达式为________。
(2)实验三:木炭在氧气中燃烧后,验证产物的方法是________。
(3)实验四的实验目的是________;正确选择药品是实验成功的关键,实验中对药品的选择合理的是________(填序号)。
A.可以用铁丝代替红磷实验
B.红磷需要足量
C.产物不能为气体
(4)实验一、二、四中都要在集气瓶底部放少量的水,实验一中放水的作用是吸收二氧化硫,防止污染空气,由此推测,二氧化硫具有的物理性质之一是________。在实验一、二、四中,可以把水换成细沙的实验有________。
(5)从反应角度分析:以上四个反应的相同点是________(填序号)。
A.都是分解反应
B.都放出热量
C.产物在常温下均为固体
D.都是化合反应
18.(15分)某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快。对于此现象,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
实验步骤
实验现象
结论及解释
Ⅰ.
A中无明显现象,B中产生大量能使带火星的木条复燃的气体
产生的气体是氧气,淀粉能________
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣
又产生大量使带火星的木条复燃的气体,滤渣的质量为_______
淀粉质量和化学性质在反应前后均没有发生变化,能作过氧化氢分解的催化剂
(1)写出淀粉催化过氧化氢分解的文字表达式:_______。
【实验拓展】
(2)该小组设计了如图甲所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据如表:
实验编号
3%过氧化氢溶液的体积
其他物质质量
待测数据
Ⅰ
20mL
淀粉0.5g
x
Ⅱ
20mL
二氧化锰0.5g
y
上述实验中“待测数据”是指_______;若x>y,则可得出的结论是_______。
【拓展探究】
(3)某兴趣小组用如图乙所示装置进行了几组实验,取几个集气瓶,分别装入不同体积的水。用排水法收集氧气,恰好把几个集气瓶中的水排尽。将带火星的木条依次插入集气瓶中,发现当集气瓶预装水体积分数最低为35%时,木条复燃。这时集气瓶中氧气的体积分数是_______(计算结果保留一位小数),以上实验证明用带火星的木条检验氧气是否纯净的做法_______(填“可靠”或“不可靠”)。
答案以及解析
1.答案:C
解析:氧气的化学性质比较活泼,所以食品包装袋中不能填充氧气防腐,A错误;空气污染指数越高,空气质量越差,B错误;氧循环对维持自然界中物质、能量及生态的平衡有重要意义,C正确;分离液态空气得到氧气和氮气的过程中没有新物质生成,属于物理变化,D错误。
2.答案:D
解析:氧气不易溶于水,A不正确;氧气是一种化学性质比较活泼的气体,B不正确;氧气由氧分子构成,1个氧分子由2个氧原子构成,C不正确;氧气能够支持燃烧,可用于炼钢、气焊以及化工生产和航空航天等领域,D正确。
3.答案:B
解析:生物的呼吸作用、物质在空气中的燃烧及物质在空气中的缓慢氧化,都消耗氧气;绿色植物的光合作用消耗二氧化碳,生成氧气。
4.答案:A
解析:地壳中含量最多的金属元素是Al,含量最多的非金属元素是O,空气中含量最多的元素是N,所以由它们组成的化合物是,A正确。
5.答案:B
解析:点所示铁元素显+2价,氧元素显-2价,所以a点上形成化合物的化学式为FeO。
6.答案:A
解析:可表示1个氮分子;氯化钠是由钠离子和氯离子构成的;除了表示二氧化硫由硫、氧两种元素组成,还能表示1个二氧化硫分子等。
7.答案:D
解析:中铝和氧元素的质量比为,则。
8.答案:A
解析:乙烯中碳元素的质量分数为,因为混合气体的碳元素质量分数为87%,而乙烯中碳元素的质量分数小于87%,所以另一种气体中碳元素的质量分数一定大于87%。中碳元素的质量分数为;中碳元素的质量分数为;中不含有碳元素,碳元素的质量分数为0;中碳元素的质量分数为。故选A。
9.答案:B
10.答案:D
11.答案:D
12.答案:D
解析:A、加热高锰酸钾时有氧气生成,故固体的质量减少,故错误;
B、加热高锰酸钾刚开始时没有氧气生成,故错误;
C、刚开始反应时,固体中含有锰元素,故锰元素的质量分数不可能是0,故错误;
D、由于氧气的生成,故固体中氧元素的质量分数减少,当反应停止后,氧元素的质量分数不变,故正确。故选D。
13.答案:D
解析:乙改用玻璃管进行实验,比甲中集气瓶体积小,空气体积小,所以药品消耗更少,故A正确;乙反应容器装置简洁,减少了甲装置中导管引起的误差,故B正确;甲装置中反应前若上水夹未夹紧,白磷燃烧放热,导致部分气体通过导管逸出,则进入集气瓶中的水量偏大,故C正确;乙反应容器中点燃白磷,白磷燃烧放热,气体压强增大,胶塞向右移动,完全反应后温度降低,由于氧气被消耗,所以气体压强比开始时小,胶塞向左移动,故D不正确。
14.答案:D
解析:白磷燃烧产生大量白烟,而不是白雾,A错误;当氧气耗尽,反应停止,温度会下降,B错误;空气中氧气约占空气体积的五分之一,C错误;白磷燃烧消耗左侧装置中的氧气,导致左侧装置中气压小于外界大气压,s时打开活塞,烧杯中的水进入左侧装置中,占据一部分体积,导致左侧装置中气体体积减小,气压增大至与外界大气压相等,D正确。
15.答案:C
解析:A项,甲中加入了二氧化猛,过氧化氢分解速率增大,图像体现出来了这一点;B项,催化剂不能改变生成物的质量,故甲、乙两份等质量且浓度均相同的过氧化氢溶液完全反应后生
成氧气的质量相等,此图像能体现出来这一点;C项,在此反应中,二氧化锰为催化剂,其质量和化学性质在反应前后均不改变,但是此图像没有体现出来这一点;D项,反应过程中,甲溶液产生氧气的速率比乙溶液的大,由图像可知,a线表示甲溶液生成氧气的质量随反应时间的变化情况。
16.答案:(1)①②③④⑧
(2)⑤⑥⑨
(3)⑦⑩
(4)⑤⑥
(5)①
17.答案:(1)引燃铁丝;铁+氧气四氧化三铁
(2)在瓶中加入少量的澄清石灰水,振荡,若澄清石灰水变浑浊,则产物为二氧化碳
(3)测定空气中氧气的含量;BC
(4)能溶于水;实验二
(5)BD
解析:(1)铁丝在氧气中剧烈燃烧,生成了四氧化三铁,实验时,系火柴的作用是引燃铁丝。
(2)木炭在氧气中燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以木炭在氧气中燃烧后,验证产物的方法是在瓶中加入少量的澄清石灰水,振荡,若澄清石灰水变浑浊,则产物为二氧化碳。
(3)由实验四的装置图可知,实验四的实验目的是测定空气中氧气的含量;铁丝在空气中不能燃烧,不能代替红磷实验;红磷需要足量,目的是将容器内的氧气耗尽;产物不能为气体,否则集气瓶内的压强变化不明显,无法测定空气中氧气的含量。
(4)水能吸收二氧化硫,说明二氧化硫具有的物理性质之一是能溶于水。实验二中水的作用是防止反应生成的高温熔融物溅落炸裂瓶底,故可以把水换成细沙,而实验一和实验四中的水均有吸收生成物的作用。
(5)从反应角度分析:题述四个反应的相同点是都放出热量、都是化合反应。
18.答案:Ⅰ.加快过氧化氢的分解速率
Ⅱ.ag
(1)过氧化氢水+氧气
(2)收集25mL氧气所需的时间;在其他条件相同的情况下,二氧化锰的催化效果比淀粉好
(3)48.7%;不可靠
解析:Ⅰ.分析图示可知,由于A试管中无明显现象,B试管中产生大量能使带火星的木条复燃的气体,则产生的气体是氧气并且淀粉能加快过氧化氢的分解速率;Ⅱ.催化剂在化学反应前后其本身的质量和化学性质不变,由实验结论及解释可知,滤渣为淀粉,是该反应的催化剂,则质量仍为ag。
(1)过氧化氢在淀粉催化下分解生成氧气和水,反应的文字表达式:过氧化氢水+氧气。
(2)小组设计了如图甲所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,分析实验方案可知,“待测数据”是指收集25mL氧气所需的时间,若x>y,则可得出的结论是在其他条件相同的情况下,二氧化锰的催化效果比淀粉好。
(3)空气中氧气的体积分数约为21%,分析题中数据可知,木条复燃时集气瓶中氧气的体积分数是35%+(1-35%)×21%≈48.7%<100%,则以上实验证明用带火星的木条检验氧气是否纯净的做法不可靠。
我们周围的空气
B卷
能力提升
—2021-2022学年鲁教版九年级上册化学单元测试AB卷
(时间:
45分钟
满分:100分)
一、选择题:本大题共15小题,每小题4分,共60分
1.空气是一种重要的资源。下列有关空气的说法正确的是(
)
A.食品包装袋中充入氧气可延长食品的保质期
B.空气污染指数越高,空气质量越好
C.氧循环对维持自然界中物质、能量及生态的平衡有重要意义
D.分离液态空气得到氧气和氮气的过程中发生了化学变化
2.下列有关氧气的组成、结构、性质和用途的说法中,正确的是(
)
A.氧气极易溶于水
B.氧气是一种化学性质非常活泼的气体
C.氧气由氧元素组成,氧气由2个氧原子构成
D.炼钢、气焊以及化工生产和航空航天等都要用到氧气
3.下列选项不属于氧气在自然界中消耗途径的是(
)
A.生物的呼吸作用
B.绿色植物的光合作用
C.物质在空气中的燃烧
D.物质在空气中的缓慢氧化
4.地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成的化合物是(
)
A.
B.
C.
D.
5.如图是铁元素和氧元素常见化合价的坐标图,试判断点上形成化合物的化学式为(
)
A.
B.
C.
D.
6.下列化学符号所表示的含义正确的是(
)
A.He可表示氦气
B.表示2个氮原子
C.NaCl可表示1个氯化钠分子
D.只表示二氧化硫由硫、氧两种元素组成
7.景德镇的高岭土[主要成分:]是制造陶瓷器的优良原料。经分析,其中铝、氧元素质量比为3:8,则(
)
A.
B.
C.
D.
8.乙烯()是石油炼制的重要产物之一,常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是(
)
A.
B.
C.
D.
9.下列化学符号中数字“2”表示的意义不正确的是(
)。
A.:2个铵根离子
B.:一个水分子中含有一个氢分子
C.:1个镁离子带2个单位的正电荷
D.:氧化铜中铜元素的化合价为+2
10.下列各图所示装置的气密性检查中,漏气的是(
)。
A.
B.
C.
D.
11.厨房中食醋的主要成分是乙酸,其化学式为
,相对分子质量是
60。下列说法正确的是(
)
A.乙酸属于氧化物
B.每个乙酸分子中含有一个氧分子
C.X=3
D.乙酸中氧元素的质量分数最大
12.实验室常用加热高锰酸钾固体制取氧气,现对一定量的高锰酸钾固体进行加热,加热过程中涉及的相关量随反应时间变化的图象正确的是(
)
A.
B.
C.
D.
13.某校兴趣小组同学在课题组老师的指导下,将“测定空气中氧气的含量”实验装置(如甲图)改进为新的实验装置(如乙图),下列说法不恰当的是(
)
A.乙反应容器与甲相比体积更小,药品消耗更少
B.乙反应容器装置简洁,减少了甲装置中导管引起的误差
C.甲装置中反应前若止水夹未夹紧,则进入集气瓶中的水量偏大
D.乙反应容器中点燃白磷,胶塞会先向左后向右移动
14.小乐利用图甲所示装置测定空气中氧气的含量,其中燃烧匙内的白磷用电加热装置点燃,瓶内气压用气体压强传感器测定,其变化如图乙所示,则下列分析合理的是(
)
A.s后的一段时间内瓶内气压显著增加,其原因是白磷燃烧产生大量白雾
B.从瓶内气压达到最高点直至s,瓶内温度始终保持不变
C.通过s瓶内的气压值,可以计算得出氧气约占空气质量的五分之一
D.s后的一段时间内瓶内气压又显著增加,其原因是气体的体积减小
15.取甲、乙两份质量和浓度均相同的过氧化氢溶液,向甲中加入适量的二氧化锰,反应生成氧气的质量与反应时间的关系如图所示。从图中不能获取的信息是(
)
A.二氧化锰可改变过氧化氢的分解速率
B.甲、乙两份溶液最终生成氧气的质量相同
C.反应前后二氧化锰的质量和化学性质均不变
D.a线表示甲溶液生成氧气的质量随反应时间的变化情况
二、填空题:本大题共3小题,共40分
16.(10分)现有下列物质:
①氧气和臭氧
②稀有气体
③高锰酸钾加热制氧气后的剩余物
④食盐水
⑤冰和水的混合物
⑥五氧化二磷
⑦水银
(提示:其中⑧、⑨、⑩图分别表示气体粒子的示意图,“”和“”分别表示两种不同的原子)
请用序号填空:
(1)属于混合物的是_______。
(2)属于化合物的是_______。
(3)属于单质的是_______。
(4)一定属于氧化物的是_______。
(5)一定含有氧分子的是_______。
17.(15分)以下是初中化学中涉及的几个实验,请回答问题。
(1)实验二:铁丝在氧气中剧烈燃烧,实验时,系火柴的作用是________;该反应的文字表达式为________。
(2)实验三:木炭在氧气中燃烧后,验证产物的方法是________。
(3)实验四的实验目的是________;正确选择药品是实验成功的关键,实验中对药品的选择合理的是________(填序号)。
A.可以用铁丝代替红磷实验
B.红磷需要足量
C.产物不能为气体
(4)实验一、二、四中都要在集气瓶底部放少量的水,实验一中放水的作用是吸收二氧化硫,防止污染空气,由此推测,二氧化硫具有的物理性质之一是________。在实验一、二、四中,可以把水换成细沙的实验有________。
(5)从反应角度分析:以上四个反应的相同点是________(填序号)。
A.都是分解反应
B.都放出热量
C.产物在常温下均为固体
D.都是化合反应
18.(15分)某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快。对于此现象,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
实验步骤
实验现象
结论及解释
Ⅰ.
A中无明显现象,B中产生大量能使带火星的木条复燃的气体
产生的气体是氧气,淀粉能________
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣
又产生大量使带火星的木条复燃的气体,滤渣的质量为_______
淀粉质量和化学性质在反应前后均没有发生变化,能作过氧化氢分解的催化剂
(1)写出淀粉催化过氧化氢分解的文字表达式:_______。
【实验拓展】
(2)该小组设计了如图甲所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据如表:
实验编号
3%过氧化氢溶液的体积
其他物质质量
待测数据
Ⅰ
20mL
淀粉0.5g
x
Ⅱ
20mL
二氧化锰0.5g
y
上述实验中“待测数据”是指_______;若x>y,则可得出的结论是_______。
【拓展探究】
(3)某兴趣小组用如图乙所示装置进行了几组实验,取几个集气瓶,分别装入不同体积的水。用排水法收集氧气,恰好把几个集气瓶中的水排尽。将带火星的木条依次插入集气瓶中,发现当集气瓶预装水体积分数最低为35%时,木条复燃。这时集气瓶中氧气的体积分数是_______(计算结果保留一位小数),以上实验证明用带火星的木条检验氧气是否纯净的做法_______(填“可靠”或“不可靠”)。
答案以及解析
1.答案:C
解析:氧气的化学性质比较活泼,所以食品包装袋中不能填充氧气防腐,A错误;空气污染指数越高,空气质量越差,B错误;氧循环对维持自然界中物质、能量及生态的平衡有重要意义,C正确;分离液态空气得到氧气和氮气的过程中没有新物质生成,属于物理变化,D错误。
2.答案:D
解析:氧气不易溶于水,A不正确;氧气是一种化学性质比较活泼的气体,B不正确;氧气由氧分子构成,1个氧分子由2个氧原子构成,C不正确;氧气能够支持燃烧,可用于炼钢、气焊以及化工生产和航空航天等领域,D正确。
3.答案:B
解析:生物的呼吸作用、物质在空气中的燃烧及物质在空气中的缓慢氧化,都消耗氧气;绿色植物的光合作用消耗二氧化碳,生成氧气。
4.答案:A
解析:地壳中含量最多的金属元素是Al,含量最多的非金属元素是O,空气中含量最多的元素是N,所以由它们组成的化合物是,A正确。
5.答案:B
解析:点所示铁元素显+2价,氧元素显-2价,所以a点上形成化合物的化学式为FeO。
6.答案:A
解析:可表示1个氮分子;氯化钠是由钠离子和氯离子构成的;除了表示二氧化硫由硫、氧两种元素组成,还能表示1个二氧化硫分子等。
7.答案:D
解析:中铝和氧元素的质量比为,则。
8.答案:A
解析:乙烯中碳元素的质量分数为,因为混合气体的碳元素质量分数为87%,而乙烯中碳元素的质量分数小于87%,所以另一种气体中碳元素的质量分数一定大于87%。中碳元素的质量分数为;中碳元素的质量分数为;中不含有碳元素,碳元素的质量分数为0;中碳元素的质量分数为。故选A。
9.答案:B
10.答案:D
11.答案:D
12.答案:D
解析:A、加热高锰酸钾时有氧气生成,故固体的质量减少,故错误;
B、加热高锰酸钾刚开始时没有氧气生成,故错误;
C、刚开始反应时,固体中含有锰元素,故锰元素的质量分数不可能是0,故错误;
D、由于氧气的生成,故固体中氧元素的质量分数减少,当反应停止后,氧元素的质量分数不变,故正确。故选D。
13.答案:D
解析:乙改用玻璃管进行实验,比甲中集气瓶体积小,空气体积小,所以药品消耗更少,故A正确;乙反应容器装置简洁,减少了甲装置中导管引起的误差,故B正确;甲装置中反应前若上水夹未夹紧,白磷燃烧放热,导致部分气体通过导管逸出,则进入集气瓶中的水量偏大,故C正确;乙反应容器中点燃白磷,白磷燃烧放热,气体压强增大,胶塞向右移动,完全反应后温度降低,由于氧气被消耗,所以气体压强比开始时小,胶塞向左移动,故D不正确。
14.答案:D
解析:白磷燃烧产生大量白烟,而不是白雾,A错误;当氧气耗尽,反应停止,温度会下降,B错误;空气中氧气约占空气体积的五分之一,C错误;白磷燃烧消耗左侧装置中的氧气,导致左侧装置中气压小于外界大气压,s时打开活塞,烧杯中的水进入左侧装置中,占据一部分体积,导致左侧装置中气体体积减小,气压增大至与外界大气压相等,D正确。
15.答案:C
解析:A项,甲中加入了二氧化猛,过氧化氢分解速率增大,图像体现出来了这一点;B项,催化剂不能改变生成物的质量,故甲、乙两份等质量且浓度均相同的过氧化氢溶液完全反应后生
成氧气的质量相等,此图像能体现出来这一点;C项,在此反应中,二氧化锰为催化剂,其质量和化学性质在反应前后均不改变,但是此图像没有体现出来这一点;D项,反应过程中,甲溶液产生氧气的速率比乙溶液的大,由图像可知,a线表示甲溶液生成氧气的质量随反应时间的变化情况。
16.答案:(1)①②③④⑧
(2)⑤⑥⑨
(3)⑦⑩
(4)⑤⑥
(5)①
17.答案:(1)引燃铁丝;铁+氧气四氧化三铁
(2)在瓶中加入少量的澄清石灰水,振荡,若澄清石灰水变浑浊,则产物为二氧化碳
(3)测定空气中氧气的含量;BC
(4)能溶于水;实验二
(5)BD
解析:(1)铁丝在氧气中剧烈燃烧,生成了四氧化三铁,实验时,系火柴的作用是引燃铁丝。
(2)木炭在氧气中燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以木炭在氧气中燃烧后,验证产物的方法是在瓶中加入少量的澄清石灰水,振荡,若澄清石灰水变浑浊,则产物为二氧化碳。
(3)由实验四的装置图可知,实验四的实验目的是测定空气中氧气的含量;铁丝在空气中不能燃烧,不能代替红磷实验;红磷需要足量,目的是将容器内的氧气耗尽;产物不能为气体,否则集气瓶内的压强变化不明显,无法测定空气中氧气的含量。
(4)水能吸收二氧化硫,说明二氧化硫具有的物理性质之一是能溶于水。实验二中水的作用是防止反应生成的高温熔融物溅落炸裂瓶底,故可以把水换成细沙,而实验一和实验四中的水均有吸收生成物的作用。
(5)从反应角度分析:题述四个反应的相同点是都放出热量、都是化合反应。
18.答案:Ⅰ.加快过氧化氢的分解速率
Ⅱ.ag
(1)过氧化氢水+氧气
(2)收集25mL氧气所需的时间;在其他条件相同的情况下,二氧化锰的催化效果比淀粉好
(3)48.7%;不可靠
解析:Ⅰ.分析图示可知,由于A试管中无明显现象,B试管中产生大量能使带火星的木条复燃的气体,则产生的气体是氧气并且淀粉能加快过氧化氢的分解速率;Ⅱ.催化剂在化学反应前后其本身的质量和化学性质不变,由实验结论及解释可知,滤渣为淀粉,是该反应的催化剂,则质量仍为ag。
(1)过氧化氢在淀粉催化下分解生成氧气和水,反应的文字表达式:过氧化氢水+氧气。
(2)小组设计了如图甲所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,分析实验方案可知,“待测数据”是指收集25mL氧气所需的时间,若x>y,则可得出的结论是在其他条件相同的情况下,二氧化锰的催化效果比淀粉好。
(3)空气中氧气的体积分数约为21%,分析题中数据可知,木条复燃时集气瓶中氧气的体积分数是35%+(1-35%)×21%≈48.7%<100%,则以上实验证明用带火星的木条检验氧气是否纯净的做法不可靠。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
