2021-2022学年初中化学人教版九年级下册 第九单元 课题2 第2课时 溶解度 课件(31张PPT)
文档属性
| 名称 | 2021-2022学年初中化学人教版九年级下册 第九单元 课题2 第2课时 溶解度 课件(31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-28 00:00:00 | ||
图片预览








文档简介
(共31张PPT)
第2课时
溶解度
R·九年级化学下册
第九单元
溶液
课题2
溶解度
课前自学准备
课标要求
学习目标
1.了解固体物质溶解度的涵义。
2.会利用溶解性表或溶解度曲线,查阅相关物质的溶解性或溶解度,能依据给定的数据绘制溶解度曲线。
3.知道影响气体溶解度的一些因素,会利用有关气体溶解度的知识解释身边的一些现象。
利用溶解度曲线获得相关信息。
3.影响气体溶解度的因素有
和
。气体的溶解度
随温度的升高而
,随压强的增大而
。
2.大多数固体物质的溶解度随着温度的升高而
,如
;少数物质的溶解度随着温度的升高而
,
如
;极少数物质的溶解度随着温度的升高而
,
如
。
课前自学准备
预习检测
1.在一定温度下,某固态物质在
溶剂里达到饱和状态
时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
增大
100g
KNO3
变化不大
NaCl
减小
Ca(OH)2
温度
压强
减小
增大
课堂教学展示
新课导入
为什么只有在“两个一定”的条件下,饱和溶液的定义才有意义?
我们常说某种物质易溶、难溶,那么这种特性又是如何定义的呢?
课堂教学展示
课堂探究
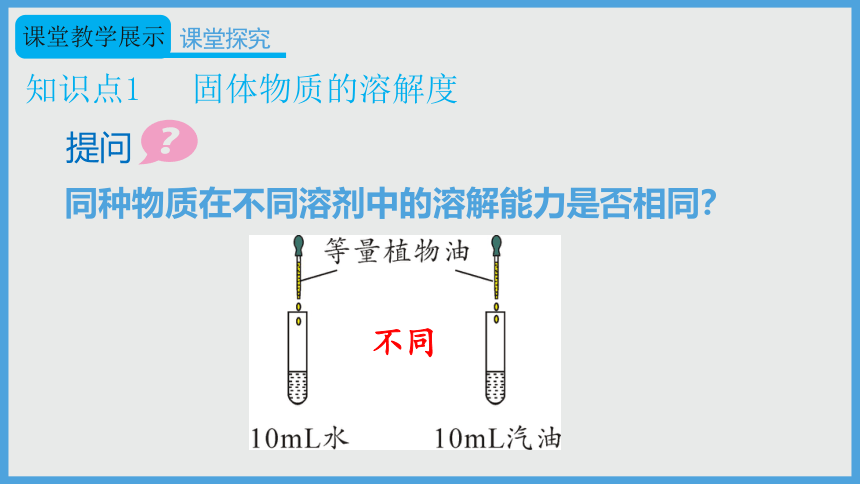
知识点1
固体物质的溶解度
同种物质在不同溶剂中的溶解能力是否相同?
不同
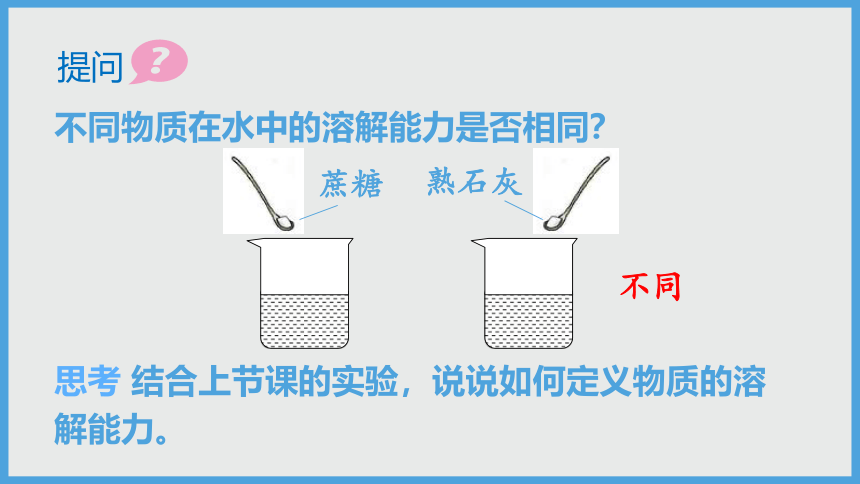
不同物质在水中的溶解能力是否相同?
不同
蔗糖
熟石灰
思考
结合上节课的实验,说说如何定义物质的溶解能力。
在一定量水中,最多溶解NaCl的量是一定的。
在一定温度下,在一定量溶剂里溶质的溶解量是有限度的。
溶解度
固体物质的溶解度是指在一定温度下,该物质在100g溶剂(通常溶剂为水)达到饱和状态时所溶解的质量。
注意
1
2
3
4
一定温度下;
100g溶剂里;
溶液为饱和状态;
溶质的质量。
描述溶解度时要注意以下几点:
例:蔗糖在20
℃时的溶解度是203.9
g。
固体溶解度的意义
在20
℃时,100
g水中溶解203.9
g蔗糖,溶液
达到饱和。在20
℃时,100
g水中最多可溶解
203.9
g蔗糖。
思考:蔗糖溶解度大于氯化钠的溶解度,这种说法
对么?
表示:
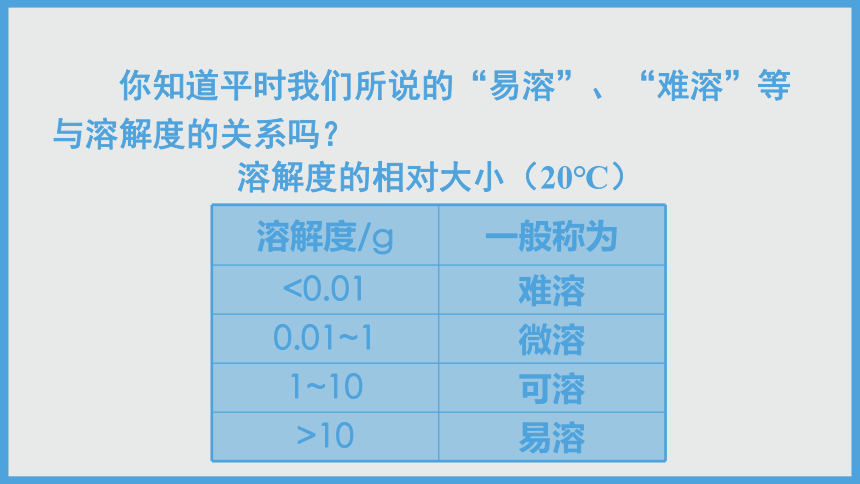
你知道平时我们所说的“易溶”、“难溶”等与溶解度的关系吗?
溶解度/g
一般称为
<0.01
难溶
0.01~1
微溶
1~10
可溶
>10
易溶
溶解度的相对大小(20℃)
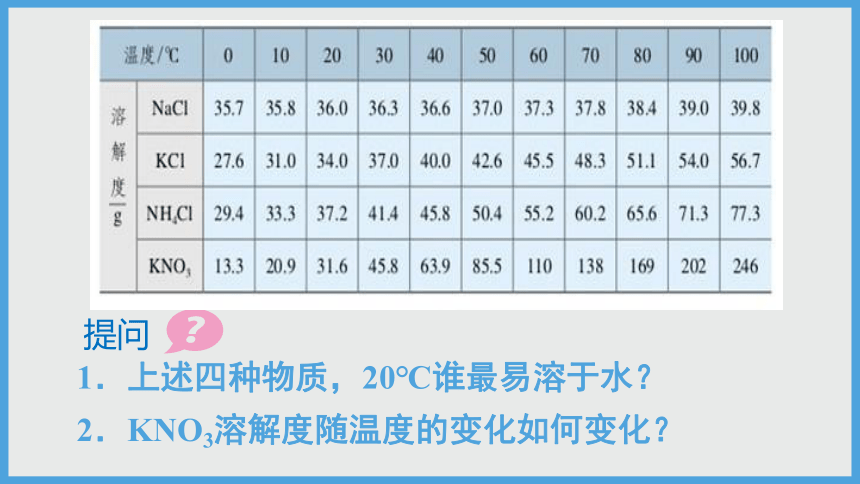
1.上述四种物质,20℃谁最易溶于水?
2.KNO3溶解度随温度的变化如何变化?
课堂教学展示
典例剖析
例
20℃时,氯化钠的溶解度是36g,这表示(
)
A.20℃时,100g氯化钠饱和溶液中含氯化钠36g
B.20℃时,100g水中溶解36g氯化钠,溶液达到饱
和状态
C.100g水中最多溶解36g氯化钠
D.20℃时,氯化钠在水中溶解36g,溶液达到饱和
状态
B
×
×
×
√
知识点2
溶解度曲线
课堂教学展示
课堂探究
某种物质的溶解度除了列表表示,还有更直观的表示方法吗?
溶解度曲线
溶解度曲线如何绘制呢?
探究
温度℃
0
20
40
60
70
80
90
溶解度
g/100
g水
13.3
31.6
63.9
110
138
169
202
例:硝酸钾
0
t
/℃
40
80
120
160
200
g/100
g水
s
70
20
40
60
80
100
90
思考:
KNO3的溶解度随温度变化有什么规律?
思考:
A点对应的溶液状态是?
A
1.曲线上任一点:表示某物质在某温度时的溶解度;
溶液所处的状态是饱和溶液;
2.曲线上方的点:表示某温度下某物质的溶液中溶质有剩余;溶液所处的状态是饱和溶液
;
3.曲线下方的点:表示某温度下某物质溶液中溶质的量不足;溶液所处的状态是不饱和溶液。
0
t
/℃
40
80
120
160
200
g/100
g水
S
70
20
40
60
80
100
90
思考:你还能获得哪些信息?
(硝酸钾在任意温度时的溶解度)
列表法是以实验为基础,数据准确,但不能看出任意温度下的溶解度,有一定局限性。
两种溶解度的表示方法有什么不同?
交流讨论
1
2
溶解度曲线可以直观表示溶解度随温度变化趋势,能查到任一温度下的溶解度,但数据存在误差。
1.
溶解度的三种情况:
(1)大多数物质的溶解度随温度的升高而增大,
如KNO3。
(2)少数物质的溶解度受温度的影响不大,如
NaCl。
(3)极少数物质的溶解度随温度的升高而减小,
如Ca(OH)2。
2.
影响固体溶解度的因素是:温度。
我们研究了固体物质的溶解度,那么气体物质的溶解度又该如何定义,又与什么有关呢?
定义:气体溶解度是指在101kPa和一定温度时,溶解在1体积水里达到饱和状态时的气体体积。
交流讨论
1.
打开汽水盖时,汽水会自动喷出来,这说明气体在水中的溶解度与什么有关?
2.喝了汽水后,常常会打嗝。这说明气体的溶解度还与什么有关?
压强:压强减小,气体在水中的溶解度减小。
温度:温度升高,气体在水中的溶解度减小。
3.烧开水刚开始一会儿,锅底会有很多小气泡,为什么?
水中溶解有气体,这说明温度升高气体的溶解度变小。
气体的溶解度与压强有关。压强越大,溶解度越大,压强越小,溶解度越小;
气体的溶解度与温度有关。温度越高,溶解度越小。
课堂教学展示
典例剖析
例
如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是(
)
A.20℃时,甲的溶解度大于乙的溶解度
B.40℃时,甲、乙两种物质的溶解度相等
C.采用降温的方法可以将乙的不饱
和溶液转化为饱和溶液
D.60℃时,在100g水中加入100g甲,
充分溶解后溶液质量为200g
B
课堂教学展示
课堂小结
第2课时
溶解度
一、固体的溶解度
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
三、溶解度曲线的意义:
1.溶解度的三种情况:
(1)大多数物质的溶解度随温度的升高而
增大,如KNO3。
(2)少数物质的溶解度受温度的影响不大,
如NaCl。
(3)极少数物质的溶解度随温度的升高而
减小,如Ca(OH)2。
2.交点P表示,在该温度下,A、B两种物质的溶解度相等。
3.影响固体溶解度的因素是:温度。
四、气体的溶解度
1.定义:在压强为101KPa和一定温度时,气
体溶解在1体积水里达到饱和状态时的气体体积。
2.影响因素
温度:随温度升高,气体溶解度减小。
压强:随压强增大,气体溶解度增大。
1.从课后习题中选取;
2.完成练习册本课时的习题。
课后反馈总结
课后作业
2.在60℃时,硝酸钾的溶解度是110g。这句话的含义是
。
在60℃时,110g硝酸钾溶解在100g水中,所得溶液恰好为该温度下硝酸钾的饱和溶液(或在60℃时,100g水最多能溶解110g硝酸钾固体)
课后反馈总结
课本习题
练习与应用(P40)
3.查溶解度曲线,在表中空白处填上该物质的溶解度。
4.甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答下列问题:
(1)a3℃时,三种物质的溶解度
由大到小的顺序是
;
(2)a2℃时,
和
的溶解度
大小相等;?
(3)三种物质中,
的溶解度受温度的影响最大,
的溶解度受温度的影响最小,
的溶解度随温度的升高而减小。
甲>丙>乙
甲
丙
甲
乙
丙
5.甲、乙两种物质的溶解度曲线如右图所示。下列说法中正确的是(
)
A.a1℃时甲和乙的饱和溶液,
升温到a2℃时仍是饱和溶液?
B.甲和乙的溶解度相等?
C.a1℃时,甲和乙各30g分别
加入100g水中,均形成饱和溶液?
D.a2℃时,在100g水中加入60g甲,形成不饱和溶液
C
9.加热冷水,当温度尚未达到沸点时,为什么水中常有气泡冒出?天气闷热时,鱼塘里的鱼为什么总是接近水面游动?
解:在水中总是溶解有一些气体,冷水受热时,温度升高,气体的溶解度减小,因此即使尚未达到沸点,也常有气泡冒出。天气闷热时,水温高,水中氧气的溶解度变小,溶解的氧气少了,而水面与空气接触,溶解的氧气相对多些,因此鱼总是接近水面游动。
第2课时
溶解度
R·九年级化学下册
第九单元
溶液
课题2
溶解度
课前自学准备
课标要求
学习目标
1.了解固体物质溶解度的涵义。
2.会利用溶解性表或溶解度曲线,查阅相关物质的溶解性或溶解度,能依据给定的数据绘制溶解度曲线。
3.知道影响气体溶解度的一些因素,会利用有关气体溶解度的知识解释身边的一些现象。
利用溶解度曲线获得相关信息。
3.影响气体溶解度的因素有
和
。气体的溶解度
随温度的升高而
,随压强的增大而
。
2.大多数固体物质的溶解度随着温度的升高而
,如
;少数物质的溶解度随着温度的升高而
,
如
;极少数物质的溶解度随着温度的升高而
,
如
。
课前自学准备
预习检测
1.在一定温度下,某固态物质在
溶剂里达到饱和状态
时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
增大
100g
KNO3
变化不大
NaCl
减小
Ca(OH)2
温度
压强
减小
增大
课堂教学展示
新课导入
为什么只有在“两个一定”的条件下,饱和溶液的定义才有意义?
我们常说某种物质易溶、难溶,那么这种特性又是如何定义的呢?
课堂教学展示
课堂探究
知识点1
固体物质的溶解度
同种物质在不同溶剂中的溶解能力是否相同?
不同
不同物质在水中的溶解能力是否相同?
不同
蔗糖
熟石灰
思考
结合上节课的实验,说说如何定义物质的溶解能力。
在一定量水中,最多溶解NaCl的量是一定的。
在一定温度下,在一定量溶剂里溶质的溶解量是有限度的。
溶解度
固体物质的溶解度是指在一定温度下,该物质在100g溶剂(通常溶剂为水)达到饱和状态时所溶解的质量。
注意
1
2
3
4
一定温度下;
100g溶剂里;
溶液为饱和状态;
溶质的质量。
描述溶解度时要注意以下几点:
例:蔗糖在20
℃时的溶解度是203.9
g。
固体溶解度的意义
在20
℃时,100
g水中溶解203.9
g蔗糖,溶液
达到饱和。在20
℃时,100
g水中最多可溶解
203.9
g蔗糖。
思考:蔗糖溶解度大于氯化钠的溶解度,这种说法
对么?
表示:
你知道平时我们所说的“易溶”、“难溶”等与溶解度的关系吗?
溶解度/g
一般称为
<0.01
难溶
0.01~1
微溶
1~10
可溶
>10
易溶
溶解度的相对大小(20℃)
1.上述四种物质,20℃谁最易溶于水?
2.KNO3溶解度随温度的变化如何变化?
课堂教学展示
典例剖析
例
20℃时,氯化钠的溶解度是36g,这表示(
)
A.20℃时,100g氯化钠饱和溶液中含氯化钠36g
B.20℃时,100g水中溶解36g氯化钠,溶液达到饱
和状态
C.100g水中最多溶解36g氯化钠
D.20℃时,氯化钠在水中溶解36g,溶液达到饱和
状态
B
×
×
×
√
知识点2
溶解度曲线
课堂教学展示
课堂探究
某种物质的溶解度除了列表表示,还有更直观的表示方法吗?
溶解度曲线
溶解度曲线如何绘制呢?
探究
温度℃
0
20
40
60
70
80
90
溶解度
g/100
g水
13.3
31.6
63.9
110
138
169
202
例:硝酸钾
0
t
/℃
40
80
120
160
200
g/100
g水
s
70
20
40
60
80
100
90
思考:
KNO3的溶解度随温度变化有什么规律?
思考:
A点对应的溶液状态是?
A
1.曲线上任一点:表示某物质在某温度时的溶解度;
溶液所处的状态是饱和溶液;
2.曲线上方的点:表示某温度下某物质的溶液中溶质有剩余;溶液所处的状态是饱和溶液
;
3.曲线下方的点:表示某温度下某物质溶液中溶质的量不足;溶液所处的状态是不饱和溶液。
0
t
/℃
40
80
120
160
200
g/100
g水
S
70
20
40
60
80
100
90
思考:你还能获得哪些信息?
(硝酸钾在任意温度时的溶解度)
列表法是以实验为基础,数据准确,但不能看出任意温度下的溶解度,有一定局限性。
两种溶解度的表示方法有什么不同?
交流讨论
1
2
溶解度曲线可以直观表示溶解度随温度变化趋势,能查到任一温度下的溶解度,但数据存在误差。
1.
溶解度的三种情况:
(1)大多数物质的溶解度随温度的升高而增大,
如KNO3。
(2)少数物质的溶解度受温度的影响不大,如
NaCl。
(3)极少数物质的溶解度随温度的升高而减小,
如Ca(OH)2。
2.
影响固体溶解度的因素是:温度。
我们研究了固体物质的溶解度,那么气体物质的溶解度又该如何定义,又与什么有关呢?
定义:气体溶解度是指在101kPa和一定温度时,溶解在1体积水里达到饱和状态时的气体体积。
交流讨论
1.
打开汽水盖时,汽水会自动喷出来,这说明气体在水中的溶解度与什么有关?
2.喝了汽水后,常常会打嗝。这说明气体的溶解度还与什么有关?
压强:压强减小,气体在水中的溶解度减小。
温度:温度升高,气体在水中的溶解度减小。
3.烧开水刚开始一会儿,锅底会有很多小气泡,为什么?
水中溶解有气体,这说明温度升高气体的溶解度变小。
气体的溶解度与压强有关。压强越大,溶解度越大,压强越小,溶解度越小;
气体的溶解度与温度有关。温度越高,溶解度越小。
课堂教学展示
典例剖析
例
如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是(
)
A.20℃时,甲的溶解度大于乙的溶解度
B.40℃时,甲、乙两种物质的溶解度相等
C.采用降温的方法可以将乙的不饱
和溶液转化为饱和溶液
D.60℃时,在100g水中加入100g甲,
充分溶解后溶液质量为200g
B
课堂教学展示
课堂小结
第2课时
溶解度
一、固体的溶解度
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
三、溶解度曲线的意义:
1.溶解度的三种情况:
(1)大多数物质的溶解度随温度的升高而
增大,如KNO3。
(2)少数物质的溶解度受温度的影响不大,
如NaCl。
(3)极少数物质的溶解度随温度的升高而
减小,如Ca(OH)2。
2.交点P表示,在该温度下,A、B两种物质的溶解度相等。
3.影响固体溶解度的因素是:温度。
四、气体的溶解度
1.定义:在压强为101KPa和一定温度时,气
体溶解在1体积水里达到饱和状态时的气体体积。
2.影响因素
温度:随温度升高,气体溶解度减小。
压强:随压强增大,气体溶解度增大。
1.从课后习题中选取;
2.完成练习册本课时的习题。
课后反馈总结
课后作业
2.在60℃时,硝酸钾的溶解度是110g。这句话的含义是
。
在60℃时,110g硝酸钾溶解在100g水中,所得溶液恰好为该温度下硝酸钾的饱和溶液(或在60℃时,100g水最多能溶解110g硝酸钾固体)
课后反馈总结
课本习题
练习与应用(P40)
3.查溶解度曲线,在表中空白处填上该物质的溶解度。
4.甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答下列问题:
(1)a3℃时,三种物质的溶解度
由大到小的顺序是
;
(2)a2℃时,
和
的溶解度
大小相等;?
(3)三种物质中,
的溶解度受温度的影响最大,
的溶解度受温度的影响最小,
的溶解度随温度的升高而减小。
甲>丙>乙
甲
丙
甲
乙
丙
5.甲、乙两种物质的溶解度曲线如右图所示。下列说法中正确的是(
)
A.a1℃时甲和乙的饱和溶液,
升温到a2℃时仍是饱和溶液?
B.甲和乙的溶解度相等?
C.a1℃时,甲和乙各30g分别
加入100g水中,均形成饱和溶液?
D.a2℃时,在100g水中加入60g甲,形成不饱和溶液
C
9.加热冷水,当温度尚未达到沸点时,为什么水中常有气泡冒出?天气闷热时,鱼塘里的鱼为什么总是接近水面游动?
解:在水中总是溶解有一些气体,冷水受热时,温度升高,气体的溶解度减小,因此即使尚未达到沸点,也常有气泡冒出。天气闷热时,水温高,水中氧气的溶解度变小,溶解的氧气少了,而水面与空气接触,溶解的氧气相对多些,因此鱼总是接近水面游动。
同课章节目录
