化学平衡图像-----评估
文档属性
| 名称 | 化学平衡图像-----评估 |
|
|
| 格式 | zip | ||
| 文件大小 | 68.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-06-14 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
化学反应速率和化学平衡的图象
1、化学反应速率图象
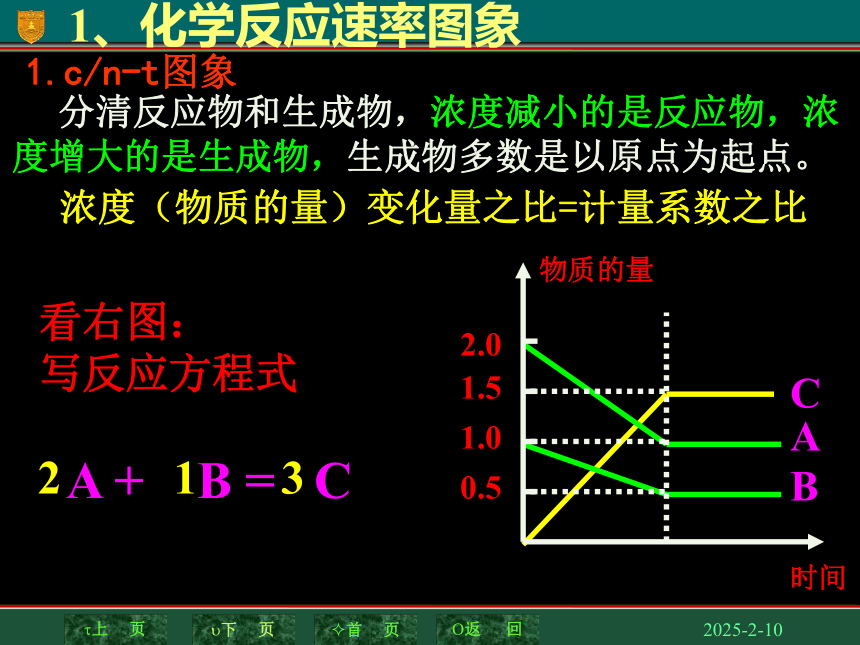
1.c/n-t图象
分清反应物和生成物,浓度减小的是反应物,浓度增大的是生成物,生成物多数是以原点为起点。
看右图:
写反应方程式
0.5
1.5
1.0
2.0
物质的量
C
A
B
时间
A + B = C
2
1
3
浓度(物质的量)变化量之比=计量系数之比
2.V-t图象
分清正反应和逆反应; 分清放热反应和吸热反应; 分清“突变”和“渐变”
V正
V逆
V'正
V'逆
V
t
此图表示:增大反应物浓度时,正反应、逆反应的速率变化情况,平衡向正反应方向移动。
1、化学反应速率图象分析
V正
V逆
V'正
V'逆
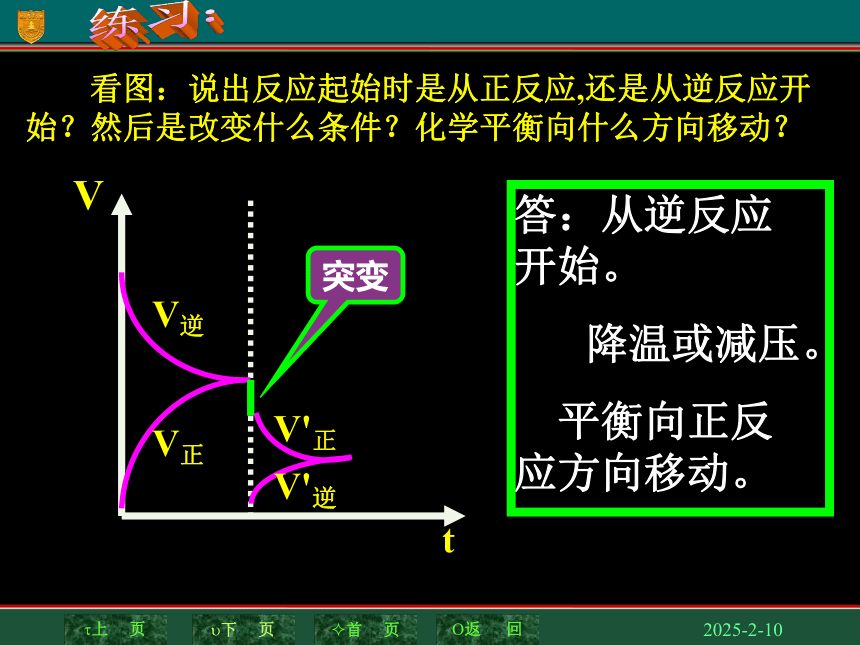
答:从逆反应开始。
降温或减压。
平衡向正反应方向移动。
t
V
看图:说出反应起始时是从正反应,还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?
突变
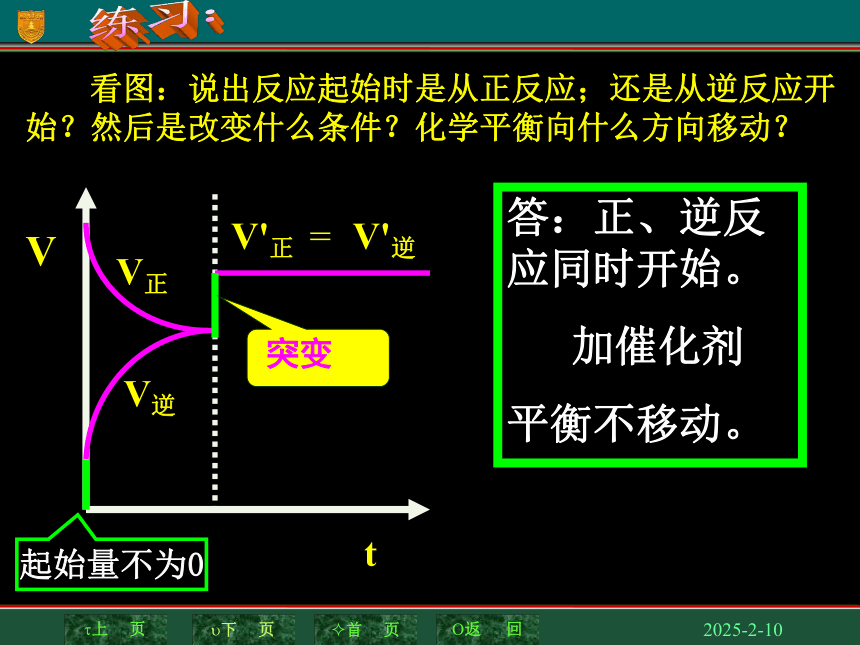
看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?
V正
V逆
V'正
V'逆
=
起始量不为0
突变
答:正、逆反应同时开始。
加催化剂
平衡不移动。
t
V
V正
V逆
看图:说出反应起始时是从正反应;还是从逆反应开始?化学平衡向什么方向移动?
V
T(温度)
答:正、逆同时反应开始。
平衡向正反应方向移动。
V正
V逆
V
t
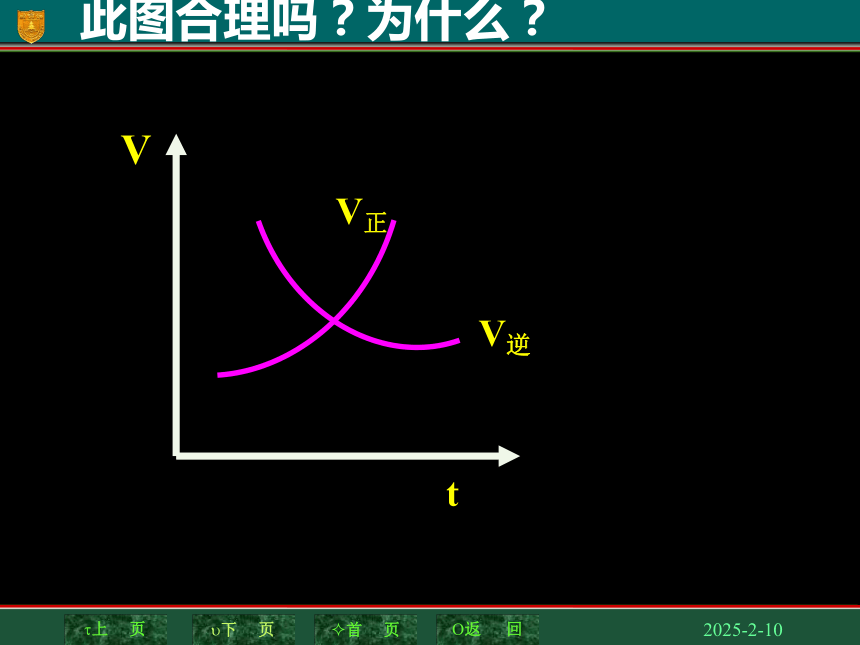
此图合理吗?为什么?
小结
1.认清坐标系,搞清纵、横坐标所代表的意义
2.看清起点,分清反应物、生成物,浓度减小的是反应物,浓度增大的是生成物。一般生成物多数以原点为起点。
3.注意终点。例如在浓度-时间图上,一定要看清终点时反应物的消耗量、生成物的增加量,并结合有关原理进行推理判断。
4.抓住变化趋势.升高温度时,v(吸)>v(放);在速率-时间图上,要注意看清曲线是连续的还是跳跃的,分轻渐变和突变,大变和小变。例如,升高温度,v(吸)大增,v(放)小增;增大反应物浓度,v(正)突变,v(逆)渐变。
转
化
率
温度
0
1.01 107Pa
1.01 106Pa
1.01 105Pa
二.化学平衡图象
1.转化率——压强/温度曲线
解法:
作等
温线
T
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
m+n p+q
>
Q 0
等温线
<
200 C
300 C
100 C
转
化
率
压强
0
P
m+n p+q
>
Q 0
看图技巧:图象中 有三个量时,“定一看二”, 先看曲线的高低,再看曲线的变化趋势。
等压线
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
>
200 C
300 C
100 C
P
Q 0
等压线
压强
0
A%
2.物质百分含量——压强/温度曲线
m+n p+q
<
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
<
3.物质百分含量——时间曲线
T1 C
T2 C
C%
时间
0
t1
t2
看图技巧:先拐先平衡,先平衡则速率快,速率快则温度高。
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
1、T1与T2的高低
2、是放热反应还是吸热反应
问
题
1、T1>T2
2、是放热反应
答案
mA(g)+nB(g) pC(g)+qD(g)
时间
P1
P2
A%
P1
P2
>
m+n p+q
>
0
问题:
1、P1与P2的相对大小
2、 m+n 与 p+q 的大小
答案
4.转化率——时间曲线
1.01 107Pa
1.01 106Pa
A的
转化率
时间
0
t1
t2
m+nmA(g)+nB(g) pC(g)+qD(g) ΔH=Q
问题: m+nm+n>p+p
5.物质产率——时间曲线
mA(g)+nB(g) pC(g)+qD(g)
时间
T1
T2
产率
0
问题:
1、T1与T2的相对大小
2、该反应是放热反应还是吸热反应
0
2A(g) + B(g) 2C(g)
T2 P1
T1 P2
T1 P1
C%
t
P1
P2
正反应是 热反应.
<
吸
0
转化率——时间曲线
mA(g)+nB(g) pC(g)+qD(g)
1.01 107Pa
1.01 106Pa
A转化率
时间
m+n = p+q
如图所示,图中a曲线表示X(g) +Y(g) 2Z(g)+ W(s) ΔH>0 的反应过程,若使a曲线变为b曲线,可采取的措施是( )
0
Z%
t
a
b
A. 加入催化剂
B. 增大Y的浓度
C. 降低温度
D. 增大体系压强
A.D
练 习:
0
1、下图是在其它条件一定时,反应2NO+O2 2NO2+ Q(Q>0)中NO 的最大转化率与温度的关系曲线。图中坐标有A、B、C、D、E 5点,其中表示未达平衡状态且
V正>V逆的点是 。
A
B
C
E
D
C点
T
NO转化率
小结
1.认清坐标系,搞清纵、横坐标所代表的意义,并与勒沙特列原理挂钩。
2.紧扣可逆反应的特征,搞清正反应方向是吸还是放热、体积增大还是减小、不变、有无固体、纯液体物质参加或生成等。
3.看清速率的变化及变化量的大小,在条件与变化之间搭桥。
4.看清起点、拐点、终点,看清曲线的变化趋势。
5.先拐先平。例如,在转化率-时间图上,先出现拐点的曲线先达到平衡,此时逆向推理可得该变化的温度高、浓度大、压强高。
6.定一议二。当图像中有三个量时,先确定一个量不变在讨论另外两个量的关系。
化学反应速率和化学平衡的图象
1、化学反应速率图象
1.c/n-t图象
分清反应物和生成物,浓度减小的是反应物,浓度增大的是生成物,生成物多数是以原点为起点。
看右图:
写反应方程式
0.5
1.5
1.0
2.0
物质的量
C
A
B
时间
A + B = C
2
1
3
浓度(物质的量)变化量之比=计量系数之比
2.V-t图象
分清正反应和逆反应; 分清放热反应和吸热反应; 分清“突变”和“渐变”
V正
V逆
V'正
V'逆
V
t
此图表示:增大反应物浓度时,正反应、逆反应的速率变化情况,平衡向正反应方向移动。
1、化学反应速率图象分析
V正
V逆
V'正
V'逆
答:从逆反应开始。
降温或减压。
平衡向正反应方向移动。
t
V
看图:说出反应起始时是从正反应,还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?
突变
看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?
V正
V逆
V'正
V'逆
=
起始量不为0
突变
答:正、逆反应同时开始。
加催化剂
平衡不移动。
t
V
V正
V逆
看图:说出反应起始时是从正反应;还是从逆反应开始?化学平衡向什么方向移动?
V
T(温度)
答:正、逆同时反应开始。
平衡向正反应方向移动。
V正
V逆
V
t
此图合理吗?为什么?
小结
1.认清坐标系,搞清纵、横坐标所代表的意义
2.看清起点,分清反应物、生成物,浓度减小的是反应物,浓度增大的是生成物。一般生成物多数以原点为起点。
3.注意终点。例如在浓度-时间图上,一定要看清终点时反应物的消耗量、生成物的增加量,并结合有关原理进行推理判断。
4.抓住变化趋势.升高温度时,v(吸)>v(放);在速率-时间图上,要注意看清曲线是连续的还是跳跃的,分轻渐变和突变,大变和小变。例如,升高温度,v(吸)大增,v(放)小增;增大反应物浓度,v(正)突变,v(逆)渐变。
转
化
率
温度
0
1.01 107Pa
1.01 106Pa
1.01 105Pa
二.化学平衡图象
1.转化率——压强/温度曲线
解法:
作等
温线
T
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
m+n p+q
>
Q 0
等温线
<
200 C
300 C
100 C
转
化
率
压强
0
P
m+n p+q
>
Q 0
看图技巧:图象中 有三个量时,“定一看二”, 先看曲线的高低,再看曲线的变化趋势。
等压线
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
>
200 C
300 C
100 C
P
Q 0
等压线
压强
0
A%
2.物质百分含量——压强/温度曲线
m+n p+q
<
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
<
3.物质百分含量——时间曲线
T1 C
T2 C
C%
时间
0
t1
t2
看图技巧:先拐先平衡,先平衡则速率快,速率快则温度高。
mA(g)+nB(g) pC(g)+qD(g) ΔH=Q
1、T1与T2的高低
2、是放热反应还是吸热反应
问
题
1、T1>T2
2、是放热反应
答案
mA(g)+nB(g) pC(g)+qD(g)
时间
P1
P2
A%
P1
P2
>
m+n p+q
>
0
问题:
1、P1与P2的相对大小
2、 m+n 与 p+q 的大小
答案
4.转化率——时间曲线
1.01 107Pa
1.01 106Pa
A的
转化率
时间
0
t1
t2
m+n
问题: m+n
5.物质产率——时间曲线
mA(g)+nB(g) pC(g)+qD(g)
时间
T1
T2
产率
0
问题:
1、T1与T2的相对大小
2、该反应是放热反应还是吸热反应
0
2A(g) + B(g) 2C(g)
T2 P1
T1 P2
T1 P1
C%
t
P1
P2
正反应是 热反应.
<
吸
0
转化率——时间曲线
mA(g)+nB(g) pC(g)+qD(g)
1.01 107Pa
1.01 106Pa
A转化率
时间
m+n = p+q
如图所示,图中a曲线表示X(g) +Y(g) 2Z(g)+ W(s) ΔH>0 的反应过程,若使a曲线变为b曲线,可采取的措施是( )
0
Z%
t
a
b
A. 加入催化剂
B. 增大Y的浓度
C. 降低温度
D. 增大体系压强
A.D
练 习:
0
1、下图是在其它条件一定时,反应2NO+O2 2NO2+ Q(Q>0)中NO 的最大转化率与温度的关系曲线。图中坐标有A、B、C、D、E 5点,其中表示未达平衡状态且
V正>V逆的点是 。
A
B
C
E
D
C点
T
NO转化率
小结
1.认清坐标系,搞清纵、横坐标所代表的意义,并与勒沙特列原理挂钩。
2.紧扣可逆反应的特征,搞清正反应方向是吸还是放热、体积增大还是减小、不变、有无固体、纯液体物质参加或生成等。
3.看清速率的变化及变化量的大小,在条件与变化之间搭桥。
4.看清起点、拐点、终点,看清曲线的变化趋势。
5.先拐先平。例如,在转化率-时间图上,先出现拐点的曲线先达到平衡,此时逆向推理可得该变化的温度高、浓度大、压强高。
6.定一议二。当图像中有三个量时,先确定一个量不变在讨论另外两个量的关系。
