2021-2022学年人教版九年级化学下册第9单元 课题1《溶液的形成》第1课时课件(33张PPT)
文档属性
| 名称 | 2021-2022学年人教版九年级化学下册第9单元 课题1《溶液的形成》第1课时课件(33张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-29 00:00:00 | ||
图片预览










文档简介
(共37张PPT)
第九单元
溶
液
学习目标:
1)了解溶质、溶剂、溶液的基本概念。
(2)认识溶液的基本特征是均一性、稳定性。
(3)了解溶液在工农业生产和生活中的应用。
重点
1、建立溶液的概念。
2、从微观上认识溶液。
3、认识溶液、溶质、溶剂三者的关系。
【思考】同学们都了解,糖水是甜的,盐水是咸的,但在糖水中为什么看不到糖?在盐水中为什么看不到盐呢?
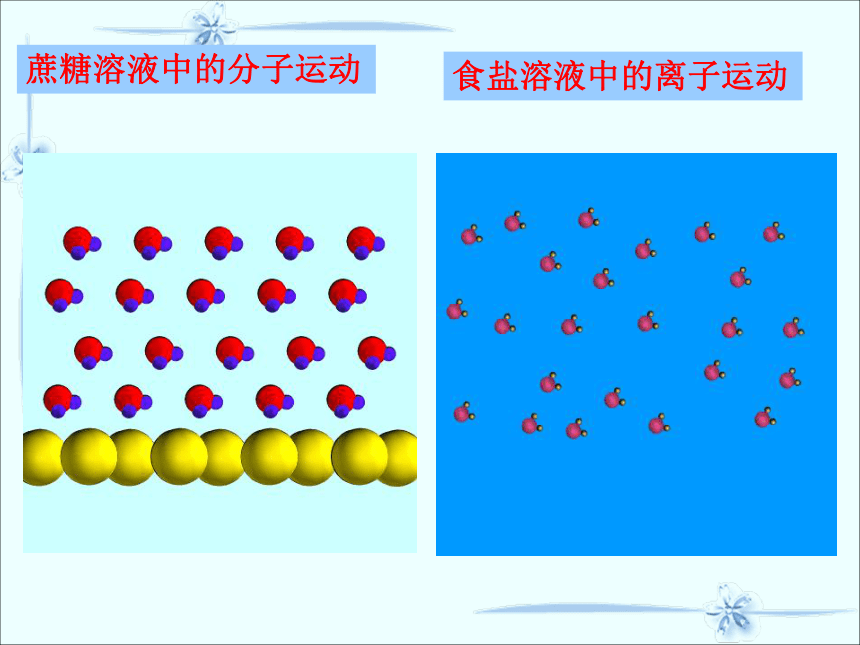
怎样解释食盐、蔗糖在水中的变化呢?
蔗糖溶液中的分子运动
食盐溶液中的离子运动
你能从微观的角度来解释溶解的过程吗?
蔗糖溶解到水中
食盐溶解到水中
形成
蔗糖溶液
形成
食盐溶液
蔗糖分子在水分子作用下分散到水分子的间隔之中。
Na+和Cl-在水分子作用下分散到水分子的间隔之中。
物质溶解于水的本质是构成物质的微粒(分子、离子)分散到水分子之间。
思考:此时的溶液是纯净物还是混合物?
溶液是混合物
2.溶液的特征:
①均一性:溶液各部分的组成和性质相同。
②稳定性:外界条件不变时,久置不会分层。
1.溶液的定义
:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
③混合物
一、溶液
3.溶液的形成过程
:是溶质的分子(或离子)均匀扩散到溶剂分子之间
练一练!
一瓶长期存放的茅台酒,若倒出第
一
杯酒其酒精度为54度,那么倒出第二杯
酒的酒精度为(
)
A大于54度
B小于54度
C等于54度
D无法判断
C
均一性:溶液各部分的组成和性质相同。
关于溶液的认识
(2)溶液一定是无色透明的吗?
(3)均一、稳定的液体一定是溶液吗?
(1)溶液的特征是什么?
均一性、稳定性、混合物。
不一定。如CuSO4溶液是蓝色的。
不一定。如水就不是溶液、
酒精也不是溶液。
溶质是蔗糖,氯化钠,溶剂是水
被水溶解
讨论:在蔗糖溶液和氯化钠溶液中,溶质是什么?溶剂是什么?
能溶解蔗糖,氯化钠
水
蔗糖,氯化钠
溶
液
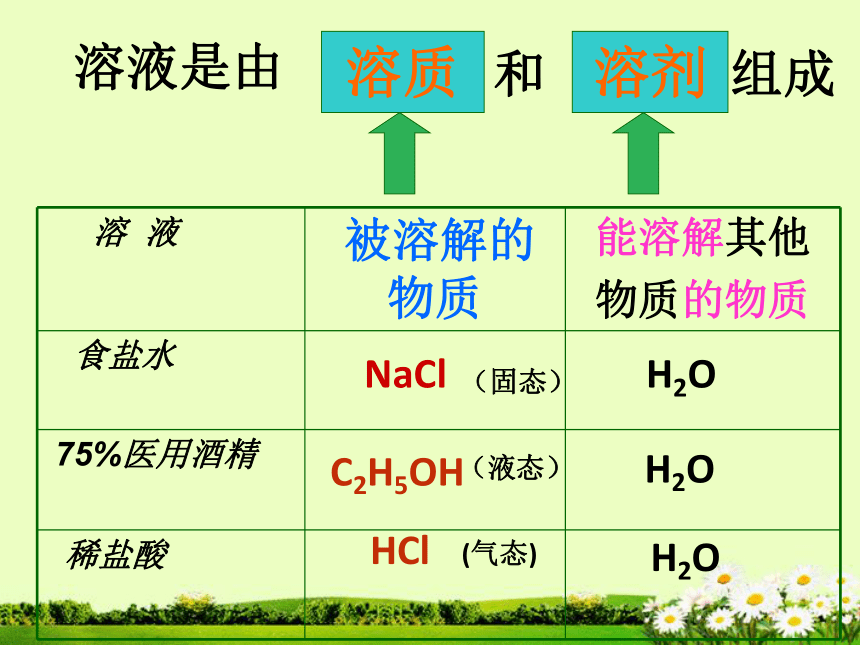
被溶解的物质
能溶解其他
物质的物质
食盐水
75%医用酒精
稀盐酸
NaCl
H2O
C2H5OH
H2O
HCl
H2O
溶质
溶剂
溶液是由
和
组成
(固态)
(气态)
(液态)
4、溶液的组成:
溶液
溶质:
溶剂:
被溶解的物质。
能溶解其他物质的物质。
(≥1种)
(1种)
5、溶液、溶质与溶剂之间的量的关系
质量:m溶液
m质+m剂
=
体积:
V溶液
V质+
V剂
<
水能溶解所有的物质吗?
除了水还有其他的溶剂吗?
6.水是最常用的溶剂,除此之外,汽油、酒精等也可作溶剂。如:碘酒。
通过下列实验你能得到哪些结论
[实验]9-2
不同的溶质在不同的溶剂中的溶解性
实验现象记录:
溶剂
溶质
现象
1
水
碘
2
水
高锰酸钾
3
汽油
碘
4
汽油
高锰酸钾
碘几乎不溶于水
高锰酸钾溶于水,溶液紫色
碘溶于汽油,溶液棕色
高锰酸钾几乎不溶于汽油
结论:物质的溶解性大小与溶质和溶剂的性质有关
水可以溶解高锰酸钾但不能溶解碘,汽油可溶解碘但不可溶解高锰酸钾说明物质的溶解性与溶质的性质有关。高锰酸钾可溶于水但不溶于汽油,碘可溶于汽油但不溶于水说明物质的溶解性与溶剂的性质有关
7.物质的溶解性大小与溶质和溶剂的性质有关
①相同的溶质在不同的溶剂中溶解性不同
②不同的溶质在相同的溶剂中溶解性不同
如:高锰酸钾可溶于水但不溶于汽油,碘可溶于汽油但不溶于水。
如:水可以溶解高锰酸钾但不能溶解碘,汽油可溶解碘但不可溶解高锰酸钾。
[实验9-3
]水和乙醇能够互溶吗?
溶剂
溶质
振荡前现象
震荡后现象
静置后现象
结论
水
酒精
分层
均匀混合
不分层
水和乙醇能够互溶
阅读课本P28探讨:
怎样确定溶液中谁是溶质?谁是溶剂?
溶质可以是固体、气体或液体。若两种液体互相溶解时,把量多的叫溶剂,量少的叫溶质。如果其中有一种是水,一般把水叫溶剂。
溶质:CuSO4(固体)
溶剂:H2O
CuSO4溶液
溶质:HCl(气体)
溶剂:H2O
盐酸
溶质:酒精(液体)
溶剂:H2O
酒精溶液
8.溶质可以是固体、气体或液体。
9、溶液中溶质和溶剂的判断
固液混合固为质;气液混合气为质;
液液混合少为质;有水存在水为剂;
水为最常见的溶剂
10.溶液的命名(根据溶质名称):溶质的溶剂的溶液(若溶剂为水可省略不读)
(1)全称:(溶质)的(溶剂)溶液。
如,氯化钠的水溶液,碘的汽油溶液。
(2)简称:若溶剂为水,可直接读(溶质)溶液。
如,氯化钠溶液,硫酸铜溶液。
(3)俗称:
如,糖水、碘酒、石灰水、盐酸
练习:
指出下列溶液中溶质、溶剂各是什么?
溶质
溶剂
(1)硫酸铜溶液
(2)稀硫酸
(3)75%的医用酒精
(4)油脂溶解在汽油里
(5)白磷的二硫化碳溶液
(6)盐酸
(7)
CO2溶于水的溶液
CuSO4
水
H2SO4
水
C2H5OH
水
油脂
汽油
白磷
二硫化碳
HCl
水
H2CO3
水
如:过量的铁投入到稀硫酸中,则形成的
溶液中溶质是新生成的硫酸亚铁
FeSO4。
思考:(1)少量铁与过量稀硫酸反应,溶质是否一样?
___________________________。
(2)试写出新生成的化合物不都是溶质的一个化学方程式:
____________________________________________。
不一样,溶质是H2SO4和FeSO4
CaCO3+2HCl===CaCl2+H2O+CO2↑(合理即可)
11.注意:当发生化学变化时,新生成的化合物可能是溶质。
[典例]下列各组溶液的溶质判断正确的是(
)。
A.澄清的石灰水中溶质为石灰石
B.将Zn加入到稀H2SO4中恰好完全反应后溶液的溶质为Zn
C.少量Fe和CuSO4溶液反应后溶液的溶质为FeSO4
D.少量KMnO4加入水中形成的溶液溶质为KMnO4
点拨:溶质的判定要看是否发生了化学变化,澄清石灰水
中的溶质是氢氧化钙Ca(OH)2;锌加入到稀硫酸中恰好完全反
应,新生成的ZnSO4为溶质;少量Fe
和CuSO4
溶液反应后,溶
液中新的溶质为FeSO4,还有过量的CuSO4;KMnO4加入水中
不发生化学反应。
D
无土栽培的植物
在营养液中
激情无限----可口可乐
溶液具有广泛的用途
这节课,我的收获是什么?
2.溶液的特征:
①均一性:溶液各部分的组成和性质相同。
②稳定性:外界条件不变时,久置不会分层。
1.溶液的定义
:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
③混合物
一、溶液
3.溶液的形成过程
:是溶质的分子(或离子)均匀扩散到溶剂分子之间
4、溶液的组成:
溶液
溶质:
溶剂:
被溶解的物质。
能溶解其他物质的物质。
(≥1种)
(1种)
5、溶液、溶质与溶剂之间的量的关系
质量:m溶液
m质+m剂
=
体积:
V溶液
V质+
V剂
<
6.水是最常用的溶剂,除此之外,汽油、酒精等也可作溶剂。如:碘酒。
7.物质的溶解性大小与溶质和溶剂的性质有关
①相同的溶质在不同的溶剂中溶解性不同
②不同的溶质在相同的溶剂中溶解性不同
如:高锰酸钾可溶于水但不溶于汽油,碘可溶于汽油但不溶于水。
如:水可以溶解高锰酸钾但不能溶解碘,汽油可溶解碘但不可溶解高锰酸钾。
8.溶质可以是固体、气体或液体。
9、溶液中溶质和溶剂的判断
固液混合固为质;气液混合气为质;
液液混合少为质;有水存在水为剂;
水为最常见的溶剂
10.溶液的命名(根据溶质名称):溶质的溶剂的溶液(若溶剂为水可省略不读)
11.当发生化学变化时,新生成的化合物可能是溶质。
12.溶液在具有广泛的用途
随堂练习
一、判断下列说法是否正确
(1)凡是无色、透明的液体都是溶液
(
)
(2)溶液都是均一、稳定、无色透明的液体。
(
)
(3)食盐水和蔗糖水混合后仍为溶液
(
)
(4)所有的溶液都是由一种溶质和一种溶剂组成的。
(
)
(5)98%的硫酸溶液中水做溶质,硫酸做溶剂。
(
)
(6)食盐溶于水,得到食盐溶液的过程属于化合反应。
(
)
×
×
×
×
×
√
(
)1、溶液的基本特征是
A、无色透明
B、无色均一
C、均一、稳定
D、纯净的液体
(
)2、下列液体不属于溶液的是
A氯化钠投入水中
B、冰投入水中
C、碘酒
D、二氧化碳通入水中
(
)3、溶液是一种
(
)
A、化合物
B、混合物
C、纯净物
D、无色透明液体
(
)4、下列属于溶液的是
A、豆浆
B、泥水
C、稀硫酸
D、牛奶
C
B
B
C
(
)5、t℃时从200克氯化钠溶液中取出20克溶液,剩下的溶液中不变的是
A、溶液质量
B、溶剂质量
C、溶质质量
D、溶液的密度
(
)6、
各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用水洗去盘子中的水果渣
D.用盐酸洗去水壶的水垢(含CaCO3)
D
B
第九单元
溶
液
学习目标:
1)了解溶质、溶剂、溶液的基本概念。
(2)认识溶液的基本特征是均一性、稳定性。
(3)了解溶液在工农业生产和生活中的应用。
重点
1、建立溶液的概念。
2、从微观上认识溶液。
3、认识溶液、溶质、溶剂三者的关系。
【思考】同学们都了解,糖水是甜的,盐水是咸的,但在糖水中为什么看不到糖?在盐水中为什么看不到盐呢?
怎样解释食盐、蔗糖在水中的变化呢?
蔗糖溶液中的分子运动
食盐溶液中的离子运动
你能从微观的角度来解释溶解的过程吗?
蔗糖溶解到水中
食盐溶解到水中
形成
蔗糖溶液
形成
食盐溶液
蔗糖分子在水分子作用下分散到水分子的间隔之中。
Na+和Cl-在水分子作用下分散到水分子的间隔之中。
物质溶解于水的本质是构成物质的微粒(分子、离子)分散到水分子之间。
思考:此时的溶液是纯净物还是混合物?
溶液是混合物
2.溶液的特征:
①均一性:溶液各部分的组成和性质相同。
②稳定性:外界条件不变时,久置不会分层。
1.溶液的定义
:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
③混合物
一、溶液
3.溶液的形成过程
:是溶质的分子(或离子)均匀扩散到溶剂分子之间
练一练!
一瓶长期存放的茅台酒,若倒出第
一
杯酒其酒精度为54度,那么倒出第二杯
酒的酒精度为(
)
A大于54度
B小于54度
C等于54度
D无法判断
C
均一性:溶液各部分的组成和性质相同。
关于溶液的认识
(2)溶液一定是无色透明的吗?
(3)均一、稳定的液体一定是溶液吗?
(1)溶液的特征是什么?
均一性、稳定性、混合物。
不一定。如CuSO4溶液是蓝色的。
不一定。如水就不是溶液、
酒精也不是溶液。
溶质是蔗糖,氯化钠,溶剂是水
被水溶解
讨论:在蔗糖溶液和氯化钠溶液中,溶质是什么?溶剂是什么?
能溶解蔗糖,氯化钠
水
蔗糖,氯化钠
溶
液
被溶解的物质
能溶解其他
物质的物质
食盐水
75%医用酒精
稀盐酸
NaCl
H2O
C2H5OH
H2O
HCl
H2O
溶质
溶剂
溶液是由
和
组成
(固态)
(气态)
(液态)
4、溶液的组成:
溶液
溶质:
溶剂:
被溶解的物质。
能溶解其他物质的物质。
(≥1种)
(1种)
5、溶液、溶质与溶剂之间的量的关系
质量:m溶液
m质+m剂
=
体积:
V溶液
V质+
V剂
<
水能溶解所有的物质吗?
除了水还有其他的溶剂吗?
6.水是最常用的溶剂,除此之外,汽油、酒精等也可作溶剂。如:碘酒。
通过下列实验你能得到哪些结论
[实验]9-2
不同的溶质在不同的溶剂中的溶解性
实验现象记录:
溶剂
溶质
现象
1
水
碘
2
水
高锰酸钾
3
汽油
碘
4
汽油
高锰酸钾
碘几乎不溶于水
高锰酸钾溶于水,溶液紫色
碘溶于汽油,溶液棕色
高锰酸钾几乎不溶于汽油
结论:物质的溶解性大小与溶质和溶剂的性质有关
水可以溶解高锰酸钾但不能溶解碘,汽油可溶解碘但不可溶解高锰酸钾说明物质的溶解性与溶质的性质有关。高锰酸钾可溶于水但不溶于汽油,碘可溶于汽油但不溶于水说明物质的溶解性与溶剂的性质有关
7.物质的溶解性大小与溶质和溶剂的性质有关
①相同的溶质在不同的溶剂中溶解性不同
②不同的溶质在相同的溶剂中溶解性不同
如:高锰酸钾可溶于水但不溶于汽油,碘可溶于汽油但不溶于水。
如:水可以溶解高锰酸钾但不能溶解碘,汽油可溶解碘但不可溶解高锰酸钾。
[实验9-3
]水和乙醇能够互溶吗?
溶剂
溶质
振荡前现象
震荡后现象
静置后现象
结论
水
酒精
分层
均匀混合
不分层
水和乙醇能够互溶
阅读课本P28探讨:
怎样确定溶液中谁是溶质?谁是溶剂?
溶质可以是固体、气体或液体。若两种液体互相溶解时,把量多的叫溶剂,量少的叫溶质。如果其中有一种是水,一般把水叫溶剂。
溶质:CuSO4(固体)
溶剂:H2O
CuSO4溶液
溶质:HCl(气体)
溶剂:H2O
盐酸
溶质:酒精(液体)
溶剂:H2O
酒精溶液
8.溶质可以是固体、气体或液体。
9、溶液中溶质和溶剂的判断
固液混合固为质;气液混合气为质;
液液混合少为质;有水存在水为剂;
水为最常见的溶剂
10.溶液的命名(根据溶质名称):溶质的溶剂的溶液(若溶剂为水可省略不读)
(1)全称:(溶质)的(溶剂)溶液。
如,氯化钠的水溶液,碘的汽油溶液。
(2)简称:若溶剂为水,可直接读(溶质)溶液。
如,氯化钠溶液,硫酸铜溶液。
(3)俗称:
如,糖水、碘酒、石灰水、盐酸
练习:
指出下列溶液中溶质、溶剂各是什么?
溶质
溶剂
(1)硫酸铜溶液
(2)稀硫酸
(3)75%的医用酒精
(4)油脂溶解在汽油里
(5)白磷的二硫化碳溶液
(6)盐酸
(7)
CO2溶于水的溶液
CuSO4
水
H2SO4
水
C2H5OH
水
油脂
汽油
白磷
二硫化碳
HCl
水
H2CO3
水
如:过量的铁投入到稀硫酸中,则形成的
溶液中溶质是新生成的硫酸亚铁
FeSO4。
思考:(1)少量铁与过量稀硫酸反应,溶质是否一样?
___________________________。
(2)试写出新生成的化合物不都是溶质的一个化学方程式:
____________________________________________。
不一样,溶质是H2SO4和FeSO4
CaCO3+2HCl===CaCl2+H2O+CO2↑(合理即可)
11.注意:当发生化学变化时,新生成的化合物可能是溶质。
[典例]下列各组溶液的溶质判断正确的是(
)。
A.澄清的石灰水中溶质为石灰石
B.将Zn加入到稀H2SO4中恰好完全反应后溶液的溶质为Zn
C.少量Fe和CuSO4溶液反应后溶液的溶质为FeSO4
D.少量KMnO4加入水中形成的溶液溶质为KMnO4
点拨:溶质的判定要看是否发生了化学变化,澄清石灰水
中的溶质是氢氧化钙Ca(OH)2;锌加入到稀硫酸中恰好完全反
应,新生成的ZnSO4为溶质;少量Fe
和CuSO4
溶液反应后,溶
液中新的溶质为FeSO4,还有过量的CuSO4;KMnO4加入水中
不发生化学反应。
D
无土栽培的植物
在营养液中
激情无限----可口可乐
溶液具有广泛的用途
这节课,我的收获是什么?
2.溶液的特征:
①均一性:溶液各部分的组成和性质相同。
②稳定性:外界条件不变时,久置不会分层。
1.溶液的定义
:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
③混合物
一、溶液
3.溶液的形成过程
:是溶质的分子(或离子)均匀扩散到溶剂分子之间
4、溶液的组成:
溶液
溶质:
溶剂:
被溶解的物质。
能溶解其他物质的物质。
(≥1种)
(1种)
5、溶液、溶质与溶剂之间的量的关系
质量:m溶液
m质+m剂
=
体积:
V溶液
V质+
V剂
<
6.水是最常用的溶剂,除此之外,汽油、酒精等也可作溶剂。如:碘酒。
7.物质的溶解性大小与溶质和溶剂的性质有关
①相同的溶质在不同的溶剂中溶解性不同
②不同的溶质在相同的溶剂中溶解性不同
如:高锰酸钾可溶于水但不溶于汽油,碘可溶于汽油但不溶于水。
如:水可以溶解高锰酸钾但不能溶解碘,汽油可溶解碘但不可溶解高锰酸钾。
8.溶质可以是固体、气体或液体。
9、溶液中溶质和溶剂的判断
固液混合固为质;气液混合气为质;
液液混合少为质;有水存在水为剂;
水为最常见的溶剂
10.溶液的命名(根据溶质名称):溶质的溶剂的溶液(若溶剂为水可省略不读)
11.当发生化学变化时,新生成的化合物可能是溶质。
12.溶液在具有广泛的用途
随堂练习
一、判断下列说法是否正确
(1)凡是无色、透明的液体都是溶液
(
)
(2)溶液都是均一、稳定、无色透明的液体。
(
)
(3)食盐水和蔗糖水混合后仍为溶液
(
)
(4)所有的溶液都是由一种溶质和一种溶剂组成的。
(
)
(5)98%的硫酸溶液中水做溶质,硫酸做溶剂。
(
)
(6)食盐溶于水,得到食盐溶液的过程属于化合反应。
(
)
×
×
×
×
×
√
(
)1、溶液的基本特征是
A、无色透明
B、无色均一
C、均一、稳定
D、纯净的液体
(
)2、下列液体不属于溶液的是
A氯化钠投入水中
B、冰投入水中
C、碘酒
D、二氧化碳通入水中
(
)3、溶液是一种
(
)
A、化合物
B、混合物
C、纯净物
D、无色透明液体
(
)4、下列属于溶液的是
A、豆浆
B、泥水
C、稀硫酸
D、牛奶
C
B
B
C
(
)5、t℃时从200克氯化钠溶液中取出20克溶液,剩下的溶液中不变的是
A、溶液质量
B、溶剂质量
C、溶质质量
D、溶液的密度
(
)6、
各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用水洗去盘子中的水果渣
D.用盐酸洗去水壶的水垢(含CaCO3)
D
B
同课章节目录
