江苏省盐城市新洋高中2020-2021学年高一上学期期中考试化学试题 Word版含答案
文档属性
| 名称 | 江苏省盐城市新洋高中2020-2021学年高一上学期期中考试化学试题 Word版含答案 |

|
|
| 格式 | doc | ||
| 文件大小 | 381.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-31 00:00:00 | ||
图片预览

文档简介
盐城市新洋高级中学
2020-2021学年度第一学期高一年级期中考试
化
学
试
卷
时间:60分钟
满分100分
第I卷(选择题共78分)
选择题(本题共26小题,每小题3分,共78分)
1.2019
年,我国第一艘国产航空母舰山东舰正式列装。优质钢材是建造航空母舰的基础材料,钢材中含量最高的元素是
(
)
A.铁
B.碳
C.硅
D.锰
2.
科学家研究发现Pb具有杀死癌细胞的功效。下列关于Pb的说法正确的是(
)
A.质子数是212
B.中子数是130
C.电子数是194
D.质量数是82
3.欲配制浓度为1.00mol/L的氯化钠溶液100mL,用不到的仪器是
(
)
A.容量瓶
B.分液漏斗
C.玻璃棒
D.烧杯
4.为充分利用资源和保护环境,近年来逐步实施了生活垃圾的分类处理。废弃的塑料袋、纸张、橡胶制品均属于
(
)
A.单质
B.有机物
C.盐
D.氧化物
5.下列变化属于化学变化的是(
)
A.碘的升华
B.氮气液化
C.钢铁锈蚀
D.汽油挥发
6.标准状况下,1
mol
O2的体积约为(
)
A.5.6
L
B.11.2
L
C.22.4
L
D.33.6
L
7.下列物质在溶液中电离出的Cl—与1molCaCl2电离出的Cl—数目相同的是
(
)
A.1molKClO3
B.1mol
KCl
C.1molMgCl2
D.1molAlCl3
8.许多化学物质在日常生活中有俗名。下列物质的俗名与化学式对应正确的是(
)
A.双氧水—Na2O2
B.小苏打—NaOH
C.胆矾—Cu(OH)2
D.干冰—CO2
9.下列说法正确的是
(
)
A.20Ne和22Ne互为同位素
B.石墨和金刚石是同一种物质
C.氯化铵、蔗糖都属于电解质
D.碘单质和碘蒸气不是同一物质
10.下列实验或操作方法正确的是
(
)
11.用化学方法可制得高纯度硅,其化学方程式为
:
①SiO2
+
2C
Si
+
2CO
②Si
+
2Cl2SiCl4
③SiCl4
+
2H2Si
+
4HCl,其中,反应①和③属于(
)
A.
化合反应
B.
分解反应
C.
氧化还原反应
D.
复分解反应
12.下列有关说法不正确的是
(
)
A.青蒿素的分子式为C15H22O5,它属于有机物
B.经过长期的实验探索,终于获得成功,实验是化学研究的重要手段之一
C.用萃取的方法,从青蒿中提取青蒿素。萃取是一种化学变化
D.现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O三种元素
13.当光束通过鸡蛋清水溶液时,可观察到一条光亮的“通路”,说明鸡蛋清水溶液是(
)
A.溶液
B.胶体
C.悬浊液
D.乳浊液
14.“脚印”、“笑脸”、“五环”等焰火让08北京奥运会开幕式更加辉煌壮观,这些五彩缤纷的焰火与元素的焰色反应有关。下列说法错误的是
(
)
A.观察K2SO4的焰色应透过蓝色的钴玻璃
B.Na与NaCl在灼烧时火焰颜色相同
C.可以用焰色反应来区别NaCl和KCl
D.焰色反应一定发生化学变化
15.下列各项中,在容量瓶上必须标明的是( )
①容量
②刻度线
③温度
④
压强
⑤物质的量浓度
⑥用于配制酸溶液或碱溶液
A.只有①②③
B.只有①③⑤
C.只有②④⑥
D.只有③⑤⑥
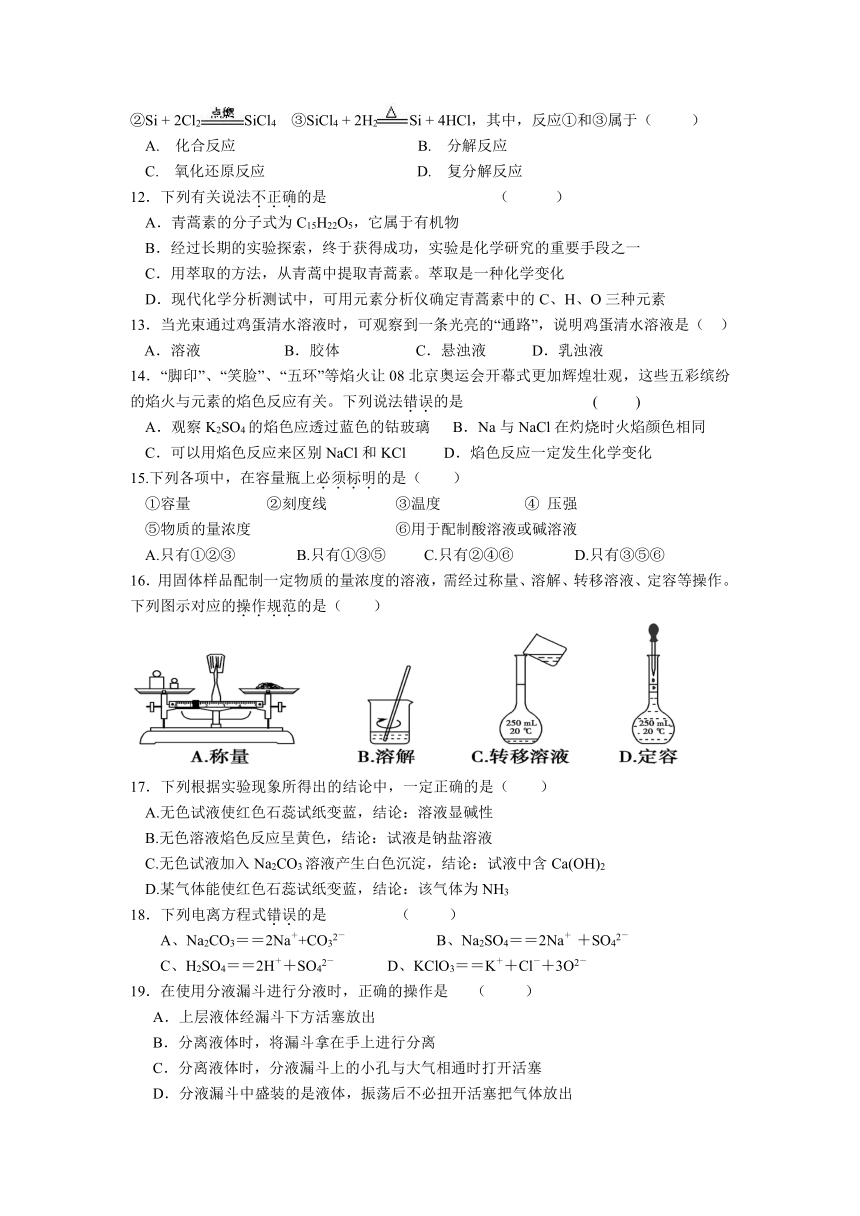
16.用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是(
)
17.下列根据实验现象所得出的结论中,一定正确的是( )
A.无色试液使红色石蕊试纸变蓝,结论:溶液显碱性
B.无色溶液焰色反应呈黄色,结论:试液是钠盐溶液
C.无色试液加入Na2CO3溶液产生白色沉淀,结论:试液中含Ca(OH)2
D.某气体能使红色石蕊试纸变蓝,结论:该气体为NH3
18.下列电离方程式错误的是
(
)
A、Na2CO3==2Na++CO32-
B、Na2SO4==2Na+
+SO42-
C、H2SO4==2H++SO42-
D、KClO3==K++Cl-+3O2-
19.在使用分液漏斗进行分液时,正确的操作是
(
)
A.上层液体经漏斗下方活塞放出
B.分离液体时,将漏斗拿在手上进行分离
C.分离液体时,分液漏斗上的小孔与大气相通时打开活塞
D.分液漏斗中盛装的是液体,振荡后不必扭开活塞把气体放出
20.现有一瓶物质A和B的混合物,已知A和B的某些性质如下:据此,将甲和乙互相分离的最佳方法是( )。
物质
分子式
熔点/℃
沸点/℃
密度/(g·cm-3)
水中溶解性
A
C3H6O2
-98
57.5
0.93
可溶
B
C4H8O2
-84
778
0.90
可溶
A.
萃取法
B.升华法
C.蒸馏法
D.分液法
21.碘缺乏病是目前已知的导致人类智力障碍的主要原因。为解决这一全国性问题,我国很
久以前就已经开始实施“智力工程”,最经济可行的措施是
(
)
A.食盐加碘盐
B.面包加碘盐
C.大量食用海带
D.注射含碘药剂
22.下列气体的收集中,既能用向上排空气法又能用排水集气法收集的气体是(
)
A.H2
B.O2
C.CO2
D.HCl
23.配制250mL
0.100mol·L-1NaCl溶液时,下列操作会使配得溶液中HCl的物质的量浓度偏大的是
(
)
A.移液后未洗涤烧杯
B.定容后摇匀,发现液面低于刻度线,再加水至刻度线
C.在容量瓶中进行定容时,俯视刻度线
D.在容量瓶中进行定容时,仰视刻度线
24.下列判断正确的是
(
)
A.28g
N2含有的氮原子数目为6.02×1023
B.常温常压下,22.4L
Cl2含有的分子数目为
6.02×1023
C.1molNa变为Na+时失去的电子数目为
6.02×1023
D.1L
1mol·L—1K2CO3溶液中含有的钾离子数目为
6.02×1023
25.关于某溶液中离子的检验,下列说法中不正确的是
(
)
A.加浓NaOH溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中含NH4+
B.加入盐酸后产生能够使澄清的石灰水变浑浊的气体,则原溶液中可能含CO32—
C.用铂丝蘸取某溶液在酒精灯的火焰上灼烧时,火焰呈黄色,说明原溶液中含有钠元素
D.加入BaCl2溶液时,产生白色沉淀,加稀硝酸沉淀不溶解,说明原溶液中一定存在SO42
26.如右图是某溶液在稀释过程中溶质的物质的量浓度随溶液
体积的变化曲线图,根据图中数据分析可计算出a值为(
)
A.2
B.3
C.4
D.5
第Ⅱ卷(非选择题共22分)
27.(8分)在中学实验中学过的可用于分离或提纯物质的方法很多,如①过滤、②蒸发结晶,③降温结晶,④蒸馏,⑤萃取,⑥分液,⑦升华等。请将分离或提纯下列各混合物最适宜的方法名称的序号填入横线上。
(1)除去粗盐中的泥沙______________。(2)从饱和食盐水中提取食盐______________。
(3)分离植物油和水________________。(4)分离碘的CCl4溶液____________________。
28.(8分)固态CO2俗称干冰,常用于人工降雨,
44g干冰与A、B、C、D有如图所示的转化关系,试完成下图中的部分方框。
A.
B.
D.
E.
29.(6分)浓硫酸与铜在加热时反应,生成二氧化硫气体的体积为2.24L(标准状况).
方程式如下:Cu
+
2H2SO4
====
CuSO4
+
SO2
↑+
2H2O
试计算:
(1)二氧化硫的物质的量;
(2)反应后生成硫酸铜的质量.
加热
2020-2021学年度第一学期高一年级期中考试
化
学
试
卷
时间:60分钟
满分100分
第I卷(选择题共78分)
选择题(本题共26小题,每小题3分,共78分)
1.2019
年,我国第一艘国产航空母舰山东舰正式列装。优质钢材是建造航空母舰的基础材料,钢材中含量最高的元素是
(
)
A.铁
B.碳
C.硅
D.锰
2.
科学家研究发现Pb具有杀死癌细胞的功效。下列关于Pb的说法正确的是(
)
A.质子数是212
B.中子数是130
C.电子数是194
D.质量数是82
3.欲配制浓度为1.00mol/L的氯化钠溶液100mL,用不到的仪器是
(
)
A.容量瓶
B.分液漏斗
C.玻璃棒
D.烧杯
4.为充分利用资源和保护环境,近年来逐步实施了生活垃圾的分类处理。废弃的塑料袋、纸张、橡胶制品均属于
(
)
A.单质
B.有机物
C.盐
D.氧化物
5.下列变化属于化学变化的是(
)
A.碘的升华
B.氮气液化
C.钢铁锈蚀
D.汽油挥发
6.标准状况下,1
mol
O2的体积约为(
)
A.5.6
L
B.11.2
L
C.22.4
L
D.33.6
L
7.下列物质在溶液中电离出的Cl—与1molCaCl2电离出的Cl—数目相同的是
(
)
A.1molKClO3
B.1mol
KCl
C.1molMgCl2
D.1molAlCl3
8.许多化学物质在日常生活中有俗名。下列物质的俗名与化学式对应正确的是(
)
A.双氧水—Na2O2
B.小苏打—NaOH
C.胆矾—Cu(OH)2
D.干冰—CO2
9.下列说法正确的是
(
)
A.20Ne和22Ne互为同位素
B.石墨和金刚石是同一种物质
C.氯化铵、蔗糖都属于电解质
D.碘单质和碘蒸气不是同一物质
10.下列实验或操作方法正确的是
(
)
11.用化学方法可制得高纯度硅,其化学方程式为
:
①SiO2
+
2C
Si
+
2CO
②Si
+
2Cl2SiCl4
③SiCl4
+
2H2Si
+
4HCl,其中,反应①和③属于(
)
A.
化合反应
B.
分解反应
C.
氧化还原反应
D.
复分解反应
12.下列有关说法不正确的是
(
)
A.青蒿素的分子式为C15H22O5,它属于有机物
B.经过长期的实验探索,终于获得成功,实验是化学研究的重要手段之一
C.用萃取的方法,从青蒿中提取青蒿素。萃取是一种化学变化
D.现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O三种元素
13.当光束通过鸡蛋清水溶液时,可观察到一条光亮的“通路”,说明鸡蛋清水溶液是(
)
A.溶液
B.胶体
C.悬浊液
D.乳浊液
14.“脚印”、“笑脸”、“五环”等焰火让08北京奥运会开幕式更加辉煌壮观,这些五彩缤纷的焰火与元素的焰色反应有关。下列说法错误的是
(
)
A.观察K2SO4的焰色应透过蓝色的钴玻璃
B.Na与NaCl在灼烧时火焰颜色相同
C.可以用焰色反应来区别NaCl和KCl
D.焰色反应一定发生化学变化
15.下列各项中,在容量瓶上必须标明的是( )
①容量
②刻度线
③温度
④
压强
⑤物质的量浓度
⑥用于配制酸溶液或碱溶液
A.只有①②③
B.只有①③⑤
C.只有②④⑥
D.只有③⑤⑥
16.用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是(
)
17.下列根据实验现象所得出的结论中,一定正确的是( )
A.无色试液使红色石蕊试纸变蓝,结论:溶液显碱性
B.无色溶液焰色反应呈黄色,结论:试液是钠盐溶液
C.无色试液加入Na2CO3溶液产生白色沉淀,结论:试液中含Ca(OH)2
D.某气体能使红色石蕊试纸变蓝,结论:该气体为NH3
18.下列电离方程式错误的是
(
)
A、Na2CO3==2Na++CO32-
B、Na2SO4==2Na+
+SO42-
C、H2SO4==2H++SO42-
D、KClO3==K++Cl-+3O2-
19.在使用分液漏斗进行分液时,正确的操作是
(
)
A.上层液体经漏斗下方活塞放出
B.分离液体时,将漏斗拿在手上进行分离
C.分离液体时,分液漏斗上的小孔与大气相通时打开活塞
D.分液漏斗中盛装的是液体,振荡后不必扭开活塞把气体放出
20.现有一瓶物质A和B的混合物,已知A和B的某些性质如下:据此,将甲和乙互相分离的最佳方法是( )。
物质
分子式
熔点/℃
沸点/℃
密度/(g·cm-3)
水中溶解性
A
C3H6O2
-98
57.5
0.93
可溶
B
C4H8O2
-84
778
0.90
可溶
A.
萃取法
B.升华法
C.蒸馏法
D.分液法
21.碘缺乏病是目前已知的导致人类智力障碍的主要原因。为解决这一全国性问题,我国很
久以前就已经开始实施“智力工程”,最经济可行的措施是
(
)
A.食盐加碘盐
B.面包加碘盐
C.大量食用海带
D.注射含碘药剂
22.下列气体的收集中,既能用向上排空气法又能用排水集气法收集的气体是(
)
A.H2
B.O2
C.CO2
D.HCl
23.配制250mL
0.100mol·L-1NaCl溶液时,下列操作会使配得溶液中HCl的物质的量浓度偏大的是
(
)
A.移液后未洗涤烧杯
B.定容后摇匀,发现液面低于刻度线,再加水至刻度线
C.在容量瓶中进行定容时,俯视刻度线
D.在容量瓶中进行定容时,仰视刻度线
24.下列判断正确的是
(
)
A.28g
N2含有的氮原子数目为6.02×1023
B.常温常压下,22.4L
Cl2含有的分子数目为
6.02×1023
C.1molNa变为Na+时失去的电子数目为
6.02×1023
D.1L
1mol·L—1K2CO3溶液中含有的钾离子数目为
6.02×1023
25.关于某溶液中离子的检验,下列说法中不正确的是
(
)
A.加浓NaOH溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中含NH4+
B.加入盐酸后产生能够使澄清的石灰水变浑浊的气体,则原溶液中可能含CO32—
C.用铂丝蘸取某溶液在酒精灯的火焰上灼烧时,火焰呈黄色,说明原溶液中含有钠元素
D.加入BaCl2溶液时,产生白色沉淀,加稀硝酸沉淀不溶解,说明原溶液中一定存在SO42
26.如右图是某溶液在稀释过程中溶质的物质的量浓度随溶液
体积的变化曲线图,根据图中数据分析可计算出a值为(
)
A.2
B.3
C.4
D.5
第Ⅱ卷(非选择题共22分)
27.(8分)在中学实验中学过的可用于分离或提纯物质的方法很多,如①过滤、②蒸发结晶,③降温结晶,④蒸馏,⑤萃取,⑥分液,⑦升华等。请将分离或提纯下列各混合物最适宜的方法名称的序号填入横线上。
(1)除去粗盐中的泥沙______________。(2)从饱和食盐水中提取食盐______________。
(3)分离植物油和水________________。(4)分离碘的CCl4溶液____________________。
28.(8分)固态CO2俗称干冰,常用于人工降雨,
44g干冰与A、B、C、D有如图所示的转化关系,试完成下图中的部分方框。
A.
B.
D.
E.
29.(6分)浓硫酸与铜在加热时反应,生成二氧化硫气体的体积为2.24L(标准状况).
方程式如下:Cu
+
2H2SO4
====
CuSO4
+
SO2
↑+
2H2O
试计算:
(1)二氧化硫的物质的量;
(2)反应后生成硫酸铜的质量.
加热
同课章节目录
