6.4 到实验室去:二氧化碳的实验室制取与性质-2021-2022学年鲁教版九年级化学上册同步讲解及练习(含解析)
文档属性
| 名称 | 6.4 到实验室去:二氧化碳的实验室制取与性质-2021-2022学年鲁教版九年级化学上册同步讲解及练习(含解析) |
|
|
| 格式 | doc | ||
| 文件大小 | 554.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-31 00:00:00 | ||
图片预览




文档简介
到实验室去:二氧化碳的实验室制取与性质
知识集结
知识元
制取二氧化碳的研究
知识讲解
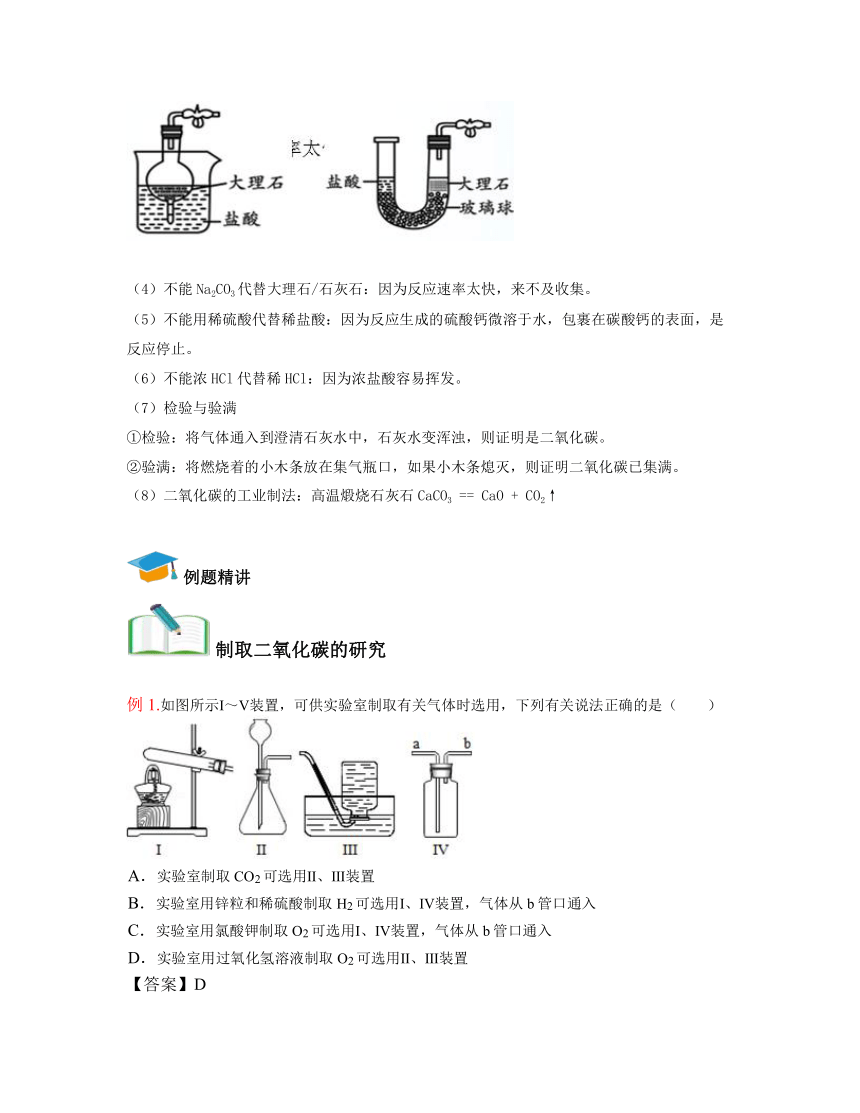
实验室制法:
(1)原料:大理石/石灰石、稀HCl;注:大理石和石灰石都是混合物,他们的主要成分是碳酸钙。
(2)原理:CaCO3
+?
HCl?
==CaCl2
+H2O
+CO2↑
(3)装置:
(4)不能Na2CO3代替大理石/石灰石:因为反应速率太快,来不及收集。
(5)不能用稀硫酸代替稀盐酸:因为反应生成的硫酸钙微溶于水,包裹在碳酸钙的表面,是反应停止。
(6)不能浓HCl代替稀HCl:因为浓盐酸容易挥发。
(7)检验与验满
①检验:将气体通入到澄清石灰水中,石灰水变浑浊,则证明是二氧化碳。
②验满:将燃烧着的小木条放在集气瓶口,如果小木条熄灭,则证明二氧化碳已集满。
(8)二氧化碳的工业制法:高温煅烧石灰石CaCO3
==
CaO
+
CO2↑
?
例题精讲
制取二氧化碳的研究
例1.如图所示Ⅰ~Ⅴ装置,可供实验室制取有关气体时选用,下列有关说法正确的是( )
A.实验室制取CO2可选用Ⅱ、Ⅲ装置
B.实验室用锌粒和稀硫酸制取H2可选用Ⅰ、Ⅳ装置,气体从b管口通入
C.实验室用氯酸钾制取O2可选用Ⅰ、Ⅳ装置,气体从b管口通入
D.实验室用过氧化氢溶液制取O2可选用Ⅱ、Ⅲ装置
【答案】D
【解析】
题干解析:A.因为二氧化碳气体能溶与水,故不能用排水法来收集,故A错误;
B.实验室制取氢气所用的药品分别为固体和液体,反应是在常温下进行的,故选择B来制取,氢气的密度比空气小,应该从b管进入,故错误;
C.氧气的密度比空气大,用Ⅳ来收集时,应从a进入,故错误;
D.过氧化氢溶液是液体,二氧化锰是固体,反应是在常温下进行的,故选B来制取,氧气不易溶于水,故可用排水法来收集,故正确.
例2.实验室要制取干燥的二氧化碳气体,应该选用的试剂为( )
A.大理石、盐酸、浓硫酸
B.石灰石、盐酸、氢氧化钠
C.大理石、稀硫酸、氢氧化钠固体
D.石灰石、稀硫酸、浓硫酸
【答案】A
【解析】
题干解析:A.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,二氧化碳可以用浓硫酸干燥,故选项正确;
B.石灰石、盐酸可行,氢氧化钠能吸收二氧化碳,因为氢氧化钠和二氧化碳反应,故选项错误;
C.大理石、稀硫酸不可行,因为生成物微溶于水,阻碍反应的进行,氢氧化钠固体不能干燥二氧化碳,故选项错误;
D.稀硫酸不可行,因为生成物微溶于水,阻碍反应的进行,故选项错误;
例3.实验室制取气体选择收集方法时,下列性质:①颜色;②密度;③溶解性;④可燃性;⑤能否与水反应,必须考虑的是(??
)
A.①②③
B.②③④
C.③④⑤
D.②③⑤
【答案】D
【解析】
题干解析:收集装置的选择要充分考虑所收集气体密度、溶解性,能否与空气成分反应以及能否与水反应等因素。
例4.实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究,请回答有关问题:
(1)请写出图中标有字母的仪器名称:a ?
b ??
.
(2)实验室用氯酸钾和二氧化锰混合制取氧气时,应选用的发生装置是 ?
(填写装置的字母代号,下同),请写出该反应的化学方程式: ??????
,其中二氧化锰起 ??????
作用。
(3)实验室制取二氧化碳气体时,应选择的发生装置和收集装置是 ?????
.请写出用澄清石灰水检验二氧化碳时发生反应的化学方程式: ?????
.
(4)如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是 、 且密度比空气的大,因此,二氧化碳可用于 .
【答案】
(1)铁架台,酒精灯
(2)B,2KClO32KCl+3O2↑,催化
(3)AC,CO2+Ca(OH)2=CaCO3↓+H2O
(4)不能燃烧(或不能支持燃烧),不能支持燃烧(或不能燃烧),灭火
【解析】
题干解析:(1)依据实验室常用仪器认识解决此题.
(2)实验室用氯酸钾和二氧化锰混合制取氧气时,选用的是固态物质反应需加热的发生装置;会写该反应原理的化学方程式;知道该反应中二氧化锰做反应条件催化剂起什么作用.
(3)实验室制取二氧化碳气体时,应选用的是固态物质和液态物质反应不需加热的发生装置;收集装置是根据其密度比空气大的性质决定,不能用排水法收集(因二氧化碳既能溶于水又能和水反应);检验该气体是将此气体通入澄清的石灰水观察是否变浑浊,并能写出其反应的化学方程式.
(4)如图F实验向烧杯中“倾倒”二氧化碳,说明二氧化碳的密度比空气的大,下层蜡烛先熄灭,上层蜡烛后熄灭,更进一步说明二氧化碳具有的性质,这样能探究二氧化碳的性质和重要用途。
例5.某钙片的标签如图,且知此钙片成分中只有碳酸钙含有钙元素:
(1)请通过计算说明此标签中的含钙量是错误的.
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生的化学反应是:CaCO3+2HCl═CaCl2+H2O+CO2↑,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验,数据如下
?
物质的质量
?
第一次
?
第二次
?
第三次
?
平均值
反应前:烧杯+盐酸
???
22
g
???
22
g
???
22
g
???
22
g
???
10片钙片
???
8
g
???
8
g
???
8
g
???
8
g
反应后:烧杯十剩余物
??
26.7
g
??
26.5
g
??
26.9
g
??
26.7g
①请列式计算每片此钙片含碳酸钙的质量.
②请列式计算每片此钙片的含钙量,并建议厂家如何修改标签.
【答案】
(1)此标签中的含钙量错误.
(2)①因此本品每片不可能含钙0.75g,此标签中的含钙量错误.
②将含钙量“每片含钙0.75g”改为“每片含钙0.3g”.
【解析】
题干解析:(1)本品若为纯碳酸钙,碳酸钙的相对分子质量为100,钙元素的质量分数为40
100×100%=40%,每片含钙量为:40g
50×40%=0.32g因此本品每片不可能含钙0.75g,此标签中的含钙量错误.
(2)设:10片钙片含碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100?????????????????
44
x??????????????????
3.3g
x=
=7.5g
每片此钙片含碳酸钙?
=0.75g
纯碳酸钙含钙质量分数
×100%=40%
每片此钙片的含钙量:0.75g×40%=0.3g
答:①因此本品每片不可能含钙0.75g,此标签中的含钙量错误.
②将含钙量“每片含钙0.75g”改为“每片含钙0.3g”.
?
二氧化碳
知识讲解
1.
二氧化碳的倾倒实验
实验方法
:在一烧杯中放入两个有高度差的蜡烛,向烧杯中缓慢倒入二氧化碳。
实验现象:发现低的蜡烛先灭,高的蜡烛后灭。
实验分析:二氧化碳气体不支持燃烧,且密度比空气大,倾倒时会在烧杯底部先聚集较多的二氧化碳,使下方的蜡烛首先接触到较多二氧化碳而先熄灭,上方的蜡烛后接触到二氧化碳而后熄灭。
2.二氧化碳的水溶性实验
实验方法
:在一矿泉水瓶中装满二氧化碳,向水瓶中倒入适量的水,迅速拧紧瓶盖。
实验现象:一段时间后发现矿泉水瓶变瘪。
实验分析:二氧化碳能溶于水,使瓶内气压减小,所以瓶会变瘪。
3.二氧化碳和水反应实验
实验方法:取四朵用石蕊试液染成的紫色的干燥纸花,在第一朵上喷稀盐酸,第二朵上喷水,第三朵放入装有二氧化碳的瓶中,第四朵先喷水再放入装有二氧化碳的瓶中。然后将第四朵取出小心的用吹风机吹干。
实验原理:酸性溶液会使紫色石蕊变红。
实验现象:第一朵干燥纸花会变为红色。第二朵干燥的纸花仍为紫色。第三朵干燥纸花仍为紫色。第四朵干燥的纸花会变为红色,用吹风机吹干后纸花又变成紫色。
实验分析:因为盐酸显酸性,而石蕊试液遇酸则会变红,则喷稀盐酸的话,干燥纸花会变为红色。因为水显中性,而石蕊试液遇中性物质不会变颜色,则喷水的话,干燥的纸花仍为紫色。
因为二氧化碳气体可以与水反应生成碳酸,CO2+H2O
═
H2CO3,而碳酸显酸性,则喷了水的纸花放在二氧化碳气体中会变为红色。而干燥的纸花上没有水,则二氧化碳不会与其反应,所以直接放到二氧化碳中的纸花不会变色。因为碳酸容易分解,H2CO3
═
CO2↑
+
H2O,所以当烘干时,碳酸分解,所以红色石蕊溶液又变成紫色。
4.二氧化碳与还原性金属或非金属单质反应
(1)镁在二氧化碳中燃烧实验
实验方法:镁条去除氧化膜后用酒精灯点燃,放入充满二氧化碳气体的烧瓶中。
实验原理:2Mg+CO22MgO+C
实验现象:镁条在烧杯中燃烧耀眼的白光,杯壁有黑色的颗粒,还有白色的金属物存在。
实验分析:黑色颗粒是炭单质,白色金属是氧化镁。
(2)二氧化碳与碳的反应
方程式:CO2+C
?2CO
结论:(1)燃烧不一定需要氧气参加。
?????
(2)二氧化碳在特殊情况下也能参与燃烧。
?????
(3)上述两反应中二氧化碳是氧化剂,镁、碳是还原剂.
5.二氧化碳与澄清石灰水反应
实验方法:将二氧化碳气体通入澄清石灰水中。
实验原理:CO2+Ca(OH)2
=
CaCO3↓+H2O
实验现象:澄清石灰水变浑浊。
结论:此反应原理可以用来检验或者鉴定二氧化碳气体。
6.二氧化碳的用途
灭火。因为二氧化碳既不参与燃烧,也不支持燃烧,且密度比空气大,所以,二氧化碳能覆盖在可燃物的表面,使可燃物隔绝氧气而熄灭。(注意二氧化碳灭火器不能用于还原性金属灭火)
干冰作致冷剂。在一定条件下二氧化碳会变成固体或者液体,固态二氧化碳叫做干冰,干冰升华时会吸收大量的热,因此干冰可以作为制冷剂。
植物光合作用作气肥。
工业原料
7.二氧化碳对环境的影响(温室效应)
大气中的二氧化碳气体能像温室中的玻璃或者塑料薄膜那样,使地面吸收的太阳光的能量而不易扩散,从而使全球变暖,这种现象叫做温室效应
危害:(1)两极冰川融化,海平面上升。
(2)气候反常,海洋风暴变多。
(3)土地干旱,沙漠化面积增大。
防范措施:
(1)尽量减少使用化石燃料。
????????
(2)利用太阳能、风能、水能等清洁燃料。
????????
(3)大力植树造林,退耕还林,严禁乱砍滥伐。
例题精讲
二氧化碳
例1.利用如图所示装置,能完成实验室制取气体的是( )
A.用①③制取氧气
B.用②③制取二氧化碳
C.用②④制取氧气
D.用①⑤制取二氧化碳
【答案】C
【解析】
题干解析:(1)装置①②均可以用于实验室制取氧气;装置④⑤均可以用于实验室收集氧气(2)实验室中只能利用装置②制取二氧化碳;只能用装置④收集二氧化碳.
例2.下列实验现象中,可以用来判断集气瓶里盛有CO2的是( )
A.集气瓶正立桌上,瓶中气体是无色的
B.往集气瓶里倒入少量紫色石蕊试液,振荡,试液变成浅红色
C.将燃着的木条伸入集气瓶里,火焰熄灭了
D.往集气瓶里倒入少量澄清的石灰水,振荡,石灰水变浑浊了
【答案】D
【解析】
题干解析:A.集气瓶正立桌上,瓶中气体是无色,只能说明此气体的密度大于空气的密度,不能证明是二氧化碳,因为氧气的密度也大于空气的密度;
B.往集气瓶里倒入少量紫色石蕊试液,振荡,试液变成浅红色,只能说明气体是酸性气体,不能证明是二氧化碳,因为二氧化硫等也是酸性气体;
C.将燃着的木条伸入集气瓶里,火焰熄灭了,只能说明此气体不支持燃烧,不能证明是二氧化碳,因为氮气、稀有气体也不支持燃烧;
D.二氧化碳可使澄清的石灰水变浑浊,这是二氧化碳的特性,所以往集气瓶里倒入少量澄清的石灰水,振荡,石灰水变浑浊了,可以说明是二氧化碳.
例3.关于二氧化碳的自述中,你认为不符合事实的是( )
A.我能使澄清的石灰水变浑浊
B.我承认“温室效应”主要是我惹的祸
C.我能帮助绿色植物进行光合作用
D.我能与人体血红蛋白结合,使人中毒
【答案】D
【解析】
题干解析:A.二氧化碳与氢氧化钙反应生成碳酸钙和水,所以二氧化碳能使澄清石灰水变浑浊,故此答案错误;
B.温室气体中二氧化碳是主要气体,故此答案错误;
C.光合作用时二氧化碳是主要原料之一,故此答案错误;
D.一氧化碳能与血红蛋白结合,使人产生一氧化碳中毒,这不是二氧化碳的性质,故此答案正确.
例4.已知A.B为两种黑色粉末,D为红色单质.A.B.C.D.E五种物质之间的转化关系如图所示.请回答:
(1)C的化学式为 ??????????
;D的化学式为 ??????
.
(2)A中金属元素的化合价是 ???????????????
.
(3)反应①的化学方程式为 ?????
;该反应的基本类型是 ???????????
.
【答案】
(1)C为CO2,D为Cu(2)+2价.(3)C+2CuO
2Cu+CO2↑;置换反应
【解析】
题干解析:(1)两种黑色粉末为碳和氧化铜,反应后生成CO2、和Cu,C能与澄清石灰水继续反应,则D为Cu,C为CO2,
(2)A中有金属元素,则A为氧化铜,其中铜化合价为+2价.
(3)碳和氧化铜在高温下发生了置换反应,则化学方程式为
C+2CuO
2Cu+CO2↑;置换反应
?
例5.用紫色石蕊试液浸泡几朵小纸花,并晾干。
(1)实验Ⅰ只说明了石蕊遇酸变红色,与本实验没有任何关系该说法是 (
选填“正确”或“不正确”)
(2)实验Ⅱ为对照实验,说明 ?????????????????????
(3)实验Ⅲ为对照实验,说明 ?????????????????????
(4)实验Ⅳ为验证实验,说明 ??????????????
(用化学方程式表示)
【答案】
(1)不正确;(2)水不能使石蕊试液变红;(3)二氧化碳也不能使石蕊试液变红;(4)CO2+H2O═H2CO3.
【解析】
题干解析:(1)实验I说明石蕊遇酸溶液变红,为实验IV中的石蕊花变红作对比,从而说明了二氧化碳与水作用形成了酸.所以说实验I并非可有可无,反而是起到重要的对比作用.
(2)实验Ⅱ为对照实验,说明水不能使石蕊变红;
(3)实验Ⅲ为对照实验,说明二氧化碳不能使石蕊变红.
(4)实验Ⅳ为验证实验,由纸花变红,说明二氧化碳能与水反应生成了酸,反应的化学方程式是:CO2+H2O═H2CO3.
当堂练习
单选题
练习1.
(2019?慈溪市模拟)甲乙是某同学设计的两套制取二氧化碳的发生装置,对两套装置分析不正确的是( )
A.此时甲装置中的止水夹M处于关闭状态
B.甲装置气体导出过程中容器内外气压相等
C.甲装置优点可以控制化学反应的发生与停止
D.乙装置N处添加止水夹可以与甲装置具有相同功能
【答案】D
【解析】
题干解析:
A、此时甲装置中的止水夹M处于关闭状态,正确但不符合题意,故选项错误;
B、甲装置气体导出过程中容器内外气压相等,气体才会顺利导出,正确但不符合题意,故选项错误;
C、甲装置的优点是:可以控制反应的发生和停止,具有启普发生器的功能,正确但不符合题意,故选项错误;
D、乙装置N处添加止水夹也与甲装置具有的功能不同,因为乙中固体与液体不能分离,错误符合题意,故选项正确;
练习2.
(2019?绍兴模拟)根据如图所示实验,下列对应的实验结果描述正确的是( )
A.甲读数偏小
B.乙测量结果偏大
C.丙易收集满CO2
D.丁集气瓶易破裂
【答案】D
【解析】
题干解析:
A、测量液体的体积,俯视读数比实际药品偏大,不是偏小,故选项错误;
B、空气中氧气含量的测定中,用木炭结果偏小,因为碳和氧气点燃生成二氧化碳,不是偏大。故选项错误;
C、实验室制取并收集二氧化碳,应该从长管进入,因为二氧化碳的密度比空气大;故选项错误;
D、铁丝在氧气中燃烧,集气瓶底部没有水或细沙,容易炸裂集气瓶,故选项正确;
填空题
练习1.
(2019春?嵊州市期末)实验室中常用石灰石和稀盐酸反应制取CO2,根据如图所示装置回答下列问题。
(1)实验中应选择的发生装置是___(填字母)。(2)如果选用E装置来收集CO2气体,则气体应从___(选填“a”或“b”)端进入。
【答案】
(1)B;
(2)a
【解析】
题干解析:(1)实验室中常用石灰石和稀盐酸反应制取CO2,不需要加热,为了防止生成的气体从长颈漏斗下端逸出,长颈漏斗下端应该靠近锥形瓶底部,故发生装置应选B;(2)因为二氧化碳的密度比空气大,应该用向上排空气法收集,若E装置收集,气体应该长进短出,则气体应从a端进入。
练习2.
(2019春?泰顺县校级月考)神舟七号载人飞船成功返航,标志着我国已跨入航天领域国际领先行列。某研究性学习小组查阅资料得知,宇宙飞船中可用超氧化钾(KO2)作为氧气再生剂。超氧化钾是一种固体,它与人呼出的二氧化碳反应生成氧气:4KO2+2CO2=2K2CO3+3O2为了验证这个反应能够产生氧气,该小组同学以大理石和盐酸反应生成的CO2来与KO2反应制取O2,设计了如下实验装置:
(1)C处应从A、B两种装置中选择___作CO2发生装置。检验G中集气瓶内收集的气体是否为氧气,可以在取出集气瓶后,用________检验;(2)A装置中仪器a的名称是______;
(3)为了除去O2中可能混有的CO2,F中可盛放______溶液;
【答案】
(1)锥形瓶;
(2)DM;
(3)反应条件
【解析】
题干解析:(1)制取二氧化碳用固体和液体反应,并且不需要加热,所以应选择A装置;检验氧气使用的是带火星的木条;故填:A;带火星的木条;(2)A装置中仪器a的名称是分液漏斗;故填:分液漏斗;(3)除去O2中可能混有的CO2的方法是通过氢氧化钠溶液,二氧化碳能和氢氧化钠溶液反应,氧气不能;故填:氢氧化钠。
练习3.
(2019?南关区校级一模)如图所示是实验室制取气体的常用仪器,回答下列问题。
(1)仪器E的名称是_____;
(2)在实验室用石灰石和稀盐酸反应并用排空气法收集二氧化碳气体,组装一套制取装置,需要用到上图仪器中A、C、F、___和毛玻璃片;
(3)确定气体的发生装置时,需要考虑反应物的状态和______;
(4)取5g石灰石(石灰石中的杂质不溶解且不与盐酸反应),加入足量的盐酸,充分反应后,过滤、洗涤、烘干,称量剩余固体的质量为1g计算:所用大理石中碳酸钙的质量分数为_____。
【答案】
(1)酒精灯;(2)B(3)反应条件(4)80%
【解析】
题干解析:(1)仪器E的名称是酒精灯;(2)在实验室用石灰石和稀盐酸反应制取二氧化碳,不需要加热,反应物的状态是固体和液体,属于固、液常温型反应;二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集;组装一套制取装置,需要用到上图仪器中A、C、F、B和毛玻璃片;(3)确定气体的发生装置时,需要考虑反应物的状态和反应条件;(4)所用大理石中碳酸钙的质量分数为:=80%
练习4.
(2019?北京模拟)下列为实验室制取氧气,并验证气体的化学性质。
(1)实验1中反应的化学方程式为________________________,氧气可用排水法收集的原因是_________。
(2)实验2中观察到的现象是______________________________,实验3中,打开K1,观察到蜡烛缓慢的熄灭。蜡烛熄灭的原因_________________________________。
【答案】
(1)2KMnO4K2MnO4+MnO2+O2↑;氧气不易溶于水;%%(2)发白光、放出大量的热、生成一种能使澄清石灰水变浑浊的气体;二氧化碳不可燃,不助燃,密度比空气大,使蜡烛与氧气隔绝。
【解析】
题干解析:(1)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4K2MnO4+MnO2+O2↑;氧气不易溶于水,故可以用排水法收集;(2)木炭在氧气中燃烧,发白光、放出大量的热、生成一种能使澄清石灰水变浑浊的气体;二氧化碳不可燃,不助燃,密度比空气大,稀盐酸和石灰石反应生成二氧化碳进入烧杯中,使蜡烛与氧气隔绝而熄灭。故填:(1)2KMnO4K2MnO4+MnO2+O2↑;氧气不易溶于水;(2)发白光、放出大量的热、生成一种能使澄清石灰水变浑浊的气体;二氧化碳不可燃,不助燃,密度比空气大,使蜡烛与氧气隔绝。
知识集结
知识元
制取二氧化碳的研究
知识讲解
实验室制法:
(1)原料:大理石/石灰石、稀HCl;注:大理石和石灰石都是混合物,他们的主要成分是碳酸钙。
(2)原理:CaCO3
+?
HCl?
==CaCl2
+H2O
+CO2↑
(3)装置:
(4)不能Na2CO3代替大理石/石灰石:因为反应速率太快,来不及收集。
(5)不能用稀硫酸代替稀盐酸:因为反应生成的硫酸钙微溶于水,包裹在碳酸钙的表面,是反应停止。
(6)不能浓HCl代替稀HCl:因为浓盐酸容易挥发。
(7)检验与验满
①检验:将气体通入到澄清石灰水中,石灰水变浑浊,则证明是二氧化碳。
②验满:将燃烧着的小木条放在集气瓶口,如果小木条熄灭,则证明二氧化碳已集满。
(8)二氧化碳的工业制法:高温煅烧石灰石CaCO3
==
CaO
+
CO2↑
?
例题精讲
制取二氧化碳的研究
例1.如图所示Ⅰ~Ⅴ装置,可供实验室制取有关气体时选用,下列有关说法正确的是( )
A.实验室制取CO2可选用Ⅱ、Ⅲ装置
B.实验室用锌粒和稀硫酸制取H2可选用Ⅰ、Ⅳ装置,气体从b管口通入
C.实验室用氯酸钾制取O2可选用Ⅰ、Ⅳ装置,气体从b管口通入
D.实验室用过氧化氢溶液制取O2可选用Ⅱ、Ⅲ装置
【答案】D
【解析】
题干解析:A.因为二氧化碳气体能溶与水,故不能用排水法来收集,故A错误;
B.实验室制取氢气所用的药品分别为固体和液体,反应是在常温下进行的,故选择B来制取,氢气的密度比空气小,应该从b管进入,故错误;
C.氧气的密度比空气大,用Ⅳ来收集时,应从a进入,故错误;
D.过氧化氢溶液是液体,二氧化锰是固体,反应是在常温下进行的,故选B来制取,氧气不易溶于水,故可用排水法来收集,故正确.
例2.实验室要制取干燥的二氧化碳气体,应该选用的试剂为( )
A.大理石、盐酸、浓硫酸
B.石灰石、盐酸、氢氧化钠
C.大理石、稀硫酸、氢氧化钠固体
D.石灰石、稀硫酸、浓硫酸
【答案】A
【解析】
题干解析:A.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,二氧化碳可以用浓硫酸干燥,故选项正确;
B.石灰石、盐酸可行,氢氧化钠能吸收二氧化碳,因为氢氧化钠和二氧化碳反应,故选项错误;
C.大理石、稀硫酸不可行,因为生成物微溶于水,阻碍反应的进行,氢氧化钠固体不能干燥二氧化碳,故选项错误;
D.稀硫酸不可行,因为生成物微溶于水,阻碍反应的进行,故选项错误;
例3.实验室制取气体选择收集方法时,下列性质:①颜色;②密度;③溶解性;④可燃性;⑤能否与水反应,必须考虑的是(??
)
A.①②③
B.②③④
C.③④⑤
D.②③⑤
【答案】D
【解析】
题干解析:收集装置的选择要充分考虑所收集气体密度、溶解性,能否与空气成分反应以及能否与水反应等因素。
例4.实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究,请回答有关问题:
(1)请写出图中标有字母的仪器名称:a ?
b ??
.
(2)实验室用氯酸钾和二氧化锰混合制取氧气时,应选用的发生装置是 ?
(填写装置的字母代号,下同),请写出该反应的化学方程式: ??????
,其中二氧化锰起 ??????
作用。
(3)实验室制取二氧化碳气体时,应选择的发生装置和收集装置是 ?????
.请写出用澄清石灰水检验二氧化碳时发生反应的化学方程式: ?????
.
(4)如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是 、 且密度比空气的大,因此,二氧化碳可用于 .
【答案】
(1)铁架台,酒精灯
(2)B,2KClO32KCl+3O2↑,催化
(3)AC,CO2+Ca(OH)2=CaCO3↓+H2O
(4)不能燃烧(或不能支持燃烧),不能支持燃烧(或不能燃烧),灭火
【解析】
题干解析:(1)依据实验室常用仪器认识解决此题.
(2)实验室用氯酸钾和二氧化锰混合制取氧气时,选用的是固态物质反应需加热的发生装置;会写该反应原理的化学方程式;知道该反应中二氧化锰做反应条件催化剂起什么作用.
(3)实验室制取二氧化碳气体时,应选用的是固态物质和液态物质反应不需加热的发生装置;收集装置是根据其密度比空气大的性质决定,不能用排水法收集(因二氧化碳既能溶于水又能和水反应);检验该气体是将此气体通入澄清的石灰水观察是否变浑浊,并能写出其反应的化学方程式.
(4)如图F实验向烧杯中“倾倒”二氧化碳,说明二氧化碳的密度比空气的大,下层蜡烛先熄灭,上层蜡烛后熄灭,更进一步说明二氧化碳具有的性质,这样能探究二氧化碳的性质和重要用途。
例5.某钙片的标签如图,且知此钙片成分中只有碳酸钙含有钙元素:
(1)请通过计算说明此标签中的含钙量是错误的.
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生的化学反应是:CaCO3+2HCl═CaCl2+H2O+CO2↑,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验,数据如下
?
物质的质量
?
第一次
?
第二次
?
第三次
?
平均值
反应前:烧杯+盐酸
???
22
g
???
22
g
???
22
g
???
22
g
???
10片钙片
???
8
g
???
8
g
???
8
g
???
8
g
反应后:烧杯十剩余物
??
26.7
g
??
26.5
g
??
26.9
g
??
26.7g
①请列式计算每片此钙片含碳酸钙的质量.
②请列式计算每片此钙片的含钙量,并建议厂家如何修改标签.
【答案】
(1)此标签中的含钙量错误.
(2)①因此本品每片不可能含钙0.75g,此标签中的含钙量错误.
②将含钙量“每片含钙0.75g”改为“每片含钙0.3g”.
【解析】
题干解析:(1)本品若为纯碳酸钙,碳酸钙的相对分子质量为100,钙元素的质量分数为40
100×100%=40%,每片含钙量为:40g
50×40%=0.32g因此本品每片不可能含钙0.75g,此标签中的含钙量错误.
(2)设:10片钙片含碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100?????????????????
44
x??????????????????
3.3g
x=
=7.5g
每片此钙片含碳酸钙?
=0.75g
纯碳酸钙含钙质量分数
×100%=40%
每片此钙片的含钙量:0.75g×40%=0.3g
答:①因此本品每片不可能含钙0.75g,此标签中的含钙量错误.
②将含钙量“每片含钙0.75g”改为“每片含钙0.3g”.
?
二氧化碳
知识讲解
1.
二氧化碳的倾倒实验
实验方法
:在一烧杯中放入两个有高度差的蜡烛,向烧杯中缓慢倒入二氧化碳。
实验现象:发现低的蜡烛先灭,高的蜡烛后灭。
实验分析:二氧化碳气体不支持燃烧,且密度比空气大,倾倒时会在烧杯底部先聚集较多的二氧化碳,使下方的蜡烛首先接触到较多二氧化碳而先熄灭,上方的蜡烛后接触到二氧化碳而后熄灭。
2.二氧化碳的水溶性实验
实验方法
:在一矿泉水瓶中装满二氧化碳,向水瓶中倒入适量的水,迅速拧紧瓶盖。
实验现象:一段时间后发现矿泉水瓶变瘪。
实验分析:二氧化碳能溶于水,使瓶内气压减小,所以瓶会变瘪。
3.二氧化碳和水反应实验
实验方法:取四朵用石蕊试液染成的紫色的干燥纸花,在第一朵上喷稀盐酸,第二朵上喷水,第三朵放入装有二氧化碳的瓶中,第四朵先喷水再放入装有二氧化碳的瓶中。然后将第四朵取出小心的用吹风机吹干。
实验原理:酸性溶液会使紫色石蕊变红。
实验现象:第一朵干燥纸花会变为红色。第二朵干燥的纸花仍为紫色。第三朵干燥纸花仍为紫色。第四朵干燥的纸花会变为红色,用吹风机吹干后纸花又变成紫色。
实验分析:因为盐酸显酸性,而石蕊试液遇酸则会变红,则喷稀盐酸的话,干燥纸花会变为红色。因为水显中性,而石蕊试液遇中性物质不会变颜色,则喷水的话,干燥的纸花仍为紫色。
因为二氧化碳气体可以与水反应生成碳酸,CO2+H2O
═
H2CO3,而碳酸显酸性,则喷了水的纸花放在二氧化碳气体中会变为红色。而干燥的纸花上没有水,则二氧化碳不会与其反应,所以直接放到二氧化碳中的纸花不会变色。因为碳酸容易分解,H2CO3
═
CO2↑
+
H2O,所以当烘干时,碳酸分解,所以红色石蕊溶液又变成紫色。
4.二氧化碳与还原性金属或非金属单质反应
(1)镁在二氧化碳中燃烧实验
实验方法:镁条去除氧化膜后用酒精灯点燃,放入充满二氧化碳气体的烧瓶中。
实验原理:2Mg+CO22MgO+C
实验现象:镁条在烧杯中燃烧耀眼的白光,杯壁有黑色的颗粒,还有白色的金属物存在。
实验分析:黑色颗粒是炭单质,白色金属是氧化镁。
(2)二氧化碳与碳的反应
方程式:CO2+C
?2CO
结论:(1)燃烧不一定需要氧气参加。
?????
(2)二氧化碳在特殊情况下也能参与燃烧。
?????
(3)上述两反应中二氧化碳是氧化剂,镁、碳是还原剂.
5.二氧化碳与澄清石灰水反应
实验方法:将二氧化碳气体通入澄清石灰水中。
实验原理:CO2+Ca(OH)2
=
CaCO3↓+H2O
实验现象:澄清石灰水变浑浊。
结论:此反应原理可以用来检验或者鉴定二氧化碳气体。
6.二氧化碳的用途
灭火。因为二氧化碳既不参与燃烧,也不支持燃烧,且密度比空气大,所以,二氧化碳能覆盖在可燃物的表面,使可燃物隔绝氧气而熄灭。(注意二氧化碳灭火器不能用于还原性金属灭火)
干冰作致冷剂。在一定条件下二氧化碳会变成固体或者液体,固态二氧化碳叫做干冰,干冰升华时会吸收大量的热,因此干冰可以作为制冷剂。
植物光合作用作气肥。
工业原料
7.二氧化碳对环境的影响(温室效应)
大气中的二氧化碳气体能像温室中的玻璃或者塑料薄膜那样,使地面吸收的太阳光的能量而不易扩散,从而使全球变暖,这种现象叫做温室效应
危害:(1)两极冰川融化,海平面上升。
(2)气候反常,海洋风暴变多。
(3)土地干旱,沙漠化面积增大。
防范措施:
(1)尽量减少使用化石燃料。
????????
(2)利用太阳能、风能、水能等清洁燃料。
????????
(3)大力植树造林,退耕还林,严禁乱砍滥伐。
例题精讲
二氧化碳
例1.利用如图所示装置,能完成实验室制取气体的是( )
A.用①③制取氧气
B.用②③制取二氧化碳
C.用②④制取氧气
D.用①⑤制取二氧化碳
【答案】C
【解析】
题干解析:(1)装置①②均可以用于实验室制取氧气;装置④⑤均可以用于实验室收集氧气(2)实验室中只能利用装置②制取二氧化碳;只能用装置④收集二氧化碳.
例2.下列实验现象中,可以用来判断集气瓶里盛有CO2的是( )
A.集气瓶正立桌上,瓶中气体是无色的
B.往集气瓶里倒入少量紫色石蕊试液,振荡,试液变成浅红色
C.将燃着的木条伸入集气瓶里,火焰熄灭了
D.往集气瓶里倒入少量澄清的石灰水,振荡,石灰水变浑浊了
【答案】D
【解析】
题干解析:A.集气瓶正立桌上,瓶中气体是无色,只能说明此气体的密度大于空气的密度,不能证明是二氧化碳,因为氧气的密度也大于空气的密度;
B.往集气瓶里倒入少量紫色石蕊试液,振荡,试液变成浅红色,只能说明气体是酸性气体,不能证明是二氧化碳,因为二氧化硫等也是酸性气体;
C.将燃着的木条伸入集气瓶里,火焰熄灭了,只能说明此气体不支持燃烧,不能证明是二氧化碳,因为氮气、稀有气体也不支持燃烧;
D.二氧化碳可使澄清的石灰水变浑浊,这是二氧化碳的特性,所以往集气瓶里倒入少量澄清的石灰水,振荡,石灰水变浑浊了,可以说明是二氧化碳.
例3.关于二氧化碳的自述中,你认为不符合事实的是( )
A.我能使澄清的石灰水变浑浊
B.我承认“温室效应”主要是我惹的祸
C.我能帮助绿色植物进行光合作用
D.我能与人体血红蛋白结合,使人中毒
【答案】D
【解析】
题干解析:A.二氧化碳与氢氧化钙反应生成碳酸钙和水,所以二氧化碳能使澄清石灰水变浑浊,故此答案错误;
B.温室气体中二氧化碳是主要气体,故此答案错误;
C.光合作用时二氧化碳是主要原料之一,故此答案错误;
D.一氧化碳能与血红蛋白结合,使人产生一氧化碳中毒,这不是二氧化碳的性质,故此答案正确.
例4.已知A.B为两种黑色粉末,D为红色单质.A.B.C.D.E五种物质之间的转化关系如图所示.请回答:
(1)C的化学式为 ??????????
;D的化学式为 ??????
.
(2)A中金属元素的化合价是 ???????????????
.
(3)反应①的化学方程式为 ?????
;该反应的基本类型是 ???????????
.
【答案】
(1)C为CO2,D为Cu(2)+2价.(3)C+2CuO
2Cu+CO2↑;置换反应
【解析】
题干解析:(1)两种黑色粉末为碳和氧化铜,反应后生成CO2、和Cu,C能与澄清石灰水继续反应,则D为Cu,C为CO2,
(2)A中有金属元素,则A为氧化铜,其中铜化合价为+2价.
(3)碳和氧化铜在高温下发生了置换反应,则化学方程式为
C+2CuO
2Cu+CO2↑;置换反应
?
例5.用紫色石蕊试液浸泡几朵小纸花,并晾干。
(1)实验Ⅰ只说明了石蕊遇酸变红色,与本实验没有任何关系该说法是 (
选填“正确”或“不正确”)
(2)实验Ⅱ为对照实验,说明 ?????????????????????
(3)实验Ⅲ为对照实验,说明 ?????????????????????
(4)实验Ⅳ为验证实验,说明 ??????????????
(用化学方程式表示)
【答案】
(1)不正确;(2)水不能使石蕊试液变红;(3)二氧化碳也不能使石蕊试液变红;(4)CO2+H2O═H2CO3.
【解析】
题干解析:(1)实验I说明石蕊遇酸溶液变红,为实验IV中的石蕊花变红作对比,从而说明了二氧化碳与水作用形成了酸.所以说实验I并非可有可无,反而是起到重要的对比作用.
(2)实验Ⅱ为对照实验,说明水不能使石蕊变红;
(3)实验Ⅲ为对照实验,说明二氧化碳不能使石蕊变红.
(4)实验Ⅳ为验证实验,由纸花变红,说明二氧化碳能与水反应生成了酸,反应的化学方程式是:CO2+H2O═H2CO3.
当堂练习
单选题
练习1.
(2019?慈溪市模拟)甲乙是某同学设计的两套制取二氧化碳的发生装置,对两套装置分析不正确的是( )
A.此时甲装置中的止水夹M处于关闭状态
B.甲装置气体导出过程中容器内外气压相等
C.甲装置优点可以控制化学反应的发生与停止
D.乙装置N处添加止水夹可以与甲装置具有相同功能
【答案】D
【解析】
题干解析:
A、此时甲装置中的止水夹M处于关闭状态,正确但不符合题意,故选项错误;
B、甲装置气体导出过程中容器内外气压相等,气体才会顺利导出,正确但不符合题意,故选项错误;
C、甲装置的优点是:可以控制反应的发生和停止,具有启普发生器的功能,正确但不符合题意,故选项错误;
D、乙装置N处添加止水夹也与甲装置具有的功能不同,因为乙中固体与液体不能分离,错误符合题意,故选项正确;
练习2.
(2019?绍兴模拟)根据如图所示实验,下列对应的实验结果描述正确的是( )
A.甲读数偏小
B.乙测量结果偏大
C.丙易收集满CO2
D.丁集气瓶易破裂
【答案】D
【解析】
题干解析:
A、测量液体的体积,俯视读数比实际药品偏大,不是偏小,故选项错误;
B、空气中氧气含量的测定中,用木炭结果偏小,因为碳和氧气点燃生成二氧化碳,不是偏大。故选项错误;
C、实验室制取并收集二氧化碳,应该从长管进入,因为二氧化碳的密度比空气大;故选项错误;
D、铁丝在氧气中燃烧,集气瓶底部没有水或细沙,容易炸裂集气瓶,故选项正确;
填空题
练习1.
(2019春?嵊州市期末)实验室中常用石灰石和稀盐酸反应制取CO2,根据如图所示装置回答下列问题。
(1)实验中应选择的发生装置是___(填字母)。(2)如果选用E装置来收集CO2气体,则气体应从___(选填“a”或“b”)端进入。
【答案】
(1)B;
(2)a
【解析】
题干解析:(1)实验室中常用石灰石和稀盐酸反应制取CO2,不需要加热,为了防止生成的气体从长颈漏斗下端逸出,长颈漏斗下端应该靠近锥形瓶底部,故发生装置应选B;(2)因为二氧化碳的密度比空气大,应该用向上排空气法收集,若E装置收集,气体应该长进短出,则气体应从a端进入。
练习2.
(2019春?泰顺县校级月考)神舟七号载人飞船成功返航,标志着我国已跨入航天领域国际领先行列。某研究性学习小组查阅资料得知,宇宙飞船中可用超氧化钾(KO2)作为氧气再生剂。超氧化钾是一种固体,它与人呼出的二氧化碳反应生成氧气:4KO2+2CO2=2K2CO3+3O2为了验证这个反应能够产生氧气,该小组同学以大理石和盐酸反应生成的CO2来与KO2反应制取O2,设计了如下实验装置:
(1)C处应从A、B两种装置中选择___作CO2发生装置。检验G中集气瓶内收集的气体是否为氧气,可以在取出集气瓶后,用________检验;(2)A装置中仪器a的名称是______;
(3)为了除去O2中可能混有的CO2,F中可盛放______溶液;
【答案】
(1)锥形瓶;
(2)DM;
(3)反应条件
【解析】
题干解析:(1)制取二氧化碳用固体和液体反应,并且不需要加热,所以应选择A装置;检验氧气使用的是带火星的木条;故填:A;带火星的木条;(2)A装置中仪器a的名称是分液漏斗;故填:分液漏斗;(3)除去O2中可能混有的CO2的方法是通过氢氧化钠溶液,二氧化碳能和氢氧化钠溶液反应,氧气不能;故填:氢氧化钠。
练习3.
(2019?南关区校级一模)如图所示是实验室制取气体的常用仪器,回答下列问题。
(1)仪器E的名称是_____;
(2)在实验室用石灰石和稀盐酸反应并用排空气法收集二氧化碳气体,组装一套制取装置,需要用到上图仪器中A、C、F、___和毛玻璃片;
(3)确定气体的发生装置时,需要考虑反应物的状态和______;
(4)取5g石灰石(石灰石中的杂质不溶解且不与盐酸反应),加入足量的盐酸,充分反应后,过滤、洗涤、烘干,称量剩余固体的质量为1g计算:所用大理石中碳酸钙的质量分数为_____。
【答案】
(1)酒精灯;(2)B(3)反应条件(4)80%
【解析】
题干解析:(1)仪器E的名称是酒精灯;(2)在实验室用石灰石和稀盐酸反应制取二氧化碳,不需要加热,反应物的状态是固体和液体,属于固、液常温型反应;二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集;组装一套制取装置,需要用到上图仪器中A、C、F、B和毛玻璃片;(3)确定气体的发生装置时,需要考虑反应物的状态和反应条件;(4)所用大理石中碳酸钙的质量分数为:=80%
练习4.
(2019?北京模拟)下列为实验室制取氧气,并验证气体的化学性质。
(1)实验1中反应的化学方程式为________________________,氧气可用排水法收集的原因是_________。
(2)实验2中观察到的现象是______________________________,实验3中,打开K1,观察到蜡烛缓慢的熄灭。蜡烛熄灭的原因_________________________________。
【答案】
(1)2KMnO4K2MnO4+MnO2+O2↑;氧气不易溶于水;%%(2)发白光、放出大量的热、生成一种能使澄清石灰水变浑浊的气体;二氧化碳不可燃,不助燃,密度比空气大,使蜡烛与氧气隔绝。
【解析】
题干解析:(1)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4K2MnO4+MnO2+O2↑;氧气不易溶于水,故可以用排水法收集;(2)木炭在氧气中燃烧,发白光、放出大量的热、生成一种能使澄清石灰水变浑浊的气体;二氧化碳不可燃,不助燃,密度比空气大,稀盐酸和石灰石反应生成二氧化碳进入烧杯中,使蜡烛与氧气隔绝而熄灭。故填:(1)2KMnO4K2MnO4+MnO2+O2↑;氧气不易溶于水;(2)发白光、放出大量的热、生成一种能使澄清石灰水变浑浊的气体;二氧化碳不可燃,不助燃,密度比空气大,使蜡烛与氧气隔绝。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
