黑龙江省哈尔滨萧红中学2021-2022学年上学期9月份开学化学测试(word版有答案)
文档属性
| 名称 | 黑龙江省哈尔滨萧红中学2021-2022学年上学期9月份开学化学测试(word版有答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 405.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-07 00:00:00 | ||
图片预览



文档简介
萧红中学九学年(上)暑假学情监测
可能用到的相对原子质量:H-1
C-12
N-14
O-16
S-32
Fe-56
Zn-65
Cu-64
Ag-108
一、选择题(每小题只有1个正确答案,每小题2分,共40分)
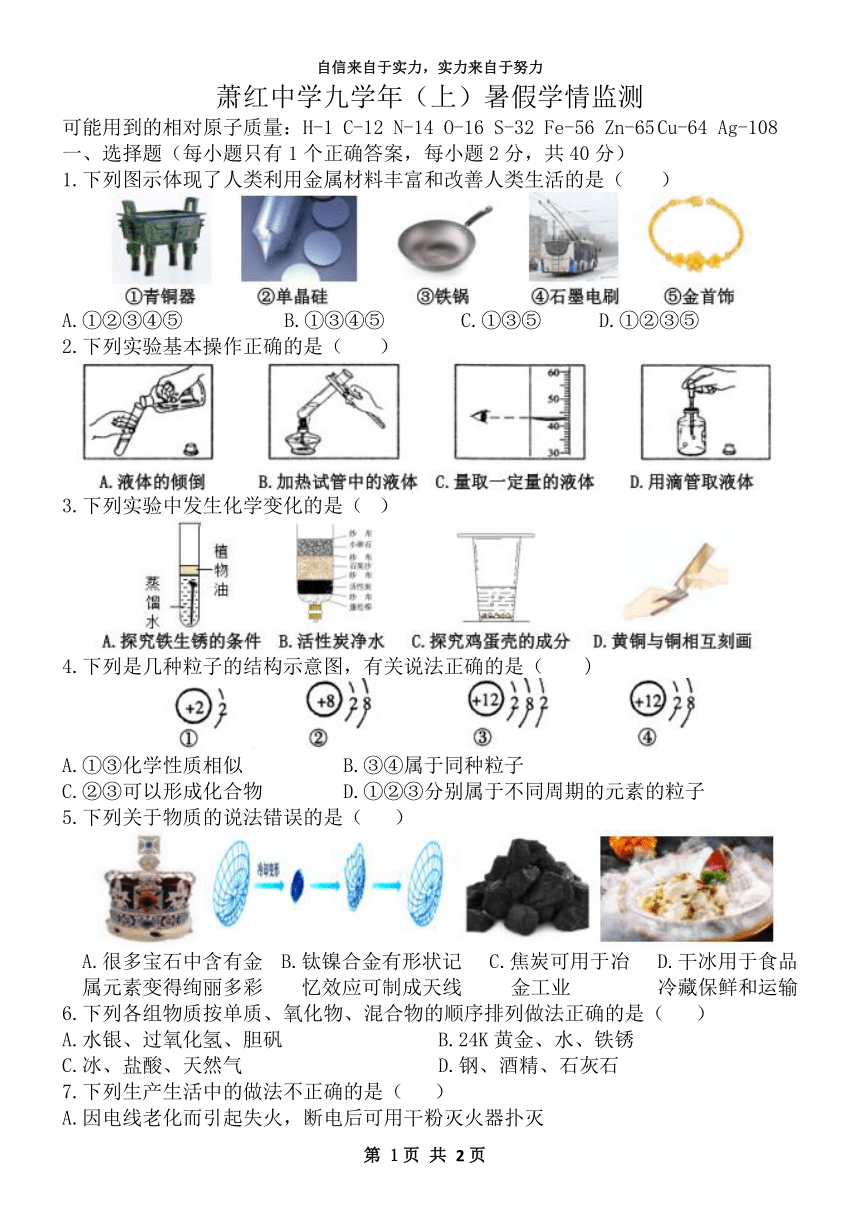
1.下列图示体现了人类利用金属材料丰富和改善人类生活的是(
)
A.①②③④⑤
B.①③④⑤
C.①③⑤
D.①②③⑤
2.下列实验基本操作正确的是(
)
3.下列实验中发生化学变化的是(
)
4.下列是几种粒子的结构示意图,有关说法正确的是(
)
A.①③化学性质相似
B.③④属于同种粒子
C.②③可以形成化合物
D.①②③分别属于不同周期的元素的粒子
5.下列关于物质的说法错误的是(
)
A.很多宝石中含有金
B.钛镍合金有形状记
C.焦炭可用于冶
D.干冰用于食品
属元素变得绚丽多彩
忆效应可制成天线
金工业
冷藏保鲜和运输
6.下列各组物质按单质、氧化物、混合物的顺序排列做法正确的是(
)
A.水银、过氧化氢、胆矾
B.24K黄金、水、铁锈
C.冰、盐酸、天然气
D.钢、酒精、石灰石
7.下列生产生活中的做法不正确的是(
)
A.因电线老化而引起失火,断电后可用干粉灭火器扑灭
B.燃气灶的火焰出现橙色或黄色时,可调小进气口或调大炉具进风口
C.被雨水淋湿的自行车要立刻用带油的抹布擦拭
D.铝的冶炼方法得到改进,且自身具有密度小、抗腐蚀性能好的优点,因而得到广泛应用
8.下列物质的用途,主要利用化学性质的是(
)
9.下列关于金属的说法正确的是(
)
A.含有金属元素的物质都是金属材料
B.目前已制得的纯金属只有90种,但是合金已达几千种
C.自然界中的金、银都是以单质形式存在的
D.目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零部件等
10.下列实验现象记录正确的是(
)
A.在空气中点燃镁带,银白色固体燃烧发出耀眼的白光,放热,产生黄白色火焰
B.加热通入二氧化碳的紫色石蕊溶液,紫色溶液变为红色
C.把铜丝放入稀硫酸中,紫红色固体表面产生气泡,无色溶液变成蓝色
D.将一氧化碳通入灼热的氧化铁中,红棕色粉末状固体逐渐变为黑色
11.下列有关叙述、对应的化学方程式、所属基本反应类型都正确的是(
)
A.工业上制取生石灰:
CaCO3
CaO
+
CO2
分解反应
B.铝具有很好抗腐蚀性的原因:
4Al
+
3O2
2Al2O3
化合反应
C.盐酸除铁锈时间不宜过长的原因:
Fe
+
2HCl
=
FeCl2
+
H2↑
置换反应
D.铁制容器配制农药波尔多液:
Fe
+
CuSO4
=
Cu
+
FeSO4
置换反应
12.下列与人体健康或生命安全有关的说法或做法中错误的是(
)
A.进入久未开启的菜窖、干涸的深井、矿井时,要先做灯火试验
B.长期饮用硬水不利于身体健康,可利用煮沸的方法降低水的硬度
C.经常使用铁锅炒菜,能适当补充铁元素
D.世界卫生组织将铝列为食品污染源之一,所以应尽量减少铝制食品或饮料包装
13.食醋是厨房中的一种调味品,其中含有少量醋酸。下列有关醋酸的说法正确的是(
)
A.醋酸是由碳、氢、氧三种原子构成的化合物
B.醋酸中含有碳原子、氢原子和氧原子
C.醋酸分子中碳、氢、氧元素的质量比为6:1:8
D.醋酸分子中有8个原子核
14.下列关于资源和能源的叙述中错误的是(
)
A.空气是一种宝贵的资源,空气中的各成分作为原料广泛应用于化肥、化工原料、电光源等
领域
B.地球上的陆地淡水储量约占全球总水量的2.53%,其中可以利用的淡水资源不足全球总水量的1%
C.现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~50%
D.有效地提高化石燃料的燃烧利用率,就相当于延长了化石能源的使用期限
15.对下列事实的微观解释错误的是(
)
选项
事实
解释
A
物质都有三态变化
构成物质的粒子间间隔不同
B
水蒸发为水蒸气,所占体积变大
水分子间隔变大
C
金刚石、石墨物理性质存在明显差异
碳原子的排列方式不同
D
打破的体温计中的水银使人中毒
汞分子不断运动且有毒
16.区分下列各组物质的两种方法都正确的是(
)
选项
待区分物质
方法一
方法二
A
软水与硬水
蒸干观察
加肥皂水观察
B
一氧化碳与二氧化碳
通入澄清石灰水中
通入氧化铜中
C
铁丝与铝丝
用磁铁吸引
加入硫酸铜溶液中
D
黄铜与18K黄金
观察颜色
空气中加热后观察颜色
17.下列有关说法错误的是(
)
A.在金属活动性顺序里,位于氢前的金属一定能置换出盐酸、稀硫酸中的氢气
B.置换反应中一定有元素化合价的改变
C.由同种元素组成的物质,一定不是化合物
D.合金一般比组成它的纯金属熔点更低、硬度更大、抗腐蚀性更好
18.除去下列物质中的少量杂质,所用试剂和操作方法都正确的是(
)
选项
物质
杂质
试剂和操作方法
A
CO2
CO
通入足量02后,点燃
B
CaCO3
Ca0
加足量水溶解、过滤、蒸发结晶
C
铜粉
Fe
加足量的稀盐酸,过滤
D
FeCl2溶液
CuCl2
加过量铁粉,过滤
19.等质量的稀盐酸分别与等质量且过量的铁、锌、镁反应。下列图像能正确反应产生氢气质量与时间之间关系的是(
)
20.某炼铁厂欲利用赤铁矿石(主要成分是氧化铁,杂质不含铁元素,也不参与反应)来炼铁。若要炼制含铁96%的生铁63t,则理论上需要含杂质20%的赤铁矿石的质量是(
)
A.120t
B.108t
C.96t
D.84t
二、非选择题(每空1分,共30分)
21.(5分)按要求回答下列问题
(1)①
与人体具有很好的“②
”,因此可以用来制造人造骨等。
(2)水龙头上镀铬的目的是
。
(3)
“真金不怕火炼”说明金即使在高温时
。
(4)铁锈主要成分的化学式
。
22.(5分)2021年哈尔滨市共享单车总量最大为12万台,电单车总量最大为3万台。
(1)电单车车体内自带发电设计,电单车蓄电池工作过程中的能量转化为:
化学能→①
→②
。
(2)—体化车身材料中大多含有金属铝。这主要利用铝的
等物理性能(填字母)
A.密度小、耐腐蚀
B.韧性好、硬度大
C.密度小、强度好
(3)电线大多用铜丝制作。铜单质也可以与某些酸反应,只是不生成氢气。如:铜与浓硫酸反应,生成硫酸铜、二氧化硫和水,写出此反应的化学方程式:①
;此反应前后硫元素的化合价分别为②
。
23.
(4分)分类是学习化学常用的方法。
(1)化学实验培养了我们科学思维的方法,也增强了我们学习化学的兴趣。如下为初中化学常见的实验。请根据实验所体现出物质的性质,应将下列实验中的D与①
(填“A”或“B”或“C”)归为一类,依据是②
。
(2)通过课外阅读发现有下列反应:C12+2NaBr=2NaCl+Br2
Br2+2KI=2KBr+I2
C12、Br2、I2是氯、溴、碘三种元素组成的三种非金属单质。经过类比分析,发现非金属单质与某些化合物发生的置换反应跟金属与某些化合物发生的置换反应有类似的规律。因此可以判断Cl2、Br2、I2三种非金属中活泼性最强的是①
(写化学式)。
查阅资料又得知结论:硫的活泼性比上述三种单质的活泼性都弱。
请仿照上述反应,用硫元素和钠元素组成的化合物与其发生的一个反应来证明此结论(用化学方程式回答)②
。
24.(6分)实验室现有如下实验用品:氯酸钾、稀盐酸、大理石、火柴、药匙、镊子、升降台及以下仪器。请回答下列问题,并按要求填写相应空白:
(1)利用上述仪器及药品能制取的气体是①
,发生反应的化学方程式为②
,制取这种气体需要的仪器标号有③
。
(2)若利用药品①
(填俗称)检验二氧化碳,实验中会观察到液面下的导管口有气泡冒出,这是因为发生装置内物质反应时气体②
,压强③
,大于外界压强,在压强差的作用下,气体从导管口冒出。
25.(5分)某为了测定某含杂质7%的黄铜(Cu、Zn)样品中铜的质量分数(杂质中不含铜、
锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
(1)发生反应的化学方程式为
。
(2)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为
。
(3)反应生成的硫酸锌的质量为
。
(4)该黄铜样品中铜的质量分数是
。
(5)实验中所用的稀硫酸中水与硫酸的质量比为
。
26.(5分)金属在日常生活中有着广泛的用途。常见金属的活动性顺序如下:
请回答下面问题:
(1)金属活动性顺序表中的X是
(填写相应的元素符号)元素。
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为
。
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中逐渐加入Zn粉至过量,溶
液质量随反应时间的变化情况如右图所示。
①反应开始时看不到“银白色固体表面有紫红色固体出现”的原因是
。
②图中B点溶液中除水外还含有
(填化学式);
③图中C点滤渣成分有
(填化学式)。
参考答案
一、选择题(每小题
2
分,共
40
分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
C
D
A
B
C
B
D
D
题号
11
12
13
14
15
16
17
18
19
20
答案
C
A
B
C
D
C
A
D
B
B
二、非选择题(每空
1
分,共
30
分)
21.
(5
分)
①钛合金;②相容性
防锈、美观、耐磨,延长使用寿命;
也不与氧气反应;
Fe2O3·xH2O
22.
(5
分)
(1)①电能→②机械能
(2)C
(3)
①
Cu
+
(浓)2H2SO4
CuSO4
+
SO2↑+
2H2O
;
②
+6
价;+6、+4
价。23.(4
分)
①A
②都体现了金属能与氧气反应的实验
①Cl2
;②
Na2S+I2
2NaI+
S
24.(6
分)
①二氧化碳[或
CO2];
②CaCO3
+2HCl
CaCl2
+
H2O
+
CO2↑
③bcehi
①(澄清)石灰水;
②增多;
③变大。25.(5
分)
(1)Zn
+
H2SO4
==
ZnSO4
+
H2↑
(2)65/2
==
X
/
0.4g
(3)32.2g
(4)80%
(5)201:49
(
自信来自于实力,实力来自于努力
)
(
第
1
页
共
2
页
)
26.(5
分)
(1)Hg
(2)2Al
+
3CuSO4
3Cu
+
Al2(SO4)3
(4)
①铁片插入硝酸银和硝酸铜混合溶液中,铁片先与硝酸银溶液发生反应;
②Cu(NO3)2
和
Zn(NO3)2
;
③Ag、Cu、Zn
。
可能用到的相对原子质量:H-1
C-12
N-14
O-16
S-32
Fe-56
Zn-65
Cu-64
Ag-108
一、选择题(每小题只有1个正确答案,每小题2分,共40分)
1.下列图示体现了人类利用金属材料丰富和改善人类生活的是(
)
A.①②③④⑤
B.①③④⑤
C.①③⑤
D.①②③⑤
2.下列实验基本操作正确的是(
)
3.下列实验中发生化学变化的是(
)
4.下列是几种粒子的结构示意图,有关说法正确的是(
)
A.①③化学性质相似
B.③④属于同种粒子
C.②③可以形成化合物
D.①②③分别属于不同周期的元素的粒子
5.下列关于物质的说法错误的是(
)
A.很多宝石中含有金
B.钛镍合金有形状记
C.焦炭可用于冶
D.干冰用于食品
属元素变得绚丽多彩
忆效应可制成天线
金工业
冷藏保鲜和运输
6.下列各组物质按单质、氧化物、混合物的顺序排列做法正确的是(
)
A.水银、过氧化氢、胆矾
B.24K黄金、水、铁锈
C.冰、盐酸、天然气
D.钢、酒精、石灰石
7.下列生产生活中的做法不正确的是(
)
A.因电线老化而引起失火,断电后可用干粉灭火器扑灭
B.燃气灶的火焰出现橙色或黄色时,可调小进气口或调大炉具进风口
C.被雨水淋湿的自行车要立刻用带油的抹布擦拭
D.铝的冶炼方法得到改进,且自身具有密度小、抗腐蚀性能好的优点,因而得到广泛应用
8.下列物质的用途,主要利用化学性质的是(
)
9.下列关于金属的说法正确的是(
)
A.含有金属元素的物质都是金属材料
B.目前已制得的纯金属只有90种,但是合金已达几千种
C.自然界中的金、银都是以单质形式存在的
D.目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零部件等
10.下列实验现象记录正确的是(
)
A.在空气中点燃镁带,银白色固体燃烧发出耀眼的白光,放热,产生黄白色火焰
B.加热通入二氧化碳的紫色石蕊溶液,紫色溶液变为红色
C.把铜丝放入稀硫酸中,紫红色固体表面产生气泡,无色溶液变成蓝色
D.将一氧化碳通入灼热的氧化铁中,红棕色粉末状固体逐渐变为黑色
11.下列有关叙述、对应的化学方程式、所属基本反应类型都正确的是(
)
A.工业上制取生石灰:
CaCO3
CaO
+
CO2
分解反应
B.铝具有很好抗腐蚀性的原因:
4Al
+
3O2
2Al2O3
化合反应
C.盐酸除铁锈时间不宜过长的原因:
Fe
+
2HCl
=
FeCl2
+
H2↑
置换反应
D.铁制容器配制农药波尔多液:
Fe
+
CuSO4
=
Cu
+
FeSO4
置换反应
12.下列与人体健康或生命安全有关的说法或做法中错误的是(
)
A.进入久未开启的菜窖、干涸的深井、矿井时,要先做灯火试验
B.长期饮用硬水不利于身体健康,可利用煮沸的方法降低水的硬度
C.经常使用铁锅炒菜,能适当补充铁元素
D.世界卫生组织将铝列为食品污染源之一,所以应尽量减少铝制食品或饮料包装
13.食醋是厨房中的一种调味品,其中含有少量醋酸。下列有关醋酸的说法正确的是(
)
A.醋酸是由碳、氢、氧三种原子构成的化合物
B.醋酸中含有碳原子、氢原子和氧原子
C.醋酸分子中碳、氢、氧元素的质量比为6:1:8
D.醋酸分子中有8个原子核
14.下列关于资源和能源的叙述中错误的是(
)
A.空气是一种宝贵的资源,空气中的各成分作为原料广泛应用于化肥、化工原料、电光源等
领域
B.地球上的陆地淡水储量约占全球总水量的2.53%,其中可以利用的淡水资源不足全球总水量的1%
C.现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~50%
D.有效地提高化石燃料的燃烧利用率,就相当于延长了化石能源的使用期限
15.对下列事实的微观解释错误的是(
)
选项
事实
解释
A
物质都有三态变化
构成物质的粒子间间隔不同
B
水蒸发为水蒸气,所占体积变大
水分子间隔变大
C
金刚石、石墨物理性质存在明显差异
碳原子的排列方式不同
D
打破的体温计中的水银使人中毒
汞分子不断运动且有毒
16.区分下列各组物质的两种方法都正确的是(
)
选项
待区分物质
方法一
方法二
A
软水与硬水
蒸干观察
加肥皂水观察
B
一氧化碳与二氧化碳
通入澄清石灰水中
通入氧化铜中
C
铁丝与铝丝
用磁铁吸引
加入硫酸铜溶液中
D
黄铜与18K黄金
观察颜色
空气中加热后观察颜色
17.下列有关说法错误的是(
)
A.在金属活动性顺序里,位于氢前的金属一定能置换出盐酸、稀硫酸中的氢气
B.置换反应中一定有元素化合价的改变
C.由同种元素组成的物质,一定不是化合物
D.合金一般比组成它的纯金属熔点更低、硬度更大、抗腐蚀性更好
18.除去下列物质中的少量杂质,所用试剂和操作方法都正确的是(
)
选项
物质
杂质
试剂和操作方法
A
CO2
CO
通入足量02后,点燃
B
CaCO3
Ca0
加足量水溶解、过滤、蒸发结晶
C
铜粉
Fe
加足量的稀盐酸,过滤
D
FeCl2溶液
CuCl2
加过量铁粉,过滤
19.等质量的稀盐酸分别与等质量且过量的铁、锌、镁反应。下列图像能正确反应产生氢气质量与时间之间关系的是(
)
20.某炼铁厂欲利用赤铁矿石(主要成分是氧化铁,杂质不含铁元素,也不参与反应)来炼铁。若要炼制含铁96%的生铁63t,则理论上需要含杂质20%的赤铁矿石的质量是(
)
A.120t
B.108t
C.96t
D.84t
二、非选择题(每空1分,共30分)
21.(5分)按要求回答下列问题
(1)①
与人体具有很好的“②
”,因此可以用来制造人造骨等。
(2)水龙头上镀铬的目的是
。
(3)
“真金不怕火炼”说明金即使在高温时
。
(4)铁锈主要成分的化学式
。
22.(5分)2021年哈尔滨市共享单车总量最大为12万台,电单车总量最大为3万台。
(1)电单车车体内自带发电设计,电单车蓄电池工作过程中的能量转化为:
化学能→①
→②
。
(2)—体化车身材料中大多含有金属铝。这主要利用铝的
等物理性能(填字母)
A.密度小、耐腐蚀
B.韧性好、硬度大
C.密度小、强度好
(3)电线大多用铜丝制作。铜单质也可以与某些酸反应,只是不生成氢气。如:铜与浓硫酸反应,生成硫酸铜、二氧化硫和水,写出此反应的化学方程式:①
;此反应前后硫元素的化合价分别为②
。
23.
(4分)分类是学习化学常用的方法。
(1)化学实验培养了我们科学思维的方法,也增强了我们学习化学的兴趣。如下为初中化学常见的实验。请根据实验所体现出物质的性质,应将下列实验中的D与①
(填“A”或“B”或“C”)归为一类,依据是②
。
(2)通过课外阅读发现有下列反应:C12+2NaBr=2NaCl+Br2
Br2+2KI=2KBr+I2
C12、Br2、I2是氯、溴、碘三种元素组成的三种非金属单质。经过类比分析,发现非金属单质与某些化合物发生的置换反应跟金属与某些化合物发生的置换反应有类似的规律。因此可以判断Cl2、Br2、I2三种非金属中活泼性最强的是①
(写化学式)。
查阅资料又得知结论:硫的活泼性比上述三种单质的活泼性都弱。
请仿照上述反应,用硫元素和钠元素组成的化合物与其发生的一个反应来证明此结论(用化学方程式回答)②
。
24.(6分)实验室现有如下实验用品:氯酸钾、稀盐酸、大理石、火柴、药匙、镊子、升降台及以下仪器。请回答下列问题,并按要求填写相应空白:
(1)利用上述仪器及药品能制取的气体是①
,发生反应的化学方程式为②
,制取这种气体需要的仪器标号有③
。
(2)若利用药品①
(填俗称)检验二氧化碳,实验中会观察到液面下的导管口有气泡冒出,这是因为发生装置内物质反应时气体②
,压强③
,大于外界压强,在压强差的作用下,气体从导管口冒出。
25.(5分)某为了测定某含杂质7%的黄铜(Cu、Zn)样品中铜的质量分数(杂质中不含铜、
锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
(1)发生反应的化学方程式为
。
(2)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为
。
(3)反应生成的硫酸锌的质量为
。
(4)该黄铜样品中铜的质量分数是
。
(5)实验中所用的稀硫酸中水与硫酸的质量比为
。
26.(5分)金属在日常生活中有着广泛的用途。常见金属的活动性顺序如下:
请回答下面问题:
(1)金属活动性顺序表中的X是
(填写相应的元素符号)元素。
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为
。
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中逐渐加入Zn粉至过量,溶
液质量随反应时间的变化情况如右图所示。
①反应开始时看不到“银白色固体表面有紫红色固体出现”的原因是
。
②图中B点溶液中除水外还含有
(填化学式);
③图中C点滤渣成分有
(填化学式)。
参考答案
一、选择题(每小题
2
分,共
40
分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
C
D
A
B
C
B
D
D
题号
11
12
13
14
15
16
17
18
19
20
答案
C
A
B
C
D
C
A
D
B
B
二、非选择题(每空
1
分,共
30
分)
21.
(5
分)
①钛合金;②相容性
防锈、美观、耐磨,延长使用寿命;
也不与氧气反应;
Fe2O3·xH2O
22.
(5
分)
(1)①电能→②机械能
(2)C
(3)
①
Cu
+
(浓)2H2SO4
CuSO4
+
SO2↑+
2H2O
;
②
+6
价;+6、+4
价。23.(4
分)
①A
②都体现了金属能与氧气反应的实验
①Cl2
;②
Na2S+I2
2NaI+
S
24.(6
分)
①二氧化碳[或
CO2];
②CaCO3
+2HCl
CaCl2
+
H2O
+
CO2↑
③bcehi
①(澄清)石灰水;
②增多;
③变大。25.(5
分)
(1)Zn
+
H2SO4
==
ZnSO4
+
H2↑
(2)65/2
==
X
/
0.4g
(3)32.2g
(4)80%
(5)201:49
(
自信来自于实力,实力来自于努力
)
(
第
1
页
共
2
页
)
26.(5
分)
(1)Hg
(2)2Al
+
3CuSO4
3Cu
+
Al2(SO4)3
(4)
①铁片插入硝酸银和硝酸铜混合溶液中,铁片先与硝酸银溶液发生反应;
②Cu(NO3)2
和
Zn(NO3)2
;
③Ag、Cu、Zn
。
同课章节目录
