云南省元谋县高中2020-2021学年高一下学期末考试化学试题(Word版含答案)
文档属性
| 名称 | 云南省元谋县高中2020-2021学年高一下学期末考试化学试题(Word版含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-08 00:00:00 | ||
图片预览




文档简介
元谋县高中2020-2021学年高一下学期末考试
化学试卷
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答题前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
3.回答第II卷时,将答案写在答题卡上,写在本试卷上无效。
可能用到的相对原子质量:H
1
C
12
O
16
S
32
Cl
35.5
Na
23
Mg
24
Al
27
第Ⅰ卷
(选择题
共40分)
一、选择题:本大题共20小题,每小题2分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.为了“蓝天工程”的实施,许多公交车的燃料都作了调整,现有公交车上标有“CNG(压缩天然气)”标志,说明其燃料主要成分是(
)
A.煤油
B.乙醇
C.甲烷
D.汽油
2.下列叙述中正确的是(
)
A.医用酒精的浓度通常为95%
B.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
C.淀粉、纤维素和油脂都属于天然高分子化合物
D.合成纤维和光导纤维都是新型无机非金属材料
3.下列物质不能用作食品添加剂的是(
)
A.柠檬黄
B.山梨酸钾
C.硫酸锌
D.三聚氰胺
4.下列有关燃料的说法错误的是(
)
A.化石燃料完全燃烧不会造成大气污染
B.以液化石油气代替燃油可减少大气污染
C.燃料燃烧产物CO2是温室气体之一
D.燃料不完全燃烧排放的CO是大气污染物之一
5.化学与生活密切相关。下列说法错误的是(
)
A.疫苗一般应冷藏存放,以避免蛋白质变性
B.绿色化学要求从源头上消除或减少生产活动对环境的污染
C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
6.探究乙醇性质的实验中,下列描述正确的是(
)
A.金属钠沉在乙醇液面之下,熔化成小球,剧烈反应
B.向乙醇的水溶液滴入几滴酚酞,溶液变红色
C.将灼烧的铜丝伸入乙醇中,铜丝溶解,生成刺激性物质
D.向乙醇中滴加酸性KMnO4溶液,紫红色褪去
7.如图为实验室制取乙酸乙酯的装置。下列关于该实验的叙述中,不正确的是(
)
A.b试管中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
B.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
C.实验时加热a试管的目的是及时将乙酸乙酯蒸出并加快反应速率
D.b试管中饱和Na2CO3溶液的作用是除去随乙酸乙酯蒸出的少量乙酸和乙醇,降低乙酸乙酯在溶液中的溶解度
8.一定温度下,在2
L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是(
)
A.t
min时该反应达到化学平衡状态
B.反应开始到10
min,用X表示的反应速率为0.079
mol·L?1·min?1
C.反应开始到10
min时,Y的转化率为79%
D.反应的化学方程式为X(g)+2Y(g)
??3Z(g)
9.枸橼酸其结构简式为
,下列物质中不能与枸橼酸反应的是(
)
A.乙酸
B.乙醇
C.碳酸钠溶液
D.溴水
10.下列实验过程中,始终无明显现象的是
A.SO2通入Ba(NO3)2溶液中
B.NO2通入FeSO4溶液中
C.CO2通入CaCl2溶液中
D.NH3通入AlCl3溶液中
11.我国科学家屠呦呦因研究治疗疟疾的药物青蒿素,2015年10月获得诺贝尔生理医学奖。其结构简式如图所示,下列有关青蒿素叙述正确的是(
)
A.青蒿素的化学式为C15H21O5
B.青蒿素结构中含有酯基
C.青蒿素与乙酸互为同系物
D.青蒿素属于芳香烃
12.宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。下列说法错误的是(
)
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱
D.Cu(OH)2·2CuCO3与焦炭一起加热可以生成Cu
13.某有机物的结构简式为HO-CH2CH=CHCH2-COOH,下列关于该有机化合物的说法不正确的是(
)
A.可与氢气发生加成反应
B.能与乙酸发生酯化反应
C.能使酸性高锰酸钾溶液褪色
D.不能与金属钠反应
14.下列各组中的物质均能发生加成反应的是(
)
A.乙烯和乙醇
B.丙烯和氯乙烯
C.乙酸和溴乙烷
D.丙烯和丙烷
15.实验室制备下列气体方法可行的是(
)
选项
气体
方法
A.
氨气
加热氯化铵固体
B.
二氧化氮
将铝片加到冷浓硝酸中
C.
硫化氢
向硫化钠固体滴加浓硫酸
D.
氧气
加热氯酸钾和二氧化锰的混合物
16.下列说法错误的是(
)
A.乙烷室温下能与浓盐酸发生取代反应
B.乙烯可以用作生产食品包装材料的原料
C.用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
D.乙酸与甲酸甲酯(C2H4O2)互为同分异构体
17.海水开发利用的部分过程如图所示。下列说法错误的是(
)
A.向苦卤中通入Cl2是为了提取溴
B.用SO2和水吸收液通入Cl2氧化为Br2后蒸发
C.工业生产中常选用Ca(OH)2作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
18.下列由实验得出的结论正确的是(
)
实验
结论
A
将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明
生成的1,2―二溴乙烷无色、可溶于四氯化碳
B
乙醇和水都可与金属钠反应产生可燃性气体
乙醇分子中的氢与水分子中的氢具有相同的活性
C
用乙酸浸泡水壶中的水垢,可将其清除
乙酸的酸性小于碳酸的酸性
D
甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红
生成的氯甲烷具有酸性
19.如图所示的氢氧燃料电池,下列有关该电池的说法错误的(
)
A.b电极是正极
B.电子由b电极经过灯泡流向a电极
C.电池总反应式为O2
+
2H2
==
2H2O
D.氢氧燃料电池能量转化率可以达到80%以上
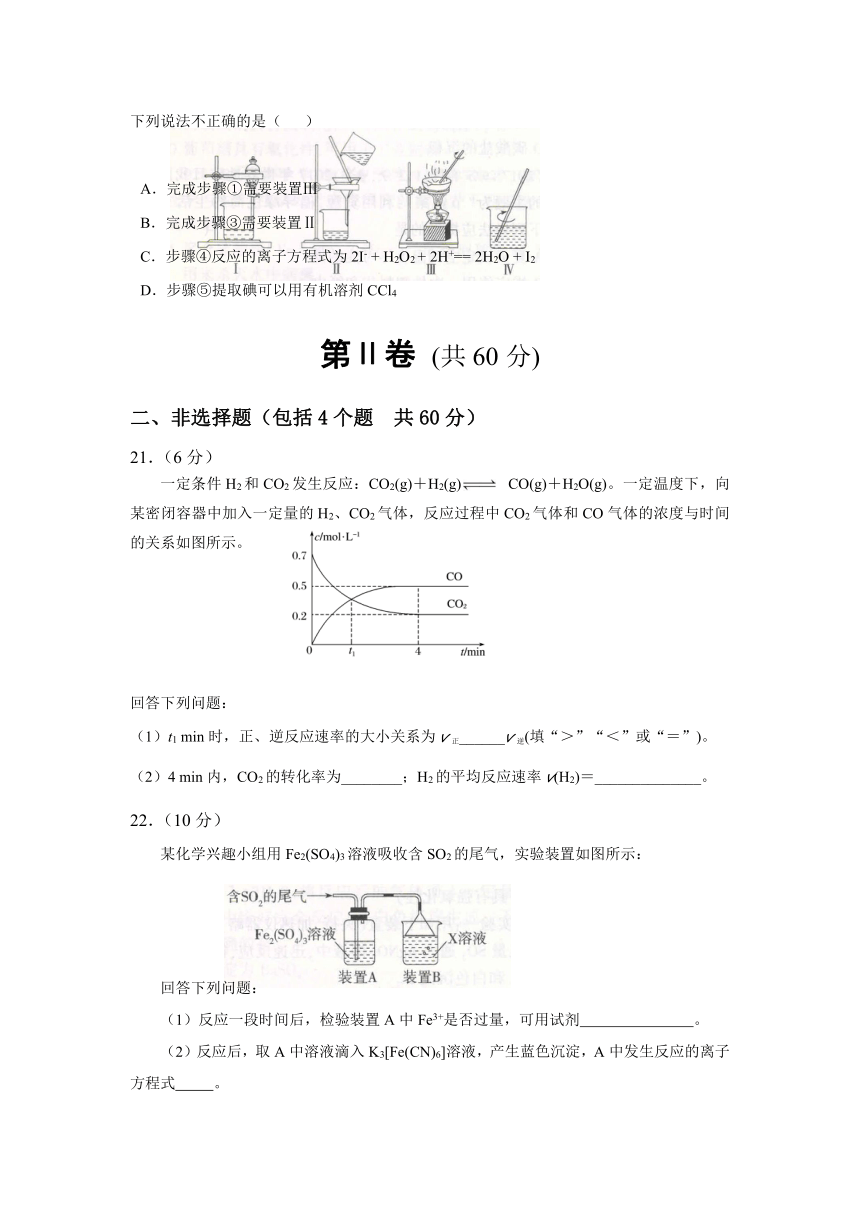
20.海带中含有碘元素,实验室从海带中提取碘的部分流程如图:
下列说法不正确的是(
)
A.完成步骤①需要装置Ⅲ
B.完成步骤③需要装置Ⅱ
C.步骤④反应的离子方程式为2I-
+
H2O2
+
2H+==
2H2O
+
I2
D.步骤⑤提取碘可以用有机溶剂CCl4
第Ⅱ卷
(共60分)
二、非选择题(包括4个题
共60分)
21.(6分)
一定条件H2和CO2发生反应:CO2(g)+H2(g)
CO(g)+H2O(g)。一定温度下,向某密闭容器中加入一定量的H2、CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
回答下列问题:
(1)t1
min时,正、逆反应速率的大小关系为v正______v逆(填“>”“<”或“=”)。
(2)4
min内,CO2的转化率为________;H2的平均反应速率v(H2)=______________。
22.(10分)
某化学兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气,实验装置如图所示:
回答下列问题:
(1)反应一段时间后,检验装置A中Fe3+是否过量,可用试剂
。
(2)反应后,取A中溶液滴入K3[Fe(CN)6]溶液,产生蓝色沉淀,A中发生反应的离子方程式
。
(3)装置B中X溶液为
,其作用是
。
(4)实验时通入标准状况下22.4
L尾气(SO2的体积分数为10%),反应后测得A中不含SO2,反应Fe3+的物质的量为0.18mol,则SO2吸收率(
)
。
23.(16分)
某实验小组用下列装置进行乙醇催化氧化的实验。
已知:乙醛的熔点:-123℃、沸点:20.8℃
回答下列问题:
(1)实验过程中铜网出现红色和黑色交替的现象,实际上是发生了两个化学反应,请写出它们的化学方程式
、
。
(2)甲和乙两个水浴作用不相同。甲的作用是
,乙的作用是
。
(3)反应进行一段时间后,试管a中收集到混合物,它们是
;集气瓶中收集到的气体的主要成分是
。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有
。要除去该物质,可先在混合液中加入________(填字母),然后再通过蒸馏即可除去。
a.
氯化钠溶液
b.
溴的四氯化碳溶液
c.
碳酸氢钠溶液
d.
酸性高锰酸钾溶液
24.(18分)
已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B是石油化学工业重要的基本原料,相对分子质量为28,有关物质的转化关系如下图所示(部分反应条件、产物省略)。
回答下列问题:
(1)工业上,由石油获得B的方法称为
。
(2)A中含有的官能团的名称为
;H的化学名称为
。
(3)B到A的反应类型为
;A到E的反应类型为
。
(4)C的分子式为
;F的结构简式为
。
(5)由A生成G的化学方程式为
。
(6)A与D反应生成E的化学方程式为
。
25.(10分)
硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的过程如下:
回答下列问题:
(1)为提高硫酸“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有
(写出两条)。
(2)MgCO3溶于稀硫酸的离子方程式是
。
(3)“氧化”步骤中,加入H2O2溶液的目的是___________(用离子方程式表示)。
(4)部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子
Mg2+
Fe2+
Fe3+
开始沉淀
9.1
7.6
1.9
完全沉淀
11.1
9.7
3.2
“沉淀”除杂步骤中,用氨水调节溶液pH的范围是___________。
(5)“过滤”所得滤液中含有的阳离子是___________。
元谋县高中2020-2021学年高一下学期末考试
化学答案
第Ⅰ卷(选择题
共40分)
1、C
2、B
3、D
4、A
5、C
6、D
7、B
8、C
9、D
10、C
11、B
12、C
13、D
14、B
15、D
16、A
17、B
18、A
19、B
20、A
第Ⅱ卷
(选择题
共60分)
21.(6分,每空2分)
(1)
>
(2)71.4%
0.125
mol·L?1·min?1
22.(10分,每空2分)
(1)KSCN溶液
(2)2Fe3++SO2
+2H2O==
2Fe2++
SO42?
+
4H+
(3)NaOH溶液
吸收SO2,防止污染环境
(4)90%
23.(16分,每空2分)
(1)2Cu
+O2
2CuO
CH3CH2OH
+
CuO
CH3CHO
+
H2O
+
Cu
(2)加热,使乙醇汽化
冷凝,使乙醛液化
(3)2Na2O2
+2H2O==
4NaOH
+
O2↑
(
2H2O22H2O+O2↑
)
生成砖红色物质(沉淀)
(4)乙酸
c
24.(18分,每空2分)
(1)裂化、裂解
(2)羟基
CH2ClCH2CH3、CH3CHClCH3
(3)
加成反应
酯化反应(取代反应)
(4)C3H6O
(5)nCH2
=
CHCH3
CH3CH2COOH
+
CH3CH2CH2OH
CH3CH2COOCH2CH2CH3
25.(10分,每空2分)
(1)将矿石粉碎、适当升高温度
(2)MgCO3
+
2H+==Mg2++CO2↑
+
H2O
(3)2Fe2++H2O2
+
2H+
==
2Fe3++2H2O
(4)3.2~9.1
(5)Mg2+
、NH4+
化学试卷
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答题前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
3.回答第II卷时,将答案写在答题卡上,写在本试卷上无效。
可能用到的相对原子质量:H
1
C
12
O
16
S
32
Cl
35.5
Na
23
Mg
24
Al
27
第Ⅰ卷
(选择题
共40分)
一、选择题:本大题共20小题,每小题2分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.为了“蓝天工程”的实施,许多公交车的燃料都作了调整,现有公交车上标有“CNG(压缩天然气)”标志,说明其燃料主要成分是(
)
A.煤油
B.乙醇
C.甲烷
D.汽油
2.下列叙述中正确的是(
)
A.医用酒精的浓度通常为95%
B.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
C.淀粉、纤维素和油脂都属于天然高分子化合物
D.合成纤维和光导纤维都是新型无机非金属材料
3.下列物质不能用作食品添加剂的是(
)
A.柠檬黄
B.山梨酸钾
C.硫酸锌
D.三聚氰胺
4.下列有关燃料的说法错误的是(
)
A.化石燃料完全燃烧不会造成大气污染
B.以液化石油气代替燃油可减少大气污染
C.燃料燃烧产物CO2是温室气体之一
D.燃料不完全燃烧排放的CO是大气污染物之一
5.化学与生活密切相关。下列说法错误的是(
)
A.疫苗一般应冷藏存放,以避免蛋白质变性
B.绿色化学要求从源头上消除或减少生产活动对环境的污染
C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
6.探究乙醇性质的实验中,下列描述正确的是(
)
A.金属钠沉在乙醇液面之下,熔化成小球,剧烈反应
B.向乙醇的水溶液滴入几滴酚酞,溶液变红色
C.将灼烧的铜丝伸入乙醇中,铜丝溶解,生成刺激性物质
D.向乙醇中滴加酸性KMnO4溶液,紫红色褪去
7.如图为实验室制取乙酸乙酯的装置。下列关于该实验的叙述中,不正确的是(
)
A.b试管中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
B.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
C.实验时加热a试管的目的是及时将乙酸乙酯蒸出并加快反应速率
D.b试管中饱和Na2CO3溶液的作用是除去随乙酸乙酯蒸出的少量乙酸和乙醇,降低乙酸乙酯在溶液中的溶解度
8.一定温度下,在2
L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是(
)
A.t
min时该反应达到化学平衡状态
B.反应开始到10
min,用X表示的反应速率为0.079
mol·L?1·min?1
C.反应开始到10
min时,Y的转化率为79%
D.反应的化学方程式为X(g)+2Y(g)
??3Z(g)
9.枸橼酸其结构简式为
,下列物质中不能与枸橼酸反应的是(
)
A.乙酸
B.乙醇
C.碳酸钠溶液
D.溴水
10.下列实验过程中,始终无明显现象的是
A.SO2通入Ba(NO3)2溶液中
B.NO2通入FeSO4溶液中
C.CO2通入CaCl2溶液中
D.NH3通入AlCl3溶液中
11.我国科学家屠呦呦因研究治疗疟疾的药物青蒿素,2015年10月获得诺贝尔生理医学奖。其结构简式如图所示,下列有关青蒿素叙述正确的是(
)
A.青蒿素的化学式为C15H21O5
B.青蒿素结构中含有酯基
C.青蒿素与乙酸互为同系物
D.青蒿素属于芳香烃
12.宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。下列说法错误的是(
)
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱
D.Cu(OH)2·2CuCO3与焦炭一起加热可以生成Cu
13.某有机物的结构简式为HO-CH2CH=CHCH2-COOH,下列关于该有机化合物的说法不正确的是(
)
A.可与氢气发生加成反应
B.能与乙酸发生酯化反应
C.能使酸性高锰酸钾溶液褪色
D.不能与金属钠反应
14.下列各组中的物质均能发生加成反应的是(
)
A.乙烯和乙醇
B.丙烯和氯乙烯
C.乙酸和溴乙烷
D.丙烯和丙烷
15.实验室制备下列气体方法可行的是(
)
选项
气体
方法
A.
氨气
加热氯化铵固体
B.
二氧化氮
将铝片加到冷浓硝酸中
C.
硫化氢
向硫化钠固体滴加浓硫酸
D.
氧气
加热氯酸钾和二氧化锰的混合物
16.下列说法错误的是(
)
A.乙烷室温下能与浓盐酸发生取代反应
B.乙烯可以用作生产食品包装材料的原料
C.用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
D.乙酸与甲酸甲酯(C2H4O2)互为同分异构体
17.海水开发利用的部分过程如图所示。下列说法错误的是(
)
A.向苦卤中通入Cl2是为了提取溴
B.用SO2和水吸收液通入Cl2氧化为Br2后蒸发
C.工业生产中常选用Ca(OH)2作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
18.下列由实验得出的结论正确的是(
)
实验
结论
A
将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明
生成的1,2―二溴乙烷无色、可溶于四氯化碳
B
乙醇和水都可与金属钠反应产生可燃性气体
乙醇分子中的氢与水分子中的氢具有相同的活性
C
用乙酸浸泡水壶中的水垢,可将其清除
乙酸的酸性小于碳酸的酸性
D
甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红
生成的氯甲烷具有酸性
19.如图所示的氢氧燃料电池,下列有关该电池的说法错误的(
)
A.b电极是正极
B.电子由b电极经过灯泡流向a电极
C.电池总反应式为O2
+
2H2
==
2H2O
D.氢氧燃料电池能量转化率可以达到80%以上
20.海带中含有碘元素,实验室从海带中提取碘的部分流程如图:
下列说法不正确的是(
)
A.完成步骤①需要装置Ⅲ
B.完成步骤③需要装置Ⅱ
C.步骤④反应的离子方程式为2I-
+
H2O2
+
2H+==
2H2O
+
I2
D.步骤⑤提取碘可以用有机溶剂CCl4
第Ⅱ卷
(共60分)
二、非选择题(包括4个题
共60分)
21.(6分)
一定条件H2和CO2发生反应:CO2(g)+H2(g)
CO(g)+H2O(g)。一定温度下,向某密闭容器中加入一定量的H2、CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
回答下列问题:
(1)t1
min时,正、逆反应速率的大小关系为v正______v逆(填“>”“<”或“=”)。
(2)4
min内,CO2的转化率为________;H2的平均反应速率v(H2)=______________。
22.(10分)
某化学兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气,实验装置如图所示:
回答下列问题:
(1)反应一段时间后,检验装置A中Fe3+是否过量,可用试剂
。
(2)反应后,取A中溶液滴入K3[Fe(CN)6]溶液,产生蓝色沉淀,A中发生反应的离子方程式
。
(3)装置B中X溶液为
,其作用是
。
(4)实验时通入标准状况下22.4
L尾气(SO2的体积分数为10%),反应后测得A中不含SO2,反应Fe3+的物质的量为0.18mol,则SO2吸收率(
)
。
23.(16分)
某实验小组用下列装置进行乙醇催化氧化的实验。
已知:乙醛的熔点:-123℃、沸点:20.8℃
回答下列问题:
(1)实验过程中铜网出现红色和黑色交替的现象,实际上是发生了两个化学反应,请写出它们的化学方程式
、
。
(2)甲和乙两个水浴作用不相同。甲的作用是
,乙的作用是
。
(3)反应进行一段时间后,试管a中收集到混合物,它们是
;集气瓶中收集到的气体的主要成分是
。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有
。要除去该物质,可先在混合液中加入________(填字母),然后再通过蒸馏即可除去。
a.
氯化钠溶液
b.
溴的四氯化碳溶液
c.
碳酸氢钠溶液
d.
酸性高锰酸钾溶液
24.(18分)
已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B是石油化学工业重要的基本原料,相对分子质量为28,有关物质的转化关系如下图所示(部分反应条件、产物省略)。
回答下列问题:
(1)工业上,由石油获得B的方法称为
。
(2)A中含有的官能团的名称为
;H的化学名称为
。
(3)B到A的反应类型为
;A到E的反应类型为
。
(4)C的分子式为
;F的结构简式为
。
(5)由A生成G的化学方程式为
。
(6)A与D反应生成E的化学方程式为
。
25.(10分)
硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的过程如下:
回答下列问题:
(1)为提高硫酸“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有
(写出两条)。
(2)MgCO3溶于稀硫酸的离子方程式是
。
(3)“氧化”步骤中,加入H2O2溶液的目的是___________(用离子方程式表示)。
(4)部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子
Mg2+
Fe2+
Fe3+
开始沉淀
9.1
7.6
1.9
完全沉淀
11.1
9.7
3.2
“沉淀”除杂步骤中,用氨水调节溶液pH的范围是___________。
(5)“过滤”所得滤液中含有的阳离子是___________。
元谋县高中2020-2021学年高一下学期末考试
化学答案
第Ⅰ卷(选择题
共40分)
1、C
2、B
3、D
4、A
5、C
6、D
7、B
8、C
9、D
10、C
11、B
12、C
13、D
14、B
15、D
16、A
17、B
18、A
19、B
20、A
第Ⅱ卷
(选择题
共60分)
21.(6分,每空2分)
(1)
>
(2)71.4%
0.125
mol·L?1·min?1
22.(10分,每空2分)
(1)KSCN溶液
(2)2Fe3++SO2
+2H2O==
2Fe2++
SO42?
+
4H+
(3)NaOH溶液
吸收SO2,防止污染环境
(4)90%
23.(16分,每空2分)
(1)2Cu
+O2
2CuO
CH3CH2OH
+
CuO
CH3CHO
+
H2O
+
Cu
(2)加热,使乙醇汽化
冷凝,使乙醛液化
(3)2Na2O2
+2H2O==
4NaOH
+
O2↑
(
2H2O22H2O+O2↑
)
生成砖红色物质(沉淀)
(4)乙酸
c
24.(18分,每空2分)
(1)裂化、裂解
(2)羟基
CH2ClCH2CH3、CH3CHClCH3
(3)
加成反应
酯化反应(取代反应)
(4)C3H6O
(5)nCH2
=
CHCH3
CH3CH2COOH
+
CH3CH2CH2OH
CH3CH2COOCH2CH2CH3
25.(10分,每空2分)
(1)将矿石粉碎、适当升高温度
(2)MgCO3
+
2H+==Mg2++CO2↑
+
H2O
(3)2Fe2++H2O2
+
2H+
==
2Fe3++2H2O
(4)3.2~9.1
(5)Mg2+
、NH4+
同课章节目录
