2.3.1实验室制取氧气的原理 分解反应(课件39页)
文档属性
| 名称 | 2.3.1实验室制取氧气的原理 分解反应(课件39页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-09 00:00:00 | ||
图片预览








文档简介
(共41张PPT)
九上
化学
第1课时 实验室制取氧气的原理 分解反应
第二单元
我们周围的空气
化学用语天天练
新知学习
学完本课你应该知道
新课导入
解析
化学用语天天练
化学用语
天天听写
1.
写出下列物质的化学符号。
氧气
红磷
五氧化二磷
二氧化碳
2.
写出红磷在氧气中燃烧的符号表达式。
________________________________
[答案]
解析
化学用语天天练
文字描述
精准表达
3.
请用准确的语言表述下列问题的答案。
(1)
如何验证一瓶无色气体是氧气?
[答案]
将带火星的木条伸入集气瓶中,若木条复燃,则证明该气体为氧气。
(2)
铁丝在氧气中燃烧的现象是什么?集气瓶底放入少量的水或细沙的作用是什么?
[答案]
现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固体。作用:防止生成的高温熔融物溅落,使集气瓶底炸裂。
解析
新课导入
解析
知识点一 氧气的实验室制取原理
新知学习
排水
复燃
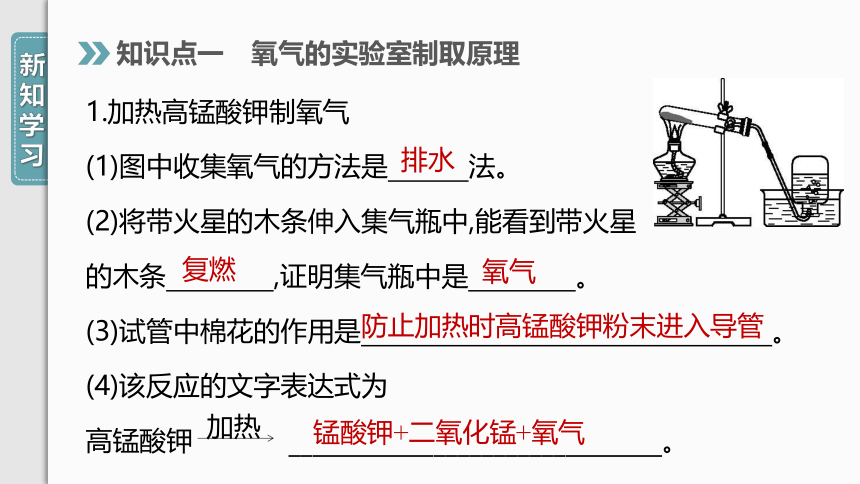
1.加热高锰酸钾制氧气
(1)图中收集氧气的方法是 法。
(2)将带火星的木条伸入集气瓶中,能看到带火星
的木条 ,证明集气瓶中是 。?
(3)试管中棉花的作用是? 。?
(4)该反应的文字表达式为
高锰酸钾
?_______________________________。
氧气
防止加热时高锰酸钾粉末进入导管
锰酸钾+二氧化锰+氧气
加热
解析
新知学习
2.分解过氧化氢制氧气
该反应的文字表达式为
过氧化氢
____________
3.加热氯酸钾制氧气
该反应的文字表达式为
氯酸钾
_________________
水+氧气
氯化钾+氧气
二氧化锰
二氧化锰
加热
解析
新知学习
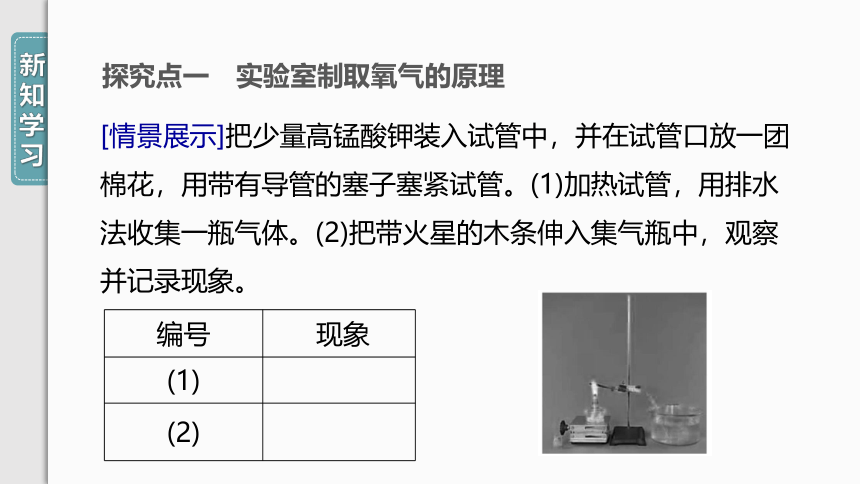
探究点一 实验室制取氧气的原理
[情景展示]把少量高锰酸钾装入试管中,并在试管口放一团棉花,用带有导管的塞子塞紧试管。(1)加热试管,用排水法收集一瓶气体。(2)把带火星的木条伸入集气瓶中,观察并记录现象。
编号
现象
(1)
(2)
解析
新知学习
[问题探究]通过哪些现象可以证明加热高锰酸钾产生了氧气?反应的文字表达式怎样书写?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]伸入集气瓶中的带火星的木条复燃,可证明加热高锰酸钾产生了氧气,反应的文字表达式为:
高锰酸钾
锰酸钾+二氧化锰+氧气
[课堂速记]
______________________________________________________________________________________________________________________________
加热
解析
新知学习
[情景展示2]
观察实验:(1)在试管中加入5
mL
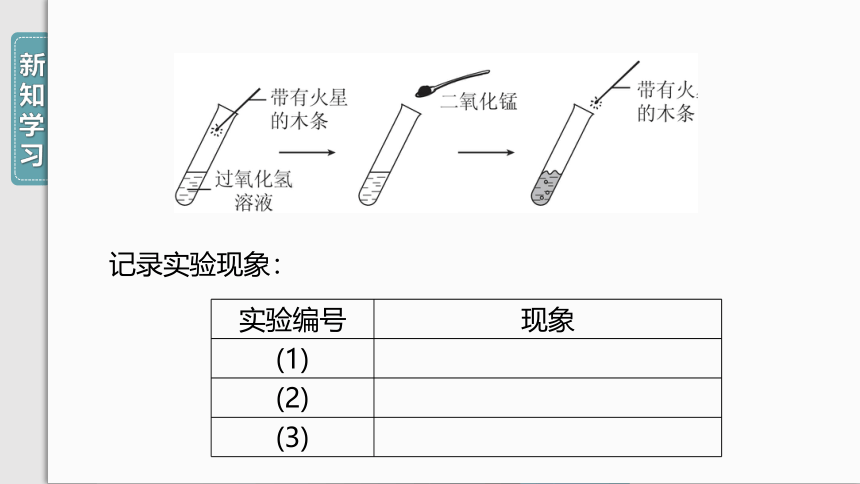
5%的过氧化氢溶液,把带火星的木条伸入试管。(2)向上述试管中加入少量二氧化锰,把带火星的木条伸入试管。(3)待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管。待上述试管中又没有现象发生时,再重复上述操作。
解析
新知学习
记录实验现象:
实验编号
现象
(1)
(2)
(3)
解析
新知学习
[问题探究]过氧化氢能否产生氧气?二氧化锰在反应中起到了什么作用?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]过氧化氢溶液在常温下分解缓慢,产生的氧气较少,加入二氧化锰后,能加快过氧化氢产生氧气的速率,是反应的催化剂。该反应的文字表达式为:过氧化氢
水+氧气
[继续探究]什么是催化剂?怎样理解催化剂的概念?
[思考交流]
__________________________________________________________________________________________________________________
二氧化锰
解析
新知学习
[归纳提升]在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有发生变化的物质叫作催化剂。催化剂在化学反应中所起的作用叫催化作用。理解催化剂的概念应注意几点:①“改变”的含义:有的催化剂可以加快反应的速率,有的催化剂可以减慢反应的速率;②一种物质可能是多个反应的催化剂,一个化学反应也可能有多种催化剂;③催化剂只能改变化学反应的速率,不能改变生成物的质量。
解析
新知学习
[继续探究]如何设计实验证明某物质是否是某反应的催化剂?
[思考交流]
________________________________________________________________________________________________________________________
解析
新知学习
[归纳提升]证明一种物质是否是催化剂的实验探究步骤:
①探究该物质是否真正改变了化学反应速率(通过对比实验证明);②探究在化学反应中该物质的质量是否改变。(在反应前、后分别对该物质进行一次称量);③探究在化学反应前后该物质的化学性质是否改变(利用该物质的化学性质证明,或将分离出来的该物质再次加入到反应中,看是否还能改变反应的速率)。
解析
新知学习
[课堂速记]
_______________________________________________________
_______________________________________________________
解析
新知学习
[情景展示3]
实验室中还可以用加热混有二氧化锰的氯酸钾固体制取氧气,反应可表示为:氯酸钾
二氧化锰加热氯化钾+氧气
二氧化锰
加热
解析
新知学习
[问题探究]三种制取氧气的方法中哪种最好?如何评价实验原理的优劣?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]用分解过氧化氢(通常加入二氧化锰)的方法最好,因为反应不需要加热且操作方便。评价反应原理的优劣标准:一般从原理是否正确、操作是否简单安全、是否节能环保、反应速率是否适中以及是否造价低廉等方面考虑。
[课堂速记]
________________________________________________________________________________________________________________________
解析
新知学习
核心应用
核心一 实验室制取氧气的原理
例1
过去教材中实验室制氧气,常用氯酸钾与二氧化锰混合加热制取,从预热到收集满一瓶
氧气大约需
,曾有同学去闻自己收集到的氧气,想找找吸氧的感觉,结果却闻到刺激性气味(少量氯酸钾发生副反应
生成有毒的氯气)。现在教材已改用过
氧化氢溶液和二氧化锰混合制取氧气。
两套实验装置如图所示。
解析
新知学习
(1)
写出两个反应的文字表达式:_________________________________;________________________________。这两个反应的基本反应类型为____________。
分解反应
(2)
从反应物和实验装置的角度比较,使用过氧化氢和二氧化锰制取氧气的优点是_________________________________;______________________________________。
常温反应,不需加热(或操作简便)
制得的氧气纯净或无污染(合理即可)
解析
新知学习
方法点拨
评价实验室制取氧气原理优劣的标准:
原料含氧,能产生氧气
KMnO4
KClO3
H2O2
KMnO4
H2O2
反应速率适中
制得的气体纯净
操作简便、安全
KMnO4
H2O2
H2O2
解析
知识点二 分解过氧化氢制氧气的反应中二氧化锰的作用
新知学习
1.探究实验
实验现象:实验(1)中带火星的木条
__________,(2)中带火星的木条
________。反应前后二氧化锰的质量
不减少;将二氧化锰分离出来,再加到过氧化氢溶液中,仍能加速过氧化氢的分解。
不复燃
复燃
解析
新知学习
实验结论:二氧化锰能________(填“加快”或“减慢”)过氧化氢的分解速率,但其________和化学性质在反应前后没有改变。
加快
质量
解析
新知学习
2.催化剂的概念
在化学反应里能________其他物质的化学反应速率,而本身的________和____________在反应前后都没有发生变化的物质叫作催化剂。
改变
质量
化学性质
解析
新知学习
核心应用
例2
科学探究是学习化学的重要途径,请你一起参与实验探究,并完成下列空白。
[发现问题]
小科用过氧化氢溶液清洗伤口时,不小心把几滴过氧化氢溶液滴到水泥地面上,发现有大量气泡产生。小科联想到实验室用二氧化锰作过氧化氢分解的催化剂,他想水泥块是否可以作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水清洗干净、干燥后,进行了如下实验:
核心二 催化剂的探究
解析
新知学习
[实验验证]
步骤
现象
结论
实
验
一
________________________________________________________________???
木条
不复燃
常温下过氧化氢溶液分解速率很慢
实
验
二
在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中
木条
复燃
水泥块能?_______
过氧化氢的分解速率
将带火星的木条伸入装有过氧化氢溶液的试管中
加快
[猜想]
水泥块能作过氧化氢分解的催化剂。
解析
新知学习
[结论]
水泥块能作过氧化氢分解的催化剂。
[讨论反思]
同学小丽认为:仅凭上述两个实验还不能证明水泥块是过氧化氢分解的催化剂,她觉得应该补做一个探究实验:①准确称量水泥块的质量;②完成实验二;③待不再产生气泡后,将试管中的物质进行过滤、洗涤、________、称量;④对比反应前后水泥块的质量。
干燥
解析
新知学习
[分析]
如果水泥块的质量在反应前后________(填“变大”
“变小”或“不变”),则说明水泥块可以作过氧化氢分解的催化剂。
小华认为,要证明小科的猜想,小丽的补充实验还是不够,还需要再补充一个探究实验:探究_______________________________________________________。
不变
水泥块的化学性质在化学反应前后有无变化
解析
新知学习
方法点拨
催化剂的探究思路:
实验步骤
示例
1.设计对照实验证明该物质能改变反应速率
2.证明该物质的质量在化学反应前后不变
3.证明该物质的化学性质在化学反应前后不变
在两支试管中分别加入5
mL3%的过氧化氢溶液,然后在一支试管中加入0.5
g二氧化锰
将试管中的二氧化锰分离出来,洗涤、烘干,称量,质量仍为0.5
g
在3%的过氧化氢溶液中加入分离出来的二氧化锰,依然能加快过氧化氢的分解速率
解析
知识点三 分解反应
新知学习
由________反应物生成____________________其他物质的反应,叫作分解反应。
一种
两种或两种以上
解析
新知学习
探究点二 分解反应
[情景展示]
氢气+氧气
水
水
氢气+氧气
点燃
通电
解析
新知学习
[问题探究]观察上述两个反应有何不同?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]化合反应的特点是“多变一”,分解反应的特点是“一变多”。
[课堂速记]
__________________________________________________________________________________________________________________________________________________________________________________________________
解析
新知学习
沸点
氮气
知识点四 氧气的工业制法
1.原理:利用氮气和氧气的________不同。
2.方法:分离液态空气,先蒸发出来的是________。
[注意]
工业上制取氧气的过程发生的是物理变化。
学完本课你应该知道
制取氧气
催化剂
分解反应
“一变,两不变”
过氧化氢
水+氧气
氯酸钾
氯化钾+氧气
二氧化锰
高锰酸钾
锰酸钾+二氧化锰+氧气
加热
检验:将带火星的木条伸入瓶内,木条复燃,证明是氧气
二氧化锰
加热
谢
谢
观
看!
https://www.21cnjy.com/help/help_extract.php
九上
化学
第1课时 实验室制取氧气的原理 分解反应
第二单元
我们周围的空气
化学用语天天练
新知学习
学完本课你应该知道
新课导入
解析
化学用语天天练
化学用语
天天听写
1.
写出下列物质的化学符号。
氧气
红磷
五氧化二磷
二氧化碳
2.
写出红磷在氧气中燃烧的符号表达式。
________________________________
[答案]
解析
化学用语天天练
文字描述
精准表达
3.
请用准确的语言表述下列问题的答案。
(1)
如何验证一瓶无色气体是氧气?
[答案]
将带火星的木条伸入集气瓶中,若木条复燃,则证明该气体为氧气。
(2)
铁丝在氧气中燃烧的现象是什么?集气瓶底放入少量的水或细沙的作用是什么?
[答案]
现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固体。作用:防止生成的高温熔融物溅落,使集气瓶底炸裂。
解析
新课导入
解析
知识点一 氧气的实验室制取原理
新知学习
排水
复燃
1.加热高锰酸钾制氧气
(1)图中收集氧气的方法是 法。
(2)将带火星的木条伸入集气瓶中,能看到带火星
的木条 ,证明集气瓶中是 。?
(3)试管中棉花的作用是? 。?
(4)该反应的文字表达式为
高锰酸钾
?_______________________________。
氧气
防止加热时高锰酸钾粉末进入导管
锰酸钾+二氧化锰+氧气
加热
解析
新知学习
2.分解过氧化氢制氧气
该反应的文字表达式为
过氧化氢
____________
3.加热氯酸钾制氧气
该反应的文字表达式为
氯酸钾
_________________
水+氧气
氯化钾+氧气
二氧化锰
二氧化锰
加热
解析
新知学习
探究点一 实验室制取氧气的原理
[情景展示]把少量高锰酸钾装入试管中,并在试管口放一团棉花,用带有导管的塞子塞紧试管。(1)加热试管,用排水法收集一瓶气体。(2)把带火星的木条伸入集气瓶中,观察并记录现象。
编号
现象
(1)
(2)
解析
新知学习
[问题探究]通过哪些现象可以证明加热高锰酸钾产生了氧气?反应的文字表达式怎样书写?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]伸入集气瓶中的带火星的木条复燃,可证明加热高锰酸钾产生了氧气,反应的文字表达式为:
高锰酸钾
锰酸钾+二氧化锰+氧气
[课堂速记]
______________________________________________________________________________________________________________________________
加热
解析
新知学习
[情景展示2]
观察实验:(1)在试管中加入5
mL
5%的过氧化氢溶液,把带火星的木条伸入试管。(2)向上述试管中加入少量二氧化锰,把带火星的木条伸入试管。(3)待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管。待上述试管中又没有现象发生时,再重复上述操作。
解析
新知学习
记录实验现象:
实验编号
现象
(1)
(2)
(3)
解析
新知学习
[问题探究]过氧化氢能否产生氧气?二氧化锰在反应中起到了什么作用?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]过氧化氢溶液在常温下分解缓慢,产生的氧气较少,加入二氧化锰后,能加快过氧化氢产生氧气的速率,是反应的催化剂。该反应的文字表达式为:过氧化氢
水+氧气
[继续探究]什么是催化剂?怎样理解催化剂的概念?
[思考交流]
__________________________________________________________________________________________________________________
二氧化锰
解析
新知学习
[归纳提升]在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有发生变化的物质叫作催化剂。催化剂在化学反应中所起的作用叫催化作用。理解催化剂的概念应注意几点:①“改变”的含义:有的催化剂可以加快反应的速率,有的催化剂可以减慢反应的速率;②一种物质可能是多个反应的催化剂,一个化学反应也可能有多种催化剂;③催化剂只能改变化学反应的速率,不能改变生成物的质量。
解析
新知学习
[继续探究]如何设计实验证明某物质是否是某反应的催化剂?
[思考交流]
________________________________________________________________________________________________________________________
解析
新知学习
[归纳提升]证明一种物质是否是催化剂的实验探究步骤:
①探究该物质是否真正改变了化学反应速率(通过对比实验证明);②探究在化学反应中该物质的质量是否改变。(在反应前、后分别对该物质进行一次称量);③探究在化学反应前后该物质的化学性质是否改变(利用该物质的化学性质证明,或将分离出来的该物质再次加入到反应中,看是否还能改变反应的速率)。
解析
新知学习
[课堂速记]
_______________________________________________________
_______________________________________________________
解析
新知学习
[情景展示3]
实验室中还可以用加热混有二氧化锰的氯酸钾固体制取氧气,反应可表示为:氯酸钾
二氧化锰加热氯化钾+氧气
二氧化锰
加热
解析
新知学习
[问题探究]三种制取氧气的方法中哪种最好?如何评价实验原理的优劣?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]用分解过氧化氢(通常加入二氧化锰)的方法最好,因为反应不需要加热且操作方便。评价反应原理的优劣标准:一般从原理是否正确、操作是否简单安全、是否节能环保、反应速率是否适中以及是否造价低廉等方面考虑。
[课堂速记]
________________________________________________________________________________________________________________________
解析
新知学习
核心应用
核心一 实验室制取氧气的原理
例1
过去教材中实验室制氧气,常用氯酸钾与二氧化锰混合加热制取,从预热到收集满一瓶
氧气大约需
,曾有同学去闻自己收集到的氧气,想找找吸氧的感觉,结果却闻到刺激性气味(少量氯酸钾发生副反应
生成有毒的氯气)。现在教材已改用过
氧化氢溶液和二氧化锰混合制取氧气。
两套实验装置如图所示。
解析
新知学习
(1)
写出两个反应的文字表达式:_________________________________;________________________________。这两个反应的基本反应类型为____________。
分解反应
(2)
从反应物和实验装置的角度比较,使用过氧化氢和二氧化锰制取氧气的优点是_________________________________;______________________________________。
常温反应,不需加热(或操作简便)
制得的氧气纯净或无污染(合理即可)
解析
新知学习
方法点拨
评价实验室制取氧气原理优劣的标准:
原料含氧,能产生氧气
KMnO4
KClO3
H2O2
KMnO4
H2O2
反应速率适中
制得的气体纯净
操作简便、安全
KMnO4
H2O2
H2O2
解析
知识点二 分解过氧化氢制氧气的反应中二氧化锰的作用
新知学习
1.探究实验
实验现象:实验(1)中带火星的木条
__________,(2)中带火星的木条
________。反应前后二氧化锰的质量
不减少;将二氧化锰分离出来,再加到过氧化氢溶液中,仍能加速过氧化氢的分解。
不复燃
复燃
解析
新知学习
实验结论:二氧化锰能________(填“加快”或“减慢”)过氧化氢的分解速率,但其________和化学性质在反应前后没有改变。
加快
质量
解析
新知学习
2.催化剂的概念
在化学反应里能________其他物质的化学反应速率,而本身的________和____________在反应前后都没有发生变化的物质叫作催化剂。
改变
质量
化学性质
解析
新知学习
核心应用
例2
科学探究是学习化学的重要途径,请你一起参与实验探究,并完成下列空白。
[发现问题]
小科用过氧化氢溶液清洗伤口时,不小心把几滴过氧化氢溶液滴到水泥地面上,发现有大量气泡产生。小科联想到实验室用二氧化锰作过氧化氢分解的催化剂,他想水泥块是否可以作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水清洗干净、干燥后,进行了如下实验:
核心二 催化剂的探究
解析
新知学习
[实验验证]
步骤
现象
结论
实
验
一
________________________________________________________________???
木条
不复燃
常温下过氧化氢溶液分解速率很慢
实
验
二
在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中
木条
复燃
水泥块能?_______
过氧化氢的分解速率
将带火星的木条伸入装有过氧化氢溶液的试管中
加快
[猜想]
水泥块能作过氧化氢分解的催化剂。
解析
新知学习
[结论]
水泥块能作过氧化氢分解的催化剂。
[讨论反思]
同学小丽认为:仅凭上述两个实验还不能证明水泥块是过氧化氢分解的催化剂,她觉得应该补做一个探究实验:①准确称量水泥块的质量;②完成实验二;③待不再产生气泡后,将试管中的物质进行过滤、洗涤、________、称量;④对比反应前后水泥块的质量。
干燥
解析
新知学习
[分析]
如果水泥块的质量在反应前后________(填“变大”
“变小”或“不变”),则说明水泥块可以作过氧化氢分解的催化剂。
小华认为,要证明小科的猜想,小丽的补充实验还是不够,还需要再补充一个探究实验:探究_______________________________________________________。
不变
水泥块的化学性质在化学反应前后有无变化
解析
新知学习
方法点拨
催化剂的探究思路:
实验步骤
示例
1.设计对照实验证明该物质能改变反应速率
2.证明该物质的质量在化学反应前后不变
3.证明该物质的化学性质在化学反应前后不变
在两支试管中分别加入5
mL3%的过氧化氢溶液,然后在一支试管中加入0.5
g二氧化锰
将试管中的二氧化锰分离出来,洗涤、烘干,称量,质量仍为0.5
g
在3%的过氧化氢溶液中加入分离出来的二氧化锰,依然能加快过氧化氢的分解速率
解析
知识点三 分解反应
新知学习
由________反应物生成____________________其他物质的反应,叫作分解反应。
一种
两种或两种以上
解析
新知学习
探究点二 分解反应
[情景展示]
氢气+氧气
水
水
氢气+氧气
点燃
通电
解析
新知学习
[问题探究]观察上述两个反应有何不同?
[思考交流]
_____________________________________
解析
新知学习
[归纳提升]化合反应的特点是“多变一”,分解反应的特点是“一变多”。
[课堂速记]
__________________________________________________________________________________________________________________________________________________________________________________________________
解析
新知学习
沸点
氮气
知识点四 氧气的工业制法
1.原理:利用氮气和氧气的________不同。
2.方法:分离液态空气,先蒸发出来的是________。
[注意]
工业上制取氧气的过程发生的是物理变化。
学完本课你应该知道
制取氧气
催化剂
分解反应
“一变,两不变”
过氧化氢
水+氧气
氯酸钾
氯化钾+氧气
二氧化锰
高锰酸钾
锰酸钾+二氧化锰+氧气
加热
检验:将带火星的木条伸入瓶内,木条复燃,证明是氧气
二氧化锰
加热
谢
谢
观
看!
https://www.21cnjy.com/help/help_extract.php
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
