【重难点突破】浙教版8年级上册科学 第6讲 溶液的计算与分析(含答案)
文档属性
| 名称 | 【重难点突破】浙教版8年级上册科学 第6讲 溶液的计算与分析(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-09-15 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
【重难点突破】浙教版8年级上册科学
第6讲
溶液的计算与分析
一、饱和溶液和不饱和溶液
概念:在一定温度下,在一定量的溶剂里不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液;还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。
在描述饱和溶液和不饱和溶液的时候,一定要强调:
①
一定温度
;②
一定量的溶剂
;③
某种溶质
。
二、浓溶液和稀溶液
人们常把溶有较多溶质的溶液称为浓溶液,溶有较少溶质的溶液称为稀溶液。
三、溶解度——物质溶解能力的定量表示方法
概念:在一定温度下,某(固体)物质在100克溶剂里达到饱和状态时所溶解的质量为该物质在这种溶剂里的溶解度。溶解度数值越大,表明该温度下,物质的溶解能力越强。如20℃时食盐的溶解度是36克,就表示在20℃时,100
克水中最多能溶解食盐36克。
溶解性等级的划分:
溶解性等级的划分依据:室温
(
20℃
)时的溶解度。
等级的划分。
四、有关溶液稀释问题的计算:
溶液稀释就是往浓溶液中加入溶剂或加入低浓度的较稀溶液变成稀溶液的过程。
溶液稀释问题的特点是:稀释前后溶液中溶质的质量保持不变,即:
浓溶液的质量×浓溶液中的溶质质量分数=稀溶液的质量×稀溶液中溶质的质量分数
由于液体称量比较麻烦,而用量筒量取体积比较方便,所以计算时有时会涉及到溶液的体积,这时要通过密度来进行换算。(ρ=m/V)
由于分子之间存在一定的间隔,所以两种不同液体混合溶解时,一般来说体积不能简单相加,因为混合后体积小于混合前两种液体体积之和。
五、有关溶液的浓缩问题的计算:
溶液的浓缩问题思考方法可以与稀释问题一样来考虑。溶液增浓的方法一般可以:加入溶质、蒸发溶剂、加入较高浓度的浓溶液。
加入溶质增浓的计算:
增浓后的溶质质量分数=
×100%
两种浓度的同种溶质的溶液混合后,所得的溶液中溶质的质量分数一定大于小浓度,小于大浓度的质量分数的值。
混合后溶质的质量分数=
×100%
六、配制一定溶质的质量分数的溶液:(以配制50克10%的氯化钠溶液为例)
实验步骤如下(主要是前3步):
计算:按配制要求计算所需的溶质和溶剂的量。
所需的氯化钠质量:50克×10%=5克
所需溶剂水的质量:50克-5克=45克,水的体积:V=m/ρ=45克/1克.cm-3=45ml
称量(或量取):用天平称取氯化钠5克,用量筒量取45ml的水。
溶解:将溶质和溶剂混合,搅拌至溶质全部溶解。
转移:将配制好的溶液移到指定容器内,贴上标签。
一、溶液的性质与分析
1.(2021·瓯海模拟)如图是对某固体物质的溶液在一定条件下进行恒温蒸发操作的实验过程,下列关于该过程中溶液的分析正确的是(
???)
A.?甲→乙的过程中,溶液的溶质质量分数不变
B.?乙→丙的过程中,溶液的溶质质量分数一定变小
C.?乙→丙的过程中,溶液的溶质质量分数可能不变
D.?甲→丙的过程中,溶液的质量减少了20克
2.(2019·杭州模拟)向盛有50克硝酸钾的烧杯中加入50克水,充分溶解后现象如图所示,此时溶液温度为30℃。下列说法正确的是(
??)
A.?烧杯中的溶液总质量为100克,溶液的溶质质量分数为50%
B.?烧杯中的溶液为30℃时硝酸钾饱和溶液,且30℃时硝酸钾的溶解度为硝酸钾100克
C.?若使烧杯中的固体全部溶解,则溶液的溶质质量分数一定增大
D.?若使烧杯中的溶液变为不饱和溶液,则溶液的溶质质量分数可能增大
3.(2020·温州模拟)无土栽培技术是植物根能直接接触培养液的栽培方法,小明在炎热的夏天从冰箱拿出一瓶硝酸钾培养液如图A,一段时间后变成了图C。下列说法不正确的是(???
)
A.?硝酸钾的溶解度随温度的升高而增大???????????B.?图C中的培养液一定是不饱和溶液
C.?图A中的培养液一定是饱和溶液??????????D.?可以通过升温把硝酸钾的饱和溶液转变为不饱和溶液
4.(2016九下·杭州开学考)某温度下,向一定质量的饱和石灰水中加入少量生石灰,当溶液恢复到原温度时,下列叙述正确的是(???
)
A.?溶液的碱性不变??????????????????????????????????????????????????B.?溶质的溶解度先变大后不变
C.?溶质的质量分数变大???????????????????????????????????????????D.?溶液中溶质质量不变
5.(2020·温州模拟)某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象。则下列分析正确的是(???
)
A.?甲试管中固体全部溶解,说明甲试管中的溶液为稀溶液
B.?乙试管底部有固体,说明乙试管中的液体为悬浊液
C.?此时蔗糖溶液肯定未饱和,而熟石灰溶液一定已饱和
D.?该实验现象说明该温度下蔗糖的溶解度比熟石灰大
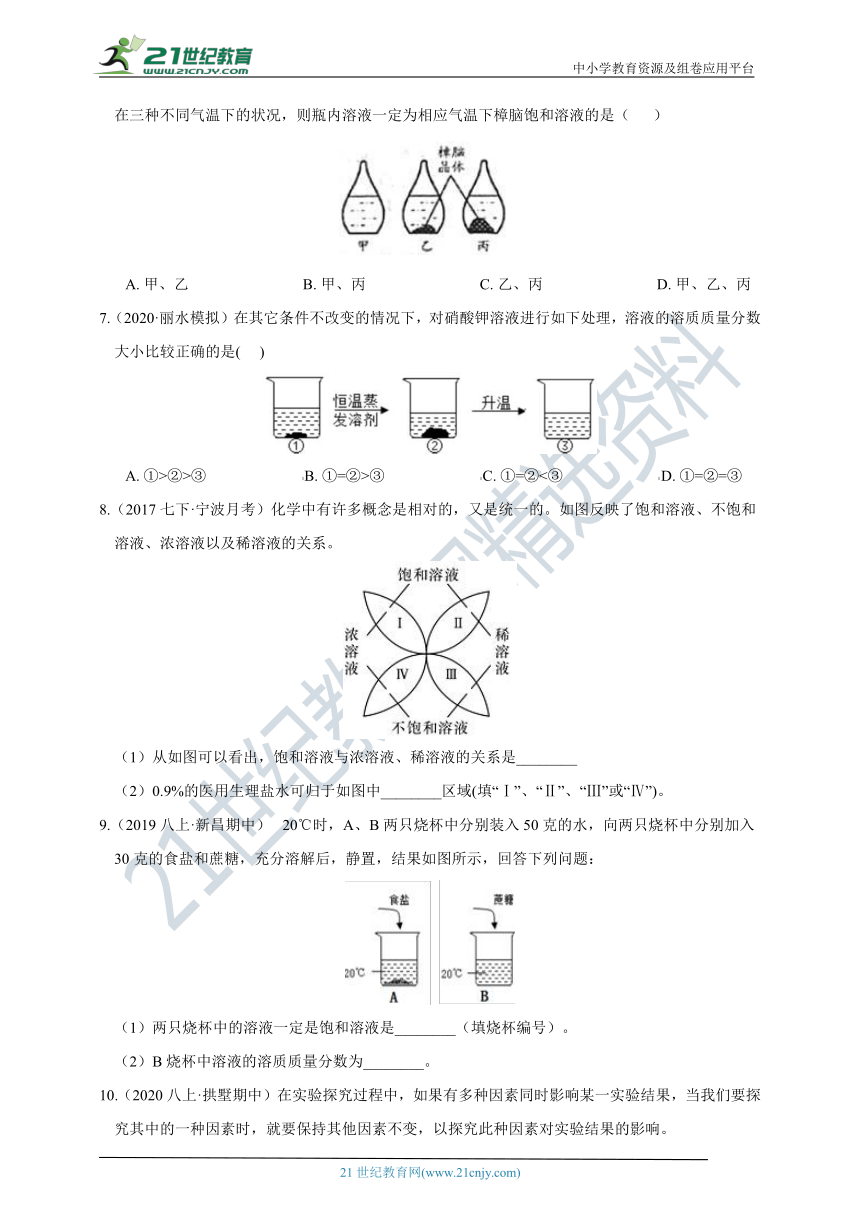
6.(2020·温州模拟)某“天气瓶"通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是(????
)
A.?甲、乙??????????????????????????????B.?甲、丙??????????????????????????????C.?乙、丙??????????????????????????????D.?甲、乙、丙
7.(2020·丽水模拟)在其它条件不改变的情况下,对硝酸钾溶液进行如下处理,溶液的溶质质量分数大小比较正确的是(???
)
A.?①>②>③?????????????????????????B.?①=②>③?????????????????????????C.?①=②<③?????????????????????????D.?①=②=③
8.(2017七下·宁波月考)化学中有许多概念是相对的,又是统一的。如图反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
(1)从如图可以看出,饱和溶液与浓溶液、稀溶液的关系是________
(2)0.9%的医用生理盐水可归于如图中________区域(填“Ⅰ”、“Ⅱ”、“Ⅲ”或“Ⅳ”)。
9.(2019八上·新昌期中)?
20℃时,A、B两只烧杯中分别装入50克的水,向两只烧杯中分别加入30克的食盐和蔗糖,充分溶解后,静置,结果如图所示,回答下列问题:
(1)两只烧杯中的溶液一定是饱和溶液是________(填烧杯编号)。
(2)B烧杯中溶液的溶质质量分数为________。
??
10.(2020八上·拱墅期中)在实验探究过程中,如果有多种因素同时影响某一实验结果,当我们要探究其中的一种因素时,就要保持其他因素不变,以探究此种因素对实验结果的影响。
[实验探究]:哪些因素影响固体物质在水中的溶解度?
因素1:溶质的种类
在实验中要改变的因素是:溶质的种类
要保持不变的因素是:温度
操作步骤:在常温下,用量筒各量取5mL蒸馏水,分别加入①、②、③三支试管中,再分别加入
氯化钠、硝酸钾、氢氧化钙各2g,振荡,观察各物质的溶解情况。
实验现象:试管①中有少量氯化钠未溶,试管②中硝酸钾全部溶解,试管③中有多量氢氧化钙
未溶。实验结论:________
因素2:温度(以硝酸钾为例)
在实验中要改变的因素是:________,要保持不变的因素是:溶质的种类(硝酸钾)
操作步骤:用量筒各量取5mL蒸馏水,分别加入①、②、③三支试管中,再分别加入5g硝酸钾晶体,将试管①保持在常温下,将试管②加热并保持在40℃,将试管③加热并保持在60℃,振荡,观察各试管中硝酸钾的溶解情况。
实验现象:试管①中有多量硝酸钾未溶,试管②中有少量硝酸钾未溶,试管③中硝酸钾全部溶解。
实验结论:在不同温度下,固体物质(硝酸钾)在水里的溶解度________(填“相等”或“不相等”)。
二、定量计算与配置溶液
11.?实验室用硝酸钾固体配制100.0g溶质质量分数为3.0%的硝酸钾溶液,下列说法正确的是( )
A.?用50mL量筒量水??????????????????????????????B.?将固体放于托盘天平的右盘称取
C.?将固体直接投入量筒中溶解??????????????D.?将配好的溶液装入贴有标签(如图)的试剂瓶中,塞好瓶塞
12.(2017·浙江竞赛)在一定温度下,某未饱和溶液蒸发掉15克水(部分)后,析出2克晶体(不含结晶水);向原溶液投入5克溶质晶体后,溶液中还剩下1克固体溶质,则此温度下该溶质的溶解度为(??
)
A.?13.3克?????????????????????????????????B.?26.7克?????????????????????????????????C.?33.3克?????????????????????????????????D.?40克
13.(2020八上·杭州月考)小孟在配置食盐水时,记录实验数据如下表:则下列叙述正确的是(??
)
实验序号
水的质量(g)
加入食盐的质量(g)
溶液的质量(g)
①
10
2
12
②
10
3
13
③
10
4
13.6
④
10
5
13.6
A.?①所得溶液的溶质质量分数为20%??????????????????????B.?②中所得溶液是不饱和溶液
C.?实验中10g水最多能溶解4g食盐?????????????????????????D.?溶质质量分数大小关系为④>③>②>①
14.(2019·杭州模拟)如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,阅读后填空:
(1)写出稀释该硫酸的正确操作方法________。
(2)欲配制92克溶质质量分数为19.6%的稀硫酸,需要这种硫酸________毫升。
15.(2020·瑞安模拟)t1℃时,将质量均为35克的氯化钾和硝酸钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图所示(t1℃时,硝酸钾的溶解度小于氯化钾的溶解度)。
(1)据图分析烧杯A中溶解的溶质为________;
(2)将t1℃时烧杯B中的溶液稀释成10%的溶液,需加水________克。
16.(2019八上·新昌期末)如图是配制50克质量分数为5%的氯化钠溶液的操作过程示意图
(1)B操作,在称量中发现指针偏向右边,接下来的操作是________;
(2)E操作中玻璃棒的作用是________。
(3)如果配制过程中出现以下情况,可能导致所配溶液的溶质质量分数偏大的是????
。
A.所用氯化钠药品不纯
B.量取水时俯视读数
C.配完后将溶液转移至试剂瓶时洒出了一些
D.将量好的水从量筒里倒入烧杯时,酒出一些水
17.注射用链霉素试验针的药液配制方法如下:
①把1.0克链霉素溶于水制成4.0毫升溶液A;
②取0.1毫升溶液A加水稀释至1.0毫升得溶液B;
③取0.1毫升溶液B加水稀释至1.0毫升得溶液C;
④取0.1毫升溶液C加水稀释至1.0毫升得溶液D。
由于在整个过程中药液很稀,其密度都可近似看作1克/厘米3
,
试求:
(1)溶液A中溶质质量分数为________;
(2)溶液D中溶质质量分数为________;
(3)1.0克链霉素可配制________克试验针药液(溶液D)。
18.(2018八上·温岭期中)用下列实验操作可分别完成“实验一:提纯粗盐并测定纯度”和“实验二:配制50克溶质的质量分数为10%的氯化钠水溶液”两个实验。
(1)请按需将实验一中“提纯粗盐”操作进行排序:________(填字母)。
(2)实验二中,俯视量取溶剂,溶质的质量分数会________(填“偏大”“偏小”或“不变”)。
(3)表一中:粗盐提纯正确说法有________。(填序号,可多选。)
表一
序号
粗盐提纯说法
1
D中玻璃棒的作用是加速溶解
2
E中滤液浑浊的原因一定是滤纸破裂
3
D中所获食盐比理论低的原因可能是食盐没有充分溶解
4
A中称量结晶出的食盐时,先把食盐放在左盘,后在右盘加减砝码
19.(2019八上·嘉兴期末)秋冬季是诺如病毒性腹泻的高发季节,脱水严重的病人应及时输液或口服补液。下表是某口服补液标签上的部分信息。
名称
x×口服补液
规格
共5克:其中含氯化钠0.6克,氯化钾0.3克,枸椽酸钠0.7克,无水葡萄糖3.4克
用法用量
临用前,将一袋溶解于245克水中,随时口服
一袋该口服补液全部溶解于245克水中,所得溶液的质量为________克,所得溶液中氯化钠的质量分数是多少________?
20.(2020八上·拱墅期中)某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示.他从瓶中倒出200毫升用于配制稀硫酸.求:
浓硫酸(H2SO4)500毫升
溶质的质量分数
98%
密度
1.84克/厘米3
强腐蚀性,阴冷,密封储藏
(1)这200毫升浓硫酸的质量是多少克,其中含溶质硫酸多少克.
(2)欲配制1000毫升(密度为1.14克/厘米3)质量分数为19.6%的稀硫酸,需要这种浓硫酸和水各多少毫升?
21.(2018八上·杭州期末)预防
H7N9
病毒最有效的预防方法之一就是用消毒液对禽类养殖、销售、宰杀、加工场所进行消毒。二氧化氯消毒液是国际上公认的新一代强力、安全、高效的消毒剂,它能够迅速、彻底杀灭各种细菌和病毒。二氧化氯消毒液瓶上的标签如下表。
(1)1000
毫升该二氧化氯消毒液的质量是________克;
(2)欲配制
30
千克质量分数为
20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少千克水?(写出计算过程)
22.(2017八上·杭州月考)某温度时,在
100g
水中最多能溶硝酸钾
25g,现有该温度下
500g
硝酸钾溶液,加热蒸发掉
300g
水以后,冷却到原温度下,发现有
50g
硝酸钾晶体析出,请计算:
(1)蒸发并冷却到原温度后,溶液中有多少克硝酸钾?此时溶液中硝酸钾的质量分数是多少?
(2)蒸发前的溶液中,硝酸钾的质量分数是多少?
答案解析部分
一、溶液的性质与分析
1.【答案】
C
2.【答案】
D
3.【答案】
B
4.【答案】
A
5.【答案】
D
6.【答案】
C
7.【答案】
C
8.【答案】
(1)饱和溶液可以是浓溶液,也可以是稀溶液(2)Ⅲ
9.【答案】
(1)A(2)37.5%
10.【答案】
在温度保持不变的情况下,不同种类固体物质在水里的溶解度不相等或在温度保持不变时,溶质种类影响固体物质在水中的溶解度;温度;不相等
二、定量计算与配置溶液
11.【答案】
D
12.【答案】
D
13.【答案】
B
14.【答案】
(1)将浓硫酸沿器壁缓慢注入水中,并用玻璃棒不断搅拌(2)10
15.【答案】
(1)硝酸钾(2)215
16.【答案】
(1)继续向左盘加药品直到天平平衡(2)搅拌,加快食盐的溶解(3)B,D
17.【答案】
(1)25%(2)0.025%(3)4000
18.【答案】
(1)BED(2)偏大(3)3、4
19.【答案】
250g;0.24%
20.【答案】
(1)200ml浓硫酸的质量为:m=ρV=1.84g/cm3×200cm3=368g;
200ml浓硫酸的溶质质量为:368g×98%=360.64g;
(2)设需浓硫酸质量为m,?
?
?
m×98%=1000cm3×1.14g/cm3×19.6%;
解得:m=228g。
这种浓硫酸的体积:;
需水质量:1140g-228g=912g;
需要加水的体积:。
21.【答案】
(1)1200(2)7.5
千克;22.5
千克
22.【答案】
(1)30g;
20%(2)16%
原溶质质量+加入的溶质质量
原溶液质量+加入的溶质质量
溶液甲的溶质质量+溶液乙的溶质质量
溶液甲的质量+溶液乙的质量
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
【重难点突破】浙教版8年级上册科学
第6讲
溶液的计算与分析
一、饱和溶液和不饱和溶液
概念:在一定温度下,在一定量的溶剂里不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液;还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。
在描述饱和溶液和不饱和溶液的时候,一定要强调:
①
一定温度
;②
一定量的溶剂
;③
某种溶质
。
二、浓溶液和稀溶液
人们常把溶有较多溶质的溶液称为浓溶液,溶有较少溶质的溶液称为稀溶液。
三、溶解度——物质溶解能力的定量表示方法
概念:在一定温度下,某(固体)物质在100克溶剂里达到饱和状态时所溶解的质量为该物质在这种溶剂里的溶解度。溶解度数值越大,表明该温度下,物质的溶解能力越强。如20℃时食盐的溶解度是36克,就表示在20℃时,100
克水中最多能溶解食盐36克。
溶解性等级的划分:
溶解性等级的划分依据:室温
(
20℃
)时的溶解度。
等级的划分。
四、有关溶液稀释问题的计算:
溶液稀释就是往浓溶液中加入溶剂或加入低浓度的较稀溶液变成稀溶液的过程。
溶液稀释问题的特点是:稀释前后溶液中溶质的质量保持不变,即:
浓溶液的质量×浓溶液中的溶质质量分数=稀溶液的质量×稀溶液中溶质的质量分数
由于液体称量比较麻烦,而用量筒量取体积比较方便,所以计算时有时会涉及到溶液的体积,这时要通过密度来进行换算。(ρ=m/V)
由于分子之间存在一定的间隔,所以两种不同液体混合溶解时,一般来说体积不能简单相加,因为混合后体积小于混合前两种液体体积之和。
五、有关溶液的浓缩问题的计算:
溶液的浓缩问题思考方法可以与稀释问题一样来考虑。溶液增浓的方法一般可以:加入溶质、蒸发溶剂、加入较高浓度的浓溶液。
加入溶质增浓的计算:
增浓后的溶质质量分数=
×100%
两种浓度的同种溶质的溶液混合后,所得的溶液中溶质的质量分数一定大于小浓度,小于大浓度的质量分数的值。
混合后溶质的质量分数=
×100%
六、配制一定溶质的质量分数的溶液:(以配制50克10%的氯化钠溶液为例)
实验步骤如下(主要是前3步):
计算:按配制要求计算所需的溶质和溶剂的量。
所需的氯化钠质量:50克×10%=5克
所需溶剂水的质量:50克-5克=45克,水的体积:V=m/ρ=45克/1克.cm-3=45ml
称量(或量取):用天平称取氯化钠5克,用量筒量取45ml的水。
溶解:将溶质和溶剂混合,搅拌至溶质全部溶解。
转移:将配制好的溶液移到指定容器内,贴上标签。
一、溶液的性质与分析
1.(2021·瓯海模拟)如图是对某固体物质的溶液在一定条件下进行恒温蒸发操作的实验过程,下列关于该过程中溶液的分析正确的是(
???)
A.?甲→乙的过程中,溶液的溶质质量分数不变
B.?乙→丙的过程中,溶液的溶质质量分数一定变小
C.?乙→丙的过程中,溶液的溶质质量分数可能不变
D.?甲→丙的过程中,溶液的质量减少了20克
2.(2019·杭州模拟)向盛有50克硝酸钾的烧杯中加入50克水,充分溶解后现象如图所示,此时溶液温度为30℃。下列说法正确的是(
??)
A.?烧杯中的溶液总质量为100克,溶液的溶质质量分数为50%
B.?烧杯中的溶液为30℃时硝酸钾饱和溶液,且30℃时硝酸钾的溶解度为硝酸钾100克
C.?若使烧杯中的固体全部溶解,则溶液的溶质质量分数一定增大
D.?若使烧杯中的溶液变为不饱和溶液,则溶液的溶质质量分数可能增大
3.(2020·温州模拟)无土栽培技术是植物根能直接接触培养液的栽培方法,小明在炎热的夏天从冰箱拿出一瓶硝酸钾培养液如图A,一段时间后变成了图C。下列说法不正确的是(???
)
A.?硝酸钾的溶解度随温度的升高而增大???????????B.?图C中的培养液一定是不饱和溶液
C.?图A中的培养液一定是饱和溶液??????????D.?可以通过升温把硝酸钾的饱和溶液转变为不饱和溶液
4.(2016九下·杭州开学考)某温度下,向一定质量的饱和石灰水中加入少量生石灰,当溶液恢复到原温度时,下列叙述正确的是(???
)
A.?溶液的碱性不变??????????????????????????????????????????????????B.?溶质的溶解度先变大后不变
C.?溶质的质量分数变大???????????????????????????????????????????D.?溶液中溶质质量不变
5.(2020·温州模拟)某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象。则下列分析正确的是(???
)
A.?甲试管中固体全部溶解,说明甲试管中的溶液为稀溶液
B.?乙试管底部有固体,说明乙试管中的液体为悬浊液
C.?此时蔗糖溶液肯定未饱和,而熟石灰溶液一定已饱和
D.?该实验现象说明该温度下蔗糖的溶解度比熟石灰大
6.(2020·温州模拟)某“天气瓶"通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是(????
)
A.?甲、乙??????????????????????????????B.?甲、丙??????????????????????????????C.?乙、丙??????????????????????????????D.?甲、乙、丙
7.(2020·丽水模拟)在其它条件不改变的情况下,对硝酸钾溶液进行如下处理,溶液的溶质质量分数大小比较正确的是(???
)
A.?①>②>③?????????????????????????B.?①=②>③?????????????????????????C.?①=②<③?????????????????????????D.?①=②=③
8.(2017七下·宁波月考)化学中有许多概念是相对的,又是统一的。如图反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
(1)从如图可以看出,饱和溶液与浓溶液、稀溶液的关系是________
(2)0.9%的医用生理盐水可归于如图中________区域(填“Ⅰ”、“Ⅱ”、“Ⅲ”或“Ⅳ”)。
9.(2019八上·新昌期中)?
20℃时,A、B两只烧杯中分别装入50克的水,向两只烧杯中分别加入30克的食盐和蔗糖,充分溶解后,静置,结果如图所示,回答下列问题:
(1)两只烧杯中的溶液一定是饱和溶液是________(填烧杯编号)。
(2)B烧杯中溶液的溶质质量分数为________。
??
10.(2020八上·拱墅期中)在实验探究过程中,如果有多种因素同时影响某一实验结果,当我们要探究其中的一种因素时,就要保持其他因素不变,以探究此种因素对实验结果的影响。
[实验探究]:哪些因素影响固体物质在水中的溶解度?
因素1:溶质的种类
在实验中要改变的因素是:溶质的种类
要保持不变的因素是:温度
操作步骤:在常温下,用量筒各量取5mL蒸馏水,分别加入①、②、③三支试管中,再分别加入
氯化钠、硝酸钾、氢氧化钙各2g,振荡,观察各物质的溶解情况。
实验现象:试管①中有少量氯化钠未溶,试管②中硝酸钾全部溶解,试管③中有多量氢氧化钙
未溶。实验结论:________
因素2:温度(以硝酸钾为例)
在实验中要改变的因素是:________,要保持不变的因素是:溶质的种类(硝酸钾)
操作步骤:用量筒各量取5mL蒸馏水,分别加入①、②、③三支试管中,再分别加入5g硝酸钾晶体,将试管①保持在常温下,将试管②加热并保持在40℃,将试管③加热并保持在60℃,振荡,观察各试管中硝酸钾的溶解情况。
实验现象:试管①中有多量硝酸钾未溶,试管②中有少量硝酸钾未溶,试管③中硝酸钾全部溶解。
实验结论:在不同温度下,固体物质(硝酸钾)在水里的溶解度________(填“相等”或“不相等”)。
二、定量计算与配置溶液
11.?实验室用硝酸钾固体配制100.0g溶质质量分数为3.0%的硝酸钾溶液,下列说法正确的是( )
A.?用50mL量筒量水??????????????????????????????B.?将固体放于托盘天平的右盘称取
C.?将固体直接投入量筒中溶解??????????????D.?将配好的溶液装入贴有标签(如图)的试剂瓶中,塞好瓶塞
12.(2017·浙江竞赛)在一定温度下,某未饱和溶液蒸发掉15克水(部分)后,析出2克晶体(不含结晶水);向原溶液投入5克溶质晶体后,溶液中还剩下1克固体溶质,则此温度下该溶质的溶解度为(??
)
A.?13.3克?????????????????????????????????B.?26.7克?????????????????????????????????C.?33.3克?????????????????????????????????D.?40克
13.(2020八上·杭州月考)小孟在配置食盐水时,记录实验数据如下表:则下列叙述正确的是(??
)
实验序号
水的质量(g)
加入食盐的质量(g)
溶液的质量(g)
①
10
2
12
②
10
3
13
③
10
4
13.6
④
10
5
13.6
A.?①所得溶液的溶质质量分数为20%??????????????????????B.?②中所得溶液是不饱和溶液
C.?实验中10g水最多能溶解4g食盐?????????????????????????D.?溶质质量分数大小关系为④>③>②>①
14.(2019·杭州模拟)如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,阅读后填空:
(1)写出稀释该硫酸的正确操作方法________。
(2)欲配制92克溶质质量分数为19.6%的稀硫酸,需要这种硫酸________毫升。
15.(2020·瑞安模拟)t1℃时,将质量均为35克的氯化钾和硝酸钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图所示(t1℃时,硝酸钾的溶解度小于氯化钾的溶解度)。
(1)据图分析烧杯A中溶解的溶质为________;
(2)将t1℃时烧杯B中的溶液稀释成10%的溶液,需加水________克。
16.(2019八上·新昌期末)如图是配制50克质量分数为5%的氯化钠溶液的操作过程示意图
(1)B操作,在称量中发现指针偏向右边,接下来的操作是________;
(2)E操作中玻璃棒的作用是________。
(3)如果配制过程中出现以下情况,可能导致所配溶液的溶质质量分数偏大的是????
。
A.所用氯化钠药品不纯
B.量取水时俯视读数
C.配完后将溶液转移至试剂瓶时洒出了一些
D.将量好的水从量筒里倒入烧杯时,酒出一些水
17.注射用链霉素试验针的药液配制方法如下:
①把1.0克链霉素溶于水制成4.0毫升溶液A;
②取0.1毫升溶液A加水稀释至1.0毫升得溶液B;
③取0.1毫升溶液B加水稀释至1.0毫升得溶液C;
④取0.1毫升溶液C加水稀释至1.0毫升得溶液D。
由于在整个过程中药液很稀,其密度都可近似看作1克/厘米3
,
试求:
(1)溶液A中溶质质量分数为________;
(2)溶液D中溶质质量分数为________;
(3)1.0克链霉素可配制________克试验针药液(溶液D)。
18.(2018八上·温岭期中)用下列实验操作可分别完成“实验一:提纯粗盐并测定纯度”和“实验二:配制50克溶质的质量分数为10%的氯化钠水溶液”两个实验。
(1)请按需将实验一中“提纯粗盐”操作进行排序:________(填字母)。
(2)实验二中,俯视量取溶剂,溶质的质量分数会________(填“偏大”“偏小”或“不变”)。
(3)表一中:粗盐提纯正确说法有________。(填序号,可多选。)
表一
序号
粗盐提纯说法
1
D中玻璃棒的作用是加速溶解
2
E中滤液浑浊的原因一定是滤纸破裂
3
D中所获食盐比理论低的原因可能是食盐没有充分溶解
4
A中称量结晶出的食盐时,先把食盐放在左盘,后在右盘加减砝码
19.(2019八上·嘉兴期末)秋冬季是诺如病毒性腹泻的高发季节,脱水严重的病人应及时输液或口服补液。下表是某口服补液标签上的部分信息。
名称
x×口服补液
规格
共5克:其中含氯化钠0.6克,氯化钾0.3克,枸椽酸钠0.7克,无水葡萄糖3.4克
用法用量
临用前,将一袋溶解于245克水中,随时口服
一袋该口服补液全部溶解于245克水中,所得溶液的质量为________克,所得溶液中氯化钠的质量分数是多少________?
20.(2020八上·拱墅期中)某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示.他从瓶中倒出200毫升用于配制稀硫酸.求:
浓硫酸(H2SO4)500毫升
溶质的质量分数
98%
密度
1.84克/厘米3
强腐蚀性,阴冷,密封储藏
(1)这200毫升浓硫酸的质量是多少克,其中含溶质硫酸多少克.
(2)欲配制1000毫升(密度为1.14克/厘米3)质量分数为19.6%的稀硫酸,需要这种浓硫酸和水各多少毫升?
21.(2018八上·杭州期末)预防
H7N9
病毒最有效的预防方法之一就是用消毒液对禽类养殖、销售、宰杀、加工场所进行消毒。二氧化氯消毒液是国际上公认的新一代强力、安全、高效的消毒剂,它能够迅速、彻底杀灭各种细菌和病毒。二氧化氯消毒液瓶上的标签如下表。
(1)1000
毫升该二氧化氯消毒液的质量是________克;
(2)欲配制
30
千克质量分数为
20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少千克水?(写出计算过程)
22.(2017八上·杭州月考)某温度时,在
100g
水中最多能溶硝酸钾
25g,现有该温度下
500g
硝酸钾溶液,加热蒸发掉
300g
水以后,冷却到原温度下,发现有
50g
硝酸钾晶体析出,请计算:
(1)蒸发并冷却到原温度后,溶液中有多少克硝酸钾?此时溶液中硝酸钾的质量分数是多少?
(2)蒸发前的溶液中,硝酸钾的质量分数是多少?
答案解析部分
一、溶液的性质与分析
1.【答案】
C
2.【答案】
D
3.【答案】
B
4.【答案】
A
5.【答案】
D
6.【答案】
C
7.【答案】
C
8.【答案】
(1)饱和溶液可以是浓溶液,也可以是稀溶液(2)Ⅲ
9.【答案】
(1)A(2)37.5%
10.【答案】
在温度保持不变的情况下,不同种类固体物质在水里的溶解度不相等或在温度保持不变时,溶质种类影响固体物质在水中的溶解度;温度;不相等
二、定量计算与配置溶液
11.【答案】
D
12.【答案】
D
13.【答案】
B
14.【答案】
(1)将浓硫酸沿器壁缓慢注入水中,并用玻璃棒不断搅拌(2)10
15.【答案】
(1)硝酸钾(2)215
16.【答案】
(1)继续向左盘加药品直到天平平衡(2)搅拌,加快食盐的溶解(3)B,D
17.【答案】
(1)25%(2)0.025%(3)4000
18.【答案】
(1)BED(2)偏大(3)3、4
19.【答案】
250g;0.24%
20.【答案】
(1)200ml浓硫酸的质量为:m=ρV=1.84g/cm3×200cm3=368g;
200ml浓硫酸的溶质质量为:368g×98%=360.64g;
(2)设需浓硫酸质量为m,?
?
?
m×98%=1000cm3×1.14g/cm3×19.6%;
解得:m=228g。
这种浓硫酸的体积:;
需水质量:1140g-228g=912g;
需要加水的体积:。
21.【答案】
(1)1200(2)7.5
千克;22.5
千克
22.【答案】
(1)30g;
20%(2)16%
原溶质质量+加入的溶质质量
原溶液质量+加入的溶质质量
溶液甲的溶质质量+溶液乙的溶质质量
溶液甲的质量+溶液乙的质量
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
