选修5有机化学基础第二章第一节脂肪烃1
文档属性
| 名称 | 选修5有机化学基础第二章第一节脂肪烃1 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-07-02 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
选修5《有机化学基础》
第二章 烃和卤代烃
(烷烃)
【知识与技能】
了解烷烃、烯烃和炔烃的物理性质的规律性变化
了解烷烃、烯烃、炔烃的结构特点
【教学重点】烷烃、烯烃、炔烃的结构特点和主要化学性质;乙炔的实验室制法。
【教学目标】
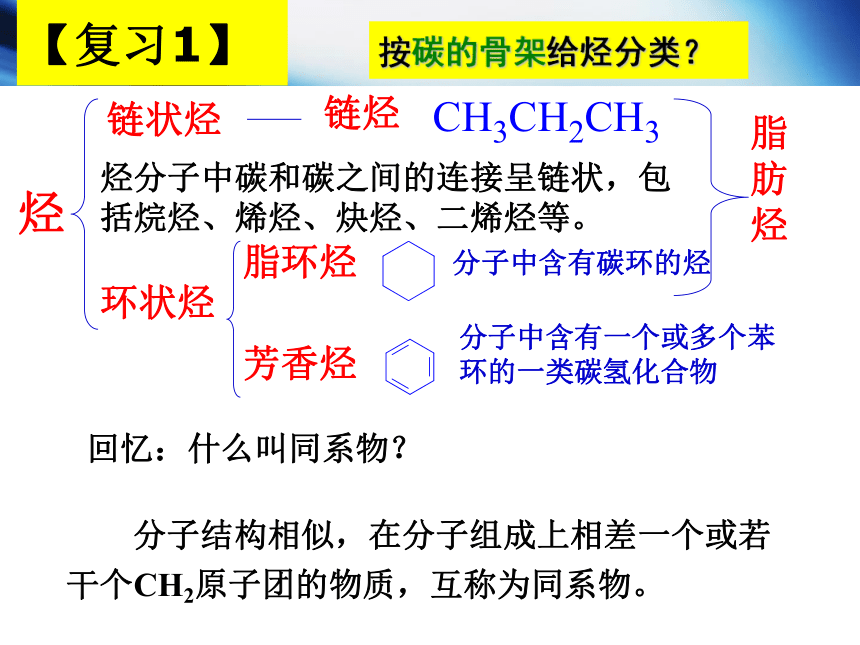
链状烃
烃分子中碳和碳之间的连接呈链状,包括烷烃、烯烃、炔烃、二烯烃等。
环状烃
脂环烃
芳香烃
分子中含有一个或多个苯环的一类碳氢化合物
链烃
脂肪烃
烃
分子中含有碳环的烃
按碳的骨架给烃分类?
【复习1】
分子结构相似,在分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。
回忆:什么叫同系物?
烃和卤代烃等有机物的反应与无机物反应相比有其特点:
(1)反应缓慢。有机分子中的原子一般以共价键结合,有机反应是分子之间的反应。
(2)反应产物复杂。有机物往往具有多个反应部位,在生成主要产物的同时,往往伴有其他副产物的生成。
(3)反应常在有机溶剂中进行。有机物一般在水中的溶解度较小,而在有机溶剂中的溶解度较大。
【复习2】
一、 烷烃、烯烃和炔烃
烯烃:分子里含有一个碳碳双键的不饱和链烃叫做烯烃。通式:CnH2n (n≥2)
(分子里含有两个双键的链烃叫做二烯烃)
烷烃:仅含C—C键和C—H键的饱和链烃,又叫烷烃。(若C—C连成环状,称为环烷烃。)通式:CnH2n+2 (n≥1)
回忆:什么叫烷烃、烯烃、炔烃?其结构有何特点?
炔烃:分子里含有碳碳三键的一类脂肪烃称为炔烃。CnH2n-2 (n≥2)
回忆:烷烃、烯烃、炔烃代表物的物性?结构?碳原子的杂化类型?
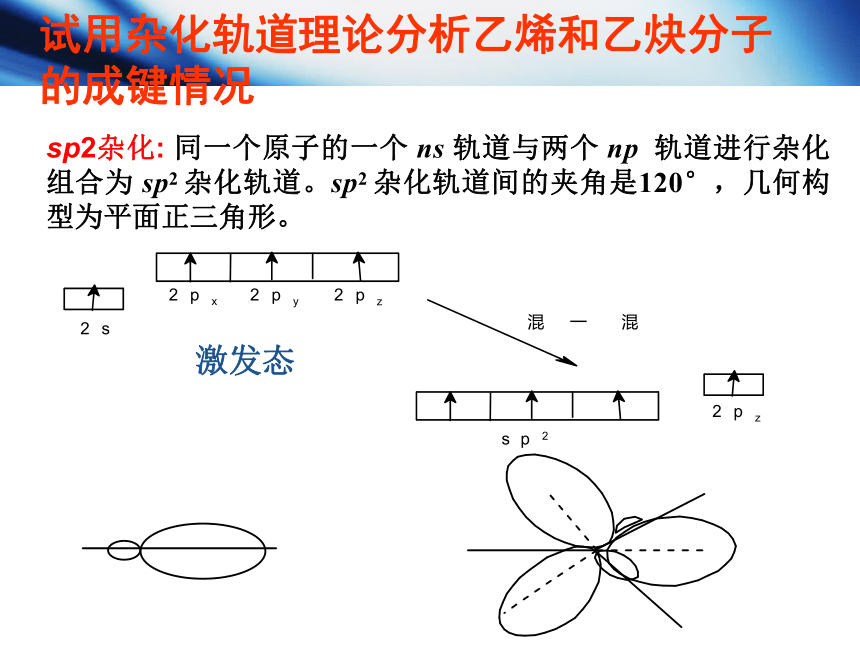
sp2杂化: 同一个原子的一个 ns 轨道与两个 np 轨道进行杂化组合为 sp2 杂化轨道。sp2 杂化轨道间的夹角是120°,几何构型为平面正三角形。
激发态
试用杂化轨道理论分析乙烯和乙炔分子的成键情况
sp杂化:一个 ns 轨道和一个np 轨道杂化组合成两个新的 sp 杂化轨道。
sp杂化轨道特点:2个sp杂化轨道在一条直线上,轨道间夹角180°
注:杂化轨道只能用于形成б键或者用来容纳未参与成键的孤对电子。
C原子在形成乙烯分子时,碳原子的2s轨道与2个2p轨道发生杂化,形成3个sp2杂化轨道,伸向平面正三角形的三个顶点。每个C原子的2个sp2杂化轨道分别与2个H原子的1s轨道形成2个相同的σ键,各自剩余的1个sp2杂化轨道相互形成一个σ键,各自没有杂化的l个2p轨道则垂直于杂化轨道所在的平面,彼此肩并肩重叠形成π键。所以,在乙烯分子中双键由一个s-sp2σ键和一个p-pπ键构成。
C原子在形成乙炔分子时发生sp杂化,两个碳原子以1个sp杂化轨道与氢原子的1s轨道结合形成σ键。各自剩余的1个sp杂化轨道相互形成1个σ键,两个碳原子的未杂化2p轨道分别在Y轴和Z轴方向重叠形成π键。所以乙炔分子中碳原子间以叁键相结合。
碳原子数与沸点变化曲线图
【思考与交流1】依据表2-1和表2-2绘制碳原子数与沸点或相对密度变化曲线图
1. 烷烃、烯烃、炔烃同系物物性递变规律
烷烃、烯烃同系物的相对密度随碳原子数的变化曲线
图2-2烷烃的相对密度随碳原子数变化曲线
图2-3 烯烃的相对密度随碳原子数变化曲线
【请归纳】烷烃和烯烃物理性质递变规律
【结论】烷烃和烯烃的物理性质随着分子中碳原子数的递增,呈规律性的变化。
同系物的沸点逐渐升高,相对密度逐渐增大,常温下的存在状态也由气态逐渐过渡到液态、固态。炔烃也有相似的规律。
【原因】对于结构相似的物质(分子晶体)来说,分子间作用力随相对分子质量的增大而逐渐增大;导致物理性质上的递变……
【说明】
① 所有烷烃均难溶于水,密度均小于1。
② 常温下烷烃的状态:
当C1-C4 时 呈气态;C5-C16时呈液态; C17以上时为固态。
③ 分子式相同的烃,支链越多,熔沸点越低。
④ 所有的烃都是无色物质,不溶于水而易溶于苯、乙醚等有机溶剂。
、氧化反应
燃烧: CH4 + 2O2 CO2 + 2H2O
点燃
通常状况下,它们很稳定,跟酸、碱及氧化物都不发生反应,也难与其他物质化合。
②、取代反应
C
H
4
C
H
3
C
l
C
H
2
C
l
2
C
H
C
l
3
C
C
l
4
C
l
2
C
l
2
C
l
2
C
l
2
CnH2n+2 +(3n+1)/2 O2 nCO2 +(n+1)H2O
点燃
取代反应:有机物分子中某些原子或原子团被其它原子或原子团所代替的反应。
烷烃特征反应
2、烷烃、烯烃、炔烃的化学性质
(1)、烷烃的化学性质
①
回忆:甲烷和氯气反应的现象?
其它烷烃与甲烷一样,一定条件下能发生取代反应。因为可以被取代的氢原子多,所以其它烷烃取代比甲烷复杂。
③、热分解
C4H10 C2H4+C2H6
△
C4H10 CH4+C3H6
△
由于其它烷烃的碳原子多,所以分解比甲烷复杂。
一般甲烷高温分解,长链烷烃高温裂化、裂解。
CH4 C+2H2
高温
烷烃的裂化
CH3CH3+Cl2 CH3CH2Cl+HCl
光
一氯乙烷与乙烷相比碳链结构不变,只是乙烷分子中的一个H被Cl取代。
选修5《有机化学基础》
第二章 烃和卤代烃
(烷烃)
【知识与技能】
了解烷烃、烯烃和炔烃的物理性质的规律性变化
了解烷烃、烯烃、炔烃的结构特点
【教学重点】烷烃、烯烃、炔烃的结构特点和主要化学性质;乙炔的实验室制法。
【教学目标】
链状烃
烃分子中碳和碳之间的连接呈链状,包括烷烃、烯烃、炔烃、二烯烃等。
环状烃
脂环烃
芳香烃
分子中含有一个或多个苯环的一类碳氢化合物
链烃
脂肪烃
烃
分子中含有碳环的烃
按碳的骨架给烃分类?
【复习1】
分子结构相似,在分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。
回忆:什么叫同系物?
烃和卤代烃等有机物的反应与无机物反应相比有其特点:
(1)反应缓慢。有机分子中的原子一般以共价键结合,有机反应是分子之间的反应。
(2)反应产物复杂。有机物往往具有多个反应部位,在生成主要产物的同时,往往伴有其他副产物的生成。
(3)反应常在有机溶剂中进行。有机物一般在水中的溶解度较小,而在有机溶剂中的溶解度较大。
【复习2】
一、 烷烃、烯烃和炔烃
烯烃:分子里含有一个碳碳双键的不饱和链烃叫做烯烃。通式:CnH2n (n≥2)
(分子里含有两个双键的链烃叫做二烯烃)
烷烃:仅含C—C键和C—H键的饱和链烃,又叫烷烃。(若C—C连成环状,称为环烷烃。)通式:CnH2n+2 (n≥1)
回忆:什么叫烷烃、烯烃、炔烃?其结构有何特点?
炔烃:分子里含有碳碳三键的一类脂肪烃称为炔烃。CnH2n-2 (n≥2)
回忆:烷烃、烯烃、炔烃代表物的物性?结构?碳原子的杂化类型?
sp2杂化: 同一个原子的一个 ns 轨道与两个 np 轨道进行杂化组合为 sp2 杂化轨道。sp2 杂化轨道间的夹角是120°,几何构型为平面正三角形。
激发态
试用杂化轨道理论分析乙烯和乙炔分子的成键情况
sp杂化:一个 ns 轨道和一个np 轨道杂化组合成两个新的 sp 杂化轨道。
sp杂化轨道特点:2个sp杂化轨道在一条直线上,轨道间夹角180°
注:杂化轨道只能用于形成б键或者用来容纳未参与成键的孤对电子。
C原子在形成乙烯分子时,碳原子的2s轨道与2个2p轨道发生杂化,形成3个sp2杂化轨道,伸向平面正三角形的三个顶点。每个C原子的2个sp2杂化轨道分别与2个H原子的1s轨道形成2个相同的σ键,各自剩余的1个sp2杂化轨道相互形成一个σ键,各自没有杂化的l个2p轨道则垂直于杂化轨道所在的平面,彼此肩并肩重叠形成π键。所以,在乙烯分子中双键由一个s-sp2σ键和一个p-pπ键构成。
C原子在形成乙炔分子时发生sp杂化,两个碳原子以1个sp杂化轨道与氢原子的1s轨道结合形成σ键。各自剩余的1个sp杂化轨道相互形成1个σ键,两个碳原子的未杂化2p轨道分别在Y轴和Z轴方向重叠形成π键。所以乙炔分子中碳原子间以叁键相结合。
碳原子数与沸点变化曲线图
【思考与交流1】依据表2-1和表2-2绘制碳原子数与沸点或相对密度变化曲线图
1. 烷烃、烯烃、炔烃同系物物性递变规律
烷烃、烯烃同系物的相对密度随碳原子数的变化曲线
图2-2烷烃的相对密度随碳原子数变化曲线
图2-3 烯烃的相对密度随碳原子数变化曲线
【请归纳】烷烃和烯烃物理性质递变规律
【结论】烷烃和烯烃的物理性质随着分子中碳原子数的递增,呈规律性的变化。
同系物的沸点逐渐升高,相对密度逐渐增大,常温下的存在状态也由气态逐渐过渡到液态、固态。炔烃也有相似的规律。
【原因】对于结构相似的物质(分子晶体)来说,分子间作用力随相对分子质量的增大而逐渐增大;导致物理性质上的递变……
【说明】
① 所有烷烃均难溶于水,密度均小于1。
② 常温下烷烃的状态:
当C1-C4 时 呈气态;C5-C16时呈液态; C17以上时为固态。
③ 分子式相同的烃,支链越多,熔沸点越低。
④ 所有的烃都是无色物质,不溶于水而易溶于苯、乙醚等有机溶剂。
、氧化反应
燃烧: CH4 + 2O2 CO2 + 2H2O
点燃
通常状况下,它们很稳定,跟酸、碱及氧化物都不发生反应,也难与其他物质化合。
②、取代反应
C
H
4
C
H
3
C
l
C
H
2
C
l
2
C
H
C
l
3
C
C
l
4
C
l
2
C
l
2
C
l
2
C
l
2
CnH2n+2 +(3n+1)/2 O2 nCO2 +(n+1)H2O
点燃
取代反应:有机物分子中某些原子或原子团被其它原子或原子团所代替的反应。
烷烃特征反应
2、烷烃、烯烃、炔烃的化学性质
(1)、烷烃的化学性质
①
回忆:甲烷和氯气反应的现象?
其它烷烃与甲烷一样,一定条件下能发生取代反应。因为可以被取代的氢原子多,所以其它烷烃取代比甲烷复杂。
③、热分解
C4H10 C2H4+C2H6
△
C4H10 CH4+C3H6
△
由于其它烷烃的碳原子多,所以分解比甲烷复杂。
一般甲烷高温分解,长链烷烃高温裂化、裂解。
CH4 C+2H2
高温
烷烃的裂化
CH3CH3+Cl2 CH3CH2Cl+HCl
光
一氯乙烷与乙烷相比碳链结构不变,只是乙烷分子中的一个H被Cl取代。
