第三章第三节《羧酸 酯》课件
文档属性
| 名称 | 第三章第三节《羧酸 酯》课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-07-02 00:00:00 | ||
图片预览


文档简介
(共19张PPT)
第三节 羧酸 酯
制作人: 雷文成
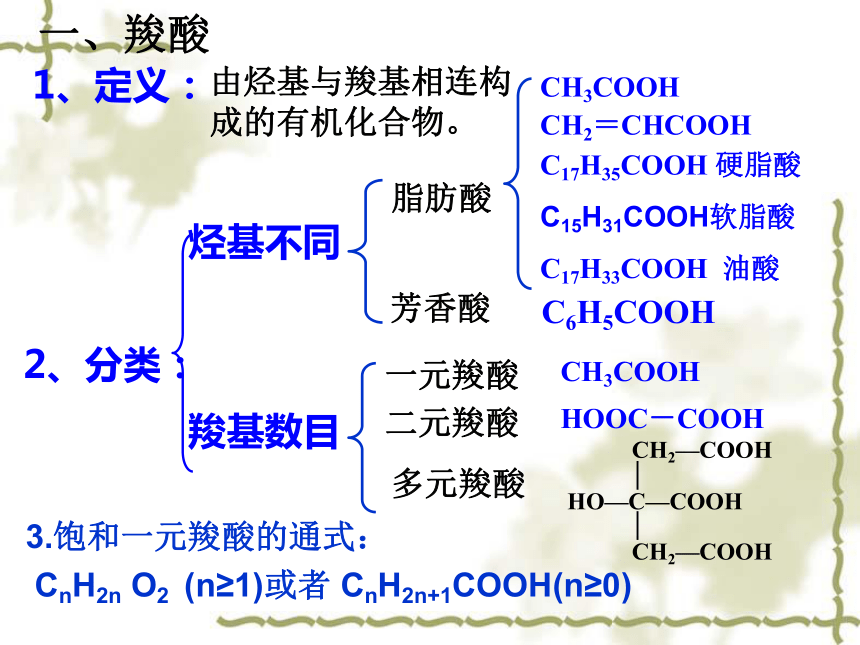
一、羧酸
1、定义:
由烃基与羧基相连构成的有机化合物。
2、分类:
烃基不同
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
CH3COOH
CH2=CHCOOH
C17H35COOH 硬脂酸
C15H31COOH软脂酸
C17H33COOH 油酸
C6H5COOH
HOOC-COOH
HO—C—COOH
CH2—COOH
CH2—COOH
CH3COOH
3.饱和一元羧酸的通式:
CnH2n O2 (n≥1)或者 CnH2n+1COOH(n≥0)
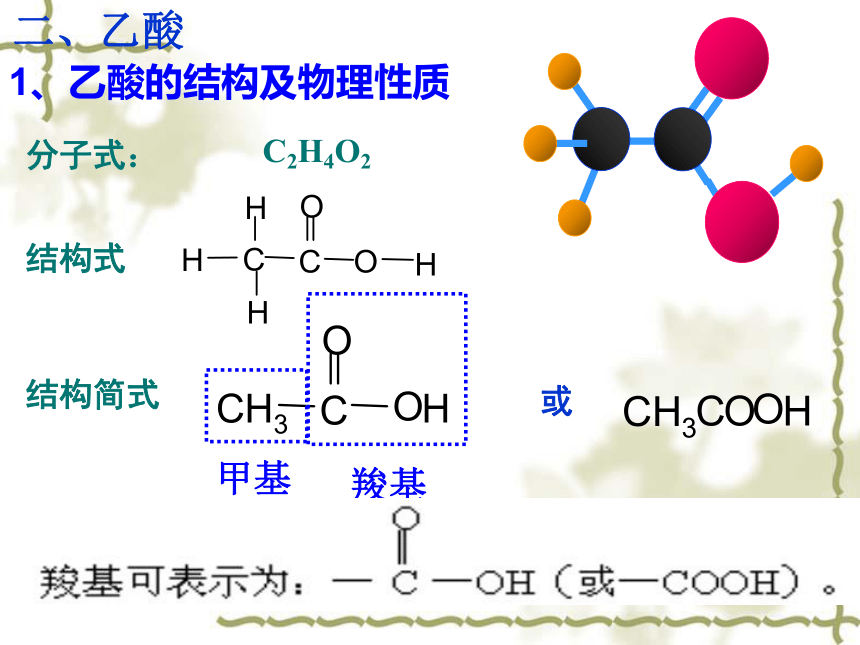
1、乙酸的结构及物理性质
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
二、乙酸
2、乙酸的化学性质
①与酸碱指示剂反应 : 乙酸能使紫色石蕊试液变红
②与活泼金属反应 : Zn+2CH3COOH→(CH3COO)2Zn+H2↑
③与碱性氧化物反应 : CuO+2CH3COOH→(CH3COO)2Cu+H2O
④与碱反应 : CH3COOH+NaOH→CH3COONa+H2O
⑤与某些盐反应 : CaCO3+2CH3COOH→(CH3COO)2Ca+H2O+CO2↑
(1).酸的通性:
乙酸的物理性质:无色液体,有强烈刺激性气味。沸点:117.9℃ (易挥发),熔点:16.6℃(无水乙酸又称为冰醋酸),易溶于水、乙醇等溶剂。
CH3COOH CH3COO-+H+
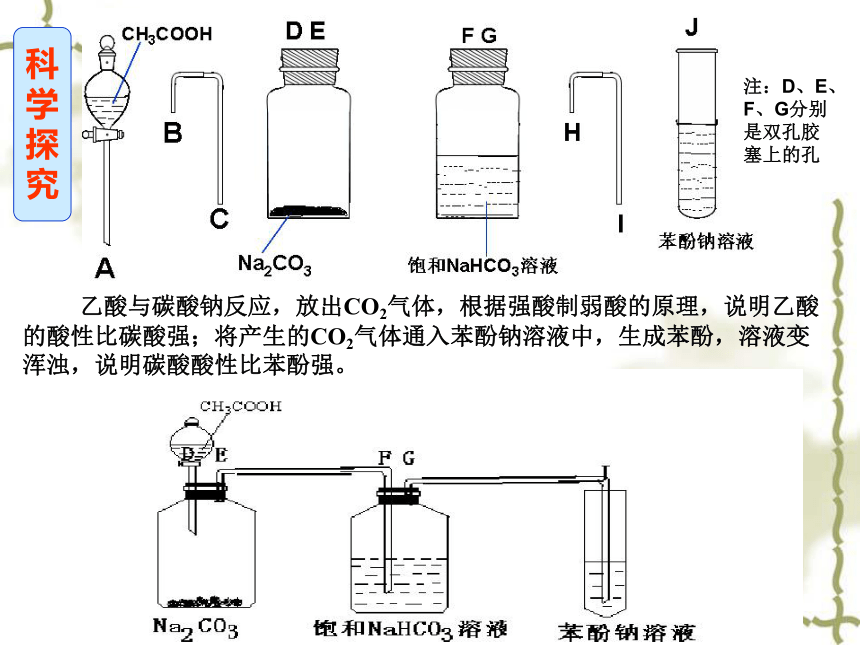
科
学
探
究
注:D、E、F、G分别是双孔胶塞上的孔
乙酸与碳酸钠反应,放出CO2气体,根据强酸制弱酸的原理,说明乙酸的酸性比碳酸强;将产生的CO2气体通入苯酚钠溶液中,生成苯酚,溶液变浑浊,说明碳酸酸性比苯酚强。
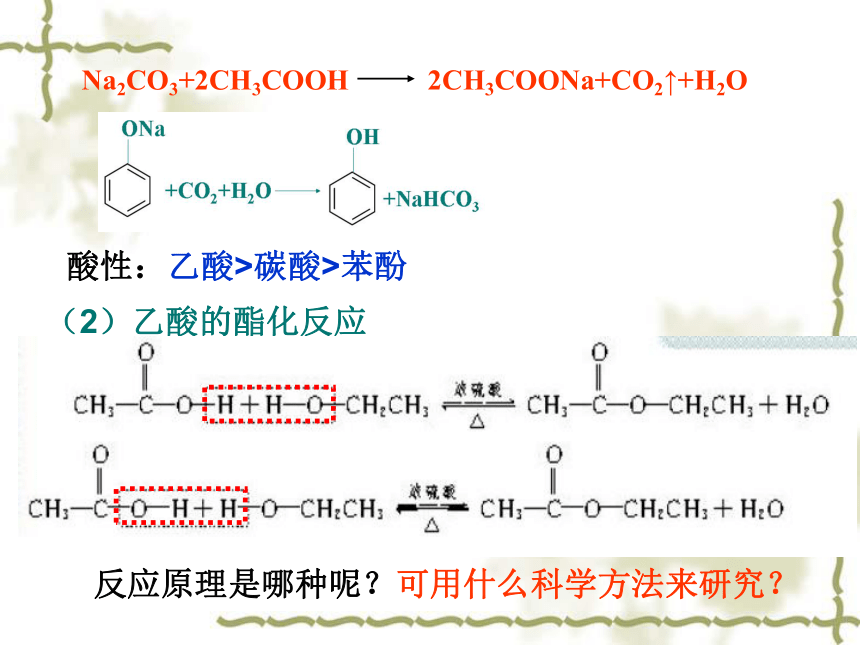
酸性:乙酸>碳酸>苯酚
Na2CO3+2CH3COOH 2CH3COONa+CO2↑+H2O
(2)乙酸的酯化反应
反应原理是哪种呢?可用什么科学方法来研究?
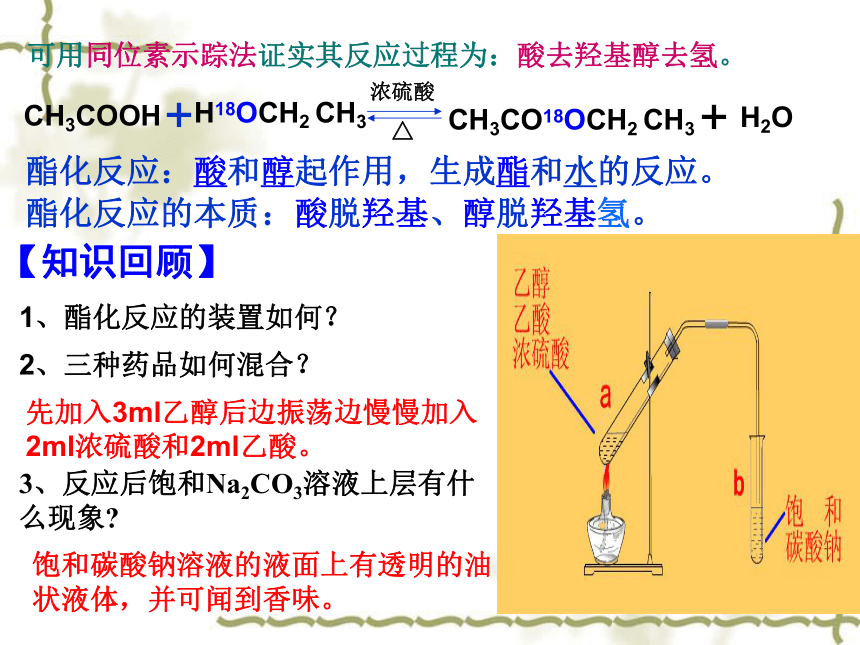
可用同位素示踪法证实其反应过程为:酸去羟基醇去氢。
酯化反应:酸和醇起作用,生成酯和水的反应。
酯化反应的本质:酸脱羟基、醇脱羟基氢。
CH3COOH
+
H18OCH2 CH3
+
H2O
CH3CO18OCH2 CH3
浓硫酸
△
【知识回顾】
1、酯化反应的装置如何?
2、三种药品如何混合?
3、反应后饱和Na2CO3溶液上层有什么现象
饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
先加入3ml乙醇后边振荡边慢慢加入2ml浓硫酸和2ml乙酸。
3. 试管倾斜加热的目的是什么
4.浓硫酸的作用是什么?
5.得到的反应产物中主要有哪些杂质?
6.饱和Na2CO3溶液有什么作用?
7. 为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂
乙酸、乙醇
①冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。② 溶解乙醇。③中和乙酸。
防止受热不匀发生倒吸。 有。
增大受热面积
【知识迁移】写出下列酸和醇的酯化反应方程式
CH3COOCH3 + H2O
CH3COOH + HOCH3
浓H2SO4
C2H5O—NO2 + H2O
C2H5OH + HO—NO2
浓H2SO4
硝酸乙酯
乙酸甲酯
足量
浓H2SO4
浓H2SO4
+ 2H2O
二乙酸乙二酯
环乙二酸乙二酯
代表物 结构简式 羟基氢的活泼性 酸性 与钠反应 与NaOH的反应 与Na2CO3的反应
乙醇
苯酚
乙酸
CH3CH2OH
C6H5OH
CH3COOH
增强
中性
比碳酸弱
比碳酸强
能
能
能
能
能
不能
不能
能
能,不产
生CO2
醇、酚、羧酸中羟基的比较
【知识归纳】
辨 析
三、两类重要的羧酸
1、甲酸——俗称蚁酸
结构特点:既有羧基又有醛基
化学性质
醛基
羧基
氧化反应(如银镜反应)
酸性,酯化反应
O
H—C—O—H
2、乙二酸——俗称草酸
浓H2SO4
+ 2H2O
四、酯
1、概念:酸跟醇起反应脱水后生成的一类化合物。
说出下列化合物的名称:
(1)CH3COOCH2CH3 (2)HCOOCH2CH3
(3)CH3CH2O—NO2
2、酯的命名——根据生成酯的酸和醇的名字命名为“某酸某酯”
3.酯的通式
RCOOR′
一元饱和羧酸酯通式:CnH2nO2
4、酯的性质及用途
酯的物理性质:①低级酯是具有芳香气味的液体。
②密度比水小。③难溶于水,易溶于乙醇和乙醚等有机溶剂。
酯的化学性质:(水解反应)
稀H2SO4
CH3—C—O—C2H5 + H2O
O
CH3—C—OH+H—O—C2H5
O
CH3—C—OC2H5 + NaOH
O
CH3—CONa + HOC2H5
O
酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的
【思考与交流】
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?
根据化学平衡原理,提高乙酸乙酯产率措施有:
由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率;
使用过量的乙醇,可提高乙酸转化为乙酸乙酯产率。
使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。
小结:几种衍生物之间的关系
酯化反应与酯水解反应的比较
酯 化 水 解
反应关系
催 化 剂
催化剂的
其他作用
加热方式
反应类型
NaOH中和酯水解生成的CH3COOH,提高酯的水
解率
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓 硫 酸
稀H2SO4或NaOH
吸水,提高CH3COOH与C2H5OH的转化率
酒精灯火焰加热
热水浴加热
酯化反应
取代反应
水解反应
取代反应
酯化
水解
祝同学们学习进步!
再 见
第三节 羧酸 酯
制作人: 雷文成
一、羧酸
1、定义:
由烃基与羧基相连构成的有机化合物。
2、分类:
烃基不同
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
CH3COOH
CH2=CHCOOH
C17H35COOH 硬脂酸
C15H31COOH软脂酸
C17H33COOH 油酸
C6H5COOH
HOOC-COOH
HO—C—COOH
CH2—COOH
CH2—COOH
CH3COOH
3.饱和一元羧酸的通式:
CnH2n O2 (n≥1)或者 CnH2n+1COOH(n≥0)
1、乙酸的结构及物理性质
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
二、乙酸
2、乙酸的化学性质
①与酸碱指示剂反应 : 乙酸能使紫色石蕊试液变红
②与活泼金属反应 : Zn+2CH3COOH→(CH3COO)2Zn+H2↑
③与碱性氧化物反应 : CuO+2CH3COOH→(CH3COO)2Cu+H2O
④与碱反应 : CH3COOH+NaOH→CH3COONa+H2O
⑤与某些盐反应 : CaCO3+2CH3COOH→(CH3COO)2Ca+H2O+CO2↑
(1).酸的通性:
乙酸的物理性质:无色液体,有强烈刺激性气味。沸点:117.9℃ (易挥发),熔点:16.6℃(无水乙酸又称为冰醋酸),易溶于水、乙醇等溶剂。
CH3COOH CH3COO-+H+
科
学
探
究
注:D、E、F、G分别是双孔胶塞上的孔
乙酸与碳酸钠反应,放出CO2气体,根据强酸制弱酸的原理,说明乙酸的酸性比碳酸强;将产生的CO2气体通入苯酚钠溶液中,生成苯酚,溶液变浑浊,说明碳酸酸性比苯酚强。
酸性:乙酸>碳酸>苯酚
Na2CO3+2CH3COOH 2CH3COONa+CO2↑+H2O
(2)乙酸的酯化反应
反应原理是哪种呢?可用什么科学方法来研究?
可用同位素示踪法证实其反应过程为:酸去羟基醇去氢。
酯化反应:酸和醇起作用,生成酯和水的反应。
酯化反应的本质:酸脱羟基、醇脱羟基氢。
CH3COOH
+
H18OCH2 CH3
+
H2O
CH3CO18OCH2 CH3
浓硫酸
△
【知识回顾】
1、酯化反应的装置如何?
2、三种药品如何混合?
3、反应后饱和Na2CO3溶液上层有什么现象
饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
先加入3ml乙醇后边振荡边慢慢加入2ml浓硫酸和2ml乙酸。
3. 试管倾斜加热的目的是什么
4.浓硫酸的作用是什么?
5.得到的反应产物中主要有哪些杂质?
6.饱和Na2CO3溶液有什么作用?
7. 为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂
乙酸、乙醇
①冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。② 溶解乙醇。③中和乙酸。
防止受热不匀发生倒吸。 有。
增大受热面积
【知识迁移】写出下列酸和醇的酯化反应方程式
CH3COOCH3 + H2O
CH3COOH + HOCH3
浓H2SO4
C2H5O—NO2 + H2O
C2H5OH + HO—NO2
浓H2SO4
硝酸乙酯
乙酸甲酯
足量
浓H2SO4
浓H2SO4
+ 2H2O
二乙酸乙二酯
环乙二酸乙二酯
代表物 结构简式 羟基氢的活泼性 酸性 与钠反应 与NaOH的反应 与Na2CO3的反应
乙醇
苯酚
乙酸
CH3CH2OH
C6H5OH
CH3COOH
增强
中性
比碳酸弱
比碳酸强
能
能
能
能
能
不能
不能
能
能,不产
生CO2
醇、酚、羧酸中羟基的比较
【知识归纳】
辨 析
三、两类重要的羧酸
1、甲酸——俗称蚁酸
结构特点:既有羧基又有醛基
化学性质
醛基
羧基
氧化反应(如银镜反应)
酸性,酯化反应
O
H—C—O—H
2、乙二酸——俗称草酸
浓H2SO4
+ 2H2O
四、酯
1、概念:酸跟醇起反应脱水后生成的一类化合物。
说出下列化合物的名称:
(1)CH3COOCH2CH3 (2)HCOOCH2CH3
(3)CH3CH2O—NO2
2、酯的命名——根据生成酯的酸和醇的名字命名为“某酸某酯”
3.酯的通式
RCOOR′
一元饱和羧酸酯通式:CnH2nO2
4、酯的性质及用途
酯的物理性质:①低级酯是具有芳香气味的液体。
②密度比水小。③难溶于水,易溶于乙醇和乙醚等有机溶剂。
酯的化学性质:(水解反应)
稀H2SO4
CH3—C—O—C2H5 + H2O
O
CH3—C—OH+H—O—C2H5
O
CH3—C—OC2H5 + NaOH
O
CH3—CONa + HOC2H5
O
酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的
【思考与交流】
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?
根据化学平衡原理,提高乙酸乙酯产率措施有:
由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率;
使用过量的乙醇,可提高乙酸转化为乙酸乙酯产率。
使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。
小结:几种衍生物之间的关系
酯化反应与酯水解反应的比较
酯 化 水 解
反应关系
催 化 剂
催化剂的
其他作用
加热方式
反应类型
NaOH中和酯水解生成的CH3COOH,提高酯的水
解率
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓 硫 酸
稀H2SO4或NaOH
吸水,提高CH3COOH与C2H5OH的转化率
酒精灯火焰加热
热水浴加热
酯化反应
取代反应
水解反应
取代反应
酯化
水解
祝同学们学习进步!
再 见
