第三单元课题3元素课件-2021-2022学年九年级化学人教版上册(共37张PPT)
文档属性
| 名称 | 第三单元课题3元素课件-2021-2022学年九年级化学人教版上册(共37张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-15 00:00:00 | ||
图片预览






文档简介
(共37张PPT)
想一想
以上的“钙”、“锌”
指的是什么?
缺“钙”吃什么好?
第三单元
物质构成的奥秘
课题3
元素
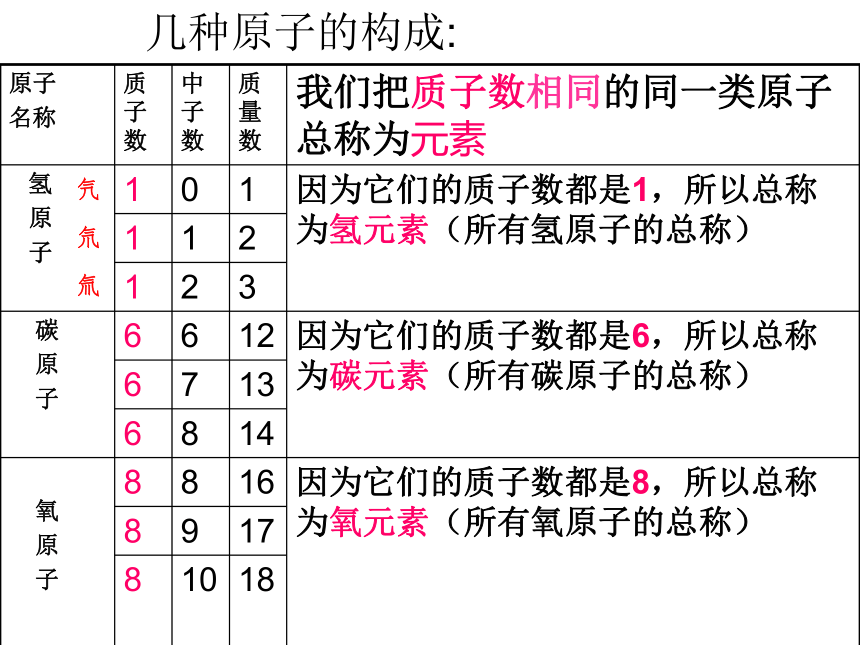
几种原子的构成:
原子
名称
质子数
中子数
质量数
我们把质子数相同的同一类原子总称为元素
氢
原
子
1
0
1
因为它们的质子数都是1,所以总称
为氢元素(所有氢原子的总称)
1
1
2
1
2
3
碳
原
子
6
6
12
因为它们的质子数都是6,所以总称为碳元素(所有碳原子的总称)
6
7
13
6
8
14
氧
原
子
8
8
16
因为它们的质子数都是8,所以总称为氧元素(所有氧原子的总称)
8
9
17
8
10
18
氕
氘
氚
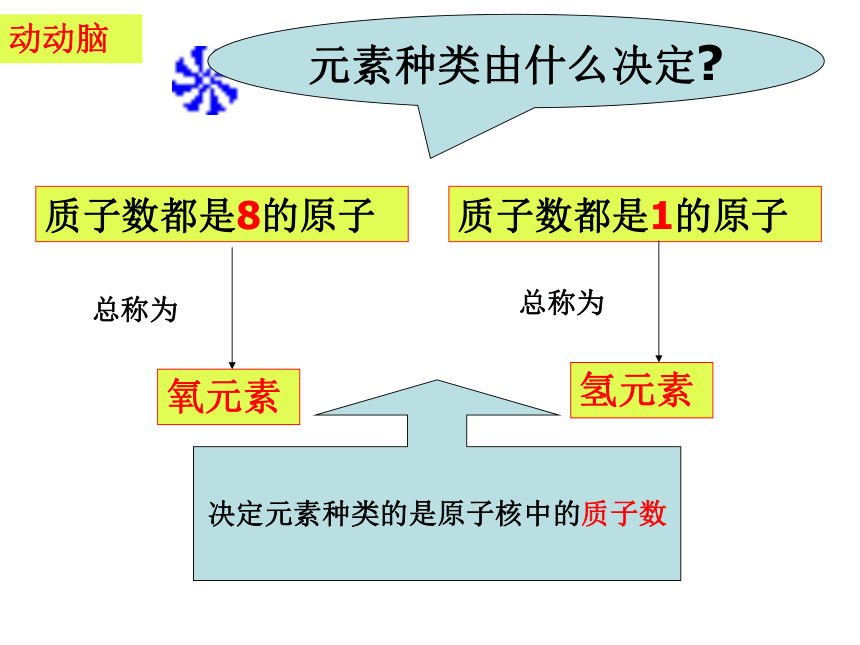
动动脑
质子数都是1的原子
总称为
氢元素
质子数都是8的原子
总称为
氧元素
决定元素种类的是原子核中的质子数
元素种类由什么决定?
一、元素:
说明(1)元素是从宏观上描述纯净物的组成,它只讲种类,不讲个数。
(2)元素种类由质子数决定,同种元素的原子质子数一定相同,不同种元素的原子质子数一定不同。
(3)“同一类原子”是指其质子数(或核电荷数)相同,而核内所含中子数并不一定相同的一类原子。
(4)“原子”不能说成“粒子”(因为粒子包括:分子、
原子、离子等)
1、定义:元素是质子数(即核电荷数)相同的同一类原子的总称
2、元素与原子的区别
元素
原子
区别
宏观概念,只讲种类,不讲个数
是微观概念,既讲种类又讲个数。
适应范围
应用实例
描述物质由元素组成。
描述分子由原子构成或
某些物质由原子构成
水是由氢元素和
氧元素组成的。
一个水分子是由两个氢原子和
一个氧原子构成的;
铁是由铁原子构成的。
元素是一类原子的总称,原子和元素是个体和总体的关系。化学反应中元素种类不变,原子种类和个数也不变。
联系
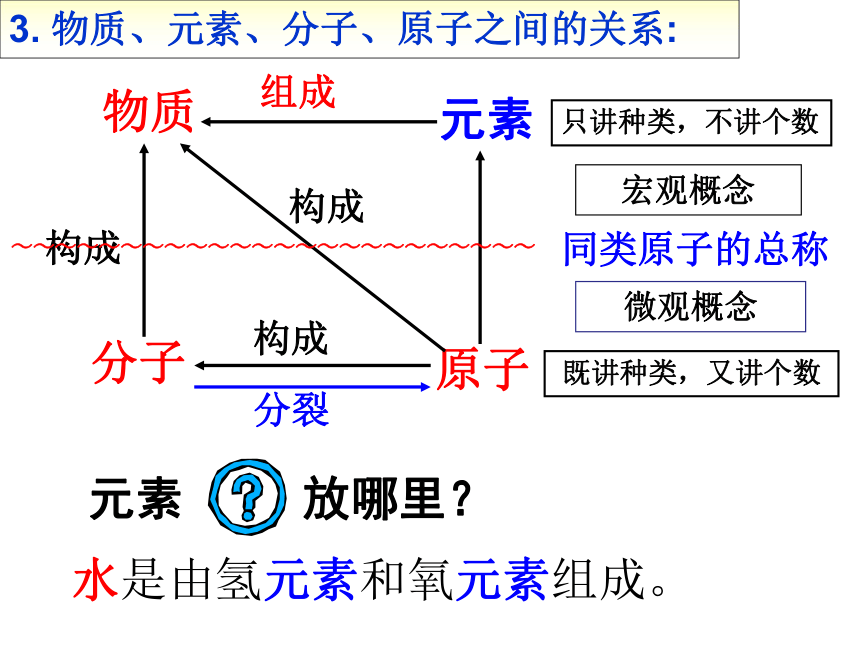
物质
分子
原子
构成
构成
构成
分裂
元素
放哪里?
元素
同类原子的总称
水是由氢元素和氧元素组成。
组成
3.
物质、元素、分子、原子之间的关系:
只讲种类,不讲个数
既讲种类,又讲个数
~~~~~~~~~~~~~~~~~~~~~~~~
宏观概念
微观概念
水由什么组成?
水由什么构成?
而水分子由什么构成?
水分子由氢原子和氧原子构成;
想一想
水由氢元素和氧元素组成;
物质由元素来组成;
分子由原子来构成
组
成
构
成
一个水分子由二个氢原子和一个氧原子构成;
构
成
水由水分子构成;
物质由微粒来构成;
分
子
物
质
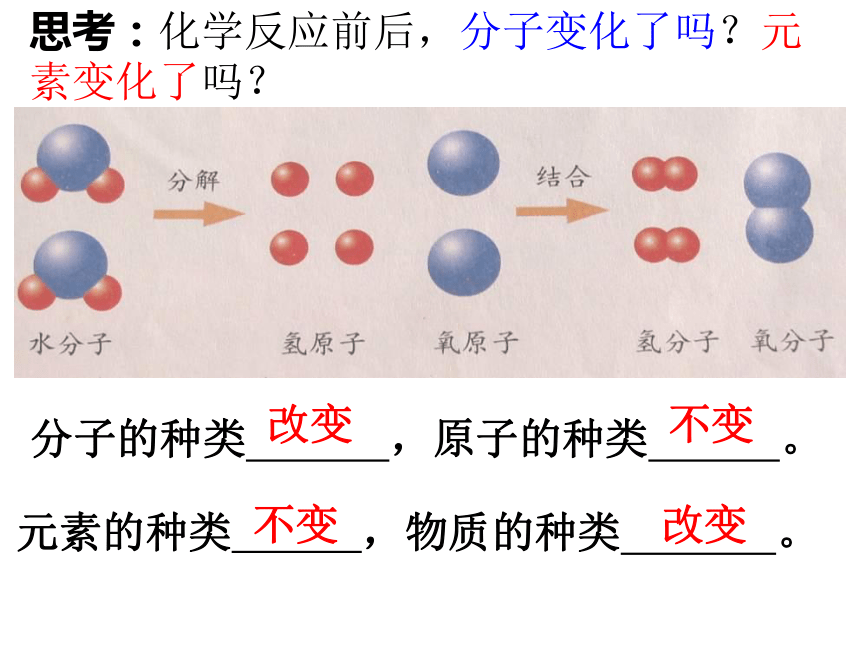
思考:化学反应前后,分子变化了吗?元素变化了吗?
分子的种类
,原子的种类
。
元素的种类
,物质的种类
。
改变
不变
不变
改变
4、化学反应前后
原子的种类、个数、质量
都不变
元素的种类和质量都不变
物质的种类一定变
分子的种类一定变,而分子的个数不一定变
化学反应前后,分子种类改变,元素种类不变。
问题:某物质隔绝空气加热后,生成氧气和氯化钾,从而推断该化合物含有哪些元素?
O2
KCl
含K、Cl、O三种元素
说出下列符号表示的物质中有几种元素,并说出元素的名称
试一试
H2O
H2O2
HCl
KClO3
KMnO4
K2MnO4
CH3COOH
C2H5OH
C6H12O6
一二组同学
三四组同学
五六组同学
已经发现的元素只有100余种,而由元素组成的物质已知的就有3000多万种!
生活中元素的身影处处可见!
都含有钙元素
四、元素的存在---生活中
都含有锌元素
四、元素的存在---生活中
N元素
氮肥
NH4HCO3
NH4H2PO4
(NH4)2SO3
NH4Cl
(NH4)2SO4
CO(NH2)2
生活中的元素
地壳中含量占前五位的元素:
氧、硅、铝、铁、钙
空气中含量最多的2种元素:
氮、氧
海水中含量占前四位的元素:
氧、氢、氯、钠
人体中含量占前五位的元素:
氧、碳、
氢、
氮、钙
含量最多的非金属元素
含量最多的金属元素
注意以下问法
(5)元素的存在:
常温下唯一的液态金属单质——汞(Hg)
常温下唯一的液态非金属单质——溴(Br2)
单质、化合物、氧化物
1、单质:由一种元素组成的纯净物叫单质。
如:H2、O2、N2、Fe、
Cu、Mg、C、S、P
等
2、化合物:由二种或二种以上元素组成的纯
净物叫化合物。
如:NaCl
、KCl
、KClO3
、KMnO4
、NH4HCO3等
3、氧化物:由二种元素组成的化合物,如其中有一种是氧元素的则叫氧化物。
如:MgO、CuO、CO、CO2、MnO2、P2O5、Fe3O4等
原子
元素
纯净物
{
单质(一种元素组成)
化合物(多种元素组成)
混合物
=
纯净物1
+
纯净物2
+
……
一面旗帜代表一种纯净物
一种元素
多种元素
单质
化合物
(6)元素的种类及分类
到目前为止,共发现了118种元素(含十几种人造元素)。
其中(分类):1、金属元素90种。
(占4/5)
2、非金属元素22种。(占1/5)
金属元素:其单质为金属的元素。
非金属元素:其单质为非金属的元素。
(7)元素存在的形态
1、游离态:组成单质的元素是游离态。
H2
O2
N2
Cu
Fe
Mg
2、化合态:组成化合物的元素是化合态。
MgO
Fe3O4
CO2
KClO3
KMnO4
5、元素的分类
碳磷硫硅碘……
溴
氢氧氮氟氯……
氦氖氩氪氙……
元素中国名称的偏旁的规律?(专用汉字)
“钅”字旁,(汞除外,俗称“水银”)
⑴金属元素
⑵非金属元素
①(“石”字旁)固态
②
(“氵”字旁)液态
③(
“气”字头)气态
⑶稀有气体元素
外国人可能不认识汉字
使用统一的符号!!
历史上,道尔顿曾用图形加字母的方式作为元素符号,如图所示。但由于后来发现的元素越来越多,符号设计越来越复杂,不便于记忆和书写,故未能被广泛采用。
1.元素符号采用的是
。
二、元素符号
2.书写原则:
第一个字母要大写,第二个字母要小写
O
C
H
N
S
氧 碳 氢 氮 硫
Fe
Cu
Al
Mg
Hg
铁 铜 铝 镁
汞
拉丁文第一个字母大写来表示
一大二小!
部分元素的拉丁文名称
氧
Oxygenium
氮
Nitorgenium
氖
Neon
氢
Hydrogenium
钠
Natrium
氦
Helium
碳
Carbonium
硫
Sulfur
钙
Calcium
硅
Silicium
铜
Cuprum
钴
Cobaltum
注意大小写:
1、Co和CO
钴元素和一氧化碳(物质)
2、Ca和Cu
钙元素和铜元素
3、
Ag和Hg
银元素和汞元素
大写表示元素,小写表示从属
3.元素符号的意义
H
一个氢原子
意义:
表示一种元素
表示该元素的一个原子
氢元素
(宏观含义)
(微观含义)
部分元素符号有三个意义:
②一个铁原子
①铁元素
Fe
C
③铁这种物质(铁单质-由原子直
接构成)
①碳元素
②一个碳原子
③碳这种物质(碳单质-组成复杂,也用元素符号直接表示)
想一想:
(1)元素符号N、Cu、Ne、C表示的意义?
Cu
N
表示氮元素
表示一个氮原子
表示铜元素
一个铜原子
Ne
表示氖元素
表示一个氖原子
C
表示碳元素
表示一个碳原子
表示铜这种物质
表示氖气
表示炭这种物质
(不能表示氮气N2)
7.思考
下列符号的意义
2O
6C
2个氧原子
6个碳原子
元素符号前面有系数,就不能再表示元素(宏观),
只表示微粒个数(微观)!
例:O
表示氧元素或一个氧原子
2个氧元素;
8Fe
8个铁原子
(2)符号H、2H、H2、2H2表示的意义?
注意:元素符号前有数字只表示微观的意义(几个原子、分子或离子),不表示宏观意义(元素或物质)。
H
:
(1)表示氢元素(宏观)
(2)表示一个氢原子(微观)
2H
:
仅表示2个氢原子(微观)
H2
:
(1)
表示氢气;(宏观)(2)表示一个氢气分子;(微观)(3)表示一个氢气分子由2个氢原子构成。(微观)
2H2
:
仅表示2个氢气分子。(微观)
三、元素周期表简介
O
氧
8
16.00
原子序数
元素符号
元素名称
相对原子质量
核电荷数
质子数
考察元素周期表,讨论下列问题:
1每周期开头的是什么类型的元素
每周期靠近尾部的是什么类型的元素
3
每一周期都以什么类型的元素结尾
金属元素
非金属元素
稀有气体元素
1、元素周期表上分两大区域
2、横行——叫周期
7个横行就是7个周期。(由电子层数决定)
3、纵行——族
18个纵行16个族。
(由最外电子层上的电子数决定)
元素周期表是学习和研究化学的重要工具。
小结:
练习
1、不同种元素最本质的区别是(
)
A
质子数
B
中子数
C
核外电子数
D
相对原子质量
A
2
、下列说法有没有错误?将错误的说法
加以改正:
水是由一个氧元素和两个氢元素组成的。
练习
3.二氧化碳是由
和
组成的,共有
种元素;
4.二氧化碳分子是由
和
构成的,共有
种原子;一个二氧化碳分子中有
个原子。
5.过氧化氢(H2O2)是由
和
组成的,1个过氧化氢分子中含有2个氢
和2个氧
。
碳元素
氧元素
两
碳原子
氧原子
两
三
氢元素
氧元素
原子
原子
想一想
以上的“钙”、“锌”
指的是什么?
缺“钙”吃什么好?
第三单元
物质构成的奥秘
课题3
元素
几种原子的构成:
原子
名称
质子数
中子数
质量数
我们把质子数相同的同一类原子总称为元素
氢
原
子
1
0
1
因为它们的质子数都是1,所以总称
为氢元素(所有氢原子的总称)
1
1
2
1
2
3
碳
原
子
6
6
12
因为它们的质子数都是6,所以总称为碳元素(所有碳原子的总称)
6
7
13
6
8
14
氧
原
子
8
8
16
因为它们的质子数都是8,所以总称为氧元素(所有氧原子的总称)
8
9
17
8
10
18
氕
氘
氚
动动脑
质子数都是1的原子
总称为
氢元素
质子数都是8的原子
总称为
氧元素
决定元素种类的是原子核中的质子数
元素种类由什么决定?
一、元素:
说明(1)元素是从宏观上描述纯净物的组成,它只讲种类,不讲个数。
(2)元素种类由质子数决定,同种元素的原子质子数一定相同,不同种元素的原子质子数一定不同。
(3)“同一类原子”是指其质子数(或核电荷数)相同,而核内所含中子数并不一定相同的一类原子。
(4)“原子”不能说成“粒子”(因为粒子包括:分子、
原子、离子等)
1、定义:元素是质子数(即核电荷数)相同的同一类原子的总称
2、元素与原子的区别
元素
原子
区别
宏观概念,只讲种类,不讲个数
是微观概念,既讲种类又讲个数。
适应范围
应用实例
描述物质由元素组成。
描述分子由原子构成或
某些物质由原子构成
水是由氢元素和
氧元素组成的。
一个水分子是由两个氢原子和
一个氧原子构成的;
铁是由铁原子构成的。
元素是一类原子的总称,原子和元素是个体和总体的关系。化学反应中元素种类不变,原子种类和个数也不变。
联系
物质
分子
原子
构成
构成
构成
分裂
元素
放哪里?
元素
同类原子的总称
水是由氢元素和氧元素组成。
组成
3.
物质、元素、分子、原子之间的关系:
只讲种类,不讲个数
既讲种类,又讲个数
~~~~~~~~~~~~~~~~~~~~~~~~
宏观概念
微观概念
水由什么组成?
水由什么构成?
而水分子由什么构成?
水分子由氢原子和氧原子构成;
想一想
水由氢元素和氧元素组成;
物质由元素来组成;
分子由原子来构成
组
成
构
成
一个水分子由二个氢原子和一个氧原子构成;
构
成
水由水分子构成;
物质由微粒来构成;
分
子
物
质
思考:化学反应前后,分子变化了吗?元素变化了吗?
分子的种类
,原子的种类
。
元素的种类
,物质的种类
。
改变
不变
不变
改变
4、化学反应前后
原子的种类、个数、质量
都不变
元素的种类和质量都不变
物质的种类一定变
分子的种类一定变,而分子的个数不一定变
化学反应前后,分子种类改变,元素种类不变。
问题:某物质隔绝空气加热后,生成氧气和氯化钾,从而推断该化合物含有哪些元素?
O2
KCl
含K、Cl、O三种元素
说出下列符号表示的物质中有几种元素,并说出元素的名称
试一试
H2O
H2O2
HCl
KClO3
KMnO4
K2MnO4
CH3COOH
C2H5OH
C6H12O6
一二组同学
三四组同学
五六组同学
已经发现的元素只有100余种,而由元素组成的物质已知的就有3000多万种!
生活中元素的身影处处可见!
都含有钙元素
四、元素的存在---生活中
都含有锌元素
四、元素的存在---生活中
N元素
氮肥
NH4HCO3
NH4H2PO4
(NH4)2SO3
NH4Cl
(NH4)2SO4
CO(NH2)2
生活中的元素
地壳中含量占前五位的元素:
氧、硅、铝、铁、钙
空气中含量最多的2种元素:
氮、氧
海水中含量占前四位的元素:
氧、氢、氯、钠
人体中含量占前五位的元素:
氧、碳、
氢、
氮、钙
含量最多的非金属元素
含量最多的金属元素
注意以下问法
(5)元素的存在:
常温下唯一的液态金属单质——汞(Hg)
常温下唯一的液态非金属单质——溴(Br2)
单质、化合物、氧化物
1、单质:由一种元素组成的纯净物叫单质。
如:H2、O2、N2、Fe、
Cu、Mg、C、S、P
等
2、化合物:由二种或二种以上元素组成的纯
净物叫化合物。
如:NaCl
、KCl
、KClO3
、KMnO4
、NH4HCO3等
3、氧化物:由二种元素组成的化合物,如其中有一种是氧元素的则叫氧化物。
如:MgO、CuO、CO、CO2、MnO2、P2O5、Fe3O4等
原子
元素
纯净物
{
单质(一种元素组成)
化合物(多种元素组成)
混合物
=
纯净物1
+
纯净物2
+
……
一面旗帜代表一种纯净物
一种元素
多种元素
单质
化合物
(6)元素的种类及分类
到目前为止,共发现了118种元素(含十几种人造元素)。
其中(分类):1、金属元素90种。
(占4/5)
2、非金属元素22种。(占1/5)
金属元素:其单质为金属的元素。
非金属元素:其单质为非金属的元素。
(7)元素存在的形态
1、游离态:组成单质的元素是游离态。
H2
O2
N2
Cu
Fe
Mg
2、化合态:组成化合物的元素是化合态。
MgO
Fe3O4
CO2
KClO3
KMnO4
5、元素的分类
碳磷硫硅碘……
溴
氢氧氮氟氯……
氦氖氩氪氙……
元素中国名称的偏旁的规律?(专用汉字)
“钅”字旁,(汞除外,俗称“水银”)
⑴金属元素
⑵非金属元素
①(“石”字旁)固态
②
(“氵”字旁)液态
③(
“气”字头)气态
⑶稀有气体元素
外国人可能不认识汉字
使用统一的符号!!
历史上,道尔顿曾用图形加字母的方式作为元素符号,如图所示。但由于后来发现的元素越来越多,符号设计越来越复杂,不便于记忆和书写,故未能被广泛采用。
1.元素符号采用的是
。
二、元素符号
2.书写原则:
第一个字母要大写,第二个字母要小写
O
C
H
N
S
氧 碳 氢 氮 硫
Fe
Cu
Al
Mg
Hg
铁 铜 铝 镁
汞
拉丁文第一个字母大写来表示
一大二小!
部分元素的拉丁文名称
氧
Oxygenium
氮
Nitorgenium
氖
Neon
氢
Hydrogenium
钠
Natrium
氦
Helium
碳
Carbonium
硫
Sulfur
钙
Calcium
硅
Silicium
铜
Cuprum
钴
Cobaltum
注意大小写:
1、Co和CO
钴元素和一氧化碳(物质)
2、Ca和Cu
钙元素和铜元素
3、
Ag和Hg
银元素和汞元素
大写表示元素,小写表示从属
3.元素符号的意义
H
一个氢原子
意义:
表示一种元素
表示该元素的一个原子
氢元素
(宏观含义)
(微观含义)
部分元素符号有三个意义:
②一个铁原子
①铁元素
Fe
C
③铁这种物质(铁单质-由原子直
接构成)
①碳元素
②一个碳原子
③碳这种物质(碳单质-组成复杂,也用元素符号直接表示)
想一想:
(1)元素符号N、Cu、Ne、C表示的意义?
Cu
N
表示氮元素
表示一个氮原子
表示铜元素
一个铜原子
Ne
表示氖元素
表示一个氖原子
C
表示碳元素
表示一个碳原子
表示铜这种物质
表示氖气
表示炭这种物质
(不能表示氮气N2)
7.思考
下列符号的意义
2O
6C
2个氧原子
6个碳原子
元素符号前面有系数,就不能再表示元素(宏观),
只表示微粒个数(微观)!
例:O
表示氧元素或一个氧原子
2个氧元素;
8Fe
8个铁原子
(2)符号H、2H、H2、2H2表示的意义?
注意:元素符号前有数字只表示微观的意义(几个原子、分子或离子),不表示宏观意义(元素或物质)。
H
:
(1)表示氢元素(宏观)
(2)表示一个氢原子(微观)
2H
:
仅表示2个氢原子(微观)
H2
:
(1)
表示氢气;(宏观)(2)表示一个氢气分子;(微观)(3)表示一个氢气分子由2个氢原子构成。(微观)
2H2
:
仅表示2个氢气分子。(微观)
三、元素周期表简介
O
氧
8
16.00
原子序数
元素符号
元素名称
相对原子质量
核电荷数
质子数
考察元素周期表,讨论下列问题:
1每周期开头的是什么类型的元素
每周期靠近尾部的是什么类型的元素
3
每一周期都以什么类型的元素结尾
金属元素
非金属元素
稀有气体元素
1、元素周期表上分两大区域
2、横行——叫周期
7个横行就是7个周期。(由电子层数决定)
3、纵行——族
18个纵行16个族。
(由最外电子层上的电子数决定)
元素周期表是学习和研究化学的重要工具。
小结:
练习
1、不同种元素最本质的区别是(
)
A
质子数
B
中子数
C
核外电子数
D
相对原子质量
A
2
、下列说法有没有错误?将错误的说法
加以改正:
水是由一个氧元素和两个氢元素组成的。
练习
3.二氧化碳是由
和
组成的,共有
种元素;
4.二氧化碳分子是由
和
构成的,共有
种原子;一个二氧化碳分子中有
个原子。
5.过氧化氢(H2O2)是由
和
组成的,1个过氧化氢分子中含有2个氢
和2个氧
。
碳元素
氧元素
两
碳原子
氧原子
两
三
氢元素
氧元素
原子
原子
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
