2021-2022学年上学期高二化学人教版(2019)选择性必修12.2.3化学平衡图像 等效平衡随堂检测
文档属性
| 名称 | 2021-2022学年上学期高二化学人教版(2019)选择性必修12.2.3化学平衡图像 等效平衡随堂检测 |
|
|
| 格式 | zip | ||
| 文件大小 | 213.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-18 00:00:00 | ||
图片预览


文档简介
2.2.3化学平衡图像
等效平衡随堂检测
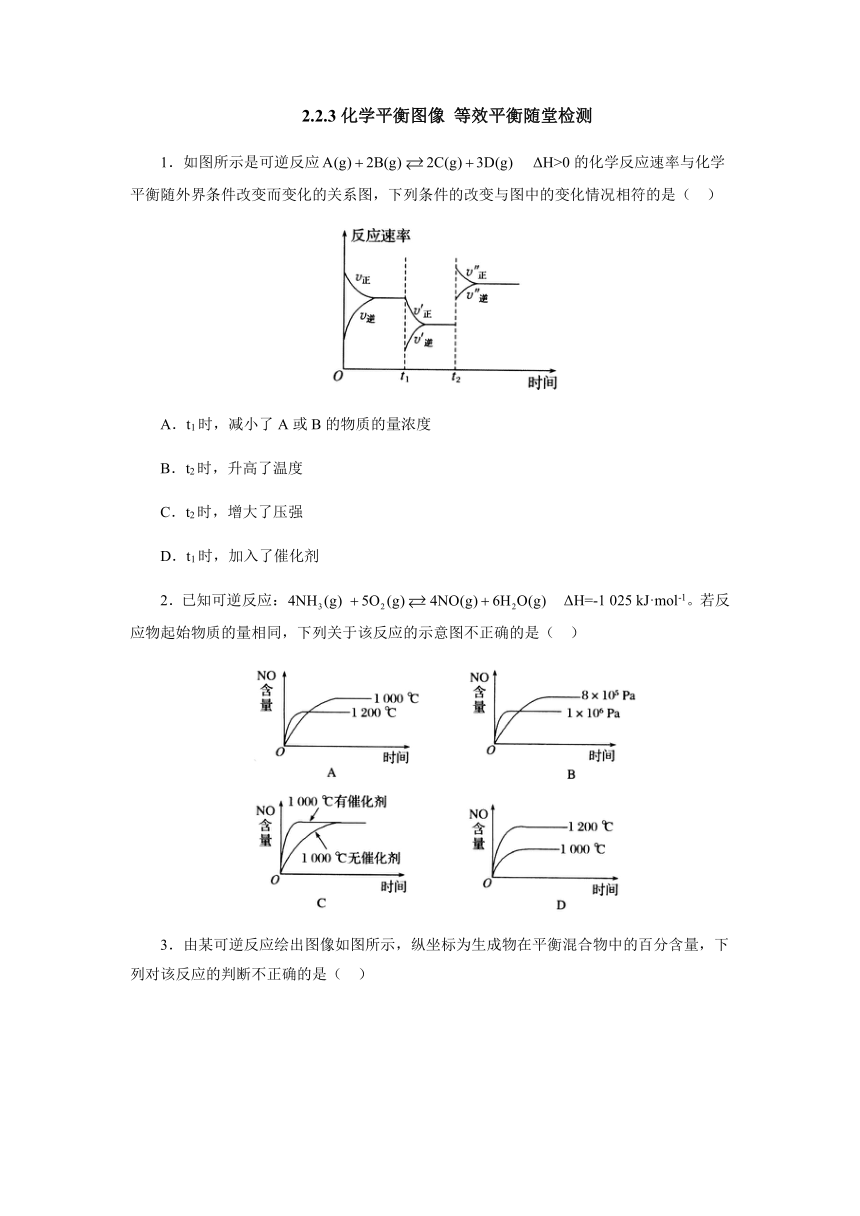
1.如图所示是可逆反应
ΔH>0的化学反应速率与化学平衡随外界条件改变而变化的关系图,下列条件的改变与图中的变化情况相符的是(
)
A.t1时,减小了A或B的物质的量浓度
B.t2时,升高了温度
C.t2时,增大了压强
D.t1时,加入了催化剂
2.已知可逆反应:
ΔH=-1
025
kJ·mol-1。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是(
)
3.由某可逆反应绘出图像如图所示,纵坐标为生成物在平衡混合物中的百分含量,下列对该反应的判断不正确的是(
)
A.反应物中可能含有气体
B.生成物中一定有气体
C.正反应一定是放热反应
D.正反应一定是吸热反应
4.(辛集市校级期中)有一可逆反应:,若按下列两种配比在同温同体积的密闭容器中进行反应:
①0.8
mol
A+1.2
mol
B+1.2
mol
C+2.4
mol
D
②1.4
mol
A+2.1
mol
B+0.6
mol
C+l.2
mol
D
达平衡后,C的质量分数相等,则方程式中x的值为(
)
A.1
B.2
C.3
D.4
5.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(下图中,p表示压强,T表示温度,n表示物质的量,t表示反应时间):
根据以上规律判断(填“>”“=”或“<”):
(1)反应Ⅰ:p2______p1,ΔH________0。
(2)反应Ⅱ:T1_________T2,ΔH_________0。
(3)反应Ⅲ:若T2_________T1,ΔH________0。
(4)反应Ⅳ:若T2_________T1,ΔH________0。
参考答案
1.B
由图像可知,t1时刻,正反应速率不变,逆反应速率减小,只能是减小生成物的浓度;t2时刻,正、逆反应速率都增大,且平衡右移,结合反应的特征,只能是升高了温度。
2.D
升高温度,平衡向逆反应方向移动,平衡时一氧化氮的含量小,且达到平衡时需要的时间短,故A正确,D错误;增大压强,平衡向逆反应方向移动,平衡时一氧化氮的含量小,且达到平衡时需要的时间短,故B正确;有无催化剂只影响到达平衡状态的时间,不影响平衡移动,故C正确。
3.C
由图示可知,随着温度的升高,生成物的含量增加,即升高温度,平衡右移,所以该反应一定为吸热反应;压强增大,生成物的含量减小,说明化学方程式中气体生成物的计量数之和大于气体反应物的计量数之和。
4.B
5.(1)>
<
(2)>
<
(3)>
>(或<
<)
(4)>
>(或<
<)
等效平衡随堂检测
1.如图所示是可逆反应
ΔH>0的化学反应速率与化学平衡随外界条件改变而变化的关系图,下列条件的改变与图中的变化情况相符的是(
)
A.t1时,减小了A或B的物质的量浓度
B.t2时,升高了温度
C.t2时,增大了压强
D.t1时,加入了催化剂
2.已知可逆反应:
ΔH=-1
025
kJ·mol-1。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是(
)
3.由某可逆反应绘出图像如图所示,纵坐标为生成物在平衡混合物中的百分含量,下列对该反应的判断不正确的是(
)
A.反应物中可能含有气体
B.生成物中一定有气体
C.正反应一定是放热反应
D.正反应一定是吸热反应
4.(辛集市校级期中)有一可逆反应:,若按下列两种配比在同温同体积的密闭容器中进行反应:
①0.8
mol
A+1.2
mol
B+1.2
mol
C+2.4
mol
D
②1.4
mol
A+2.1
mol
B+0.6
mol
C+l.2
mol
D
达平衡后,C的质量分数相等,则方程式中x的值为(
)
A.1
B.2
C.3
D.4
5.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(下图中,p表示压强,T表示温度,n表示物质的量,t表示反应时间):
根据以上规律判断(填“>”“=”或“<”):
(1)反应Ⅰ:p2______p1,ΔH________0。
(2)反应Ⅱ:T1_________T2,ΔH_________0。
(3)反应Ⅲ:若T2_________T1,ΔH________0。
(4)反应Ⅳ:若T2_________T1,ΔH________0。
参考答案
1.B
由图像可知,t1时刻,正反应速率不变,逆反应速率减小,只能是减小生成物的浓度;t2时刻,正、逆反应速率都增大,且平衡右移,结合反应的特征,只能是升高了温度。
2.D
升高温度,平衡向逆反应方向移动,平衡时一氧化氮的含量小,且达到平衡时需要的时间短,故A正确,D错误;增大压强,平衡向逆反应方向移动,平衡时一氧化氮的含量小,且达到平衡时需要的时间短,故B正确;有无催化剂只影响到达平衡状态的时间,不影响平衡移动,故C正确。
3.C
由图示可知,随着温度的升高,生成物的含量增加,即升高温度,平衡右移,所以该反应一定为吸热反应;压强增大,生成物的含量减小,说明化学方程式中气体生成物的计量数之和大于气体反应物的计量数之和。
4.B
5.(1)>
<
(2)>
<
(3)>
>(或<
<)
(4)>
>(或<
<)
