人教版九年级化学下册 名校优选精练 第九单元达标测试卷(含答案及解析)
文档属性
| 名称 | 人教版九年级化学下册 名校优选精练 第九单元达标测试卷(含答案及解析) |  | |
| 格式 | doc | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-09-17 14:45:06 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
人教版九年级化学下册
名校优选精练
第九单元达标测试卷
时间:45分钟 满分:100分
班级:
姓名:
考号:
.
可能用到的相对原子质量 O:16 Cl:35.5 K:39
第Ⅰ卷
本卷共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一个选项符合题目要求。
1.下列液体去除油污效果最好的是( )
A.洗洁精
B.食盐水
C.白醋
D.自来水
2.下列是福建人民日常饮食中常见的物质,其中容器内所盛放的物质属于溶液的是( )
A.福州锅边糊
B.莆田鲜卤面
C.厦门沙茶面
D.建瓯福矛酒
3.下列有关溶液的叙述正确的是( )
A.食盐水倒出一半后浓度降低
B.果粒橙属于溶液
C.升温会降低二氧化碳在水中的溶解度
D.蔗糖可以无限地溶解在一定量的水中
4.某同学配制16%的氯化钠溶液来选种。如图所示的下列操作中正确的是( )
5.小龙同学在工具书中查到NaOH在水和酒精中的溶解度如表所示。通过分析他得出以下结论,其中不正确的是( )
20
℃
40
℃
水
109
g
129
g
酒精
17.3
g
40
g
A.温度和溶剂种类对NaOH的溶解度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40
℃时,40
g
NaOH溶解在100
g酒精中达到饱和
D.将等质量40
℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20
℃,析出的晶体前者比后者多
6.如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀。表中的液体X和固体Y的组合,符合题意的是( )
(第6题)
①
②
③
④
X
稀盐酸
水
水
水
Y
大理石
氯化钠
氢氧化钠
硝酸铵
A.①②
B.①③
C.①③④
D.②③④
7.下列有关溶液的说法中正确的是( )
A.常温下将100
mL饱和Ca(OH)2溶液加热至50
℃,会使溶液由饱和溶液变为不饱和溶液
B.从100
mL
25%的硫酸溶液中取出10
mL,则取出的10
mL硫酸溶液溶质质量分数仍为25%
C.20
℃时,50
g水中溶解了18
g
NaCl,则20
℃时NaCl的溶解度为36
g
D.将95
g
KCl溶液蒸干得到5
g
KCl固体,则原溶液的溶质质量分数为5%
8.20
℃时,四个实验小组分别取不同质量的NaCl,逐渐加入到各盛有50
g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余NaCl的质量。记录数据如下表:
实验小组
第一组
第二组
第三组
第四组
水的质量/g
50
50
50
50
所取NaCl的质量/g
15
20
25
30
剩余NaCl的质量/g
0
2
7
12
下列说法错误的是( )
A.20
℃时,50
g
NaCl饱和溶液中含有18
g
NaCl
B.用蒸发的方法可以使不饱和溶液变成饱和溶液
C.第二组所得溶液的溶质与溶剂的质量比为9∶25
D.相同温度下,NaCl在水中的溶解度与水的质量无关
9.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
(第9题)
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
10.两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH4NO3固体,向两支试管中分别滴加适量水,现象如图1所示,结合图2(X、Y的溶解度曲线图)判断下列说法正确的是( )
(第10题)
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2
℃降温到t1
℃,溶质的质量分数变大
D.t3
℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
第Ⅱ卷
本卷共6题,共70分。
11.(12分)网红产品“天气瓶”(如图1)的制作步骤如下:
Ⅰ.将10
g樟脑溶于40
mL酒精,得溶液a(樟脑难溶于水);
Ⅱ.将2.5
g硝酸钾和2.5
g氯化铵溶于33
g水中,得溶液b;
Ⅲ.将a、b两种溶液混合、加热、搅拌直至澄清;
Ⅳ.混合液冷却至室温后,密封在玻璃容器内,即制得“天气瓶”。
根据上述步骤并结合图2的溶解度曲线,回答下列问题。
(第11题)
(1)溶液a中溶剂为________。
(2)溶液b中硝酸钾的质量分数为________________(列计算式)。
(3)瓶内出现的晶体数量会随气温的降低而增加。该晶体的成分是________,推断产生这种现象的原因是___________________________________________。
(4)图3是“天气瓶”的宣传图,根据其制作步骤,判断该宣传的真实性为________,理由是__________________________________________________
______________________________。
12.(13分)KNO3是一种重要的化工原料。
(1)宋代《开宝本草》中记载了KNO3的提纯方法
:“所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”,“霜”指KNO3,这里涉及化学实验基本操作方法:“以水淋汁”是指溶解,“煎炼而成”是指________。
(2)《天工开物》记载“凡研硝(KNO3)不以铁碾入石臼,相激火生,祸不可测”。
是指硝酸钾的性质不稳定,受到撞击会发生分解反应生成一种可助燃的气体单质是________。
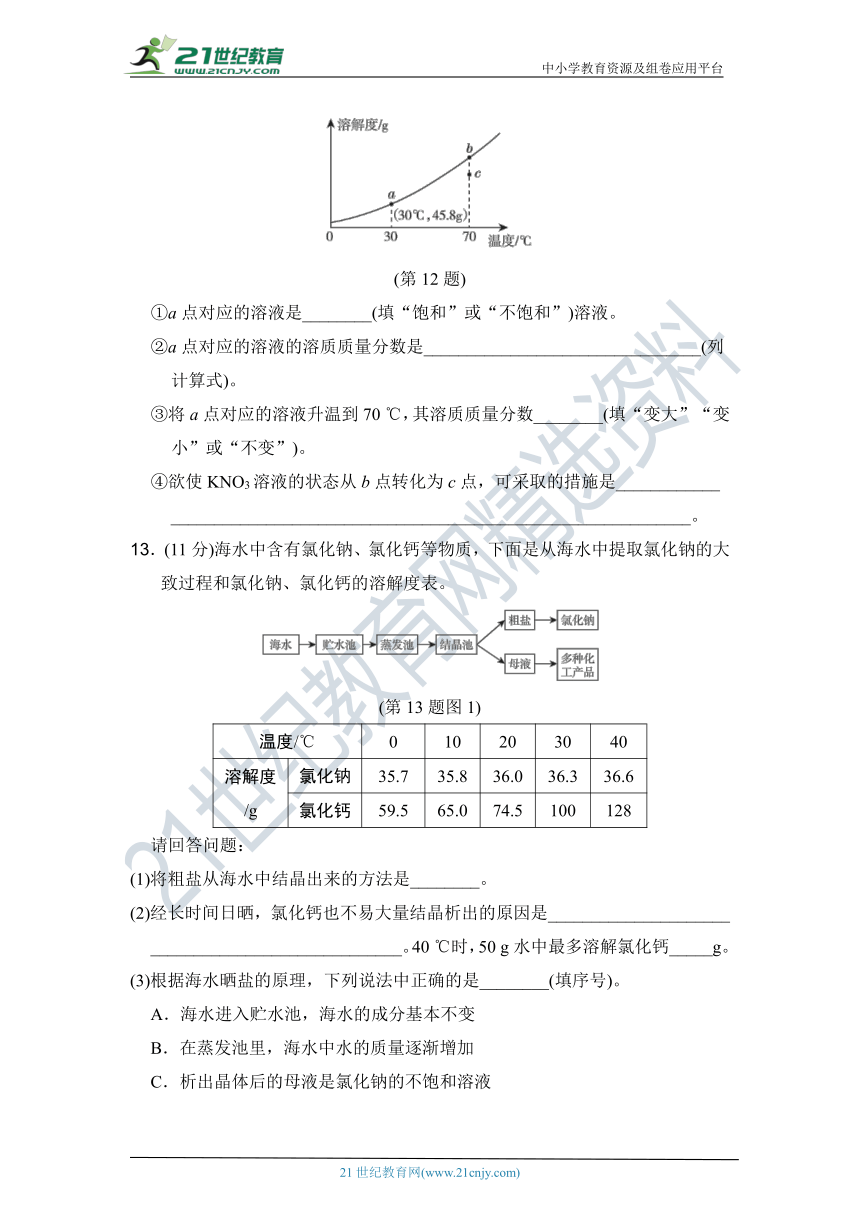
(3)如图为KNO3的溶解度曲线,a、b在溶解度曲线上。
(第12题)
①a点对应的溶液是________(填“饱和”或“不饱和”)溶液。
②a点对应的溶液的溶质质量分数是________________________________(列计算式)。
③将a点对应的溶液升温到70
℃,其溶质质量分数________(填“变大”“变小”或“不变”)。
④欲使KNO3溶液的状态从b点转化为c点,可采取的措施是____________
____________________________________________________________。
13.(11分)海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程和氯化钠、氯化钙的溶解度表。
(第13题图1)
温度/℃
0
10
20
30
40
溶解度/g
氯化钠
35.7
35.8
36.0
36.3
36.6
氯化钙
59.5
65.0
74.5
100
128
请回答问题:
(1)将粗盐从海水中结晶出来的方法是________。
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是_____________________
_____________________________。40
℃时,50
g水中最多溶解氯化钙_____g。
(3)根据海水晒盐的原理,下列说法中正确的是________(填序号)。
A.海水进入贮水池,海水的成分基本不变
B.在蒸发池里,海水中水的质量逐渐增加
C.析出晶体后的母液是氯化钠的不饱和溶液
(4)溶解度曲线图2中,能表示氯化钙溶解度曲线的是________(填“甲”或“乙”)。
(第13题图2)
14.(12分)实验室配制一定溶质质量分数的氯化钠溶液的流程如图所示:
(第14题)
(1)应称量________g氯化钠固体,需加水________mL(水的密度为1
g·cm-3)。
(2)若称量氯化钠固体时指针向左偏转,则应________________直到天平平衡。
(3)实验中发现氯化钠固体已结块,为了较快地溶解,合理的方法有________(填序号)。
A.用玻璃棒搅拌
B.用玻璃棒将固体捣碎
C.适当地加热
(4)下列操作中可能导致配制氯化钠溶液的溶质质量分数偏大的是________(填序号)。
A.氯化钠中含有杂质
B.量取水时俯视
C.用内壁有少量水的烧杯溶解氯化钠
D.转移时,有少量溶液溅出
(5)取上述溶液10
g,需加________g水稀释,可得到5%的氯化钠溶液。
15.(15分)溶液在生产、生活中起着十分重要的作用。某学习小组的同学对溶液的性质进行探究。
【引发思考】
生理盐水是医疗上常用的一种溶液,100
mL生理盐水(其密度可近似为1
g/cm3)中含有0.9
g医用氯化钠,该溶液中溶质的质量分数为________。一瓶合格的生理盐水密封放置一段时间后
,不会出现浑浊现象,原因是________________________________。
【提出问题】
溶液的某些性质是否可以通过定量实验进行验证?
【查阅资料】
电导率传感器用于测量溶液的导电性强弱;一定条件下,电导率的大小能反映离子浓度的大小。
【实验探究1】
氯化钠溶于水形成溶液的过程中氯离子浓度、电导率的测定。
第一步:读取室温为26
℃,取100
mL蒸馏水,加入烧杯中,放入磁力搅拌器磁珠;
第二步:校准传感器,组装仪器,设定搅拌档位;
第三步:用氯离子传感器和电导率传感器同时采集数据,迅速将一定质量的氯化钠加入烧杯中。实验数据如图所示。
(第15题)
分析图1、图2的实验数据:
(1)ab段曲线呈这种形态的原因是_______________________________________。
(2)请说明实验过程中液体的电导率变化的原因___________________________
_________________________________________________________________。
【交流反思1】
如何通过实验验证氯化钠溶液是均一的?
请简要说明________________
______________________________________。
【实验探究2】
用氯离子传感器和电导率传感器同时采集数据,向一定体积、一定浓度的氯化钠溶液中慢慢加入等体积、一定浓度的硝酸银溶液,恰好完全反应(NaCl+AgNO3===NaNO3+AgCl↓)。
部分实验数据如图3所示。
【交流反思2】
推测c点时溶液的电导率是否为零,并说明理由________________________________________。
16.(7分)某学习小组在实验室中用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应过程中固体质量的变化如图所示。请计算:
(1)反应结束后生成氧气的质量为________g。
(2)冷却至室温,将剩余的固体溶解在85.1
g水中,充分溶解后过滤,计算所得不饱和溶液中溶质的质量分数。
(第16题)
答案
第Ⅰ卷
1.A 2.D 3.C 4.B 5.D
6.B 点拨:气球胀大,则烧瓶中的压强一定增大,即有气体生成或放热,符合题意的只有①③。
7.B 点拨:氢氧化钙的溶解度随温度的升高而减小,升温不能使其饱和溶液变成不饱和溶液,故A错;由于溶液具有均一性,因此B正确;20
℃时50
g水中溶解了18
g
NaCl,所得溶液不一定是饱和溶液,所以不能说明20
℃时NaCl的溶解度是36
g,故C错;将95
g
KCl溶液蒸干得到5
g
KCl固体,则原溶液中溶质质量分数为×100%≈5.3%,故D错。
8.A
9.B 点拨:①→②充分溶解后固体有剩余,②中溶液是饱和溶液,②加热得到③,③中没有固体剩余,③中溶液可能是饱和溶液,也可能是不饱和溶液。
10.D 点拨:硝酸铵溶于水,溶液温度降低,Y的饱和溶液出现浑浊,所以Y的溶解度随温度的降低而减小,所以Y的溶解度曲线为a曲线,故A错误;X物质的溶解度曲线是b,所以升温可使X的饱和溶液变浑浊,故B错误;X物质的溶解度随温度的降低而增大,X的饱和溶液从t2
℃降温到t1
℃,溶质的质量分数不变,故C错误;t3
℃时,Y物质的溶解度大于X物质的溶解度,所以若X、Y的饱和溶液质量相等,则溶剂质量X>Y,故D正确。
第Ⅱ卷
11.(1)酒精
(2)×100%
(3)樟脑;樟脑在酒精中的溶解度随温度的降低而减小
(4)虚假;天气瓶中的晶体变化只与温度变化有关(或装置密封,天气瓶无法反映除温度外的其他天气变化等)
12.(1)蒸发
(2)氧气
(3)①饱和
②×100%
③不变
④加水
点拨:(1)“煎炼而成”是指蒸发。
(2)硝酸钾的性质不稳定,受到撞击会发生分解反应生成一种可助燃的气体单质是氧气。
(3)a、b点在溶解度曲线上,是饱和溶液,c在溶解度曲线下方是不饱和溶液。
①a点对应的溶液是饱和溶液。故填:饱和。
②a点对应的溶液的溶质质量分数是×100%。
③将a点对应的溶液升温到70
℃,其溶质质量分数不变,但是变成不饱和溶液。
④欲使KNO3溶液的状态从b点转化为c点,即变成不饱和溶液,可采取的措施是加水。
13.(1)蒸发结晶
(2)氯化钙的溶解度随温度升高而增大较多,不易形成饱和溶液;
64
(3)A
(4)甲
14.(1)7.5;42.5
(2)减少氯化钠
(3)AC
(4)B
(5)20
15.【引发思考】
0.9%;溶液是均一的、稳定的
【实验探究1】
(1)氯化钠在水中逐渐溶解,溶液中氯离子浓度不断增大
(2)蒸馏水不导电,液体的电导率几乎为零,加入氯化钠后,固体逐渐溶解,溶液中离子浓度不断增大,溶液的电导率不断增大,当氯化钠全部溶解后,溶液中的离子浓度不变,溶液的电导率不变
【交流反思1】
测定氯化钠溶液中不同位置的氯离子浓度,数值相同(合理即可)
【交流反思2】
不为零,因为溶液中存在钠离子和硝酸根离子
点拨:【实验探究1】
(1)根据图像可知,ab段氯离子浓度在增大,说明氯化钠在水中逐渐溶解,电离后产生氯离子;
(2)对照图1图2两图,可以看出氯离子浓度增大,溶液电导率增大,当氯离子浓度达到一定浓度后不再发生变化,电导率也不再变化,说明电导率随离子浓度发生变化,未溶解氯化钠时,电导率几乎为零,随着氯化钠的溶解,氯离子浓度增大,电导率增大,当氯化钠全部溶解后,离子浓度不再改变,电导率不再发生变化;
【交流反思1】
测定不同位置溶液的氯离子浓度,根据数值判断溶液是否均一,各个点数值一样说明溶液是均一的;
【交流反思2】
c点时氯化钠与硝酸银反应生成了氯化银和硝酸钠,此时氯离子转变为沉淀,但是有硝酸钠存在,可以电离出钠离子和硝酸根离子,溶液可以导电。
16.(1)9.6
(2)解:设反应中生成氯化钾的质量为x。
2KClO32KCl+3O2↑
149
96
x
9.6
g
=
x=14.9
g
所得溶液的溶质质量分数为×100%=14.9%
答:略。
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
人教版九年级化学下册
名校优选精练
第九单元达标测试卷
时间:45分钟 满分:100分
班级:
姓名:
考号:
.
可能用到的相对原子质量 O:16 Cl:35.5 K:39
第Ⅰ卷
本卷共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一个选项符合题目要求。
1.下列液体去除油污效果最好的是( )
A.洗洁精
B.食盐水
C.白醋
D.自来水
2.下列是福建人民日常饮食中常见的物质,其中容器内所盛放的物质属于溶液的是( )
A.福州锅边糊
B.莆田鲜卤面
C.厦门沙茶面
D.建瓯福矛酒
3.下列有关溶液的叙述正确的是( )
A.食盐水倒出一半后浓度降低
B.果粒橙属于溶液
C.升温会降低二氧化碳在水中的溶解度
D.蔗糖可以无限地溶解在一定量的水中
4.某同学配制16%的氯化钠溶液来选种。如图所示的下列操作中正确的是( )
5.小龙同学在工具书中查到NaOH在水和酒精中的溶解度如表所示。通过分析他得出以下结论,其中不正确的是( )
20
℃
40
℃
水
109
g
129
g
酒精
17.3
g
40
g
A.温度和溶剂种类对NaOH的溶解度都有影响
B.NaOH易溶于水,也易溶于酒精
C.40
℃时,40
g
NaOH溶解在100
g酒精中达到饱和
D.将等质量40
℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20
℃,析出的晶体前者比后者多
6.如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀。表中的液体X和固体Y的组合,符合题意的是( )
(第6题)
①
②
③
④
X
稀盐酸
水
水
水
Y
大理石
氯化钠
氢氧化钠
硝酸铵
A.①②
B.①③
C.①③④
D.②③④
7.下列有关溶液的说法中正确的是( )
A.常温下将100
mL饱和Ca(OH)2溶液加热至50
℃,会使溶液由饱和溶液变为不饱和溶液
B.从100
mL
25%的硫酸溶液中取出10
mL,则取出的10
mL硫酸溶液溶质质量分数仍为25%
C.20
℃时,50
g水中溶解了18
g
NaCl,则20
℃时NaCl的溶解度为36
g
D.将95
g
KCl溶液蒸干得到5
g
KCl固体,则原溶液的溶质质量分数为5%
8.20
℃时,四个实验小组分别取不同质量的NaCl,逐渐加入到各盛有50
g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余NaCl的质量。记录数据如下表:
实验小组
第一组
第二组
第三组
第四组
水的质量/g
50
50
50
50
所取NaCl的质量/g
15
20
25
30
剩余NaCl的质量/g
0
2
7
12
下列说法错误的是( )
A.20
℃时,50
g
NaCl饱和溶液中含有18
g
NaCl
B.用蒸发的方法可以使不饱和溶液变成饱和溶液
C.第二组所得溶液的溶质与溶剂的质量比为9∶25
D.相同温度下,NaCl在水中的溶解度与水的质量无关
9.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
(第9题)
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
10.两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH4NO3固体,向两支试管中分别滴加适量水,现象如图1所示,结合图2(X、Y的溶解度曲线图)判断下列说法正确的是( )
(第10题)
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2
℃降温到t1
℃,溶质的质量分数变大
D.t3
℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
第Ⅱ卷
本卷共6题,共70分。
11.(12分)网红产品“天气瓶”(如图1)的制作步骤如下:
Ⅰ.将10
g樟脑溶于40
mL酒精,得溶液a(樟脑难溶于水);
Ⅱ.将2.5
g硝酸钾和2.5
g氯化铵溶于33
g水中,得溶液b;
Ⅲ.将a、b两种溶液混合、加热、搅拌直至澄清;
Ⅳ.混合液冷却至室温后,密封在玻璃容器内,即制得“天气瓶”。
根据上述步骤并结合图2的溶解度曲线,回答下列问题。
(第11题)
(1)溶液a中溶剂为________。
(2)溶液b中硝酸钾的质量分数为________________(列计算式)。
(3)瓶内出现的晶体数量会随气温的降低而增加。该晶体的成分是________,推断产生这种现象的原因是___________________________________________。
(4)图3是“天气瓶”的宣传图,根据其制作步骤,判断该宣传的真实性为________,理由是__________________________________________________
______________________________。
12.(13分)KNO3是一种重要的化工原料。
(1)宋代《开宝本草》中记载了KNO3的提纯方法
:“所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”,“霜”指KNO3,这里涉及化学实验基本操作方法:“以水淋汁”是指溶解,“煎炼而成”是指________。
(2)《天工开物》记载“凡研硝(KNO3)不以铁碾入石臼,相激火生,祸不可测”。
是指硝酸钾的性质不稳定,受到撞击会发生分解反应生成一种可助燃的气体单质是________。
(3)如图为KNO3的溶解度曲线,a、b在溶解度曲线上。
(第12题)
①a点对应的溶液是________(填“饱和”或“不饱和”)溶液。
②a点对应的溶液的溶质质量分数是________________________________(列计算式)。
③将a点对应的溶液升温到70
℃,其溶质质量分数________(填“变大”“变小”或“不变”)。
④欲使KNO3溶液的状态从b点转化为c点,可采取的措施是____________
____________________________________________________________。
13.(11分)海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程和氯化钠、氯化钙的溶解度表。
(第13题图1)
温度/℃
0
10
20
30
40
溶解度/g
氯化钠
35.7
35.8
36.0
36.3
36.6
氯化钙
59.5
65.0
74.5
100
128
请回答问题:
(1)将粗盐从海水中结晶出来的方法是________。
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是_____________________
_____________________________。40
℃时,50
g水中最多溶解氯化钙_____g。
(3)根据海水晒盐的原理,下列说法中正确的是________(填序号)。
A.海水进入贮水池,海水的成分基本不变
B.在蒸发池里,海水中水的质量逐渐增加
C.析出晶体后的母液是氯化钠的不饱和溶液
(4)溶解度曲线图2中,能表示氯化钙溶解度曲线的是________(填“甲”或“乙”)。
(第13题图2)
14.(12分)实验室配制一定溶质质量分数的氯化钠溶液的流程如图所示:
(第14题)
(1)应称量________g氯化钠固体,需加水________mL(水的密度为1
g·cm-3)。
(2)若称量氯化钠固体时指针向左偏转,则应________________直到天平平衡。
(3)实验中发现氯化钠固体已结块,为了较快地溶解,合理的方法有________(填序号)。
A.用玻璃棒搅拌
B.用玻璃棒将固体捣碎
C.适当地加热
(4)下列操作中可能导致配制氯化钠溶液的溶质质量分数偏大的是________(填序号)。
A.氯化钠中含有杂质
B.量取水时俯视
C.用内壁有少量水的烧杯溶解氯化钠
D.转移时,有少量溶液溅出
(5)取上述溶液10
g,需加________g水稀释,可得到5%的氯化钠溶液。
15.(15分)溶液在生产、生活中起着十分重要的作用。某学习小组的同学对溶液的性质进行探究。
【引发思考】
生理盐水是医疗上常用的一种溶液,100
mL生理盐水(其密度可近似为1
g/cm3)中含有0.9
g医用氯化钠,该溶液中溶质的质量分数为________。一瓶合格的生理盐水密封放置一段时间后
,不会出现浑浊现象,原因是________________________________。
【提出问题】
溶液的某些性质是否可以通过定量实验进行验证?
【查阅资料】
电导率传感器用于测量溶液的导电性强弱;一定条件下,电导率的大小能反映离子浓度的大小。
【实验探究1】
氯化钠溶于水形成溶液的过程中氯离子浓度、电导率的测定。
第一步:读取室温为26
℃,取100
mL蒸馏水,加入烧杯中,放入磁力搅拌器磁珠;
第二步:校准传感器,组装仪器,设定搅拌档位;
第三步:用氯离子传感器和电导率传感器同时采集数据,迅速将一定质量的氯化钠加入烧杯中。实验数据如图所示。
(第15题)
分析图1、图2的实验数据:
(1)ab段曲线呈这种形态的原因是_______________________________________。
(2)请说明实验过程中液体的电导率变化的原因___________________________
_________________________________________________________________。
【交流反思1】
如何通过实验验证氯化钠溶液是均一的?
请简要说明________________
______________________________________。
【实验探究2】
用氯离子传感器和电导率传感器同时采集数据,向一定体积、一定浓度的氯化钠溶液中慢慢加入等体积、一定浓度的硝酸银溶液,恰好完全反应(NaCl+AgNO3===NaNO3+AgCl↓)。
部分实验数据如图3所示。
【交流反思2】
推测c点时溶液的电导率是否为零,并说明理由________________________________________。
16.(7分)某学习小组在实验室中用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应过程中固体质量的变化如图所示。请计算:
(1)反应结束后生成氧气的质量为________g。
(2)冷却至室温,将剩余的固体溶解在85.1
g水中,充分溶解后过滤,计算所得不饱和溶液中溶质的质量分数。
(第16题)
答案
第Ⅰ卷
1.A 2.D 3.C 4.B 5.D
6.B 点拨:气球胀大,则烧瓶中的压强一定增大,即有气体生成或放热,符合题意的只有①③。
7.B 点拨:氢氧化钙的溶解度随温度的升高而减小,升温不能使其饱和溶液变成不饱和溶液,故A错;由于溶液具有均一性,因此B正确;20
℃时50
g水中溶解了18
g
NaCl,所得溶液不一定是饱和溶液,所以不能说明20
℃时NaCl的溶解度是36
g,故C错;将95
g
KCl溶液蒸干得到5
g
KCl固体,则原溶液中溶质质量分数为×100%≈5.3%,故D错。
8.A
9.B 点拨:①→②充分溶解后固体有剩余,②中溶液是饱和溶液,②加热得到③,③中没有固体剩余,③中溶液可能是饱和溶液,也可能是不饱和溶液。
10.D 点拨:硝酸铵溶于水,溶液温度降低,Y的饱和溶液出现浑浊,所以Y的溶解度随温度的降低而减小,所以Y的溶解度曲线为a曲线,故A错误;X物质的溶解度曲线是b,所以升温可使X的饱和溶液变浑浊,故B错误;X物质的溶解度随温度的降低而增大,X的饱和溶液从t2
℃降温到t1
℃,溶质的质量分数不变,故C错误;t3
℃时,Y物质的溶解度大于X物质的溶解度,所以若X、Y的饱和溶液质量相等,则溶剂质量X>Y,故D正确。
第Ⅱ卷
11.(1)酒精
(2)×100%
(3)樟脑;樟脑在酒精中的溶解度随温度的降低而减小
(4)虚假;天气瓶中的晶体变化只与温度变化有关(或装置密封,天气瓶无法反映除温度外的其他天气变化等)
12.(1)蒸发
(2)氧气
(3)①饱和
②×100%
③不变
④加水
点拨:(1)“煎炼而成”是指蒸发。
(2)硝酸钾的性质不稳定,受到撞击会发生分解反应生成一种可助燃的气体单质是氧气。
(3)a、b点在溶解度曲线上,是饱和溶液,c在溶解度曲线下方是不饱和溶液。
①a点对应的溶液是饱和溶液。故填:饱和。
②a点对应的溶液的溶质质量分数是×100%。
③将a点对应的溶液升温到70
℃,其溶质质量分数不变,但是变成不饱和溶液。
④欲使KNO3溶液的状态从b点转化为c点,即变成不饱和溶液,可采取的措施是加水。
13.(1)蒸发结晶
(2)氯化钙的溶解度随温度升高而增大较多,不易形成饱和溶液;
64
(3)A
(4)甲
14.(1)7.5;42.5
(2)减少氯化钠
(3)AC
(4)B
(5)20
15.【引发思考】
0.9%;溶液是均一的、稳定的
【实验探究1】
(1)氯化钠在水中逐渐溶解,溶液中氯离子浓度不断增大
(2)蒸馏水不导电,液体的电导率几乎为零,加入氯化钠后,固体逐渐溶解,溶液中离子浓度不断增大,溶液的电导率不断增大,当氯化钠全部溶解后,溶液中的离子浓度不变,溶液的电导率不变
【交流反思1】
测定氯化钠溶液中不同位置的氯离子浓度,数值相同(合理即可)
【交流反思2】
不为零,因为溶液中存在钠离子和硝酸根离子
点拨:【实验探究1】
(1)根据图像可知,ab段氯离子浓度在增大,说明氯化钠在水中逐渐溶解,电离后产生氯离子;
(2)对照图1图2两图,可以看出氯离子浓度增大,溶液电导率增大,当氯离子浓度达到一定浓度后不再发生变化,电导率也不再变化,说明电导率随离子浓度发生变化,未溶解氯化钠时,电导率几乎为零,随着氯化钠的溶解,氯离子浓度增大,电导率增大,当氯化钠全部溶解后,离子浓度不再改变,电导率不再发生变化;
【交流反思1】
测定不同位置溶液的氯离子浓度,根据数值判断溶液是否均一,各个点数值一样说明溶液是均一的;
【交流反思2】
c点时氯化钠与硝酸银反应生成了氯化银和硝酸钠,此时氯离子转变为沉淀,但是有硝酸钠存在,可以电离出钠离子和硝酸根离子,溶液可以导电。
16.(1)9.6
(2)解:设反应中生成氯化钾的质量为x。
2KClO32KCl+3O2↑
149
96
x
9.6
g
=
x=14.9
g
所得溶液的溶质质量分数为×100%=14.9%
答:略。
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
同课章节目录
