质量守恒定律——2021-2022学年华东师大版科学九年级上学期(含答案)
文档属性
| 名称 | 质量守恒定律——2021-2022学年华东师大版科学九年级上学期(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 119.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-09-16 00:00:00 | ||
图片预览

文档简介
2021-2022学年华师大版科学质量守恒定律
一.选择题(共6小题)
1.某化学兴趣小组的同学用右图探究质量守恒定律,结果测得反应前后质量不相等.他们更换药品后重新实验,得出了正确的结论.他们选用的试剂是( )
A.稀盐酸和镁条
B.碳酸钠和稀硫酸
C.稀盐酸和铜粉
D.碳酸钠和氯化钙
2.汽车排气管中安装催化转化器可减少尾气污染,其反应原理是2CO+2NO
2X+N2,其中X的化学式是( )
A.NO2
B.CO2
C.H2O
D.C
3.如图为某化学反应中各物质质量与时间的关系图,下列判断不正确的是( )
A.丁可能是催化剂
B.乙和丙是生成物
C.该反应属于分解反应
D.ts时,甲的质量一定等于乙和丙的质量之和
4.在一个密闭的容器有甲、乙、丙、丁四种物质,通过电火花引燃后,充分发生反应.经测定,容器内反应前后各物质的质量如表,若甲的相对分子质量为n,丁的相对分子质量为2n,则下列说法正确的是( )
物质
甲
乙
丙
丁
反应前质量/g
4
10
1
25
反应后质量/g
未测值
21
10
9
A.该反应中甲与丁的化学计量数之比为1:2
B.该反应中生成乙与丁的质量比为21:10
C.标准未测值为4g
D.该反应一定是置换反应
5.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:
下列说法正确的是( )
A.乙可能是单质
B.在该反应中丁一定没有参加化学反应
C.该反应可能是置换反应
D.甲和乙的质量之和一定等于生成丙的质量
6.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
A.丁是该反应的催化剂
B.甲、乙的质量之和一定等于生成丙的质量
C.该反应中甲、丙的质量比为7:10
D.该反应中乙、丙的质量比为3:17
二.填空题(共5小题)
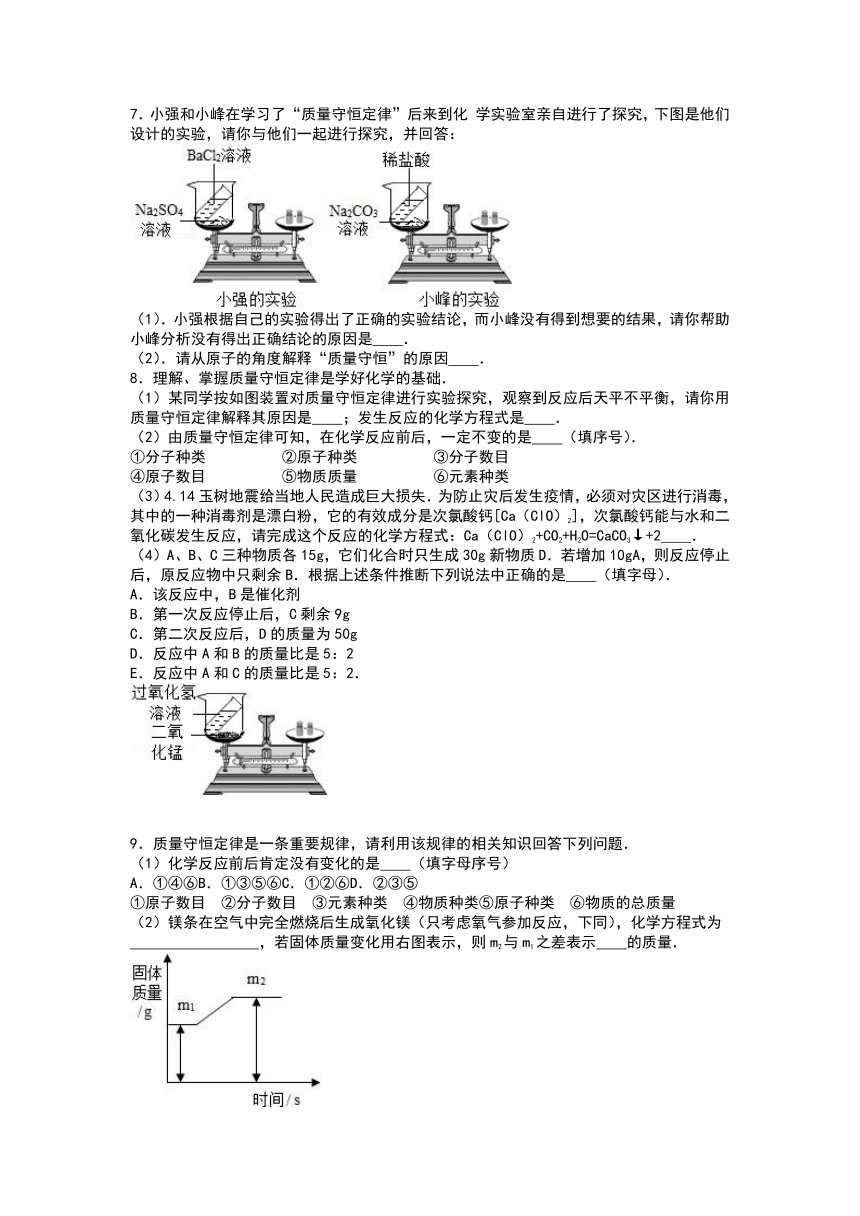
7.小强和小峰在学习了“质量守恒定律”后来到化
学实验室亲自进行了探究,下图是他们设计的实验,请你与他们一起进行探究,并回答:
(1).小强根据自己的实验得出了正确的实验结论,而小峰没有得到想要的结果,请你帮助小峰分析没有得出正确结论的原因是 .
(2).请从原子的角度解释“质量守恒”的原因 .
8.理解、掌握质量守恒定律是学好化学的基础.
(1)某同学按如图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡,请你用质量守恒定律解释其原因是 ;发生反应的化学方程式是 .
(2)由质量守恒定律可知,在化学反应前后,一定不变的是 (填序号).
①分子种类
②原子种类
③分子数目
④原子数目
⑤物质质量
⑥元素种类
(3)4.14玉树地震给当地人民造成巨大损失.为防止灾后发生疫情,必须对灾区进行消毒,其中的一种消毒剂是漂白粉,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙能与水和二氧化碳发生反应,请完成这个反应的化学方程式:Ca(ClO)2+CO2+H2O=CaCO3↓+2 .
(4)A、B、C三种物质各15g,它们化合时只生成30g新物质D.若增加10gA,则反应停止后,原反应物中只剩余B.根据上述条件推断下列说法中正确的是 (填字母).
A.该反应中,B是催化剂
B.第一次反应停止后,C剩余9g
C.第二次反应后,D的质量为50g
D.反应中A和B的质量比是5:2
E.反应中A和C的质量比是5:2.
9.质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.
(1)化学反应前后肯定没有变化的是 (填字母序号)
A.①④⑥B.①③⑤⑥C.①②⑥D.②③⑤
①原子数目
②分子数目
③元素种类
④物质种类⑤原子种类
⑥物质的总质量
(2)镁条在空气中完全燃烧后生成氧化镁(只考虑氧气参加反应,下同),化学方程式为
,若固体质量变化用右图表示,则m2与m1之差表示 的质量.
10.在3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O反应中,则问答:
(1)水分子由
构成;该反应涉及的物质中,直接由原子构成的是
;
(2)X的化学式为
;HNO3中N元素的化合价为 ;Cu(NO3)2中铜、氧元素质量比为
.
11.从宏观和微观上理解质量守恒定律可归纳为五个“不变”、两个“一定变”和一个“可能变”.请按要求填写正确选项的序号.
①物质的种类
②元素的种类
③原子的种类
④原子的质量
⑤原子的数目
⑥分子的种类
⑦分子的数目
⑧反应物和生成物的总质量
(1)五个“不变”:从宏观上看,
和 不变;从微观上看, 、 和 不变.
(2)两个“一定变”:从宏观上看,
一定变;从微观上看,
一定变.
(3)一个“可能变”:
可能变.
三.实验探究题(共1小题)
12.为了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分别设计了下面两个实验,请根据图示回答问题:
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间;
两种物质反应后,托盘天平的指针
(填“向左”、“向右”或“不”)偏转,原因是
;
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量
;
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在
装置中进行。
(4)从微观角度分析,在化学反应前后一定不变的是
(填序号)。
①原子种类②分子种类③原子数目④分子质量⑤分子数目⑥原子质量
四.解答题(共2小题)
13.
2014年7月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚.将30克邻叔丁基苯酚完全燃烧,生成88克CO2和25.2克H2O.已知邻叔丁基苯酚的相对分子质量为150,求:
(1)30克邻叔丁基苯酚中含碳元素
克,氢元素
克.
(2)邻叔丁基苯酚的化学式为
.
14.一定条件下,4.8克甲烷与16.0克氧气恰好完全反应,生成10.8克水,4.4克二氧化碳及另一种物质,写出该反应的化学方程式 .
2021-2022学年华师大版科学质量守恒定律
参考答案与试题解析
一.选择题(共6小题)
1.D
2.B.
3.D.
4.A
5.A.
6.D.
二.填空题(共5小题)
7.(1)反应生成的气体逸散于空气中
(2)化学反应前后,原子的种类、数量和质量不变.
8.(1)根据质量守恒定律,该反应中参加反应的H2O2的质量等于反应后生成的H2O和O2的质量之和,该实验未在密闭容器中进行,O2逸散到空气中,所以天平不平衡(该反应有气体生成或实验未在密闭容器中进行,答案合理给分);2H2O22H2O+O2↑;
(2)②④⑥;
(3)HClO;
(4)CD.
9.(1)B;
(2)2Mg+O22MgO,参加反应的氧气的质量.
10.(1)氢原子、氧原子;
Cu;(2)NO;+5;
2:3.
11.(1)②;⑧;③;④;⑤;(2)①;⑥;(3)⑦.
三.实验探究题(共1小题)
12.解:(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间;
两种物质反应后,托盘天平的指针向右偏转,原因是:锌和稀硫酸反应生成的氢气逸出;故答案为:向右;锌和稀硫酸反应生成的氢气逸出;
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量不变;故答案为:不变;
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在密闭装置中进行;故答案为:密闭;
(4)从微观角度分析,在化学反应前后一定不变的是:①原子种类、③原子数目、⑥原子质量;故答案为:①③⑥;
四.解答题(共2小题)
13.解:(1)根据质量守恒定律,将30克邻叔丁基苯酚完全燃烧后碳元素和氢元素的质量不变,所以88克CO2中碳元素的质量等于30克邻叔丁基苯酚中碳元素的质量,25.2克H2O中的氢元素的质量等于30克邻叔丁基苯酚中氢元素的质量.
故:碳元素的质量为:88g××100%=24g;
氢元素的质量为:25.2g×=2.8g;
(2)30克邻叔丁基苯酚中氧元素的质量为:30g﹣24g﹣2.8g=3.2g;
设邻叔丁基苯酚的化学式为CxHyOz,
m(C):m(H):m(O)=12x:y:16z=24:2.8:3.2
解得:x:y:z=10:14:1
又因为邻叔丁基苯酚的相对分子质量为150,12×10+1×14+16×1=150,所以邻叔丁基苯酚的化学式为:C10H14O.
故答案为:(1)24,2.8;
(2)C10H14O.
14.解:甲烷在氧气中不完全燃烧生成一氧化碳、二氧化碳、水,一氧化碳的质量为:4.8g+16g﹣10.8g﹣4.4g=5.6g,各物质的分子个数比为:
::::=3:5:2:1:6
化学方程式为:3CH4+5O2═2CO+CO2+6H2O;
故答案为:3CH4+5O2═2CO+CO2+6H2O.
一.选择题(共6小题)
1.某化学兴趣小组的同学用右图探究质量守恒定律,结果测得反应前后质量不相等.他们更换药品后重新实验,得出了正确的结论.他们选用的试剂是( )
A.稀盐酸和镁条
B.碳酸钠和稀硫酸
C.稀盐酸和铜粉
D.碳酸钠和氯化钙
2.汽车排气管中安装催化转化器可减少尾气污染,其反应原理是2CO+2NO
2X+N2,其中X的化学式是( )
A.NO2
B.CO2
C.H2O
D.C
3.如图为某化学反应中各物质质量与时间的关系图,下列判断不正确的是( )
A.丁可能是催化剂
B.乙和丙是生成物
C.该反应属于分解反应
D.ts时,甲的质量一定等于乙和丙的质量之和
4.在一个密闭的容器有甲、乙、丙、丁四种物质,通过电火花引燃后,充分发生反应.经测定,容器内反应前后各物质的质量如表,若甲的相对分子质量为n,丁的相对分子质量为2n,则下列说法正确的是( )
物质
甲
乙
丙
丁
反应前质量/g
4
10
1
25
反应后质量/g
未测值
21
10
9
A.该反应中甲与丁的化学计量数之比为1:2
B.该反应中生成乙与丁的质量比为21:10
C.标准未测值为4g
D.该反应一定是置换反应
5.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:
下列说法正确的是( )
A.乙可能是单质
B.在该反应中丁一定没有参加化学反应
C.该反应可能是置换反应
D.甲和乙的质量之和一定等于生成丙的质量
6.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
A.丁是该反应的催化剂
B.甲、乙的质量之和一定等于生成丙的质量
C.该反应中甲、丙的质量比为7:10
D.该反应中乙、丙的质量比为3:17
二.填空题(共5小题)
7.小强和小峰在学习了“质量守恒定律”后来到化
学实验室亲自进行了探究,下图是他们设计的实验,请你与他们一起进行探究,并回答:
(1).小强根据自己的实验得出了正确的实验结论,而小峰没有得到想要的结果,请你帮助小峰分析没有得出正确结论的原因是 .
(2).请从原子的角度解释“质量守恒”的原因 .
8.理解、掌握质量守恒定律是学好化学的基础.
(1)某同学按如图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡,请你用质量守恒定律解释其原因是 ;发生反应的化学方程式是 .
(2)由质量守恒定律可知,在化学反应前后,一定不变的是 (填序号).
①分子种类
②原子种类
③分子数目
④原子数目
⑤物质质量
⑥元素种类
(3)4.14玉树地震给当地人民造成巨大损失.为防止灾后发生疫情,必须对灾区进行消毒,其中的一种消毒剂是漂白粉,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙能与水和二氧化碳发生反应,请完成这个反应的化学方程式:Ca(ClO)2+CO2+H2O=CaCO3↓+2 .
(4)A、B、C三种物质各15g,它们化合时只生成30g新物质D.若增加10gA,则反应停止后,原反应物中只剩余B.根据上述条件推断下列说法中正确的是 (填字母).
A.该反应中,B是催化剂
B.第一次反应停止后,C剩余9g
C.第二次反应后,D的质量为50g
D.反应中A和B的质量比是5:2
E.反应中A和C的质量比是5:2.
9.质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.
(1)化学反应前后肯定没有变化的是 (填字母序号)
A.①④⑥B.①③⑤⑥C.①②⑥D.②③⑤
①原子数目
②分子数目
③元素种类
④物质种类⑤原子种类
⑥物质的总质量
(2)镁条在空气中完全燃烧后生成氧化镁(只考虑氧气参加反应,下同),化学方程式为
,若固体质量变化用右图表示,则m2与m1之差表示 的质量.
10.在3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O反应中,则问答:
(1)水分子由
构成;该反应涉及的物质中,直接由原子构成的是
;
(2)X的化学式为
;HNO3中N元素的化合价为 ;Cu(NO3)2中铜、氧元素质量比为
.
11.从宏观和微观上理解质量守恒定律可归纳为五个“不变”、两个“一定变”和一个“可能变”.请按要求填写正确选项的序号.
①物质的种类
②元素的种类
③原子的种类
④原子的质量
⑤原子的数目
⑥分子的种类
⑦分子的数目
⑧反应物和生成物的总质量
(1)五个“不变”:从宏观上看,
和 不变;从微观上看, 、 和 不变.
(2)两个“一定变”:从宏观上看,
一定变;从微观上看,
一定变.
(3)一个“可能变”:
可能变.
三.实验探究题(共1小题)
12.为了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分别设计了下面两个实验,请根据图示回答问题:
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间;
两种物质反应后,托盘天平的指针
(填“向左”、“向右”或“不”)偏转,原因是
;
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量
;
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在
装置中进行。
(4)从微观角度分析,在化学反应前后一定不变的是
(填序号)。
①原子种类②分子种类③原子数目④分子质量⑤分子数目⑥原子质量
四.解答题(共2小题)
13.
2014年7月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚.将30克邻叔丁基苯酚完全燃烧,生成88克CO2和25.2克H2O.已知邻叔丁基苯酚的相对分子质量为150,求:
(1)30克邻叔丁基苯酚中含碳元素
克,氢元素
克.
(2)邻叔丁基苯酚的化学式为
.
14.一定条件下,4.8克甲烷与16.0克氧气恰好完全反应,生成10.8克水,4.4克二氧化碳及另一种物质,写出该反应的化学方程式 .
2021-2022学年华师大版科学质量守恒定律
参考答案与试题解析
一.选择题(共6小题)
1.D
2.B.
3.D.
4.A
5.A.
6.D.
二.填空题(共5小题)
7.(1)反应生成的气体逸散于空气中
(2)化学反应前后,原子的种类、数量和质量不变.
8.(1)根据质量守恒定律,该反应中参加反应的H2O2的质量等于反应后生成的H2O和O2的质量之和,该实验未在密闭容器中进行,O2逸散到空气中,所以天平不平衡(该反应有气体生成或实验未在密闭容器中进行,答案合理给分);2H2O22H2O+O2↑;
(2)②④⑥;
(3)HClO;
(4)CD.
9.(1)B;
(2)2Mg+O22MgO,参加反应的氧气的质量.
10.(1)氢原子、氧原子;
Cu;(2)NO;+5;
2:3.
11.(1)②;⑧;③;④;⑤;(2)①;⑥;(3)⑦.
三.实验探究题(共1小题)
12.解:(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间;
两种物质反应后,托盘天平的指针向右偏转,原因是:锌和稀硫酸反应生成的氢气逸出;故答案为:向右;锌和稀硫酸反应生成的氢气逸出;
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量不变;故答案为:不变;
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在密闭装置中进行;故答案为:密闭;
(4)从微观角度分析,在化学反应前后一定不变的是:①原子种类、③原子数目、⑥原子质量;故答案为:①③⑥;
四.解答题(共2小题)
13.解:(1)根据质量守恒定律,将30克邻叔丁基苯酚完全燃烧后碳元素和氢元素的质量不变,所以88克CO2中碳元素的质量等于30克邻叔丁基苯酚中碳元素的质量,25.2克H2O中的氢元素的质量等于30克邻叔丁基苯酚中氢元素的质量.
故:碳元素的质量为:88g××100%=24g;
氢元素的质量为:25.2g×=2.8g;
(2)30克邻叔丁基苯酚中氧元素的质量为:30g﹣24g﹣2.8g=3.2g;
设邻叔丁基苯酚的化学式为CxHyOz,
m(C):m(H):m(O)=12x:y:16z=24:2.8:3.2
解得:x:y:z=10:14:1
又因为邻叔丁基苯酚的相对分子质量为150,12×10+1×14+16×1=150,所以邻叔丁基苯酚的化学式为:C10H14O.
故答案为:(1)24,2.8;
(2)C10H14O.
14.解:甲烷在氧气中不完全燃烧生成一氧化碳、二氧化碳、水,一氧化碳的质量为:4.8g+16g﹣10.8g﹣4.4g=5.6g,各物质的分子个数比为:
::::=3:5:2:1:6
化学方程式为:3CH4+5O2═2CO+CO2+6H2O;
故答案为:3CH4+5O2═2CO+CO2+6H2O.
