电解池原理及其应用
图片预览







文档简介
(共28张PPT)
电解池原理及其应用
【复习目标】
1、掌握电解池的概念及原理
2、学会正确书写电极反应及总反应方程式, 掌握常见离子放电的规律。
【复习重点】
电解池的概念及原理
一、电解池原理
1.定义:
(1)直流电源
(2)电解质溶液或熔融电解质
(3)固体电极材料(活性或惰性)
电能转化为化学能的装置为电解池.
2.构成
3.电极名称:
与电源负极相连的电极为阴极
与电源正极相连的电极为阳极
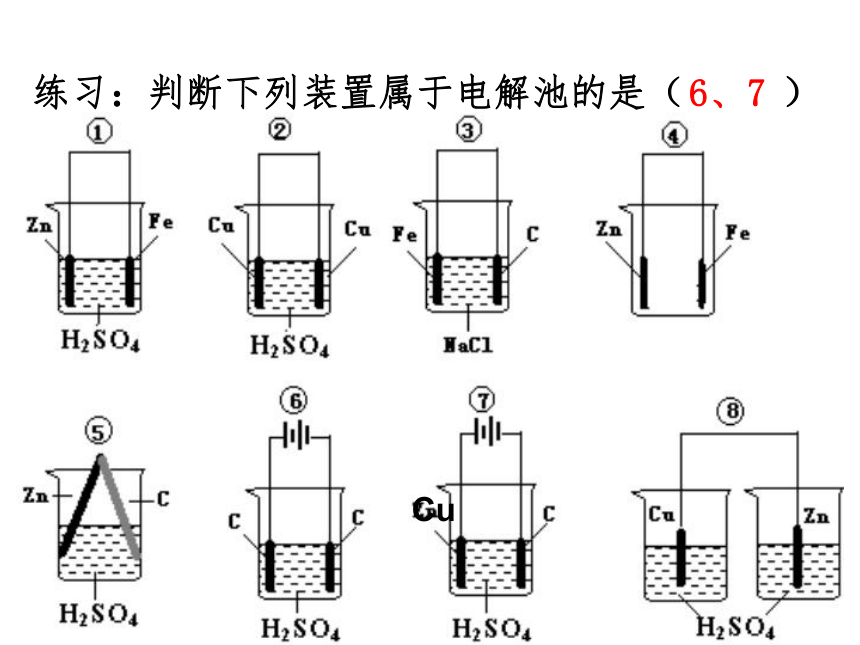
练习:判断下列装置属于电解池的是( )
Cu
6、7
4.电子、离子定向移动方向及反应
“电子由负极流向阴极,由阳极流回正极”
电解池
必发生
得电子的
还原反应
必发生
失电子的
氧化反应
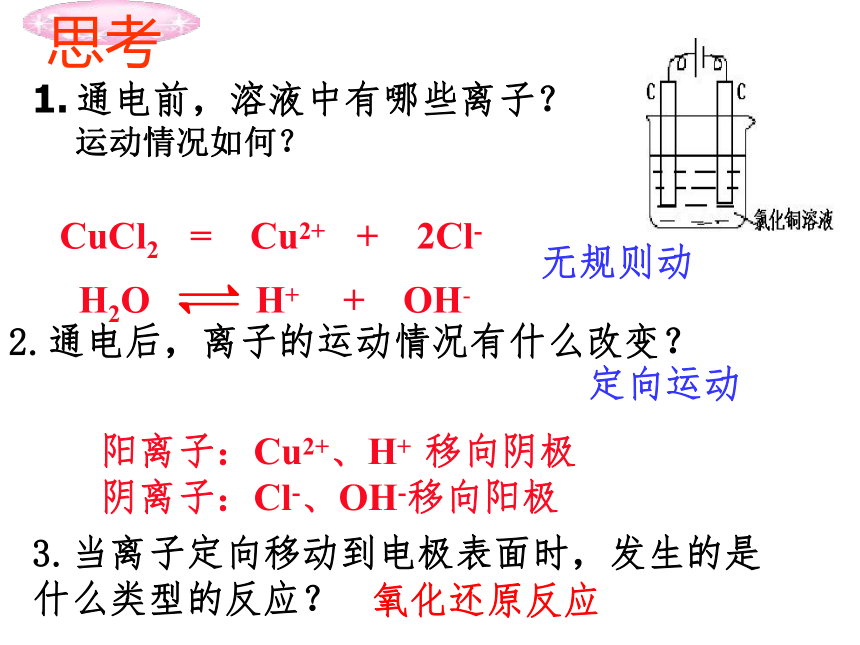
通电前,溶液中有哪些离子?运动情况如何?
思考
3.当离子定向移动到电极表面时,发生的是什么类型的反应?
2.通电后,离子的运动情况有什么改变?
CuCl2 = Cu2+ + 2Cl-
H2O H+ + OH-
阳离子:Cu2+、H+ 移向阴极
阴离子:Cl-、OH-移向阳极
无规则动
定向运动
氧化还原反应
4、指出该装置中电解池的阴阳极,
写出电极反应式及总反应的化学方
程式。
5、在CuCl2溶液中有自由移动的Cu2+、Cl-、H+、OH-,为什么只有Cu2+、Cl-得失电子,而H+、OH-却不能或很难在两极上得失电子呢?在阴、阳极上,离子的放电顺序又是怎样的?
阳极:2Cl- _ 2e- = Cl2 ↑
阴极:Cu 2++ 2e- = Cu
总反应:CuCl2 Cl2 ↑+ Cu
5.离子放电顺序及电解产物的判断
活泼金属阳极>S2->I->Br->Cl->OH->含氧酸根
(1)阳极上(氧化反应)
(2)阴极上(还原反应)
无论是惰性电极还是金属电极都不参与电极反应,发生反应的是溶液中的阳离子。阳离子在阴极上放电顺序是:
上述顺序基本上是金属活动性顺序,越活泼的金属,其阳离子越难得到电子,但Fe3+氧化性较Cu2+强。
Ag+>Hg2+>Fe3+>Cu2+ > H+>Pb2+>Sn2+>Fe2+>Zn2+ > Al3+>Mg2+>Na+>Ca2+>K+
完成下列溶液的电极反应(以石墨为电极电解)
(1)NaOH溶液:
(2)HCI溶液:
知识反馈
实例
电极反应
浓度
PH值
复原
实例
电极反应
浓度
PH值
复原
NaOH溶液
阳极: 4OH-_ 4e- = 2H2O+O2 ↑
阴极: 4H ++ 4e- = 2H2 ↑
变大
变
大
加
H2O
阳极C
阴极C
氧气
氢
气
NaOH溶液
2H2O 2H2 ↑ + O2 ↑
电解
实例
电极反应
浓度
PH值
复原
HCl
溶液
阳极:2Cl--2 e- =Cl2↑
阴极:2H+ + 2e-=H2
减小
增大
HCl
2 HCl H2 ↑ +Cl2↑
电解
阳极C
阴极C
氯气
氢
气
盐酸溶液
从H+ 、Cu2+ 、Na+ 、Cl-、SO42-五种离子中选出两种离子组成电解质,按下列要求进行电解,用电解质的化学式填空(使用惰性电极电解)
(1)电解过程中溶液的pH增大的有_______ (2)电解过程中溶液的pH减小 的有 (3)电解过程中溶液的pH不变的有 。
电解时有何规律?请小结
NaCl 、HCl
CuSO4、H2SO4
Na2SO4
例题:
(1)电解时,只生成H2而不生成O2,则溶液的pH 。
(2)电解时,只生成O2而不生成H2,则溶液的pH 。
(3)电解时,既生成H2又生成O2,则实际为电解水。
①若为酸性 pH ,
②若碱性溶液,则溶液的pH ,
③若为中性,则pH 。
增大
减小
减小
增大
不变
7.电解过程中溶液pH的变化规律
练 习:下图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是 ( )
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的PH值逐渐减小
D.CuSO4溶液的PH值不变
a
X Y
b
Pt
Cu
CuSO4溶液
NaCl和酚酞溶液
AC
练习:
(2004广东、广西) PH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的PH>a,则该电解质可能是( )
A.NaOH B.H2SO4
C.AgNO3 D.Na2SO4
A
分析电解反应的一般思路:
明确溶液中存在哪些离子
根据阴阳离子放电顺序及阳极氧化、阴极还原分析得出产物
阴阳两极附近有哪些离子
小结
想一想?
如果要在某铁制品表面镀上一层银,请你选择合适的电极材料和电镀液,并写出电极反应方程式。
阴极——某铁制品
阳极——金属银
电镀液——含有硝酸银的溶液
阳极:Ag - e- =Ag+
阴极:Ag++e- = Ag
溶液中离子浓度不变
(一)电镀
1、定义:
利用电解原理在某些金属的表面镀上一薄层其它金属或是合金的过程。
2、目的:
4、电镀的特点:
3、电镀材料的选择:
阴极——镀件
电镀液——含有镀层金属离子的溶液
阳极——镀层金属
使金属增强抗腐蚀的能力,增加美观和表面硬度。
1)阳极本身参加电极反应
2)电解质溶液的浓度保持不变
二、电解池原理的应用
(二)铜的电解精炼
阳极:
Cu - 2e- = Cu2+
阴极:
Cu2++ 2e- = Cu
杂质比铜活泼的Zn、Ni、Fe等:
Zn - 2e- = Zn2+
Ni - 2e- = Ni 2+
Fe - 2e- = Fe2+
活泼性在铜之后的银、金等:
还原性比铜差的,不能失去电子,它们以单质的形式留在溶液中,成为阳极泥。
电解质溶液硫酸铜的浓度略有减小。
(三)氯碱工业
(1)在NaCl溶液中,NaCl电离出 ,H2O电离出 。
通电后,在电场的作用下, 向阴极移动,
向阳极移动。
在阳极,由于 容易失去电子,被氧化生成 。
阳极方程式: ;
(2)在阴极,由于 容易得到电子被还原生成 .
使H2O 电离向右移动,因此阴极 浓度增大 PH 。
阴极方程式: 。
Na+、Cl-
H+、OH-
Cl-、OH-
Cl-
Cl2
H+
H2
OH-
增大
Na+、H+
2Cl- - 2e- =Cl2
2H+ + 2e- = H2
总化学方式: ;
总离子方程式: .
(3)电解前向溶液中滴加酚酞,通电后现象为:
___________ ,两极极板上都有气体产生,如何检验气体的种类?
阴极附近的溶液无色变为红色
阳极:把湿润的碘化钾淀粉试纸放在阳极附近,产生气体可以使湿润KI淀粉试纸变蓝色.
NaOH
2
H
Cl
O
H
2
NaCl
2
2
2
2
电解
+
+
+
OH
2
H
Cl
O
H
2
Cl
2
2
2
2
电解
+
+
+
练习:金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是 ( )
(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阳极发生还原反应,其电极反应式:
Ni2+ + 2e— = Ni
B.电解过程中,阳极质量的减少与阴极质量的增加
相等
C.电解后,溶液中存在的金属阳离子只有Fe2+ 和
Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
D
练习:
用两只惰性电极插入100mLCuSO4溶液中,通电电解。当溶液的pH值由6.0下降到2.0 (电解过程中溶液体积变化忽略不计),阴极析出铜的质量( )
A.16 mg B.32 mg C.64 mg D.128mg
B
(三)有关电解的计算——电子守恒规律应用
再见
(四)达标检测
1、下列叙述中不正确的是 ( B )
A.电解池的阳极上发生氧化反应,阴极上发生还原反应
B.原电池跟电解池连接后,电子从电池负极流向电解池阳极
C.电镀时,电镀池里的阳极材料发生氧化作用
D.电解饱和食盐水时,阴极得到氢氧化钠溶液和氢
2、用惰性电极实现电解,下列说法正确的是( D )
A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比
为1:2
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比
为1:1
3、用惰性电极电解下列溶液,电解一段时间后,电解液的pH增大
了的是 ( B )
A、H2SO4 B、KOH C、AgNO3 D、Na2SO4
4、关于电解NaCI水溶液,下列叙述正确的是( B )
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴人KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴人酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后落液呈中性
5、下列描述中,不符合生产实际的是( A )
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
6、把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电
解槽串联,在一定条件下通电一段时间后,析出钾、
镁、铝的物质的量之比为( D )
A.1︰2︰3 B.3︰2︰1
C.6︰3︰1 D.6︰3︰2
7、从H+ 、Cu2+ 、Na+ 、SO42- 、 Cl -五种离子中选择适
当的离子组成电解质,符合下列要求。
(1)以石墨棒为电极,电解时电解质质量减小,水量不
变,应选用的电解质是_________
(2)以石墨棒为电极,电解时电解质质量不变,水量减
小,应选用的电解质是_________ (3)以石墨棒为阳
极,铁棒为阴极,电解时电解质质量和水量都减小,应
选用的电解质是_________
8、如下图所示的装置,C、D、E、F、X、Y都是惰性电极。
将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下
问题:
(1) 电源A极的名称是_______。
(2)甲装置中电解反应的总化学方程式是______________________ ___。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______________。
(4)欲用丙装置给铜镀银,G应该是_______,电镀液的主要成分是_________(填化学式)。
电解池原理及其应用
【复习目标】
1、掌握电解池的概念及原理
2、学会正确书写电极反应及总反应方程式, 掌握常见离子放电的规律。
【复习重点】
电解池的概念及原理
一、电解池原理
1.定义:
(1)直流电源
(2)电解质溶液或熔融电解质
(3)固体电极材料(活性或惰性)
电能转化为化学能的装置为电解池.
2.构成
3.电极名称:
与电源负极相连的电极为阴极
与电源正极相连的电极为阳极
练习:判断下列装置属于电解池的是( )
Cu
6、7
4.电子、离子定向移动方向及反应
“电子由负极流向阴极,由阳极流回正极”
电解池
必发生
得电子的
还原反应
必发生
失电子的
氧化反应
通电前,溶液中有哪些离子?运动情况如何?
思考
3.当离子定向移动到电极表面时,发生的是什么类型的反应?
2.通电后,离子的运动情况有什么改变?
CuCl2 = Cu2+ + 2Cl-
H2O H+ + OH-
阳离子:Cu2+、H+ 移向阴极
阴离子:Cl-、OH-移向阳极
无规则动
定向运动
氧化还原反应
4、指出该装置中电解池的阴阳极,
写出电极反应式及总反应的化学方
程式。
5、在CuCl2溶液中有自由移动的Cu2+、Cl-、H+、OH-,为什么只有Cu2+、Cl-得失电子,而H+、OH-却不能或很难在两极上得失电子呢?在阴、阳极上,离子的放电顺序又是怎样的?
阳极:2Cl- _ 2e- = Cl2 ↑
阴极:Cu 2++ 2e- = Cu
总反应:CuCl2 Cl2 ↑+ Cu
5.离子放电顺序及电解产物的判断
活泼金属阳极>S2->I->Br->Cl->OH->含氧酸根
(1)阳极上(氧化反应)
(2)阴极上(还原反应)
无论是惰性电极还是金属电极都不参与电极反应,发生反应的是溶液中的阳离子。阳离子在阴极上放电顺序是:
上述顺序基本上是金属活动性顺序,越活泼的金属,其阳离子越难得到电子,但Fe3+氧化性较Cu2+强。
Ag+>Hg2+>Fe3+>Cu2+ > H+>Pb2+>Sn2+>Fe2+>Zn2+ > Al3+>Mg2+>Na+>Ca2+>K+
完成下列溶液的电极反应(以石墨为电极电解)
(1)NaOH溶液:
(2)HCI溶液:
知识反馈
实例
电极反应
浓度
PH值
复原
实例
电极反应
浓度
PH值
复原
NaOH溶液
阳极: 4OH-_ 4e- = 2H2O+O2 ↑
阴极: 4H ++ 4e- = 2H2 ↑
变大
变
大
加
H2O
阳极C
阴极C
氧气
氢
气
NaOH溶液
2H2O 2H2 ↑ + O2 ↑
电解
实例
电极反应
浓度
PH值
复原
HCl
溶液
阳极:2Cl--2 e- =Cl2↑
阴极:2H+ + 2e-=H2
减小
增大
HCl
2 HCl H2 ↑ +Cl2↑
电解
阳极C
阴极C
氯气
氢
气
盐酸溶液
从H+ 、Cu2+ 、Na+ 、Cl-、SO42-五种离子中选出两种离子组成电解质,按下列要求进行电解,用电解质的化学式填空(使用惰性电极电解)
(1)电解过程中溶液的pH增大的有_______ (2)电解过程中溶液的pH减小 的有 (3)电解过程中溶液的pH不变的有 。
电解时有何规律?请小结
NaCl 、HCl
CuSO4、H2SO4
Na2SO4
例题:
(1)电解时,只生成H2而不生成O2,则溶液的pH 。
(2)电解时,只生成O2而不生成H2,则溶液的pH 。
(3)电解时,既生成H2又生成O2,则实际为电解水。
①若为酸性 pH ,
②若碱性溶液,则溶液的pH ,
③若为中性,则pH 。
增大
减小
减小
增大
不变
7.电解过程中溶液pH的变化规律
练 习:下图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是 ( )
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的PH值逐渐减小
D.CuSO4溶液的PH值不变
a
X Y
b
Pt
Cu
CuSO4溶液
NaCl和酚酞溶液
AC
练习:
(2004广东、广西) PH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的PH>a,则该电解质可能是( )
A.NaOH B.H2SO4
C.AgNO3 D.Na2SO4
A
分析电解反应的一般思路:
明确溶液中存在哪些离子
根据阴阳离子放电顺序及阳极氧化、阴极还原分析得出产物
阴阳两极附近有哪些离子
小结
想一想?
如果要在某铁制品表面镀上一层银,请你选择合适的电极材料和电镀液,并写出电极反应方程式。
阴极——某铁制品
阳极——金属银
电镀液——含有硝酸银的溶液
阳极:Ag - e- =Ag+
阴极:Ag++e- = Ag
溶液中离子浓度不变
(一)电镀
1、定义:
利用电解原理在某些金属的表面镀上一薄层其它金属或是合金的过程。
2、目的:
4、电镀的特点:
3、电镀材料的选择:
阴极——镀件
电镀液——含有镀层金属离子的溶液
阳极——镀层金属
使金属增强抗腐蚀的能力,增加美观和表面硬度。
1)阳极本身参加电极反应
2)电解质溶液的浓度保持不变
二、电解池原理的应用
(二)铜的电解精炼
阳极:
Cu - 2e- = Cu2+
阴极:
Cu2++ 2e- = Cu
杂质比铜活泼的Zn、Ni、Fe等:
Zn - 2e- = Zn2+
Ni - 2e- = Ni 2+
Fe - 2e- = Fe2+
活泼性在铜之后的银、金等:
还原性比铜差的,不能失去电子,它们以单质的形式留在溶液中,成为阳极泥。
电解质溶液硫酸铜的浓度略有减小。
(三)氯碱工业
(1)在NaCl溶液中,NaCl电离出 ,H2O电离出 。
通电后,在电场的作用下, 向阴极移动,
向阳极移动。
在阳极,由于 容易失去电子,被氧化生成 。
阳极方程式: ;
(2)在阴极,由于 容易得到电子被还原生成 .
使H2O 电离向右移动,因此阴极 浓度增大 PH 。
阴极方程式: 。
Na+、Cl-
H+、OH-
Cl-、OH-
Cl-
Cl2
H+
H2
OH-
增大
Na+、H+
2Cl- - 2e- =Cl2
2H+ + 2e- = H2
总化学方式: ;
总离子方程式: .
(3)电解前向溶液中滴加酚酞,通电后现象为:
___________ ,两极极板上都有气体产生,如何检验气体的种类?
阴极附近的溶液无色变为红色
阳极:把湿润的碘化钾淀粉试纸放在阳极附近,产生气体可以使湿润KI淀粉试纸变蓝色.
NaOH
2
H
Cl
O
H
2
NaCl
2
2
2
2
电解
+
+
+
OH
2
H
Cl
O
H
2
Cl
2
2
2
2
电解
+
+
+
练习:金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是 ( )
(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阳极发生还原反应,其电极反应式:
Ni2+ + 2e— = Ni
B.电解过程中,阳极质量的减少与阴极质量的增加
相等
C.电解后,溶液中存在的金属阳离子只有Fe2+ 和
Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
D
练习:
用两只惰性电极插入100mLCuSO4溶液中,通电电解。当溶液的pH值由6.0下降到2.0 (电解过程中溶液体积变化忽略不计),阴极析出铜的质量( )
A.16 mg B.32 mg C.64 mg D.128mg
B
(三)有关电解的计算——电子守恒规律应用
再见
(四)达标检测
1、下列叙述中不正确的是 ( B )
A.电解池的阳极上发生氧化反应,阴极上发生还原反应
B.原电池跟电解池连接后,电子从电池负极流向电解池阳极
C.电镀时,电镀池里的阳极材料发生氧化作用
D.电解饱和食盐水时,阴极得到氢氧化钠溶液和氢
2、用惰性电极实现电解,下列说法正确的是( D )
A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比
为1:2
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比
为1:1
3、用惰性电极电解下列溶液,电解一段时间后,电解液的pH增大
了的是 ( B )
A、H2SO4 B、KOH C、AgNO3 D、Na2SO4
4、关于电解NaCI水溶液,下列叙述正确的是( B )
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴人KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴人酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后落液呈中性
5、下列描述中,不符合生产实际的是( A )
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
6、把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电
解槽串联,在一定条件下通电一段时间后,析出钾、
镁、铝的物质的量之比为( D )
A.1︰2︰3 B.3︰2︰1
C.6︰3︰1 D.6︰3︰2
7、从H+ 、Cu2+ 、Na+ 、SO42- 、 Cl -五种离子中选择适
当的离子组成电解质,符合下列要求。
(1)以石墨棒为电极,电解时电解质质量减小,水量不
变,应选用的电解质是_________
(2)以石墨棒为电极,电解时电解质质量不变,水量减
小,应选用的电解质是_________ (3)以石墨棒为阳
极,铁棒为阴极,电解时电解质质量和水量都减小,应
选用的电解质是_________
8、如下图所示的装置,C、D、E、F、X、Y都是惰性电极。
将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下
问题:
(1) 电源A极的名称是_______。
(2)甲装置中电解反应的总化学方程式是______________________ ___。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______________。
(4)欲用丙装置给铜镀银,G应该是_______,电镀液的主要成分是_________(填化学式)。
