2.5 物质转化的规律 学案(无答案)
图片预览
文档简介
每
课
必
记课题第5节
物质转化的规律课时数5第
4
课时?教学目标4、通过非金属单质与其化合物的转化及金属单质与其化合物的转化,以及化合物之间的相互转化,掌握物质间相互转化的规律(两条纵线、四条横线、两条交叉斜线、两条弯线等物质间的转化)。利用物质转化的规律寻找物质制取的途径,利用所学知识学会对物质的鉴别、甚至鉴定重
点掌握物质间相互转化的规律难
点掌握物质间相互转化的规律教
学手
段实验准备
教
学
预
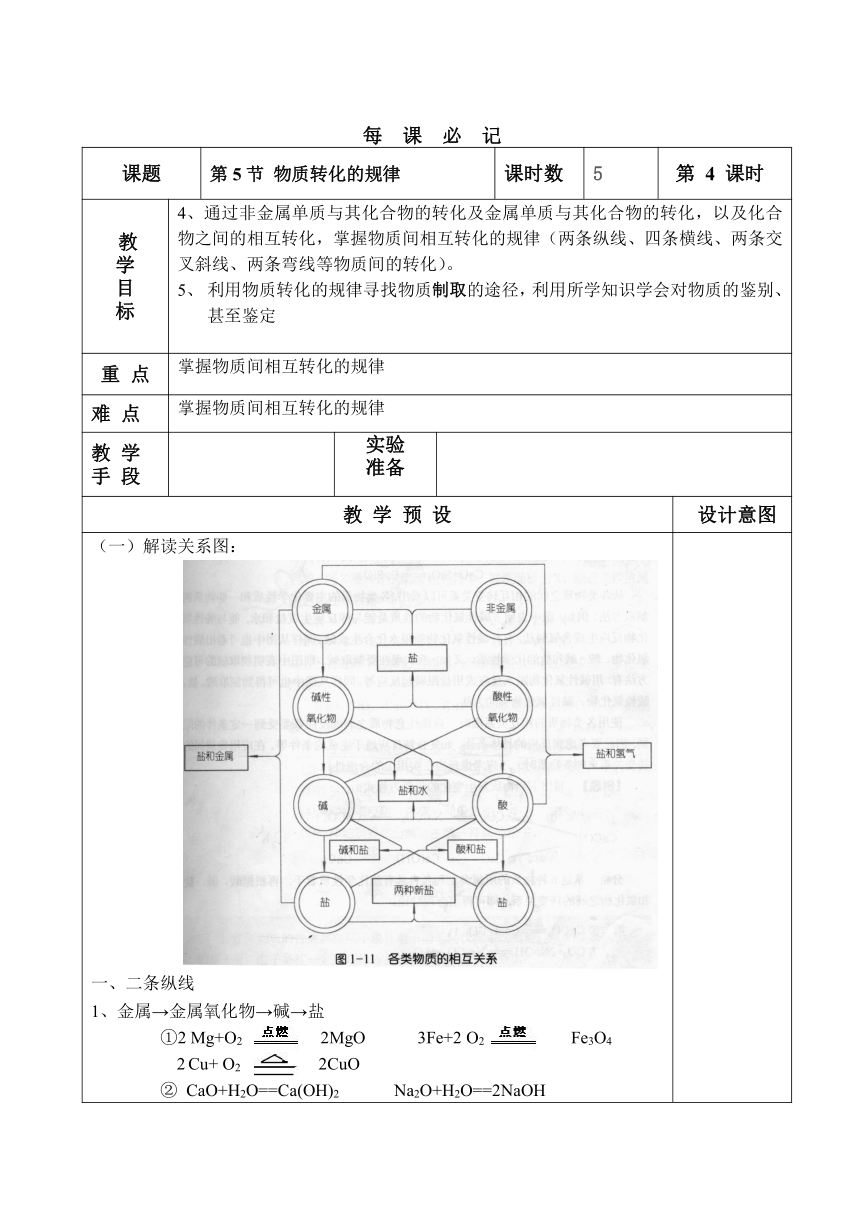
设设计意图(一)解读关系图:二条纵线1、金属→金属氧化物→碱→盐
①2
Mg+O2
2MgO
3Fe+2
O2
Fe3O4
2
Cu+
O2
2CuO②
CaO+H2O==Ca(OH)2
Na2O+H2O==2NaOHCuO
+
H2O
=
不反应③2NaOH+CO2==Na2CO3+H2O
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4Cu(OH)2+H2SO4==CuSO4+2H2O2、非金属→非金属氧化物→酸→盐
。①
S+O2
SO2
4P+5O2
2P2O5
C+O2
CO2
(碳充分燃烧)
2
C+O2
2CO
(碳不充分燃烧)
2H2+O2
2H2O②
CO2+H2O==H2CO3
SO3+O2==H2SO4
SO2+O2==
H2SO3
N2O5+H2O
=
2HNO3
③
Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
Mg(OH)2+2HNO3==Mg(NO3)2+2H2O二、四条横线金属+非金属→无氧酸盐。2Na
+
Cl2
2NaCl
Fe+S
FeS
2Fe+3Cl2
2
Fe
Cl2
2Cu+3Cl2
2
CuCl22Na+
Cl2
2
NaCl
Mg+
Cl2
MgCl2金属氧化物+非金属氧化物→含氧酸盐。CaO+CO2
=
CaCO3
Na2O+SO2=
Na2SO3CuO
+
CO2
=
不反应酸+碱→盐+水。Cu(OH)2+2HCl==CuCl2+H2O
2Fe(OH)3+3H2SO4==
Fe2(SO4)3
+
6H2O
4、盐+盐→新盐+新盐。三、两条交叉斜线。金属氧化物+酸→盐+水Fe2O3+6HCl==2FeCl3+3H2O
CuO+
H2SO4==CuSO4+H2O非金属氧化物+碱
→
盐+水。
2NaOH+SO3==Na2SO4+H2O
Ca(OH)2+CO2
==CaCO3↓+H2O四、两条弯线金属+盐→新金属+新盐。
Fe+CuSO4==FeSO4+Cu
Cu+2AgNO3==Cu(NO3)2+2Ag
金属+酸→盐+氢气。Zn+
2H2SO4==ZnSO4+
H2↑
Fe+
2HCl==FeCl2+H2↑
(二)利用物质转化的规律寻找物质制取的途径例题一、写出用空气、铜、蒸馏水、三氧化硫4种物质制取硫酸铜的化学方程式。例题二、举出5种制备氯化镁的方法。?
课
必
记课题第5节
物质转化的规律课时数5第
4
课时?教学目标4、通过非金属单质与其化合物的转化及金属单质与其化合物的转化,以及化合物之间的相互转化,掌握物质间相互转化的规律(两条纵线、四条横线、两条交叉斜线、两条弯线等物质间的转化)。利用物质转化的规律寻找物质制取的途径,利用所学知识学会对物质的鉴别、甚至鉴定重
点掌握物质间相互转化的规律难
点掌握物质间相互转化的规律教
学手
段实验准备
教
学
预
设设计意图(一)解读关系图:二条纵线1、金属→金属氧化物→碱→盐
①2
Mg+O2
2MgO
3Fe+2
O2
Fe3O4
2
Cu+
O2
2CuO②
CaO+H2O==Ca(OH)2
Na2O+H2O==2NaOHCuO
+
H2O
=
不反应③2NaOH+CO2==Na2CO3+H2O
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4Cu(OH)2+H2SO4==CuSO4+2H2O2、非金属→非金属氧化物→酸→盐
。①
S+O2
SO2
4P+5O2
2P2O5
C+O2
CO2
(碳充分燃烧)
2
C+O2
2CO
(碳不充分燃烧)
2H2+O2
2H2O②
CO2+H2O==H2CO3
SO3+O2==H2SO4
SO2+O2==
H2SO3
N2O5+H2O
=
2HNO3
③
Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
Mg(OH)2+2HNO3==Mg(NO3)2+2H2O二、四条横线金属+非金属→无氧酸盐。2Na
+
Cl2
2NaCl
Fe+S
FeS
2Fe+3Cl2
2
Fe
Cl2
2Cu+3Cl2
2
CuCl22Na+
Cl2
2
NaCl
Mg+
Cl2
MgCl2金属氧化物+非金属氧化物→含氧酸盐。CaO+CO2
=
CaCO3
Na2O+SO2=
Na2SO3CuO
+
CO2
=
不反应酸+碱→盐+水。Cu(OH)2+2HCl==CuCl2+H2O
2Fe(OH)3+3H2SO4==
Fe2(SO4)3
+
6H2O
4、盐+盐→新盐+新盐。三、两条交叉斜线。金属氧化物+酸→盐+水Fe2O3+6HCl==2FeCl3+3H2O
CuO+
H2SO4==CuSO4+H2O非金属氧化物+碱
→
盐+水。
2NaOH+SO3==Na2SO4+H2O
Ca(OH)2+CO2
==CaCO3↓+H2O四、两条弯线金属+盐→新金属+新盐。
Fe+CuSO4==FeSO4+Cu
Cu+2AgNO3==Cu(NO3)2+2Ag
金属+酸→盐+氢气。Zn+
2H2SO4==ZnSO4+
H2↑
Fe+
2HCl==FeCl2+H2↑
(二)利用物质转化的规律寻找物质制取的途径例题一、写出用空气、铜、蒸馏水、三氧化硫4种物质制取硫酸铜的化学方程式。例题二、举出5种制备氯化镁的方法。?
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
