第2章 物质转化与材料利用 基础专训(含答案)
文档属性
| 名称 | 第2章 物质转化与材料利用 基础专训(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 183.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-09-19 19:08:40 | ||
图片预览



文档简介
《物质转化与材料利用》基础专训
相对原子量:Al—27 O—16 H—1 Cl—35.5 C—12 Ca—40 S—32 Na—23
一、选择题(每小题2分,每小题只有一个正确答案,共40分)
1.
分类是学习和研究化学物质及其变化的一种常用科学方法。下列有一组物质的分类角度与其它各组不同,该组物质是(
)
A.铜与铜绿
B.红磷与白磷
C.氧气与臭氧(O3)
D.石墨与金刚石
2.
下列物质属于纯净物的是
( )
A.净化后的空气
B.部分结冰的蒸馏水
C.加工门窗的铝合金
D.经过沉淀、过滤后得到的矿泉水
3.
下列物质中,不能用来鉴别CO和CO2的是(
)。
A.澄清石灰水
B.蒸馏水
C.灼热的氧化铜
D.紫色的石蕊试剂
4.
有机合成材料的出现是材料发展史上的一次重大突破。下列物质属于有机合成材料的是(
)
A.棉花
B.蛋白质
C.维生素
D.塑料
5..下列叙述不符合实验事实的是(
)
A.将CO2气体通入CaCl2溶液中,产生白色沉淀
B.在Na2CO3、K2SO4、AgNO3溶液中分别滴加BaCl2溶液,都有白色沉淀
C.滴有酚酞试液的蒸馏水中加入BaO,溶液显红色
D.久置于空气中的熟石灰,加入稀盐酸有气泡产生
6.某工厂的废渣中混有少量的锌粉和氧化铜(其他的成分不跟酸反应),这些废与废盐酸接触时会形成污水,产生公害。若向污水中撒入铁粉,且反应后让铁粉有剩余,则此时污水中一定含有的金属离子是(
)
A、Fe2+
、Cu2+
B、Cu2+、H+
C、Zn2+、Fe2+
D、Zn2+、H+
7..下列转化不能一步完成的是(
)
A.CaO
→CaCl2
B.CaCO3
→Ca(OH)2
C.BaCl2
→
Ba(NO3)2
D.CaO→Ca(OH)2
8.
在水溶液中,一般不与其它物质发生复分解反应,这种物质是下列中的(
)
A.KCl
B.NaNO3
C.HNO3
D.Mg(OH)2
9.所谓合金,就是不同金属(或非金属)在熔化状态下形成的一种具有金属特性的熔合物。根据下列四种金属的熔沸点,其中不能形成合金的是( )
金属
Cu
Al
Fe
Na
熔点(℃)
1083
660
1535
97.5
沸点(℃)
2595
2200
3000
883
A.Fe和Na
B.Al和Na
C.Fe和Cu
D.Al和Cu
10.
甲、乙、丙、丁四瓶溶液分别是K2CO3、Ba(NO3)2、H2S04、K2S04中的一种,其中甲分别能与乙、丙、丁发生反应,甲是(
)
A.K2SO4
B.H2S04
C.Ba(NO3)2
D.K2CO3
11.下列各组物质混合后能共存的是( )
A.CaCO3和稀HCl
B.CaCl2溶液和Na2CO3溶液
C.MgCl2溶液和NaOH溶液
D.NaCl溶液和MgSO4溶液
12.
利用无色酚酞试液可以鉴别的一组溶液是(
)
A、BaCl2、H2SO4、HCl
B、NaCl、NaOH、HCl
C、K2CO3、Na2CO3
、HCl
D、NaOH、KOH、HCl
13.
有一种气体,可能是H2或CO,下列方法能够鉴别它们的是(
)
A.观察气体是否无色
B.闻气味是否具有刺激性
C.通入氧化铜中,加热,观察黑色粉末是否变红色
D.点燃,在火焰上罩一个内壁附着有澄清石灰水的烧杯,观察石灰水是否变浑浊
14.
新研制以农作物秸秆为原料的一次性餐盒,废弃后在自然条件下两个月就可以分解。下列关于此餐盒的说法不正确的是(
)
A、替代塑料餐盒可减少“白色污染”
B、这种餐盒是环保产品
C、可有效利用秸秆,减少燃烧而引发的空气污染
D、其原料秸秆属于有机合成材料
15.
下列有关对自行车的做法不合理的是(
)
A.车架表面喷涂油漆
B.钢圈表面镀防护金属
C.露天放置,日晒雨淋
D.链条表面涂机油
16.现有四种白色固体:①氯化钠,②氯化钡,③无水硫酸铜,④硫酸钠,不使用除水外的其他试剂可以把它们区分开,区分出的先后顺序是( )
A.②③④①
B.②④③①
C.③①④②
D.③②④①
16、下列关于酸、碱、盐的说法中错误的是(
)
A.硝酸应盛放在棕色试剂瓶中
B.熟石灰可用于改良酸性土壤
C.硫酸铜可配制杀菌剂波尔多液
D.亚硝酸钠代替食盐用于烹调
17.试管内壁附着的下列物质不能用稀盐酸浸泡而除去的是
( )
A.盛石灰水后留下的白色固体
B.氯化铁溶液与氢氧化钠溶液反应后留下的红褐色固体
C.用一氧化碳还原氧化铁留下的黑色物质
D.用足量的氢气还原氧化铜留下的红色物质
18.某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中;②将Zn、Cu分别加入到ZnSO4溶液中;③将Zn分别加入到FeSO4、CuSO4溶液中;④将Fe
分别加入到ZnSO4、CuSO4溶液中。其中可行的是(
)
A.①④
B.①②
C.②③
D.③④
19.从石灰浆抹的墙上掉下一块白色固体,为探究其成分,进行如下实验:
实验步骤
实验现象
①将固体研磨成粉末状,加水搅拌
固体没有完全溶解
②取上层清夜,加无色酚酞试液
溶液呈红色
③取不溶物,加稀盐酸
有气泡产生
则该白色固体的成分( )
A.一定有CaCO3和Ca(OH)2
B.一定有Ca(OH)2
,可能有CaCO3
C.
一定没有CaCO3和Ca(OH)2
D.
一定有CaCO3,可能有Ca(OH)2
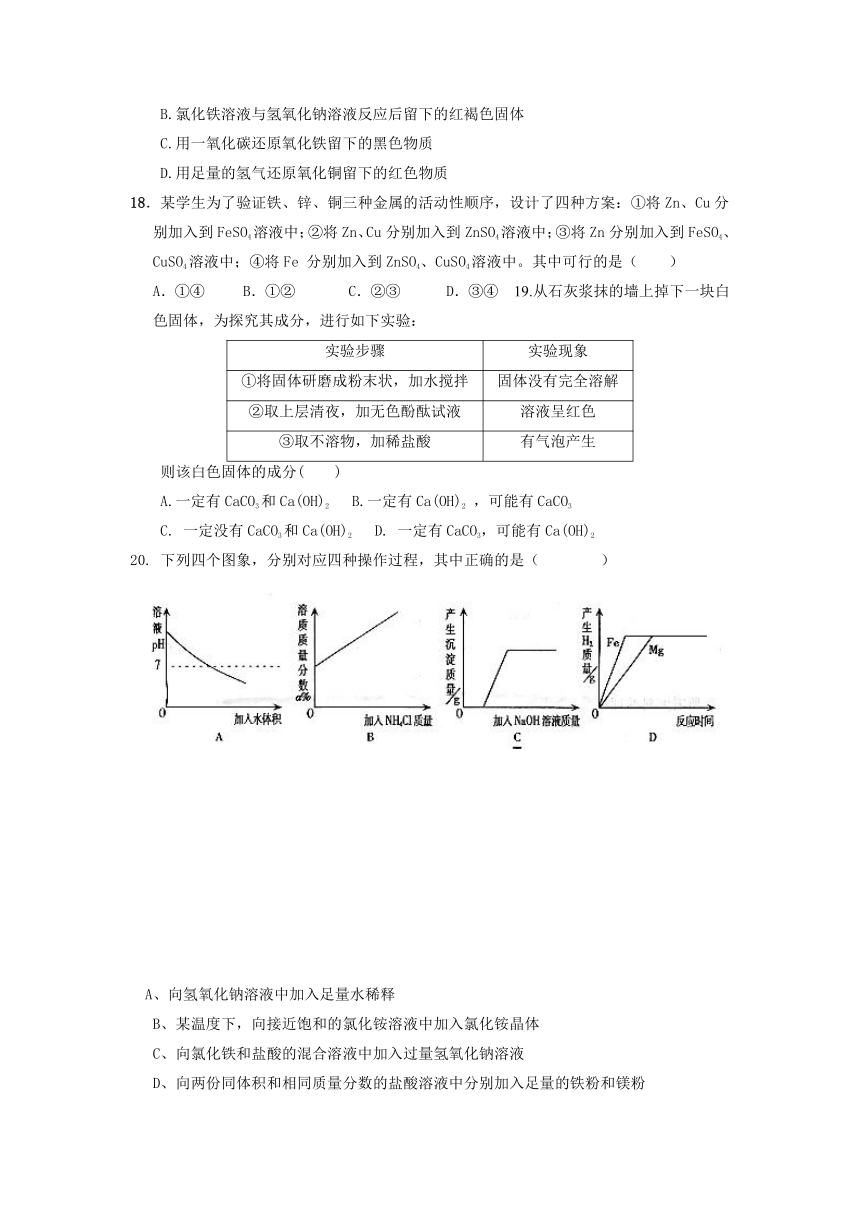
20.
下列四个图象,分别对应四种操作过程,其中正确的是(
)
A、向氢氧化钠溶液中加入足量水稀释
B、某温度下,向接近饱和的氯化铵溶液中加入氯化铵晶体
C、向氯化铁和盐酸的混合溶液中加入过量氢氧化钠溶液
D、向两份同体积和相同质量分数的盐酸溶液中分别加入足量的铁粉和镁粉
二、填空题(每个化学方程式2分,其余每空1分,共20分)
21.化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题:
(1)“沙里淘金”说明黄金在自然界中能够以 (填“单质”或“化合物”)形式存在。
(2)葡萄表皮上因喷洒“波尔多液”而呈现的蓝色魔点,可以用厨房调料 洗净。
(3)刘大爷种的小麦出现倒伏现象,你会建议他使用化肥中的 肥。
(4)长期使用的暖水瓶内胆常有一层水垢(主要成分为碳酸钙),可以用稀盐酸除去。请写出反应的化学方程式: 。
(5)通常所说的煤气中毒是指由 (填物质化学式)引起的中毒。
22.
我们已经知道,常见金属按其活动性强弱可排成如下顺序:
K、Ca、Na、Mg、Al、Zn、Fe、
、
、(H)、Cu、
、Ag、
、Au
(1)
请用相应的元素符号完成上述金属活动性顺序表。
(2)
向硝酸银和硝酸铜的混合溶液中加入一些镁粉,完全反应后过滤。若向残渣中滴加稀盐酸后有气泡冒出,则残渣中含有的金属是
;若残渣中无气泡生成,则滤液中一定含有的金属离子是
。(填符号)
23.通过化学学习,我们已经认识了很多化学反应。请用化学方程式回答下列问题。
(1)用稀硫酸可以除去铁制品表面的铁锈: ;
(2)用纯碱溶液与石灰水反应制取少量氢氧化钠 ;
24.“探险队员”—硫酸,不小心走进了有许多“吃人的野兽”(即能与硫酸发生化学反应的物质)的小山,请你帮助它走出小山(请用图中物质前的序号连接起来表示所走的路线):
入口→
→
→
→
→出口。
三、实验探究题(每空2分,共30分)
25.
实验老师请化学兴趣小组的同学帮助他将失去标签的盐酸、氢氧化钠和硝酸钾三瓶溶液鉴别出来,重新贴好标签。为了鉴别这三种溶液,他们用试管各取三种溶液少许,编号为A、B、C,分别滴加酚酞试液,观察到A溶液变红色,B、C两溶液无变化;另用两支试管再各取B、C少许,分别滴加碳酸钠溶液,观察到C溶液有气泡产生,B溶液无变化。根据上述实验现象,请你推测:
(1)A溶液中溶质的化学式为
,B溶液中溶质的化学式为
;
(2)C溶液滴加碳酸钠溶液后发生反应的化学方程式为
。
26、请你参与科学学习小组的探究活动,并回答相关问题:
[发现问题]小丽发现盛水的铁锅在与水面接触的部位最易生锈;
小茜发现自己的铜制眼镜框表面出现了绿色的铜锈;
[提出问题]这两种物质“生锈”的原因是什么?
[收集证据](1)回忆已有知识:铁生锈的条件是
。
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿)
(3)实验探究:将四小块铜片分别按下图所示放置一个月,观察现象如下:
实验装置
实验现象
铜片不生锈
铜片不生锈
铜片不生锈
铜片生锈且水面附近锈蚀最严重
由实验可知:铜生锈是铜与水、
、
等物质共同作用的结果。
[反思与应用]利用所得结论填空:
写出一种防止铁或铜等金属制品生锈的具体方法
。
27、小李同学想把一枚生锈【表面覆盖着“铜绿”(Cu2(OH)2CO3)】的铜币“复原”。她找来了废电池里的锌皮和试剂A,设计了如下实验方案。
请回答:
(1)反应Ⅱ的实验装置应选择上图中的
。
(2)反应Ⅲ的化学方程式是
。在该实验中,加热之前应先
,以防危险发生。
(3)小李同学观察到黑铜币刚变成光亮时,便停止通入气体B。则她的“复原”实验能否达到最终目的,说明理由
。
28.有A、B、C、D四种白色粉末(均为纯净物),已知它们是硫酸铜、碳酸钙、氯化钠、硝酸钾中的一种。京京同学进行了实验探究,过程与现象记录如下:
第1步:取A、B、C、D四种白色粉末各一药匙,分别入入四支洁净的试管中,各加蒸馏水2毫升,充分振荡后静置。四支试管底部均有固体存在,只有盛放A的试管中液体呈蓝色,其他均呈无色。
第2步:继续向盛放B、C、D的试管中加人适量的稀盐酸,只有盛放D的试管中有气泡产生,其他均无明显变化。
第3步:重新取少量B和C的粉末分别放人另取的2支洁净试管中.各加入适量蒸馏水使其完全溶解,再分别加入几滴硝酸银溶液,结果盛放B的试管中有白色沉淀生成,盛放C的试管中无明显变化。
试回答下列问题:
(1)根据上述实验可知:B是
。
(2)第1步实验设计的预期现象是“四支试管中只有一支底部有固体存在……”。实验结果是四支试管底部均有固体存在,你认为其余三支试管底部有固体存在的原因可能是
。
(3)写出D与稀盐酸反应的化学方程式
。
(4)第3步实验为什么不可以在第2步的试管中继续进行,而要重新取样后再继续实验?
。
四、分析计算题(共10分)
29.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。请计算:
序
号
加入稀盐酸质量(g)
剩余固体质量(g)
第1次
10
5.5
第2次
10
m
第3次
10
1.2
第4次
10
1.2
(1)8g的石灰石样品中含有杂质多少克?(2)样品中碳酸钙的质量分数是多少?
(3)上表中m的数值应为多少?(4)要得到280kg的CaO,需要质量分数为80%的石灰石多少千克?
参考答案
一、选择题(每小题只有一个正确答案,每小题2分,共40分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
B
B
D
A
C
B
B
A
C
题号
11
12
13
14
15
16
17
18
19
20
答案
D
B
D
D
C
D
D
A
A
C
二、填空题(每个化学方程式2分,其余每空1分,共20分)
21、(1)单质
(2)食醋
(3)钾
(4)CaCO3
+
2HCl=CaCl2
+
CO2↑+
H2O
(5)CO
22、(1)Sn;Pb;Hg;Pt(2)Mg、、Cu、Ag;Mg2+
23、(1)Fe2O3
+
3H2SO4
===
Fe2(SO4)3
+
3H2O
(2)Ca(OH)2
+
Na2CO3
=
CaCO3↓+
2NaOH
24、③→⑤→⑦→⑨
三、实验探究题(每空2分,共30分)
25、(1)NaOH;KNO3(2)Na2CO3
+
2HCl
=
2NaCl
+
H2O
+
CO2↑
26、潮湿的空气;CO2;O2;刷油漆
27、(1)③
(2)H2
+
CuO
加热
Cu
+
H2O
通入氢气(3)不能,这样生成的铜在高温条件下会重新氧化成氧化铜
28、NaCl;固体太多或水太少,固体不能完全溶解;CaCO3
+
2HCl
=
CaCl2
+
H2O
+
CO2↑;
避免加盐酸后对实验的干扰。
四、分析计算题(共10分)
29、(1)1.2克 (2)85% (3)3 (4)625千克
水
水
PAGE
相对原子量:Al—27 O—16 H—1 Cl—35.5 C—12 Ca—40 S—32 Na—23
一、选择题(每小题2分,每小题只有一个正确答案,共40分)
1.
分类是学习和研究化学物质及其变化的一种常用科学方法。下列有一组物质的分类角度与其它各组不同,该组物质是(
)
A.铜与铜绿
B.红磷与白磷
C.氧气与臭氧(O3)
D.石墨与金刚石
2.
下列物质属于纯净物的是
( )
A.净化后的空气
B.部分结冰的蒸馏水
C.加工门窗的铝合金
D.经过沉淀、过滤后得到的矿泉水
3.
下列物质中,不能用来鉴别CO和CO2的是(
)。
A.澄清石灰水
B.蒸馏水
C.灼热的氧化铜
D.紫色的石蕊试剂
4.
有机合成材料的出现是材料发展史上的一次重大突破。下列物质属于有机合成材料的是(
)
A.棉花
B.蛋白质
C.维生素
D.塑料
5..下列叙述不符合实验事实的是(
)
A.将CO2气体通入CaCl2溶液中,产生白色沉淀
B.在Na2CO3、K2SO4、AgNO3溶液中分别滴加BaCl2溶液,都有白色沉淀
C.滴有酚酞试液的蒸馏水中加入BaO,溶液显红色
D.久置于空气中的熟石灰,加入稀盐酸有气泡产生
6.某工厂的废渣中混有少量的锌粉和氧化铜(其他的成分不跟酸反应),这些废与废盐酸接触时会形成污水,产生公害。若向污水中撒入铁粉,且反应后让铁粉有剩余,则此时污水中一定含有的金属离子是(
)
A、Fe2+
、Cu2+
B、Cu2+、H+
C、Zn2+、Fe2+
D、Zn2+、H+
7..下列转化不能一步完成的是(
)
A.CaO
→CaCl2
B.CaCO3
→Ca(OH)2
C.BaCl2
→
Ba(NO3)2
D.CaO→Ca(OH)2
8.
在水溶液中,一般不与其它物质发生复分解反应,这种物质是下列中的(
)
A.KCl
B.NaNO3
C.HNO3
D.Mg(OH)2
9.所谓合金,就是不同金属(或非金属)在熔化状态下形成的一种具有金属特性的熔合物。根据下列四种金属的熔沸点,其中不能形成合金的是( )
金属
Cu
Al
Fe
Na
熔点(℃)
1083
660
1535
97.5
沸点(℃)
2595
2200
3000
883
A.Fe和Na
B.Al和Na
C.Fe和Cu
D.Al和Cu
10.
甲、乙、丙、丁四瓶溶液分别是K2CO3、Ba(NO3)2、H2S04、K2S04中的一种,其中甲分别能与乙、丙、丁发生反应,甲是(
)
A.K2SO4
B.H2S04
C.Ba(NO3)2
D.K2CO3
11.下列各组物质混合后能共存的是( )
A.CaCO3和稀HCl
B.CaCl2溶液和Na2CO3溶液
C.MgCl2溶液和NaOH溶液
D.NaCl溶液和MgSO4溶液
12.
利用无色酚酞试液可以鉴别的一组溶液是(
)
A、BaCl2、H2SO4、HCl
B、NaCl、NaOH、HCl
C、K2CO3、Na2CO3
、HCl
D、NaOH、KOH、HCl
13.
有一种气体,可能是H2或CO,下列方法能够鉴别它们的是(
)
A.观察气体是否无色
B.闻气味是否具有刺激性
C.通入氧化铜中,加热,观察黑色粉末是否变红色
D.点燃,在火焰上罩一个内壁附着有澄清石灰水的烧杯,观察石灰水是否变浑浊
14.
新研制以农作物秸秆为原料的一次性餐盒,废弃后在自然条件下两个月就可以分解。下列关于此餐盒的说法不正确的是(
)
A、替代塑料餐盒可减少“白色污染”
B、这种餐盒是环保产品
C、可有效利用秸秆,减少燃烧而引发的空气污染
D、其原料秸秆属于有机合成材料
15.
下列有关对自行车的做法不合理的是(
)
A.车架表面喷涂油漆
B.钢圈表面镀防护金属
C.露天放置,日晒雨淋
D.链条表面涂机油
16.现有四种白色固体:①氯化钠,②氯化钡,③无水硫酸铜,④硫酸钠,不使用除水外的其他试剂可以把它们区分开,区分出的先后顺序是( )
A.②③④①
B.②④③①
C.③①④②
D.③②④①
16、下列关于酸、碱、盐的说法中错误的是(
)
A.硝酸应盛放在棕色试剂瓶中
B.熟石灰可用于改良酸性土壤
C.硫酸铜可配制杀菌剂波尔多液
D.亚硝酸钠代替食盐用于烹调
17.试管内壁附着的下列物质不能用稀盐酸浸泡而除去的是
( )
A.盛石灰水后留下的白色固体
B.氯化铁溶液与氢氧化钠溶液反应后留下的红褐色固体
C.用一氧化碳还原氧化铁留下的黑色物质
D.用足量的氢气还原氧化铜留下的红色物质
18.某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中;②将Zn、Cu分别加入到ZnSO4溶液中;③将Zn分别加入到FeSO4、CuSO4溶液中;④将Fe
分别加入到ZnSO4、CuSO4溶液中。其中可行的是(
)
A.①④
B.①②
C.②③
D.③④
19.从石灰浆抹的墙上掉下一块白色固体,为探究其成分,进行如下实验:
实验步骤
实验现象
①将固体研磨成粉末状,加水搅拌
固体没有完全溶解
②取上层清夜,加无色酚酞试液
溶液呈红色
③取不溶物,加稀盐酸
有气泡产生
则该白色固体的成分( )
A.一定有CaCO3和Ca(OH)2
B.一定有Ca(OH)2
,可能有CaCO3
C.
一定没有CaCO3和Ca(OH)2
D.
一定有CaCO3,可能有Ca(OH)2
20.
下列四个图象,分别对应四种操作过程,其中正确的是(
)
A、向氢氧化钠溶液中加入足量水稀释
B、某温度下,向接近饱和的氯化铵溶液中加入氯化铵晶体
C、向氯化铁和盐酸的混合溶液中加入过量氢氧化钠溶液
D、向两份同体积和相同质量分数的盐酸溶液中分别加入足量的铁粉和镁粉
二、填空题(每个化学方程式2分,其余每空1分,共20分)
21.化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题:
(1)“沙里淘金”说明黄金在自然界中能够以 (填“单质”或“化合物”)形式存在。
(2)葡萄表皮上因喷洒“波尔多液”而呈现的蓝色魔点,可以用厨房调料 洗净。
(3)刘大爷种的小麦出现倒伏现象,你会建议他使用化肥中的 肥。
(4)长期使用的暖水瓶内胆常有一层水垢(主要成分为碳酸钙),可以用稀盐酸除去。请写出反应的化学方程式: 。
(5)通常所说的煤气中毒是指由 (填物质化学式)引起的中毒。
22.
我们已经知道,常见金属按其活动性强弱可排成如下顺序:
K、Ca、Na、Mg、Al、Zn、Fe、
、
、(H)、Cu、
、Ag、
、Au
(1)
请用相应的元素符号完成上述金属活动性顺序表。
(2)
向硝酸银和硝酸铜的混合溶液中加入一些镁粉,完全反应后过滤。若向残渣中滴加稀盐酸后有气泡冒出,则残渣中含有的金属是
;若残渣中无气泡生成,则滤液中一定含有的金属离子是
。(填符号)
23.通过化学学习,我们已经认识了很多化学反应。请用化学方程式回答下列问题。
(1)用稀硫酸可以除去铁制品表面的铁锈: ;
(2)用纯碱溶液与石灰水反应制取少量氢氧化钠 ;
24.“探险队员”—硫酸,不小心走进了有许多“吃人的野兽”(即能与硫酸发生化学反应的物质)的小山,请你帮助它走出小山(请用图中物质前的序号连接起来表示所走的路线):
入口→
→
→
→
→出口。
三、实验探究题(每空2分,共30分)
25.
实验老师请化学兴趣小组的同学帮助他将失去标签的盐酸、氢氧化钠和硝酸钾三瓶溶液鉴别出来,重新贴好标签。为了鉴别这三种溶液,他们用试管各取三种溶液少许,编号为A、B、C,分别滴加酚酞试液,观察到A溶液变红色,B、C两溶液无变化;另用两支试管再各取B、C少许,分别滴加碳酸钠溶液,观察到C溶液有气泡产生,B溶液无变化。根据上述实验现象,请你推测:
(1)A溶液中溶质的化学式为
,B溶液中溶质的化学式为
;
(2)C溶液滴加碳酸钠溶液后发生反应的化学方程式为
。
26、请你参与科学学习小组的探究活动,并回答相关问题:
[发现问题]小丽发现盛水的铁锅在与水面接触的部位最易生锈;
小茜发现自己的铜制眼镜框表面出现了绿色的铜锈;
[提出问题]这两种物质“生锈”的原因是什么?
[收集证据](1)回忆已有知识:铁生锈的条件是
。
(2)查阅有关资料:“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿)
(3)实验探究:将四小块铜片分别按下图所示放置一个月,观察现象如下:
实验装置
实验现象
铜片不生锈
铜片不生锈
铜片不生锈
铜片生锈且水面附近锈蚀最严重
由实验可知:铜生锈是铜与水、
、
等物质共同作用的结果。
[反思与应用]利用所得结论填空:
写出一种防止铁或铜等金属制品生锈的具体方法
。
27、小李同学想把一枚生锈【表面覆盖着“铜绿”(Cu2(OH)2CO3)】的铜币“复原”。她找来了废电池里的锌皮和试剂A,设计了如下实验方案。
请回答:
(1)反应Ⅱ的实验装置应选择上图中的
。
(2)反应Ⅲ的化学方程式是
。在该实验中,加热之前应先
,以防危险发生。
(3)小李同学观察到黑铜币刚变成光亮时,便停止通入气体B。则她的“复原”实验能否达到最终目的,说明理由
。
28.有A、B、C、D四种白色粉末(均为纯净物),已知它们是硫酸铜、碳酸钙、氯化钠、硝酸钾中的一种。京京同学进行了实验探究,过程与现象记录如下:
第1步:取A、B、C、D四种白色粉末各一药匙,分别入入四支洁净的试管中,各加蒸馏水2毫升,充分振荡后静置。四支试管底部均有固体存在,只有盛放A的试管中液体呈蓝色,其他均呈无色。
第2步:继续向盛放B、C、D的试管中加人适量的稀盐酸,只有盛放D的试管中有气泡产生,其他均无明显变化。
第3步:重新取少量B和C的粉末分别放人另取的2支洁净试管中.各加入适量蒸馏水使其完全溶解,再分别加入几滴硝酸银溶液,结果盛放B的试管中有白色沉淀生成,盛放C的试管中无明显变化。
试回答下列问题:
(1)根据上述实验可知:B是
。
(2)第1步实验设计的预期现象是“四支试管中只有一支底部有固体存在……”。实验结果是四支试管底部均有固体存在,你认为其余三支试管底部有固体存在的原因可能是
。
(3)写出D与稀盐酸反应的化学方程式
。
(4)第3步实验为什么不可以在第2步的试管中继续进行,而要重新取样后再继续实验?
。
四、分析计算题(共10分)
29.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。请计算:
序
号
加入稀盐酸质量(g)
剩余固体质量(g)
第1次
10
5.5
第2次
10
m
第3次
10
1.2
第4次
10
1.2
(1)8g的石灰石样品中含有杂质多少克?(2)样品中碳酸钙的质量分数是多少?
(3)上表中m的数值应为多少?(4)要得到280kg的CaO,需要质量分数为80%的石灰石多少千克?
参考答案
一、选择题(每小题只有一个正确答案,每小题2分,共40分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
B
B
D
A
C
B
B
A
C
题号
11
12
13
14
15
16
17
18
19
20
答案
D
B
D
D
C
D
D
A
A
C
二、填空题(每个化学方程式2分,其余每空1分,共20分)
21、(1)单质
(2)食醋
(3)钾
(4)CaCO3
+
2HCl=CaCl2
+
CO2↑+
H2O
(5)CO
22、(1)Sn;Pb;Hg;Pt(2)Mg、、Cu、Ag;Mg2+
23、(1)Fe2O3
+
3H2SO4
===
Fe2(SO4)3
+
3H2O
(2)Ca(OH)2
+
Na2CO3
=
CaCO3↓+
2NaOH
24、③→⑤→⑦→⑨
三、实验探究题(每空2分,共30分)
25、(1)NaOH;KNO3(2)Na2CO3
+
2HCl
=
2NaCl
+
H2O
+
CO2↑
26、潮湿的空气;CO2;O2;刷油漆
27、(1)③
(2)H2
+
CuO
加热
Cu
+
H2O
通入氢气(3)不能,这样生成的铜在高温条件下会重新氧化成氧化铜
28、NaCl;固体太多或水太少,固体不能完全溶解;CaCO3
+
2HCl
=
CaCl2
+
H2O
+
CO2↑;
避免加盐酸后对实验的干扰。
四、分析计算题(共10分)
29、(1)1.2克 (2)85% (3)3 (4)625千克
水
水
PAGE
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
