2012年高考试题分项解析化学 专题03 反应速率、化学平衡
文档属性
| 名称 | 2012年高考试题分项解析化学 专题03 反应速率、化学平衡 |
|
|
| 格式 | zip | ||
| 文件大小 | 733.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | |||
| 科目 | 化学 | ||
| 更新时间 | 2012-07-09 00:00:00 | ||
图片预览




文档简介
2012年高考试题分项解析化学
专题03 反应速率、化学平衡
(2012·广东)31.碘在科研与生活中有重要作用,某兴趣小组用0.50 mol·L—1KI、0.2%淀粉溶液、0.20 mol·L—1K2S2O8、0.10 mol·L—1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82—+ 2I— = 2 SO42— + I2(慢) I2 + 2 S2O32— = 2I— + S4O62— (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32—与S2O82—初始的物质的量需满足的关系为:n(S2O32—):n(S2O82—) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 体积V/ml
K2S2O8溶液 水 KI溶液 Na2S2O3溶液 淀粉溶液
① 10.0 0.0 4.0 4.0 2.0
② 9.0 1.0 4.0 4.0 2.0
③ 8.0 Vx 4.0 4.0 2.0
表中Vx = ml,理由是 。
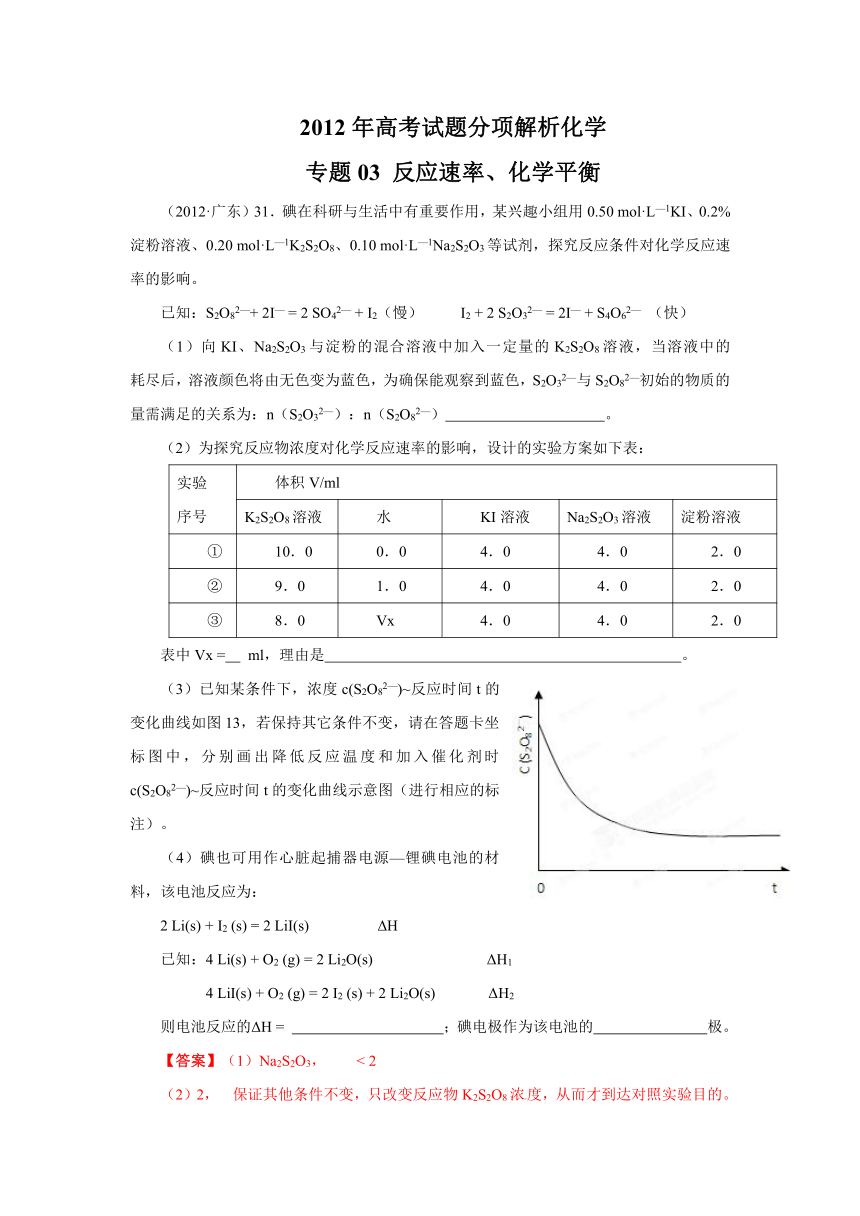
(3)已知某条件下,浓度c(S2O82—)~反应时间t的变化曲线如图13,若保持其它条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82—)~反应时间t的变化曲线示意图(进行相应的标注)。
(4)碘也可用作心脏起捕器电源—锂碘电池的材料,该电池反应为:
2 Li(s) + I2 (s) = 2 LiI(s) ΔH
已知:4 Li(s) + O2 (g) = 2 Li2O(s) ΔH1
4 LiI(s) + O2 (g) = 2 I2 (s) + 2 Li2O(s) ΔH2
则电池反应的ΔH = ;碘电极作为该电池的 极。
【答案】(1)Na2S2O3, < 2
(2)2, 保证其他条件不变,只改变反应物K2S2O8浓度,从而才到达对照实验目的。
(3)
(4) (△H1—△H2)/2; 正极
【考点定位】化学反应速度的影响因素
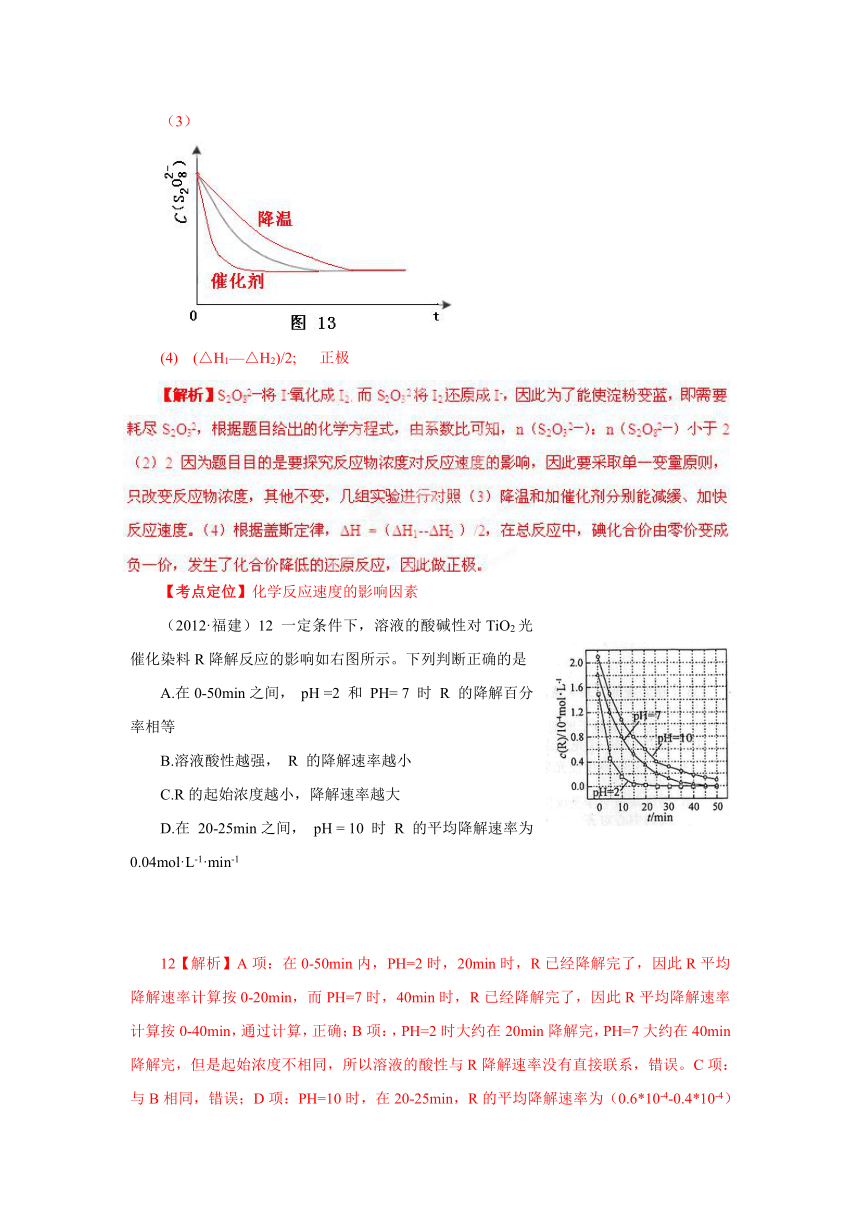
(2012·福建)12 一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如右图所示。下列判断正确的是
A.在0-50min之间, pH =2 和 PH= 7 时 R 的降解百分率相等
B.溶液酸性越强, R 的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在 20-25min之间, pH = 10 时 R 的平均降解速率为 0.04mol·L-1·min-1
12【解析】A项:在0-50min内,PH=2时,20min时,R已经降解完了,因此R平均降解速率计算按0-20min,而PH=7时,40min时,R已经降解完了,因此R平均降解速率计算按0-40min,通过计算,正确;B项:,PH=2时大约在20min降解完,PH=7大约在40min降解完,但是起始浓度不相同,所以溶液的酸性与R降解速率没有直接联系,错误。C项:与B相同,错误;D项:PH=10时,在20-25min,R的平均降解速率为(0.6*10-4-0.4*10-4)/5=0,04*10-4mol●L-1min-1
【答案】A
【考点定位】本题考查了化学反应速率的图象分析。
(2012·四川)12.在体积恒定的密闭容器中,一定量的SO2与1.100molO2在催化剂作用下加热到600℃发生反应:2SO2 + O2 2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
A.当SO3的生成速率与SO2的消耗速率相等时反应达到平衡
B.降低温度,正反应速率减小程度比逆反应速率减小程度大
C.将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为161.980g
D.达到平衡时,SO2的转化率为90%
【答案】:D
【解析】:2SO2 + O2 2SO3,
始量 amol 1.100mol 0 mol
变量 2xmol xmol 2xmol
平衡 (a-2x) mol (1.100-x) mol 2xmol
由题意可得,a+1.100-(a-2x)- (1.100-x)- 2x=0.315,(a+1.100-2x)/(a+1.100)=0.825,(2011·大纲版)8.合成氨所需的氢气可用煤和水作原料经多步反映制得,其中的一步反应为
CO(g)+ H2O(g) CO2(g) + H2(g) △H <0
反应达到平衡后,为提高CO的转化率,下列措施中正确的是
A 增加压强 B 降低温度 C 增大CO 的浓度 D 更换催化剂
【答案】B
(2011·重庆)13.在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)2c(g);<0
x(g)+3y(g)2z(g);>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
等压时,通入惰性气体,c的物质的量不变
等压时,通入z气体,反应器中温度升高
等容时,通入惰性气体,各反应速率不变
等容时,通入x气体,y的物质的量浓度增大
【答案】A
【解析】等压时充入惰性气体,体积增大,但对于第二个反应而言平衡正向移动,反应吸热,温度降低,第一个反应向正向移动,c的物质的量增加,A项错误。
【考点定位】本题考查化学反应速率、化学平衡的移动等知识。
(2011·安徽)9.一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g)2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
9、【答案】D
【解析】。由于硫为液态,因此反应前后气体分子数不等,达平衡前容器内压强逐渐变小,分离出硫对化学反应速率及平衡无影响,即A、B错误;根据平衡移动原理知升温平衡向吸热方向移动即向左移动,SO2的转化率降低,C错误;平衡常数只受温度的影响,与催化剂无关,故D项正确。
【考点定位】本题主要考查外界条件对化学平衡及反应速率的影响,考查平衡常数的知识及平衡的移动。
(2012·天津)6.已知2SO2 (g) + O2 (g) 2SO3 (g);ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2 ;(丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙 > 2P乙
B.SO3的质量m:m甲=m丙 > 2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙 > k乙
D.反应放出或吸收热量的数值Q:Q甲=G丙 > 2Q乙
【答案】:B
【考点定位】此题综合考查了化学反应速率和化学平衡知识。
(2012·上海)18.为探究锌与稀硫酸的反应速率(以v(H2)表示)。向反应混合汶中加入某些物质,下列判断正确的是
A.加入NH4HSO4固体,v(H2)不变 B,加入少量水,v(H2)减小
C.加入CH3COONa固体,v(H2)减小 D.滴加少量CuSO4溶液,v(H2)减小
【答案】BC
【解析】NH4HSO4能电离生成H+,故v (H2)应增大;滴加少量CuSO4溶液后,Zn能与其置换出的Cu形成原电池,能加快反应速率。
【考点定位】本题考查化学反应速率的影响因素
(2012·江苏)10. 下列有关说法正确的是
A.CaCO3(s) =CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H2(g) =2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2 )和H2的平衡转化率均增大
D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
【答案】B
【考点定位】化学反应原理的分析
(2012·江苏)14. 温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)=PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s 0 50 150 250 350
n(PCl3) / mol 0 0. 16 0. 19 0. 20 0. 20
下列说法正确的是
A. 反应在前50 s 的平均速率v(PCl3)= 0. 0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)= 0. 11 mol·L-1,则反应的驻H<0
C. 相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3 和0. 20 mol Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2. 0 mol PCl3 和2. 0 mol Cl2,达到平衡时,PCl3 的转化率小于80%
【答案】C
【解析】A项,v (PCl3)= mol/(L·s),错;B项,从表中看,平衡时PCl3为0.2mol/2L=0.1mol/L,升高温度时,PCl3的浓度增大,即平衡正向移动,说明正反应为吸热反应,错;C项,原平衡时,K=,充入物质后,Q=,因为Qv (逆),正确;D项,题干中充入1mol PCl5,相当于充入1mol PCl3和1mol Cl2,平衡时各组分的量相等,则PCl3的转化率为,现充入2mol PCl3和2mol Cl2,可看是两部分平衡后再加压,加压向体积减小的方向移动,即逆向移动,PCl3的转化率应增大,错。
【考点定位】化学反应速率与化学平衡
(2012·上海)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g)+Q(Q>0) 完成下列填空:
31.在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率___ mol/(L·min);该反应的平衡常数表达式K=_____
32.上述反应达到平衡后,下列说法正确的是_。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
33.一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_。
a.3v逆(N2)=v正(H2) b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
34.若平衡时H2和HCl的物质的量之比为m/n,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___m/n(填“>”、“=”或“<”)。
【答案】31.0.02;
32.bd
33.ac
34.<
【解析】31.反应生成n(Si3N4)==0.02 mol,则反应消耗n(H2)=0.12 mol,v (H2)==0.02 mol/(L·min),该反应的平衡常数的表达式为。
关。
34.降低温度,平衡向正反应方向移动,HCl的物质的量增大,H2的物质的量减小,故H2和HCl的物质的量之比大于。
【考点定位】本题主要考查化学反应速率与化学平衡得有关计算和判断。
(2012·全国新课标卷)27.(15分)光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成。
(1)实验室常用来制备氯气的化学方程式为 ;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(ΔH)分别为-890.3kJ·mol-1、-285.8kJ.mol-1和-283.0kJ.mol-1,则生成1m3(标准状况)CO所需热量为 ;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为 ;
(4)COCl2的分解反应为COCl2(g)=Cl2(g)+CO(g) ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出):
①计算反应在第8min时的平衡常数K= ;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2) T(8)
(填“<”、“>”或“=”),
③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)= mol·L-1;
④比较产物CO在2-3min、5-6min和12-13min时平均反应速率(平均反应速率分别以v(2-3)、v(5-6)、v(12-13))的大小 ;
⑤比较反应物COCl2在5-6min和15-16min时平均反应速率的大小:v(5-6) v(15-16)(填“<”、“>”或“=”),原因是 。
【答案】
(1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)5.52×103 KJ
(3)CHCl3+H2O2=COCl2+H2O+HCl
(4)①0.234 mol·L-1
②<
③0.031mol·L-1
④v(5-6)> v(2-3)=v(12-13)
ΔH=ΔH1-2ΔH2-2ΔH3=(-890.3)kJ·moL-1-2×(-285.8)kJ·moL-1-2×(-283.0)kJ·moL-1=247.3 kJ·moL-1,即生成2mol CO,需要吸热247.3 KJ,那么要得到1立方米的CO,吸热为(1000/22.4)×247.3/2=5.52×103 KJ。
(4)由图示可知8min时COCl2、Cl2、CO三种物质的浓度分别为0.04mol·L-1、0.11 mol·L-1、0.085 mol·L-1。所以此时其平衡常数为:0.11 mol·L-1×0.085 mol·L-1÷0.04 mol·L-1=0.23 4mol·L-1。第8min时反应物的浓度比第2min时减小,生成物浓度增大,平衡向正反应方向移动。又因为正反应为吸热反应,所以T(2)<T(8)。④根据图像变化可知:在2min时升温 。在10min时 增加COCl2的浓度,在12min时,反应达到平衡 。在相同温度时,该反应的反应物浓度越高,反应速率越大,v(5-6)>v(15-16)。
【考点定位】热化学方程式的书写、反应热的计算、化学反应速率、影响化学反应速率的因素、化学平衡、化学图像。
(2012·北京)26. (12分)用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。
反应A: 4HCl+O2 2Cl2+2H2O
(1)已知:i 反应A中, 4mol HCI被氧化,放出115.6kJ的热量。
ii
①H2O的电子式是_______________.
②反应A的热化学方程式是_______________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中
H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是______________.
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投
料比的关系是_________________.
⑧投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是_______________.
【答案】:(1);4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H= - 115.6 kJ/mol;32;强;(2)4:1;投料比越小时对应的温度越低;30.8%。
【解析】:(1)根据水分子的结构,其电子式为:;反应A的热化学方程式为:4HCl(g)+O2(g)2Cl2(g)+2H2O(g) △H= - 115.6 kJ/mol;由于反应中,需要断裂4mol“H—Cl“键、断开1mol“O=O”键,形成2mol“Cl-Cl”键,形成4mol“H-O”键;根据图纸数据,断开1mol“O=O”键,形成2mol“Cl-Cl”键的能量差为12kJ/mol,,反应的热效应为:-115.6 kJ/mol,故此断裂4mol“H—Cl“键和形成4mol“H-O”键的能量差为:-127.6 kJ/mol,故断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为32kJ,H2O中H—O 键比HCl中H—Cl键强;(2)根据反应方程式:4HCl+O22Cl2+2H2O,氧气的投料比越高,则HCl的转化率越高,故此曲线b对应的投料比为4:1;由于该反应正向放热,故温度越高,HCl的转化率越低,故投料比越小时温度越高;当投料比为2:1,温度为400℃时,HCl的转化率约为80%,此时为:
(2012·天津)10.(14分)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g) W (s) + 3H2O (g)
请回答下列问题:
⑴ 上述反应的化学平衡常数表达式为___________________________。
⑵ 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_____________________;随温度的升高,H2与水蒸气的体积比减小,则该反应为___________反应(填“吸热”或“放热”)。
⑶上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 25℃ ~ 550℃ ~ 600℃ ~ 700℃
主要成份 WO3 W2O5 WO2 W
第一阶段反应的化学方程式为___________________________;580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为____________________________________。
⑷ 已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g) W (s) + 2H2O (g) ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2(g) W (s) + 2H2O (g) ΔH = -137.9 kJ·mol-1
则WO2 (s) WO2 (g) 的ΔH = ______________________。
⑸ 钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) WI4 (g)。下列说法正确的有________________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
【答案】:(1)k= ;(2)60%;吸热;(3)2WO3+H2W2O5+H2O;W2O5、WO2;1:1:4;(4)+203.9kJ·mol-1;(5)ab。
【解析】:(1)根据题给的化学方程式,其中的WO3和W均为固体,平衡常数中不写入,故k= ;(2)由方程式:WO3+3H2W+3H2O,两物质的化学计量数相同,又知平衡时两者的体积比为2:3,故氢气的平衡转化率为:(3/5)×100%=60%;温度升高时,氢气和水蒸气的体积比减小,说明平衡向正向移动,说明该反应正向吸热;(3)根据表格中给出的反应的三个阶段,第一阶段,WO3转化为W2O5,方程式可表示为:2WO3+H2W2O5+H2O;在580℃时,反应进入第二阶段,固体物质的主要成分是:W2O5、WO2;第二阶段的方程式可表示为:W2O5+H22WO2+H2O、第三阶段的方程式为: WO2+2H2W+2H2O;故三阶段消耗的氢气的物质的量为:1:1:4;(4)根据题给的两个热化学方程式:WO2(s)+2H2(g)W(s)+2H2O(g) △H= +66.0 kJ·mol-1①; WO2(g)+2H2(g)W(s)+2H2O(g) △H=-137.9kJ·mol-1②;将反应①-②得到:WO2(s) WO2(g) △H= +203.9kJ·mol-1;(5)根据钨丝灯管的反应原理,可知灯管内的碘单质可循环使用,a对;加入碘单质的作用是减缓灯丝变细,故b对;由于四碘化钨是在1400℃生成,高于3000℃时分解,故应在灯丝上形成,c错;温度升高时,不管是分解速率和化合速率都加快,d错。
【考点定位】此题为以金属钨的制取为基础,综合考查了化学平衡常数、平衡转化率、化学平衡的移动、盖斯定律、化学方程式的书写等知识。
(2011·重庆)29.(14分)尿素是首个由无机物人工合成的有机物。
(1)工业上尿素和,在一定条件下合成,其反应方程式为 。
(2)当氨碳比的转化率随时间的变化关系如题29图1所示.
①A点的逆反应速率 点的正反应速率为(填“大于”、“小于”或“等于”)
②的平衡转化率为 。
版权所有:高考资源网(www.)
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图29图2.
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 。
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解).
【答案】(1)2NH3+CO2CO(NH3)2+H2O
(2)①小于
②30%
(3)①B
②2Cl-—2e-=Cl2↑, CO(NH3)2 +3 Cl2+H2O=N2+CO2+6HCl
③不变;7.2
【解析】(1)合成尿素根据原子个数守恒,还生成H2O,及2NH3+CO2CO(NH3)2+H2O。(2)①A点未达到平衡,此过程中正反应速率减小,逆反应速率增大, B点达到平衡正逆反应速率相等,对CO2来说逆反应速率达到最大,故为小于。②根据2NH3+CO2CO(NH3)2+H2O可设起始CO2为xmol
4x x 0 0
x×60% 则转化的NH3为2x×60%,所以转化率=%
(3)①由图像电解产生产物知:生成氢气的极为阴极,则B为负极。②阳极室中Cl-失电子产生Cl2。③阴极减少的H+,可通过质子交换膜补充,而使PH不变。气体物质的量为13.44L/22.4L/mol=0.6mol,由电子守恒及其原子个数守恒CO(NH2)2 ~3 Cl2~N2~CO2 ~3H2,则CO(NH2)2的物质的量为0.6mol/5=0.12mol,质量为0.12mol×60g/mol=7.2g
【考点定位】本题综合考查化学反应原理中化学反应速率、化学平衡、电化学等知识。
(2011·山东)29.(16分)偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l)+2N2O4 (l)=2CO2 (g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是_______.
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g)2NO2 (g) (Ⅱ)
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________.
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数_____(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·S-1。
(4)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是_____ (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填”正向”“不”或“逆向”)移动,所滴加氨水的浓度为__ _mol·L-1。(NH3·H2O的电离平衡常数取Kb=2X10-5 mol·L-1)
【答案】(1)N2O4 (2)放热 (3)ad 不变 0.1 (4)NH4++H2ONH3·H2O+H+逆向
【解析】(1)反应(Ⅰ)中N2O4中N由+4价变为0价,作为氧化剂。(2)温度升高不变。v(N2O4)=v(NO2)=×=0.1mol/(L·s)。(4)NH4NO3溶液由于NH4+水解溶液显酸性,滴加氨水后溶液由酸性变为中性,水的电离平衡向逆反应方向移动。Kb=,而c(OH-)=10-7mol/L,则c(NH4+)=200c(NH3·H2O),故n(NH4+)=200n(NH3·H2O),根据电荷守恒,n(NH4+)=n(NO3-),则溶液中n(NH4+)+n(NH3·H2O)=a+,根据物料守恒,滴加氨水的浓度为(a+-a)mol÷bL=mol/L。
【考点定位】氧化还原反应,化学反应中的能量变化,化学平衡的移动等。
(2012·福建)23. ( 14分)
(1)元素M 的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为_ 。
(2)硫酸铝溶液与过量氨水反应的离子方程式为 _。
(3)能证明Na2SO3溶液中存在SO32-+H2OHSO3-+OH-水解平衡的事实是 _(填序号)。
A.滴人酚酞溶液变红,再加人H2SO4溶液后红色退去
B.滴人酚酞溶液变红,再加人氯水后红色退去
C.滴人酚酞溶液变红,再加人BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y 在周期表中位于向一主族,化合物Cu2X和Cu2Y 可发生如下转化(其中D 是纤维素水解的最终产物):
① 非金属性X Y(填“>”或“<”)
② Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为
(5)在恒容绝热(不与外界交换能量)条件下进行2A (g ) + B ( g)2C ( g ) + D ( s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
物质 A B C D
起始投料/mol 2 1 2 0
23.【解析】(1)NH4+ 所含的电子数和质子数分别是10、11,与其电子数和质子数均相等的简单离子只有Na+,Na的原子结构示意图为
。
升高而减小。
【答案】(1)
。
(2) 3NH3·H2O+Al3+=Al(OH)3↓+3NH4+
(3)C
(4)①< ② Cu2O+6HNO3(浓)2Cu(NO3)2+2NO2↑+3H2O。
(5) 化学平衡常数随温度升高而减小
【考点定位】本题考查了原子结构示意图、离子方程式的书写、化学平衡的判断和实验检验。
△
C3(H2O)
C3(H2)
C3(H2O)
C3(H2)
专题03 反应速率、化学平衡
(2012·广东)31.碘在科研与生活中有重要作用,某兴趣小组用0.50 mol·L—1KI、0.2%淀粉溶液、0.20 mol·L—1K2S2O8、0.10 mol·L—1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82—+ 2I— = 2 SO42— + I2(慢) I2 + 2 S2O32— = 2I— + S4O62— (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32—与S2O82—初始的物质的量需满足的关系为:n(S2O32—):n(S2O82—) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 体积V/ml
K2S2O8溶液 水 KI溶液 Na2S2O3溶液 淀粉溶液
① 10.0 0.0 4.0 4.0 2.0
② 9.0 1.0 4.0 4.0 2.0
③ 8.0 Vx 4.0 4.0 2.0
表中Vx = ml,理由是 。
(3)已知某条件下,浓度c(S2O82—)~反应时间t的变化曲线如图13,若保持其它条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82—)~反应时间t的变化曲线示意图(进行相应的标注)。
(4)碘也可用作心脏起捕器电源—锂碘电池的材料,该电池反应为:
2 Li(s) + I2 (s) = 2 LiI(s) ΔH
已知:4 Li(s) + O2 (g) = 2 Li2O(s) ΔH1
4 LiI(s) + O2 (g) = 2 I2 (s) + 2 Li2O(s) ΔH2
则电池反应的ΔH = ;碘电极作为该电池的 极。
【答案】(1)Na2S2O3, < 2
(2)2, 保证其他条件不变,只改变反应物K2S2O8浓度,从而才到达对照实验目的。
(3)
(4) (△H1—△H2)/2; 正极
【考点定位】化学反应速度的影响因素
(2012·福建)12 一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如右图所示。下列判断正确的是
A.在0-50min之间, pH =2 和 PH= 7 时 R 的降解百分率相等
B.溶液酸性越强, R 的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在 20-25min之间, pH = 10 时 R 的平均降解速率为 0.04mol·L-1·min-1
12【解析】A项:在0-50min内,PH=2时,20min时,R已经降解完了,因此R平均降解速率计算按0-20min,而PH=7时,40min时,R已经降解完了,因此R平均降解速率计算按0-40min,通过计算,正确;B项:,PH=2时大约在20min降解完,PH=7大约在40min降解完,但是起始浓度不相同,所以溶液的酸性与R降解速率没有直接联系,错误。C项:与B相同,错误;D项:PH=10时,在20-25min,R的平均降解速率为(0.6*10-4-0.4*10-4)/5=0,04*10-4mol●L-1min-1
【答案】A
【考点定位】本题考查了化学反应速率的图象分析。
(2012·四川)12.在体积恒定的密闭容器中,一定量的SO2与1.100molO2在催化剂作用下加热到600℃发生反应:2SO2 + O2 2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
A.当SO3的生成速率与SO2的消耗速率相等时反应达到平衡
B.降低温度,正反应速率减小程度比逆反应速率减小程度大
C.将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为161.980g
D.达到平衡时,SO2的转化率为90%
【答案】:D
【解析】:2SO2 + O2 2SO3,
始量 amol 1.100mol 0 mol
变量 2xmol xmol 2xmol
平衡 (a-2x) mol (1.100-x) mol 2xmol
由题意可得,a+1.100-(a-2x)- (1.100-x)- 2x=0.315,(a+1.100-2x)/(a+1.100)=0.825,(2011·大纲版)8.合成氨所需的氢气可用煤和水作原料经多步反映制得,其中的一步反应为
CO(g)+ H2O(g) CO2(g) + H2(g) △H <0
反应达到平衡后,为提高CO的转化率,下列措施中正确的是
A 增加压强 B 降低温度 C 增大CO 的浓度 D 更换催化剂
【答案】B
(2011·重庆)13.在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)2c(g);<0
x(g)+3y(g)2z(g);>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
等压时,通入惰性气体,c的物质的量不变
等压时,通入z气体,反应器中温度升高
等容时,通入惰性气体,各反应速率不变
等容时,通入x气体,y的物质的量浓度增大
【答案】A
【解析】等压时充入惰性气体,体积增大,但对于第二个反应而言平衡正向移动,反应吸热,温度降低,第一个反应向正向移动,c的物质的量增加,A项错误。
【考点定位】本题考查化学反应速率、化学平衡的移动等知识。
(2011·安徽)9.一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g)2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
9、【答案】D
【解析】。由于硫为液态,因此反应前后气体分子数不等,达平衡前容器内压强逐渐变小,分离出硫对化学反应速率及平衡无影响,即A、B错误;根据平衡移动原理知升温平衡向吸热方向移动即向左移动,SO2的转化率降低,C错误;平衡常数只受温度的影响,与催化剂无关,故D项正确。
【考点定位】本题主要考查外界条件对化学平衡及反应速率的影响,考查平衡常数的知识及平衡的移动。
(2012·天津)6.已知2SO2 (g) + O2 (g) 2SO3 (g);ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2 ;(丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙 > 2P乙
B.SO3的质量m:m甲=m丙 > 2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙 > k乙
D.反应放出或吸收热量的数值Q:Q甲=G丙 > 2Q乙
【答案】:B
【考点定位】此题综合考查了化学反应速率和化学平衡知识。
(2012·上海)18.为探究锌与稀硫酸的反应速率(以v(H2)表示)。向反应混合汶中加入某些物质,下列判断正确的是
A.加入NH4HSO4固体,v(H2)不变 B,加入少量水,v(H2)减小
C.加入CH3COONa固体,v(H2)减小 D.滴加少量CuSO4溶液,v(H2)减小
【答案】BC
【解析】NH4HSO4能电离生成H+,故v (H2)应增大;滴加少量CuSO4溶液后,Zn能与其置换出的Cu形成原电池,能加快反应速率。
【考点定位】本题考查化学反应速率的影响因素
(2012·江苏)10. 下列有关说法正确的是
A.CaCO3(s) =CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H2(g) =2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2 )和H2的平衡转化率均增大
D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
【答案】B
【考点定位】化学反应原理的分析
(2012·江苏)14. 温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)=PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s 0 50 150 250 350
n(PCl3) / mol 0 0. 16 0. 19 0. 20 0. 20
下列说法正确的是
A. 反应在前50 s 的平均速率v(PCl3)= 0. 0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)= 0. 11 mol·L-1,则反应的驻H<0
C. 相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3 和0. 20 mol Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2. 0 mol PCl3 和2. 0 mol Cl2,达到平衡时,PCl3 的转化率小于80%
【答案】C
【解析】A项,v (PCl3)= mol/(L·s),错;B项,从表中看,平衡时PCl3为0.2mol/2L=0.1mol/L,升高温度时,PCl3的浓度增大,即平衡正向移动,说明正反应为吸热反应,错;C项,原平衡时,K=,充入物质后,Q=,因为Q
【考点定位】化学反应速率与化学平衡
(2012·上海)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g)+Q(Q>0) 完成下列填空:
31.在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率___ mol/(L·min);该反应的平衡常数表达式K=_____
32.上述反应达到平衡后,下列说法正确的是_。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
33.一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_。
a.3v逆(N2)=v正(H2) b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
34.若平衡时H2和HCl的物质的量之比为m/n,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___m/n(填“>”、“=”或“<”)。
【答案】31.0.02;
32.bd
33.ac
34.<
【解析】31.反应生成n(Si3N4)==0.02 mol,则反应消耗n(H2)=0.12 mol,v (H2)==0.02 mol/(L·min),该反应的平衡常数的表达式为。
关。
34.降低温度,平衡向正反应方向移动,HCl的物质的量增大,H2的物质的量减小,故H2和HCl的物质的量之比大于。
【考点定位】本题主要考查化学反应速率与化学平衡得有关计算和判断。
(2012·全国新课标卷)27.(15分)光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成。
(1)实验室常用来制备氯气的化学方程式为 ;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(ΔH)分别为-890.3kJ·mol-1、-285.8kJ.mol-1和-283.0kJ.mol-1,则生成1m3(标准状况)CO所需热量为 ;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为 ;
(4)COCl2的分解反应为COCl2(g)=Cl2(g)+CO(g) ΔH=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出):
①计算反应在第8min时的平衡常数K= ;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2) T(8)
(填“<”、“>”或“=”),
③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)= mol·L-1;
④比较产物CO在2-3min、5-6min和12-13min时平均反应速率(平均反应速率分别以v(2-3)、v(5-6)、v(12-13))的大小 ;
⑤比较反应物COCl2在5-6min和15-16min时平均反应速率的大小:v(5-6) v(15-16)(填“<”、“>”或“=”),原因是 。
【答案】
(1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)5.52×103 KJ
(3)CHCl3+H2O2=COCl2+H2O+HCl
(4)①0.234 mol·L-1
②<
③0.031mol·L-1
④v(5-6)> v(2-3)=v(12-13)
ΔH=ΔH1-2ΔH2-2ΔH3=(-890.3)kJ·moL-1-2×(-285.8)kJ·moL-1-2×(-283.0)kJ·moL-1=247.3 kJ·moL-1,即生成2mol CO,需要吸热247.3 KJ,那么要得到1立方米的CO,吸热为(1000/22.4)×247.3/2=5.52×103 KJ。
(4)由图示可知8min时COCl2、Cl2、CO三种物质的浓度分别为0.04mol·L-1、0.11 mol·L-1、0.085 mol·L-1。所以此时其平衡常数为:0.11 mol·L-1×0.085 mol·L-1÷0.04 mol·L-1=0.23 4mol·L-1。第8min时反应物的浓度比第2min时减小,生成物浓度增大,平衡向正反应方向移动。又因为正反应为吸热反应,所以T(2)<T(8)。④根据图像变化可知:在2min时升温 。在10min时 增加COCl2的浓度,在12min时,反应达到平衡 。在相同温度时,该反应的反应物浓度越高,反应速率越大,v(5-6)>v(15-16)。
【考点定位】热化学方程式的书写、反应热的计算、化学反应速率、影响化学反应速率的因素、化学平衡、化学图像。
(2012·北京)26. (12分)用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。
反应A: 4HCl+O2 2Cl2+2H2O
(1)已知:i 反应A中, 4mol HCI被氧化,放出115.6kJ的热量。
ii
①H2O的电子式是_______________.
②反应A的热化学方程式是_______________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中
H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是______________.
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投
料比的关系是_________________.
⑧投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是_______________.
【答案】:(1);4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H= - 115.6 kJ/mol;32;强;(2)4:1;投料比越小时对应的温度越低;30.8%。
【解析】:(1)根据水分子的结构,其电子式为:;反应A的热化学方程式为:4HCl(g)+O2(g)2Cl2(g)+2H2O(g) △H= - 115.6 kJ/mol;由于反应中,需要断裂4mol“H—Cl“键、断开1mol“O=O”键,形成2mol“Cl-Cl”键,形成4mol“H-O”键;根据图纸数据,断开1mol“O=O”键,形成2mol“Cl-Cl”键的能量差为12kJ/mol,,反应的热效应为:-115.6 kJ/mol,故此断裂4mol“H—Cl“键和形成4mol“H-O”键的能量差为:-127.6 kJ/mol,故断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为32kJ,H2O中H—O 键比HCl中H—Cl键强;(2)根据反应方程式:4HCl+O22Cl2+2H2O,氧气的投料比越高,则HCl的转化率越高,故此曲线b对应的投料比为4:1;由于该反应正向放热,故温度越高,HCl的转化率越低,故投料比越小时温度越高;当投料比为2:1,温度为400℃时,HCl的转化率约为80%,此时为:
(2012·天津)10.(14分)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g) W (s) + 3H2O (g)
请回答下列问题:
⑴ 上述反应的化学平衡常数表达式为___________________________。
⑵ 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_____________________;随温度的升高,H2与水蒸气的体积比减小,则该反应为___________反应(填“吸热”或“放热”)。
⑶上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 25℃ ~ 550℃ ~ 600℃ ~ 700℃
主要成份 WO3 W2O5 WO2 W
第一阶段反应的化学方程式为___________________________;580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为____________________________________。
⑷ 已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g) W (s) + 2H2O (g) ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2(g) W (s) + 2H2O (g) ΔH = -137.9 kJ·mol-1
则WO2 (s) WO2 (g) 的ΔH = ______________________。
⑸ 钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) WI4 (g)。下列说法正确的有________________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
【答案】:(1)k= ;(2)60%;吸热;(3)2WO3+H2W2O5+H2O;W2O5、WO2;1:1:4;(4)+203.9kJ·mol-1;(5)ab。
【解析】:(1)根据题给的化学方程式,其中的WO3和W均为固体,平衡常数中不写入,故k= ;(2)由方程式:WO3+3H2W+3H2O,两物质的化学计量数相同,又知平衡时两者的体积比为2:3,故氢气的平衡转化率为:(3/5)×100%=60%;温度升高时,氢气和水蒸气的体积比减小,说明平衡向正向移动,说明该反应正向吸热;(3)根据表格中给出的反应的三个阶段,第一阶段,WO3转化为W2O5,方程式可表示为:2WO3+H2W2O5+H2O;在580℃时,反应进入第二阶段,固体物质的主要成分是:W2O5、WO2;第二阶段的方程式可表示为:W2O5+H22WO2+H2O、第三阶段的方程式为: WO2+2H2W+2H2O;故三阶段消耗的氢气的物质的量为:1:1:4;(4)根据题给的两个热化学方程式:WO2(s)+2H2(g)W(s)+2H2O(g) △H= +66.0 kJ·mol-1①; WO2(g)+2H2(g)W(s)+2H2O(g) △H=-137.9kJ·mol-1②;将反应①-②得到:WO2(s) WO2(g) △H= +203.9kJ·mol-1;(5)根据钨丝灯管的反应原理,可知灯管内的碘单质可循环使用,a对;加入碘单质的作用是减缓灯丝变细,故b对;由于四碘化钨是在1400℃生成,高于3000℃时分解,故应在灯丝上形成,c错;温度升高时,不管是分解速率和化合速率都加快,d错。
【考点定位】此题为以金属钨的制取为基础,综合考查了化学平衡常数、平衡转化率、化学平衡的移动、盖斯定律、化学方程式的书写等知识。
(2011·重庆)29.(14分)尿素是首个由无机物人工合成的有机物。
(1)工业上尿素和,在一定条件下合成,其反应方程式为 。
(2)当氨碳比的转化率随时间的变化关系如题29图1所示.
①A点的逆反应速率 点的正反应速率为(填“大于”、“小于”或“等于”)
②的平衡转化率为 。
版权所有:高考资源网(www.)
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图29图2.
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 。
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解).
【答案】(1)2NH3+CO2CO(NH3)2+H2O
(2)①小于
②30%
(3)①B
②2Cl-—2e-=Cl2↑, CO(NH3)2 +3 Cl2+H2O=N2+CO2+6HCl
③不变;7.2
【解析】(1)合成尿素根据原子个数守恒,还生成H2O,及2NH3+CO2CO(NH3)2+H2O。(2)①A点未达到平衡,此过程中正反应速率减小,逆反应速率增大, B点达到平衡正逆反应速率相等,对CO2来说逆反应速率达到最大,故为小于。②根据2NH3+CO2CO(NH3)2+H2O可设起始CO2为xmol
4x x 0 0
x×60% 则转化的NH3为2x×60%,所以转化率=%
(3)①由图像电解产生产物知:生成氢气的极为阴极,则B为负极。②阳极室中Cl-失电子产生Cl2。③阴极减少的H+,可通过质子交换膜补充,而使PH不变。气体物质的量为13.44L/22.4L/mol=0.6mol,由电子守恒及其原子个数守恒CO(NH2)2 ~3 Cl2~N2~CO2 ~3H2,则CO(NH2)2的物质的量为0.6mol/5=0.12mol,质量为0.12mol×60g/mol=7.2g
【考点定位】本题综合考查化学反应原理中化学反应速率、化学平衡、电化学等知识。
(2011·山东)29.(16分)偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l)+2N2O4 (l)=2CO2 (g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是_______.
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g)2NO2 (g) (Ⅱ)
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________.
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数_____(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·S-1。
(4)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是_____ (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填”正向”“不”或“逆向”)移动,所滴加氨水的浓度为__ _mol·L-1。(NH3·H2O的电离平衡常数取Kb=2X10-5 mol·L-1)
【答案】(1)N2O4 (2)放热 (3)ad 不变 0.1 (4)NH4++H2ONH3·H2O+H+逆向
【解析】(1)反应(Ⅰ)中N2O4中N由+4价变为0价,作为氧化剂。(2)温度升高不变。v(N2O4)=v(NO2)=×=0.1mol/(L·s)。(4)NH4NO3溶液由于NH4+水解溶液显酸性,滴加氨水后溶液由酸性变为中性,水的电离平衡向逆反应方向移动。Kb=,而c(OH-)=10-7mol/L,则c(NH4+)=200c(NH3·H2O),故n(NH4+)=200n(NH3·H2O),根据电荷守恒,n(NH4+)=n(NO3-),则溶液中n(NH4+)+n(NH3·H2O)=a+,根据物料守恒,滴加氨水的浓度为(a+-a)mol÷bL=mol/L。
【考点定位】氧化还原反应,化学反应中的能量变化,化学平衡的移动等。
(2012·福建)23. ( 14分)
(1)元素M 的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为_ 。
(2)硫酸铝溶液与过量氨水反应的离子方程式为 _。
(3)能证明Na2SO3溶液中存在SO32-+H2OHSO3-+OH-水解平衡的事实是 _(填序号)。
A.滴人酚酞溶液变红,再加人H2SO4溶液后红色退去
B.滴人酚酞溶液变红,再加人氯水后红色退去
C.滴人酚酞溶液变红,再加人BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y 在周期表中位于向一主族,化合物Cu2X和Cu2Y 可发生如下转化(其中D 是纤维素水解的最终产物):
① 非金属性X Y(填“>”或“<”)
② Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为
(5)在恒容绝热(不与外界交换能量)条件下进行2A (g ) + B ( g)2C ( g ) + D ( s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:
物质 A B C D
起始投料/mol 2 1 2 0
23.【解析】(1)NH4+ 所含的电子数和质子数分别是10、11,与其电子数和质子数均相等的简单离子只有Na+,Na的原子结构示意图为
。
升高而减小。
【答案】(1)
。
(2) 3NH3·H2O+Al3+=Al(OH)3↓+3NH4+
(3)C
(4)①< ② Cu2O+6HNO3(浓)2Cu(NO3)2+2NO2↑+3H2O。
(5) 化学平衡常数随温度升高而减小
【考点定位】本题考查了原子结构示意图、离子方程式的书写、化学平衡的判断和实验检验。
△
C3(H2O)
C3(H2)
C3(H2O)
C3(H2)
同课章节目录
