2012年高考试题分项解析化学 专题11 无机综合与推断
文档属性
| 名称 | 2012年高考试题分项解析化学 专题11 无机综合与推断 | 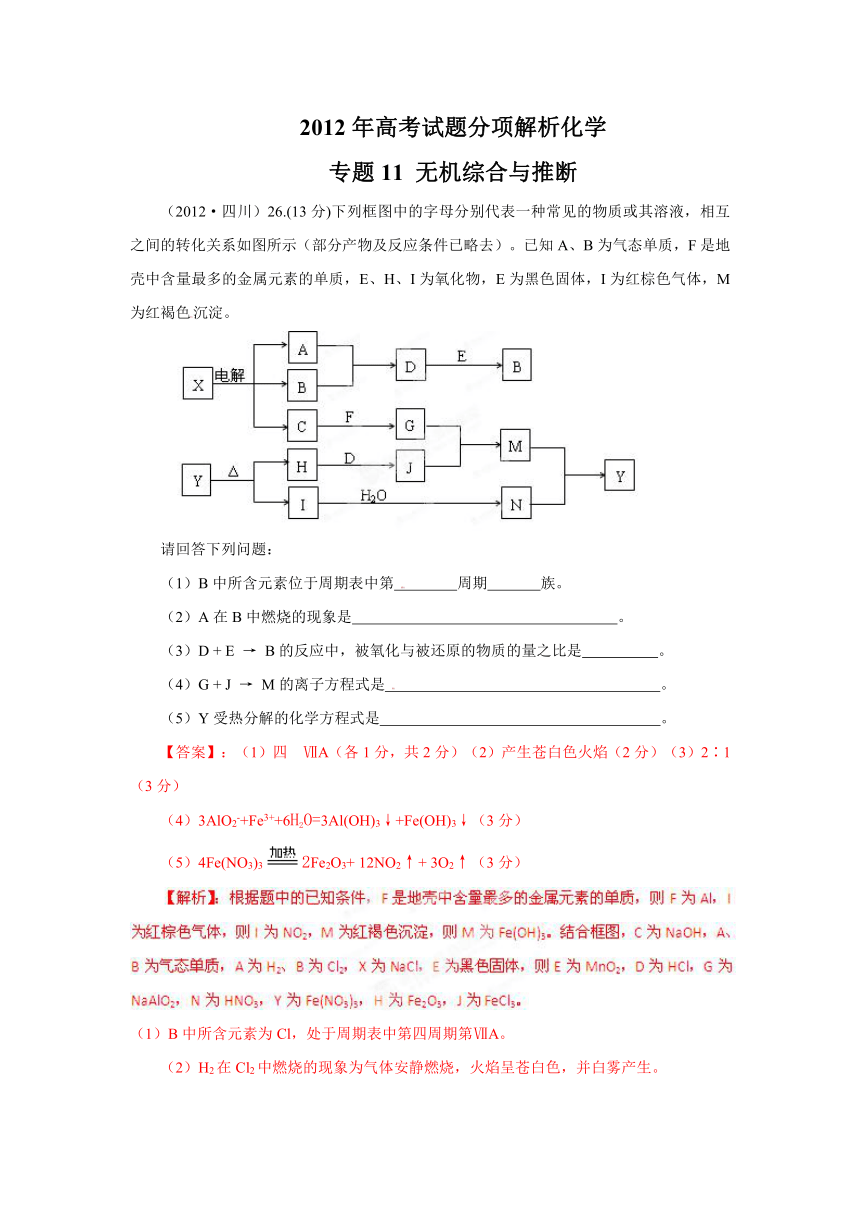 | |
| 格式 | zip | ||
| 文件大小 | 125.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | |||
| 科目 | 化学 | ||
| 更新时间 | 2012-07-09 09:40:07 | ||
图片预览


文档简介
2012年高考试题分项解析化学
专题11 无机综合与推断
(2012·四川)26.(13分)下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质,E、H、I为氧化物,E为黑色固体,I为红棕色气体,M为红褐色沉淀。
请回答下列问题:
(1)B中所含元素位于周期表中第 周期 族。
(2)A在B中燃烧的现象是 。
(3)D + E → B的反应中,被氧化与被还原的物质的量之比是 。
(4)G + J → M的离子方程式是 。
(5)Y受热分解的化学方程式是 。
【答案】:(1)四 ⅦA(各1分,共2分)(2)产生苍白色火焰(2分)(3)2∶1(3分)
(4)3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓(3分)
(5)4Fe(NO3)32Fe2O3+ 12NO2↑+ 3O2↑(3分)
(1)B中所含元素为Cl,处于周期表中第四周期第ⅦA。
(2)H2在Cl2中燃烧的现象为气体安静燃烧,火焰呈苍白色,并白雾产生。
(3)由MnO2 + 4HCl(浓)MnCl2 + H2O + Cl2↑可知,被氧化的是HCl(浓),物质的量为2mol,被还原的物质是MnO2,物质的量为1mol,物质的量之比为2∶1。
(4)NaAlO2和FeCl3在溶液中发生双水解,离子方程式为3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓
(5)Fe(NO3)3受热分解的方程式为4Fe(NO3)32Fe2O3+ 12NO2↑+ 3O2↑
【考点定位】本题考查无机推断,涉及到金属元素Na、Al、Fe、Mn和非金属元素H、O、N、Cl。
(2011·大纲版)27.(15分)(注意:在试题卷上作答无效)
原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b和d的A2B型氢化物均为V形分子,c的+1价离子比e的-1价离子少8个电子。
回答下列问题:
元素a为________;c为_______
由这些元素形成的双原子分子为__________________。
由这些元素形成的三原子分子中,分子的空间结构属于直线形的是_______,非直线形的是_______________________。(写2种)
这些元素的单质或由他们形成的AB型化合物中,其晶体类型属于原子晶体的是_______,离子晶体的是_______,金属晶体的是_______,分子晶体的是_______;(每空填一种)
元素a和b形成的一种化合物与c和b形成的一种化合物发生的反应常用于防毒面具中,该反应的化学方程式为_______________________。
(2011·重庆)26.(15分)金刚石具有优良的耐磨、耐腐蚀特性,应用广泛.
(1) 碳与周期元素的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,碳元素在周期表中的位置是 ,是 ,的电子式为 .
(2) 一定条件下,还原CCl4可制备金刚石,反应结束冷却至室温后,回收其中的实验操作名称为 ,除去粗产品中少量钠的试剂为 .
(3)碳还原制,其粗产品中杂质为和.先将20.0g粗产品加入到过量的溶液中充分反应,收集到0.1mol氢气,过滤得固体11.4g,滤液稀释到1L,生成氢气的离子方程式为 ,硅盐酸的物质量浓度为 。
(4)下列叙述正确的有 (填序号),
①还原CCl4的反应、Cl2与的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③溶液与的反应可用于推断与的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2
【答案】(1)第二周期第IVA族,氧(或O),
(2)过滤,水(或乙醇)
(3)Si+2OH-+H20=SiO32-+2H2,0.17mol/L
(4)③④
【解析】 (1) 碳元素的原子有两个电子层,最外层有四个电子,故在第二周期第IVA越强对应非金属性越强,硫酸生成硅酸,说明硫酸酸性大于硅酸,从而说明S的非金属性大于Si,C正确;钠在空气中燃烧生成Na2O2,锂燃烧生成Li2O,阴阳离子之比均为1:2,D正确。
【考点定位】本题考查硅与碳单质及化合物的结构与性质。
专题11 无机综合与推断
(2012·四川)26.(13分)下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质,E、H、I为氧化物,E为黑色固体,I为红棕色气体,M为红褐色沉淀。
请回答下列问题:
(1)B中所含元素位于周期表中第 周期 族。
(2)A在B中燃烧的现象是 。
(3)D + E → B的反应中,被氧化与被还原的物质的量之比是 。
(4)G + J → M的离子方程式是 。
(5)Y受热分解的化学方程式是 。
【答案】:(1)四 ⅦA(各1分,共2分)(2)产生苍白色火焰(2分)(3)2∶1(3分)
(4)3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓(3分)
(5)4Fe(NO3)32Fe2O3+ 12NO2↑+ 3O2↑(3分)
(1)B中所含元素为Cl,处于周期表中第四周期第ⅦA。
(2)H2在Cl2中燃烧的现象为气体安静燃烧,火焰呈苍白色,并白雾产生。
(3)由MnO2 + 4HCl(浓)MnCl2 + H2O + Cl2↑可知,被氧化的是HCl(浓),物质的量为2mol,被还原的物质是MnO2,物质的量为1mol,物质的量之比为2∶1。
(4)NaAlO2和FeCl3在溶液中发生双水解,离子方程式为3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓
(5)Fe(NO3)3受热分解的方程式为4Fe(NO3)32Fe2O3+ 12NO2↑+ 3O2↑
【考点定位】本题考查无机推断,涉及到金属元素Na、Al、Fe、Mn和非金属元素H、O、N、Cl。
(2011·大纲版)27.(15分)(注意:在试题卷上作答无效)
原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b和d的A2B型氢化物均为V形分子,c的+1价离子比e的-1价离子少8个电子。
回答下列问题:
元素a为________;c为_______
由这些元素形成的双原子分子为__________________。
由这些元素形成的三原子分子中,分子的空间结构属于直线形的是_______,非直线形的是_______________________。(写2种)
这些元素的单质或由他们形成的AB型化合物中,其晶体类型属于原子晶体的是_______,离子晶体的是_______,金属晶体的是_______,分子晶体的是_______;(每空填一种)
元素a和b形成的一种化合物与c和b形成的一种化合物发生的反应常用于防毒面具中,该反应的化学方程式为_______________________。
(2011·重庆)26.(15分)金刚石具有优良的耐磨、耐腐蚀特性,应用广泛.
(1) 碳与周期元素的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,碳元素在周期表中的位置是 ,是 ,的电子式为 .
(2) 一定条件下,还原CCl4可制备金刚石,反应结束冷却至室温后,回收其中的实验操作名称为 ,除去粗产品中少量钠的试剂为 .
(3)碳还原制,其粗产品中杂质为和.先将20.0g粗产品加入到过量的溶液中充分反应,收集到0.1mol氢气,过滤得固体11.4g,滤液稀释到1L,生成氢气的离子方程式为 ,硅盐酸的物质量浓度为 。
(4)下列叙述正确的有 (填序号),
①还原CCl4的反应、Cl2与的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③溶液与的反应可用于推断与的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2
【答案】(1)第二周期第IVA族,氧(或O),
(2)过滤,水(或乙醇)
(3)Si+2OH-+H20=SiO32-+2H2,0.17mol/L
(4)③④
【解析】 (1) 碳元素的原子有两个电子层,最外层有四个电子,故在第二周期第IVA越强对应非金属性越强,硫酸生成硅酸,说明硫酸酸性大于硅酸,从而说明S的非金属性大于Si,C正确;钠在空气中燃烧生成Na2O2,锂燃烧生成Li2O,阴阳离子之比均为1:2,D正确。
【考点定位】本题考查硅与碳单质及化合物的结构与性质。
同课章节目录
